文档内容
2019 年陕西省初中毕业学业考试(副题)
一、选择题(共7小题,每小题2分,计14分。每小题只有一个选项是符合题意的)
1. 化学推动着社会的进步和科技的发展。下列说法不正确的是( )
A. 用天然气取代燃煤作燃料,有效降低了空气污染
B. 用作食品脱氧剂的铁粉可以吸收食品袋内的氧气和二氧化碳
C. 利用稀有气体通电时发出不同颜色的光制成霓虹灯,美化了城市夜景
D. 用来制造人造卫星天线的钛镍记忆合金是金属材料
【答案】B
【解析】
【详解】A、天然气的主要成分是CH ,燃烧生成水和二氧化碳,取代燃煤作燃料,可以减少二氧化硫等有
4
害气体和烟尘的产生,有效降低了空气污染,故A正确;
B、用作食品脱氧剂的铁粉,可以和氧气、水发生反应,不能吸收二氧化碳,B错误;
C、稀有气体通电时发出不同颜色的光,故可以制成霓虹灯,美化了城市夜景,C正确;
D、金属材料包括纯金属和合金,故钛镍记忆合金属于金属材料,D正确;
故选B。
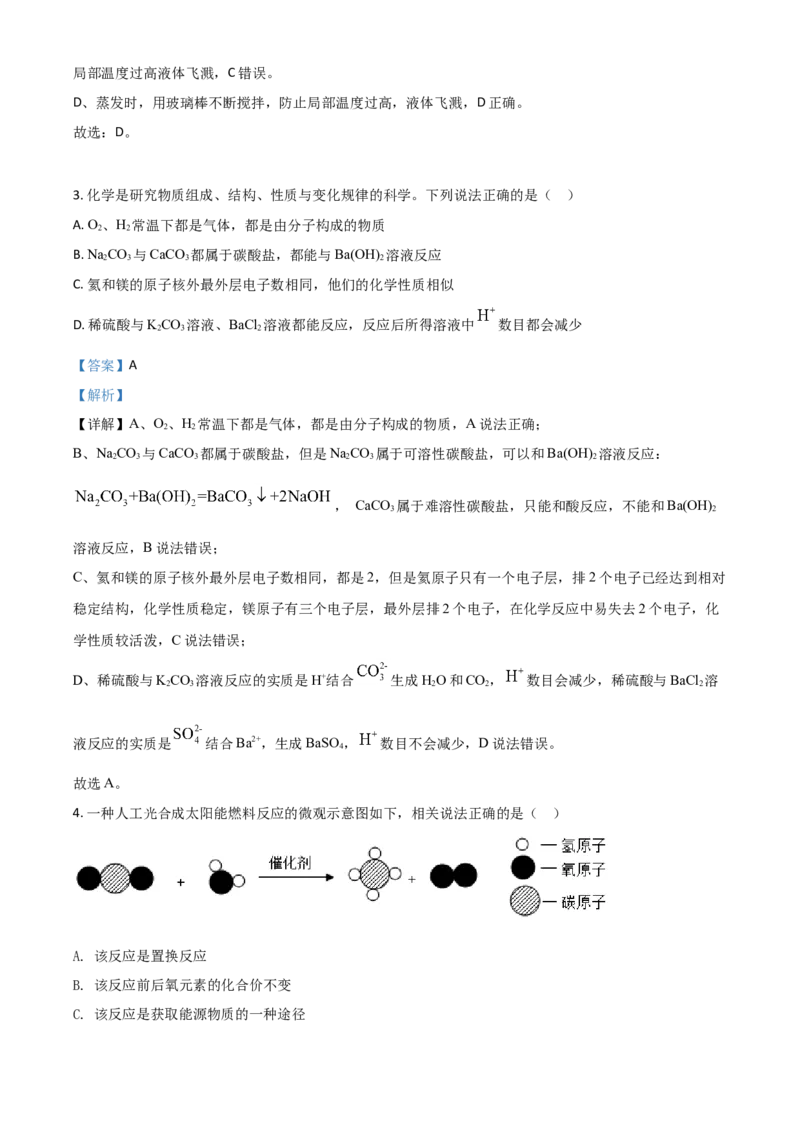
2. 下列实验基本操作正确的是( )
A. 滴加液体 B. 熄灭酒精灯
C. 稀释浓硫酸 D. 蒸发
【答案】D
【解析】
【详解】A、胶头滴管,滴加液体要垂直悬空滴加,防止药品污染,A错误。
B、酒精灯要用灯帽盖灭,不能吹灭,避免引发火灾,B错误。
C、稀释浓硫酸,要把浓硫酸沿烧杯内壁缓慢注入水中,并且用玻璃棒不断搅拌,防止浓硫酸吸水放热,局部温度过高液体飞溅,C错误。
D、蒸发时,用玻璃棒不断搅拌,防止局部温度过高,液体飞溅,D正确。
故选:D。
3. 化学是研究物质组成、结构、性质与变化规律的科学。下列说法正确的是( )
A. O、H 常温下都是气体,都是由分子构成的物质
2 2
B. NaCO 与CaCO 都属于碳酸盐,都能与Ba(OH) 溶液反应
2 3 3 2
C. 氦和镁的原子核外最外层电子数相同,他们的化学性质相似
D. 稀硫酸与KCO 溶液、BaCl 溶液都能反应,反应后所得溶液中 数目都会减少
2 3 2
【答案】A
【解析】
【详解】A、O、H 常温下都是气体,都是由分子构成的物质,A说法正确;
2 2
B、NaCO 与CaCO 都属于碳酸盐,但是NaCO 属于可溶性碳酸盐,可以和Ba(OH) 溶液反应:
2 3 3 2 3 2
, CaCO 属于难溶性碳酸盐,只能和酸反应,不能和Ba(OH)
3 2
溶液反应,B说法错误;
C、氦和镁的原子核外最外层电子数相同,都是2,但是氦原子只有一个电子层,排2个电子已经达到相对
稳定结构,化学性质稳定,镁原子有三个电子层,最外层排2个电子,在化学反应中易失去2个电子,化
学性质较活泼,C说法错误;
D、稀硫酸与KCO 溶液反应的实质是H+结合 生成HO和CO, 数目会减少,稀硫酸与BaCl 溶
2 3 2 2 2
液反应的实质是 结合Ba2+,生成BaSO, 数目不会减少,D说法错误。
4
故选A。
4. 一种人工光合成太阳能燃料反应的微观示意图如下,相关说法正确的是( )
A. 该反应是置换反应
B. 该反应前后氧元素的化合价不变
C. 该反应是获取能源物质的一种途径D. 参加反应的两种物质的分子个数比为1∶1
【答案】C
【解析】
【详解】A、单质和化合物反应生成单质和化合物的反应属于置换反应,由微观示意图可知反应物是两种
化合物,该反应不属于置换反应,A错误。
B、反应前氧元素-2价,反应氧气中氧元素零价,化合价改变,B错误。
C、甲烷是天然气的主要成分,是一种能源,该反应生成甲烷,故该反应是获取能源物质的一种途径,C
正确。
D、由图可知该反应二氧化碳和水反应生成甲烷和氧气,化学方程式为CO+2H O CH+2O ,参加
2 2 4 2
反应的两种物质的分子个数比为1∶2,D错误。
故选:C。
5. 钠、镁、铝、铁及其氢氧化物的部分信息如下表:
单质 Na Mg Al Fe
常温下与水剧 能与热水微弱 只能与高温水
与水反应的情况 能与热水反应
烈反应 反应 蒸气反应
氢氧化物(碱) NaOH Mg(OH) Al(OH) Fe(OH)
2 3 3
溶解性 易溶 难溶 难溶 难溶
热稳定性 受热不分解 受热分解 受热分解 受热分解
下列相关说法不正确的是( )
A. 四种金属与水反应的难易程度与其相应的金属活动性顺序不一致
B. 金属钠着火不能用水扑灭
C. 一般情况下,难溶性碱受热能分解
D. 四种金属的氢氧化物均能与稀硫酸反应
【答案】A
【解析】
【详解】A、钠、镁、铝、铁金属活动性逐渐减弱,与水的反应变的困难,与其相应的金属活动性顺序一
致,A错误。
B、金属钠常温下与水剧烈反应,故金属钠着火不能用水扑灭,B正确。
C、氢氧化镁、氢氧化铝、氢氧化铁属于难溶性碱,受热分解,氢氧化钠可溶性碱,受热不分解,故一般
情况下,难溶性碱受热能分解,C正确。D、酸、碱反应生成盐和水,四种金属的氢氧化物均能与稀硫酸反应,D正确。
故选:A。
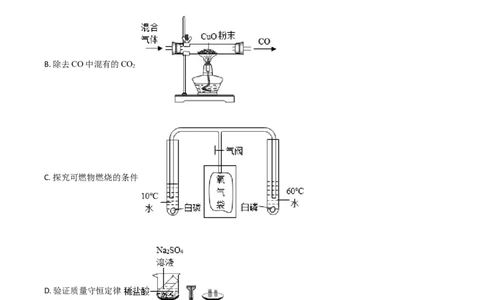
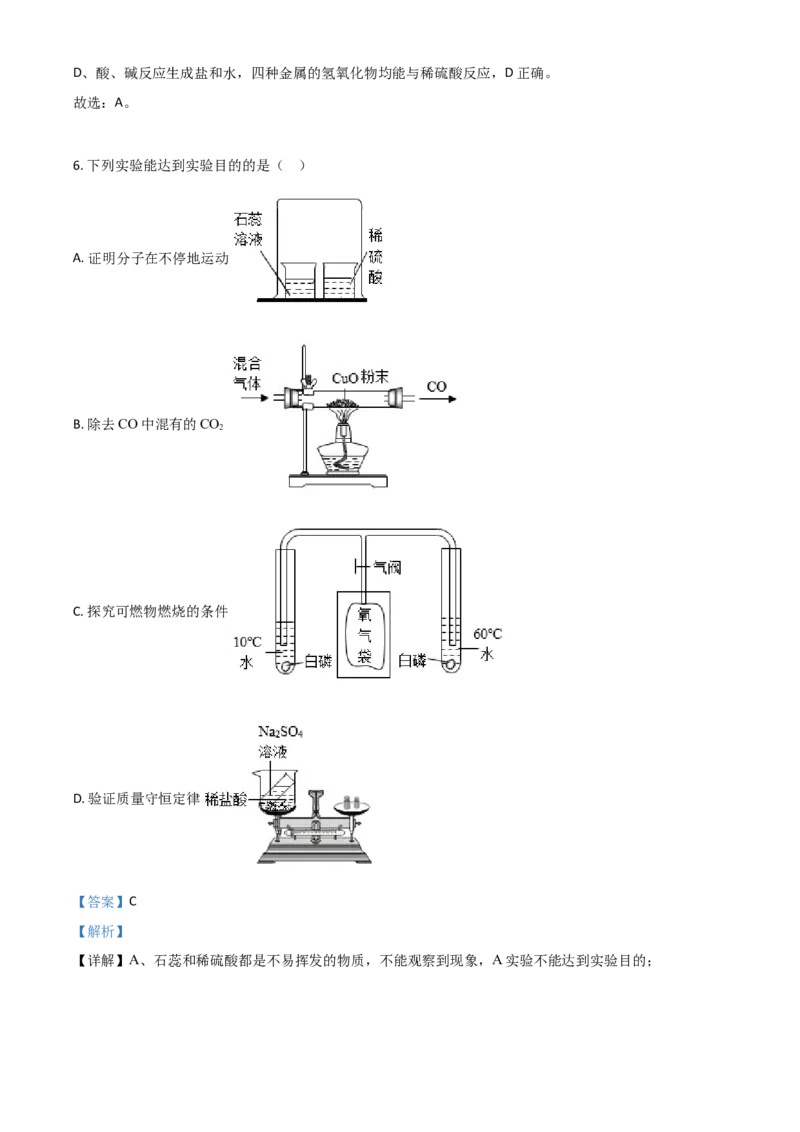
6. 下列实验能达到实验目的的是( )
A. 证明分子在不停地运动
B. 除去CO中混有的CO
2
C. 探究可燃物燃烧的条件
D. 验证质量守恒定律
【答案】C
【解析】
【详解】A、石蕊和稀硫酸都是不易挥发的物质,不能观察到现象,A实验不能达到实验目的;B、CO会和CuO发生反应, ,CO 不和CuO反应,B实验不能达到实验目的;
2
C、打开气阀前,左右两边白磷都不燃烧,打开气阀后,左边白磷不燃烧,右边白磷燃烧。由“打开气阀
前,右边白磷不燃烧,打开气阀后,右边白磷燃烧”的现象对比,可以得出燃烧需要氧气;由“打开气阀
后,左边白磷不燃烧,右边白磷燃烧” 的现象对比,可以得出燃烧需要温度达到可燃物的着火点,故C实
验可以达到实验目的;
D、硫酸钠和稀盐酸不反应,故无法验证质量守恒定律,无法达到实验目的;
故选C。
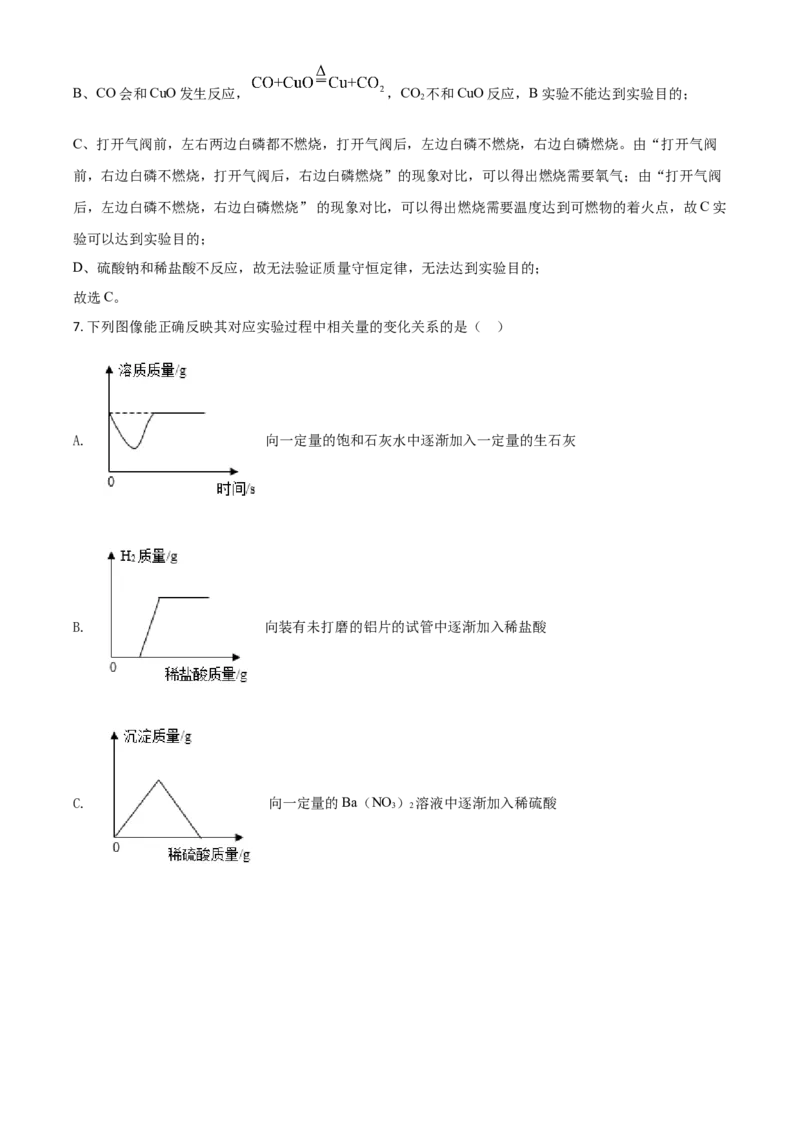
7. 下列图像能正确反映其对应实验过程中相关量的变化关系的是( )
A. 向一定量的饱和石灰水中逐渐加入一定量的生石灰
B. 向装有未打磨的铝片的试管中逐渐加入稀盐酸
C. 向一定量的Ba(NO ) 溶液中逐渐加入稀硫酸
3 2D. 向一定量的稀盐酸中逐渐加入NaOH溶液
【答案】B
【解析】
【详解】A、生石灰和水反应生成氢氧化钙,向一定量的饱和石灰水中逐渐加入一定量的生石灰,溶剂质
量减少,且反应放热,生成的氢氧化钙溶解度随温度的升高而减小,最终溶质质量会比起始小,图像不符,
A错误。
的
B、铝和氧气反应生成氧化铝,未打磨 铝片的试管中逐渐加入稀盐酸,稀盐酸和氧化铝生成氯化铝和水,
没有氢气产生,待氧化铝反应完后,盐酸再和铝反应生成氯化铝和氢气,图像相符,B正确。
C、硝酸钡和硫酸反应生成硫酸钡沉淀和硝酸,硫酸钡不溶于硝酸,反应结束后沉淀质量不变,图像不符,
C错误。
D、向一定量的稀盐酸中逐渐加入NaOH溶,溶液由酸性变为碱性,刚开始pH小于7,后来pH大于7,图
像不符,D错误。
故选:B。
二、填空及简答题(共5小题,计19分)
8. “面条像裤带、房子一边盖……”,陕西八大怪是陕西特有的地域文化。
(1)面条中富含的有机营养素是_____。
(2)为增强小麦的抗倒伏能力,应该施用_____(填字母)。
A NHNO B KCl C Ca(HPO )
4 3 2 4 2
(3)盖房子用的沙子的主要成分SiO 属于_____(填“化合物”或“混合物”)。
2
【答案】 (1). 糖类 (2). B (3). 化合物
【解析】
【详解】(1)面条中富含糖类,故填:糖类。
(2)增加小麦抗倒伏能力,需施钾肥。NH NO 属于氮肥,KCl含钾元素,属于钾肥,Ca(HPO ) 属于
4 3 2 4 2
磷肥,故填:B。
(3)二氧化硅是两种元素组成的纯净物,属于化合物,故填:化合物。
9. “垃圾分类,绿色生活新时尚。”下图是常见的垃圾分类处理模式。(1)制作垃圾筒的塑料属于_____(填“合成”或“天然”)材料。
(2)用完的中性笔芯和过期药品应分别投入_____(填字母)垃圾筒。
A 蓝色、绿色 B 蓝色、红色 C 绿色、红色
(3)从废旧电池中回收的石墨可制作电极,是因其具有_____性。
【答案】 (1). 合成 (2). B (3). 导电
【解析】
【详解】(1)有机合成材料包括塑料、合成纤维、合成橡胶;塑料属于合成材料,故填:合成。(2)用完的中性笔芯可以回收,属于可回收物,过期药品属于有害垃圾,故选:B。
(3)石墨具有导电性,可做电极,故填:导电性。
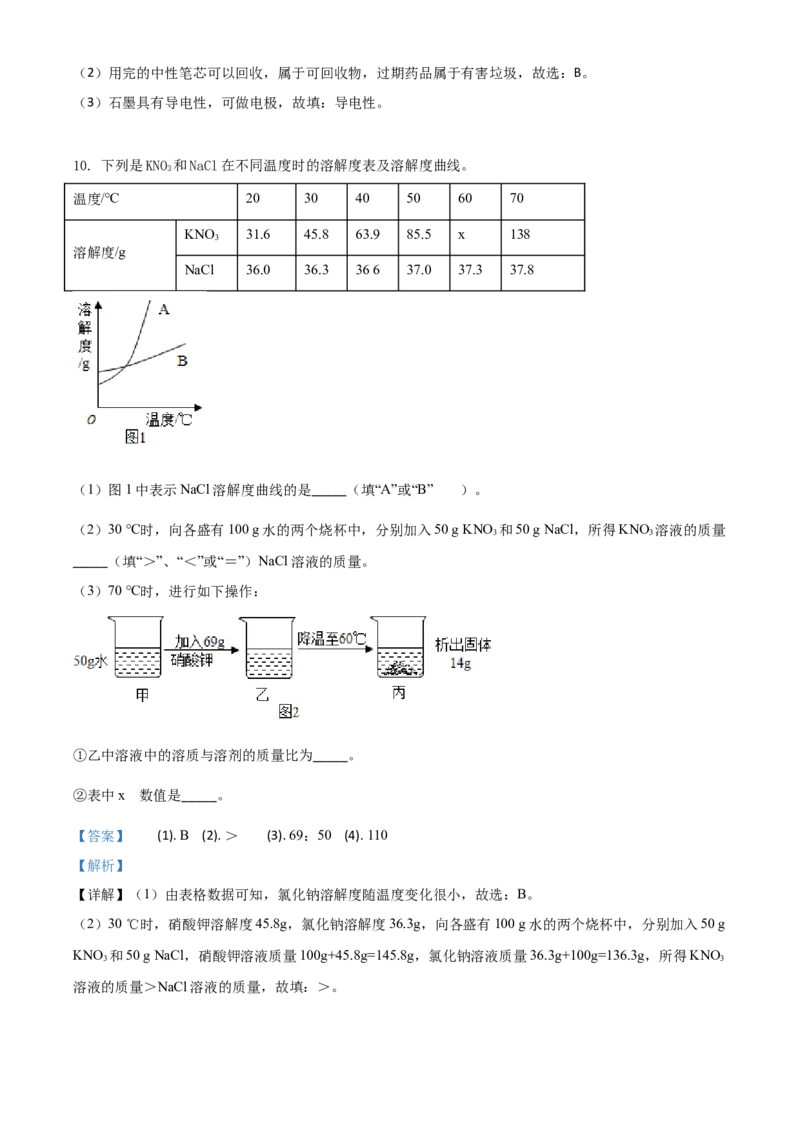
10. 下列是KNO 和NaCl在不同温度时的溶解度表及溶解度曲线。
3
温度/℃ 20 30 40 50 60 70
KNO 31.6 45.8 63.9 85.5 x 138
3
溶解度/g .
NaCl 36.0 36.3 366 37.0 37.3 37.8
(1)图1中表示NaCl溶解度曲线的是_____(填“A”或“B” )。
(2)30 ℃时,向各盛有100 g水的两个烧杯中,分别加入50 g KNO 和50 g NaCl,所得KNO 溶液的质量
3 3
_____(填“>”、“<”或“=”)NaCl溶液的质量。
(3)70 ℃时,进行如下操作:
①乙中溶液中的溶质与溶剂的质量比为_____。
的
②表中x 数值是_____。
【答案】 (1). B (2). > (3). 69:50 (4). 110
【解析】
【详解】(1)由表格数据可知,氯化钠溶解度随温度变化很小,故选:B。
(2)30 ℃时,硝酸钾溶解度45.8g,氯化钠溶解度36.3g,向各盛有100 g水的两个烧杯中,分别加入50 g
KNO 和50 g NaCl,硝酸钾溶液质量100g+45.8g=145.8g,氯化钠溶液质量36.3g+100g=136.3g,所得KNO
3 3
溶液的质量>NaCl溶液的质量,故填:>。(3)①70 ℃时,硝酸钾溶解度138g,故50g水溶解硝酸钾138g× =69g,加入的69g硝酸钾全部溶
解,溶质与溶剂的质量比为69:50,故填:69:50。
②降温至60 ℃,析出14g硝酸钾,故溶解硝酸钾69g-14g=55g,溶解度为55g× =110g,表中x的数
值110g,故填:110。
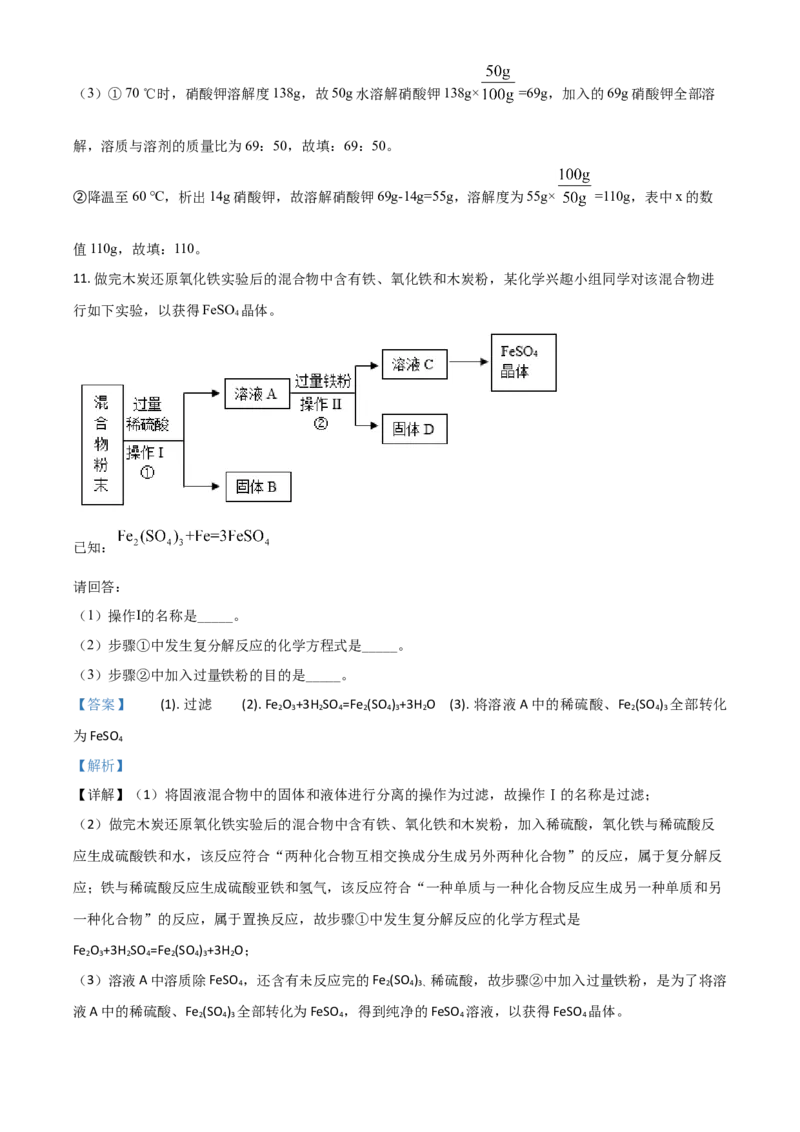
11. 做完木炭还原氧化铁实验后的混合物中含有铁、氧化铁和木炭粉,某化学兴趣小组同学对该混合物进
行如下实验,以获得FeSO 晶体。
4
已知:
请回答:
(1)操作Ⅰ的名称是_____。
(2)步骤①中发生复分解反应的化学方程式是_____。
(3)步骤②中加入过量铁粉的目的是_____。
【答案】 (1). 过滤 (2). Fe O +3H SO =Fe (SO ) +3H O (3). 将溶液A中的稀硫酸、Fe (SO ) 全部转化
2 3 2 4 2 4 3 2 2 4 3
为FeSO
4
【解析】
【详解】(1)将固液混合物中的固体和液体进行分离的操作为过滤,故操作Ⅰ的名称是过滤;
(2)做完木炭还原氧化铁实验后的混合物中含有铁、氧化铁和木炭粉,加入稀硫酸,氧化铁与稀硫酸反
应生成硫酸铁和水,该反应符合“两种化合物互相交换成分生成另外两种化合物”的反应,属于复分解反
应;铁与稀硫酸反应生成硫酸亚铁和氢气,该反应符合“一种单质与一种化合物反应生成另一种单质和另
一种化合物”的反应,属于置换反应,故步骤①中发生复分解反应的化学方程式是
Fe O +3H SO =Fe (SO ) +3H O;
2 3 2 4 2 4 3 2
(3)溶液A中溶质除FeSO ,还含有未反应完的Fe (SO ) 稀硫酸,故步骤②中加入过量铁粉,是为了将溶
4 2 4 3、
液A中的稀硫酸、Fe (SO ) 全部转化为FeSO ,得到纯净的FeSO 溶液,以获得FeSO 晶体。
2 4 3 4 4 4【点睛】在含有Fe (SO ) 和H SO 的混合溶液中,Fe会先和Fe (SO ) 反应,混合物粉末中铁粉的量不确定,
2 4 3 2 4 2 4 3
故Fe (SO ) 可能会被反应完,故步骤②中会加入过量的铁粉,将Fe (SO ) 全部转化为FeSO 。
2 4 3 2 4 3 4
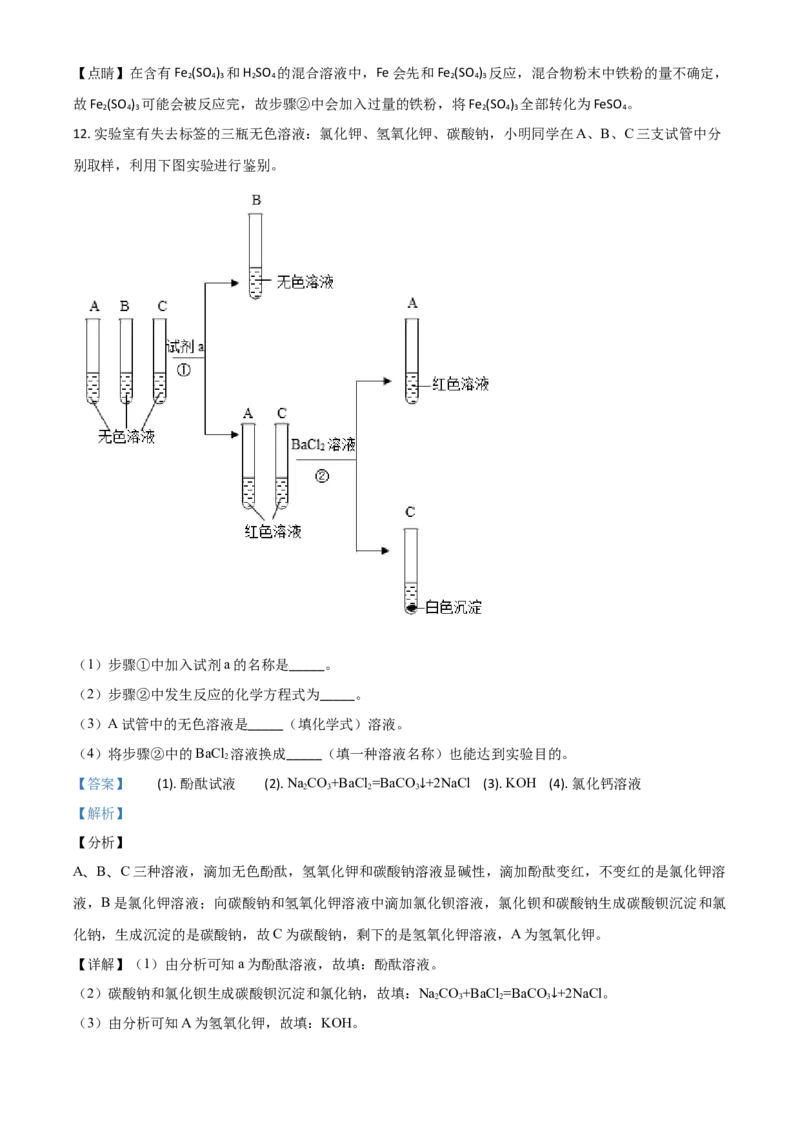
12. 实验室有失去标签的三瓶无色溶液:氯化钾、氢氧化钾、碳酸钠,小明同学在A、B、C三支试管中分
别取样,利用下图实验进行鉴别。
(1)步骤①中加入试剂a的名称是_____。
(2)步骤②中发生反应的化学方程式为_____。
(3)A试管中的无色溶液是_____(填化学式)溶液。
(4)将步骤②中的BaCl 溶液换成_____(填一种溶液名称)也能达到实验目的。
2
【答案】 (1). 酚酞试液 (2). NaCO+BaCl =BaCO +2NaCl (3). KOH (4). 氯化钙溶液
2 3 2 3
【解析】 ↓
【分析】
A、B、C三种溶液,滴加无色酚酞,氢氧化钾和碳酸钠溶液显碱性,滴加酚酞变红,不变红的是氯化钾溶
液,B是氯化钾溶液;向碳酸钠和氢氧化钾溶液中滴加氯化钡溶液,氯化钡和碳酸钠生成碳酸钡沉淀和氯
化钠,生成沉淀的是碳酸钠,故C为碳酸钠,剩下的是氢氧化钾溶液,A为氢氧化钾。
【详解】(1)由分析可知a为酚酞溶液,故填:酚酞溶液。
(2)碳酸钠和氯化钡生成碳酸钡沉淀和氯化钠,故填:NaCO+BaCl =BaCO +2NaCl。
2 3 2 3
(3)由分析可知A为氢氧化钾,故填:KOH。 ↓的
(4)氯化钙和碳酸钠生成碳酸钙沉淀和氯化钠,和氢氧化钾不反应,将步骤②中 BaCl 溶液换成氯化钙
2
溶液也能达到实验目的,故填:氯化钙溶液。
三、实验及探究题(共2小题,计12分)
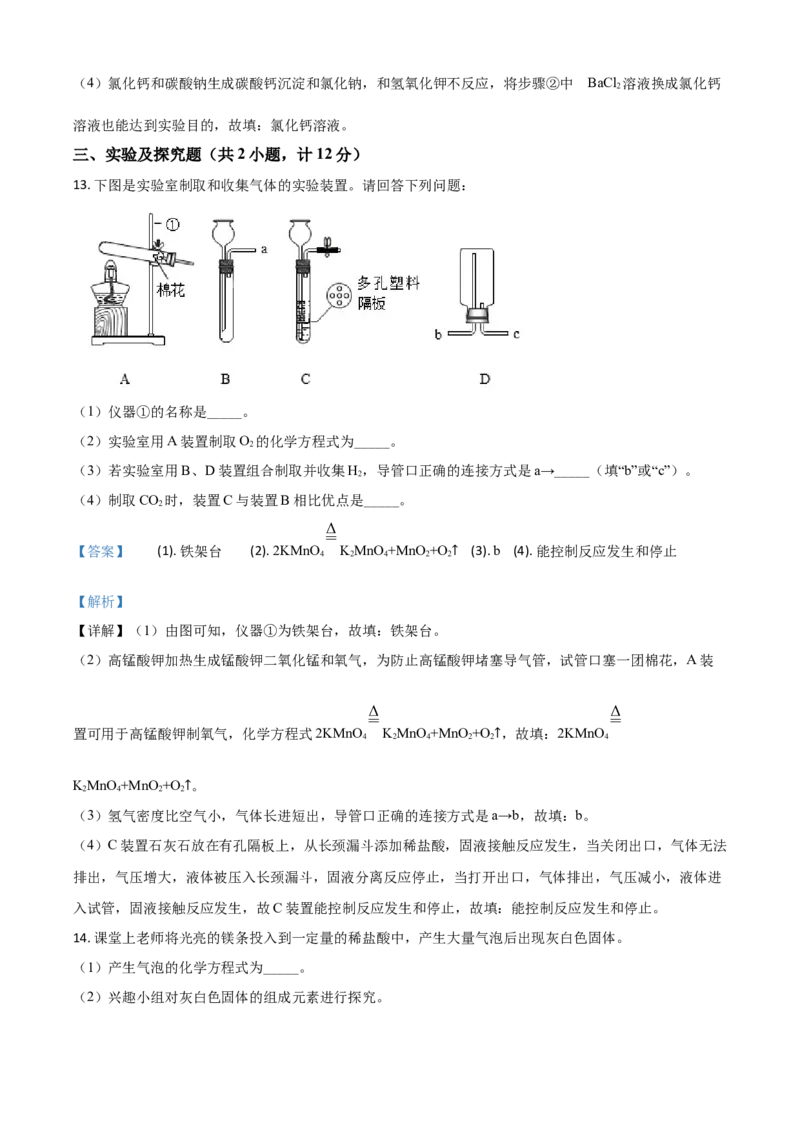
13. 下图是实验室制取和收集气体的实验装置。请回答下列问题:
(1)仪器①的名称是_____。
(2)实验室用A装置制取O 的化学方程式为_____。
2
(3)若实验室用B、D装置组合制取并收集H,导管口正确的连接方式是a→_____(填“b”或“c”)。
2
(4)制取CO 时,装置C与装置B相比优点是_____。
2
【答案】 (1). 铁架台 (2). 2KMnO KMnO +MnO+O (3). b (4). 能控制反应发生和停止
4 2 4 2 2
↑
【解析】
【详解】(1)由图可知,仪器①为铁架台,故填:铁架台。
(2)高锰酸钾加热生成锰酸钾二氧化锰和氧气,为防止高锰酸钾堵塞导气管,试管口塞一团棉花,A装
置可用于高锰酸钾制氧气,化学方程式2KMnO KMnO +MnO+O ,故填:2KMnO
4 2 4 2 2 4
↑
KMnO +MnO+O 。
2 4 2 2
(3)氢气密度比空↑气小,气体长进短出,导管口正确的连接方式是a→b,故填:b。
(4)C装置石灰石放在有孔隔板上,从长颈漏斗添加稀盐酸,固液接触反应发生,当关闭出口,气体无法
排出,气压增大,液体被压入长颈漏斗,固液分离反应停止,当打开出口,气体排出,气压减小,液体进
入试管,固液接触反应发生,故C装置能控制反应发生和停止,故填:能控制反应发生和停止。
14. 课堂上老师将光亮的镁条投入到一定量的稀盐酸中,产生大量气泡后出现灰白色固体。
(1)产生气泡的化学方程式为_____。
(2)兴趣小组对灰白色固体的组成元素进行探究。【做出猜想】
猜想一:只有镁元素,是镁单质;
猜想二:含有镁和氯两种元素,是MgCl ;
2
猜想三:含有镁、氢、氧三种元素,是Mg(OH);
2
猜想四:含有镁、氢、氧、氯四种元素。
【实验验证】
小组同学过滤出灰白色固体,经过洗涤、室温下干燥后,进行了以下实验。
①小明取少量灰白色固体样品于试管中,加入稀盐酸,观察到固体溶解,_____,证明猜想一不成立。
另取少量灰白色固体样品于烧杯中,加足量水搅拌,灰白色固体不溶解,你认为猜想_____不成立。
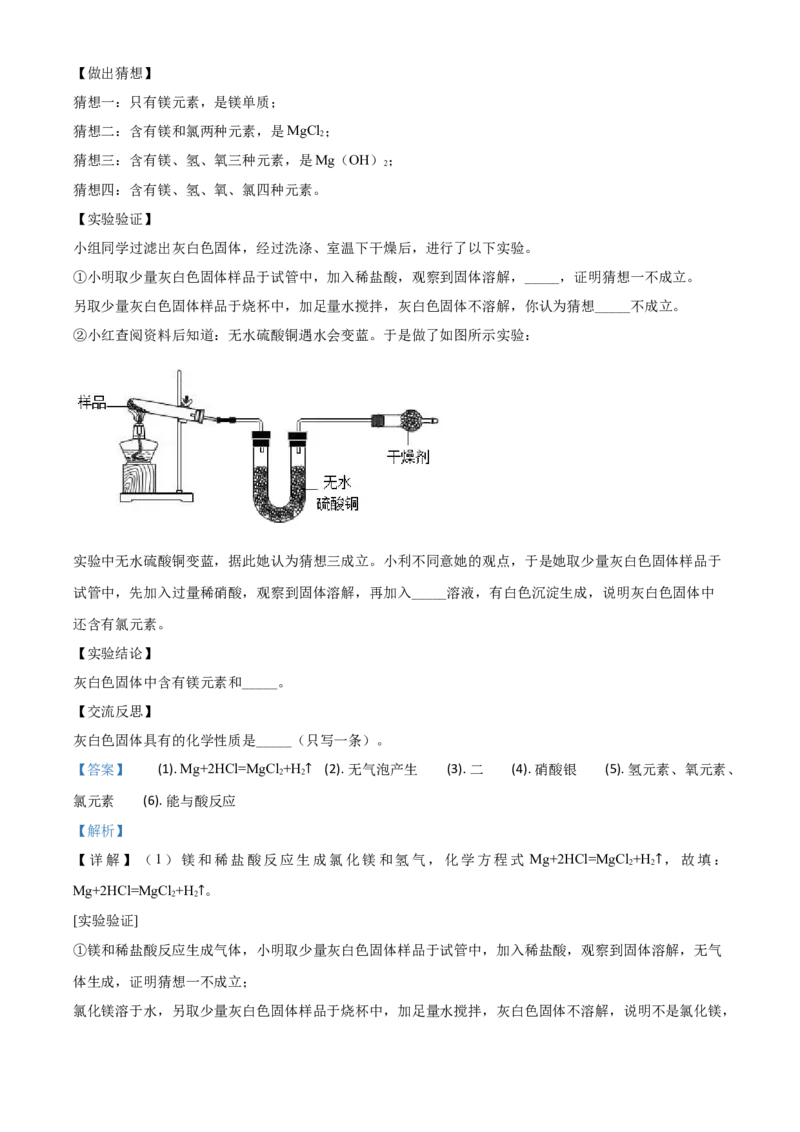
②小红查阅资料后知道:无水硫酸铜遇水会变蓝。于是做了如图所示实验:
实验中无水硫酸铜变蓝,据此她认为猜想三成立。小利不同意她的观点,于是她取少量灰白色固体样品于
试管中,先加入过量稀硝酸,观察到固体溶解,再加入_____溶液,有白色沉淀生成,说明灰白色固体中
还含有氯元素。
【实验结论】
灰白色固体中含有镁元素和_____。
【交流反思】
灰白色固体具有的化学性质是_____(只写一条)。
【答案】 (1). Mg+2HCl=MgCl +H (2). 无气泡产生 (3). 二 (4). 硝酸银 (5). 氢元素、氧元素、
2 2
氯元素 (6). 能与酸反应 ↑
【解析】
【详解】(1)镁和稀盐酸反应生成氯化镁和氢气,化学方程式 Mg+2HCl=MgCl +H ,故填:
2 2
Mg+2HCl=MgCl +H 。 ↑
2 2
[实验验证] ↑
①镁和稀盐酸反应生成气体,小明取少量灰白色固体样品于试管中,加入稀盐酸,观察到固体溶解,无气
体生成,证明猜想一不成立;
氯化镁溶于水,另取少量灰白色固体样品于烧杯中,加足量水搅拌,灰白色固体不溶解,说明不是氯化镁,猜想二不成立;
故填:无气泡产生;二。
②氯离子和银离子生成氯化银沉淀,取少量灰白色固体样品于试管中,先加入过量稀硝酸,观察到固体溶
解,再加入硝酸银溶液,有白色沉淀生成,说明灰白色固体中还含有氯元素,故填:硝酸银。
[实验结论]
固体含有氯元素,说明猜想三错误,故灰白色固体中含有镁元素和氢元素、氧元素、氯元素,故填:氢元
素、氧元素、氯元素。
[交流反思]
灰白色固体样品于试管中,加入稀盐酸,观察到固体溶解,说明能与酸反应,故填:能与酸反应。
四、计算与分析题
15. 某同学向盛有100 g过氧化氢溶液的烧杯中加入3 g二氧化锰,充分反应后,称得烧杯内剩余物质的总
质量为101.4 g。
(1)实验结束后,该同学过滤出烧杯内的固体,并对其进行洗涤、干燥、称量,得到固体的质量应为
_____g。
(2)计算过氧化氢溶液中溶质质量分数。
【答案】(1)3
(2)3.4%
解:设过氧化氢溶液中溶质质量分数x
反应生成氧气质量100g+3g-101.4g=1.6g。
答:过氧化氢溶液中溶质质量分数3.4%。
【解析】
。
【详解】(1)催化剂反应前后质量不变,故填:3
(2)见答案。