文档内容
2019年陕西省中考化学试卷
一、选择题(共7小题,每小题2分,满分14分)
1.(2分)化学使生活更美好。下列说法不正确的是( )
A.制作计算机芯片的材料硅是一种非金属
B.食用苏打饼干可缓解因胃酸过多引起的不良症状
C.低碳生活提倡使用不含碳元素的物质
D.图书资料失火可用干冰灭火减少损失
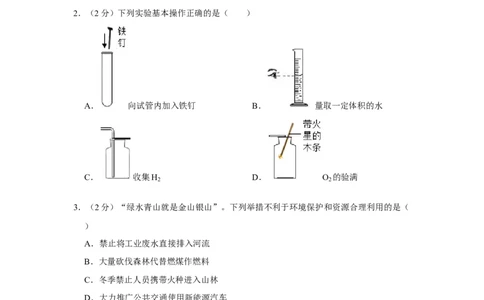
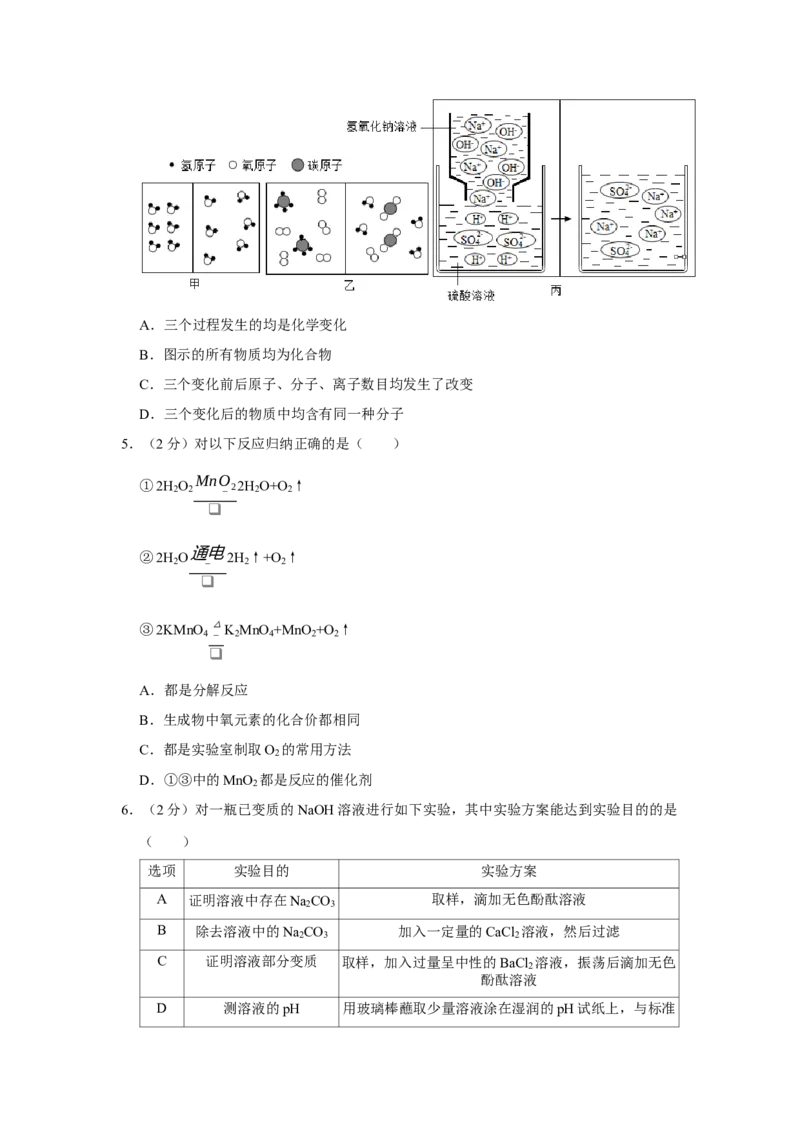
2.(2分)下列实验基本操作正确的是( )
A. 向试管内加入铁钉 B. 量取一定体积的水
C. 收集H D. O 的验满
2 2
3.(2分)“绿水青山就是金山银山”。下列举措不利于环境保护和资源合理利用的是(
)
A.禁止将工业废水直接排入河流
B.大量砍伐森林代替燃煤作燃料
C.冬季禁止人员携带火种进入山林
D.大力推广公共交通使用新能源汽车
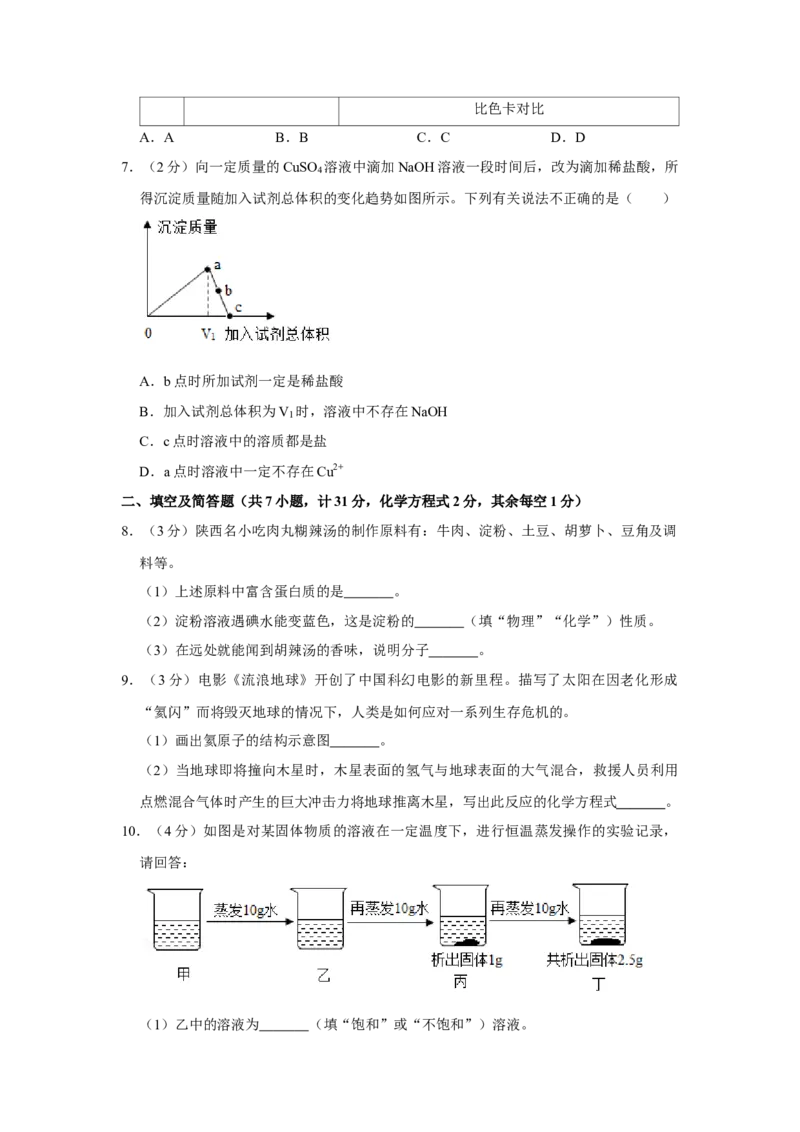
4.(2分)“宏观﹣微观﹣符号”是学习化学的重要内容和方法。甲、乙、丙是三个变化
过程的微观示意图,下列各项分析正确的是( )A.三个过程发生的均是化学变化
B.图示的所有物质均为化合物
C.三个变化前后原子、分子、离子数目均发生了改变
D.三个变化后的物质中均含有同一种分子
5.(2分)对以下反应归纳正确的是( )
MnO
①2H
2
O
2
22H
2
O+O
2
↑
¯
❑
通电
②2H O 2H ↑+O ↑
2 2 2
¯
❑
△
③2KMnO K MnO +MnO +O ↑
4 2 4 2 2
¯
❑
A.都是分解反应
B.生成物中氧元素的化合价都相同
C.都是实验室制取O 的常用方法
2
D.①③中的MnO 都是反应的催化剂
2
6.(2分)对一瓶已变质的NaOH溶液进行如下实验,其中实验方案能达到实验目的的是
( )
选项 实验目的 实验方案
A 证明溶液中存在Na CO 取样,滴加无色酚酞溶液
2 3
B 除去溶液中的Na CO 加入一定量的CaCl 溶液,然后过滤
2 3 2
C 证明溶液部分变质 取样,加入过量呈中性的BaCl 溶液,振荡后滴加无色
2
酚酞溶液
D 测溶液的pH 用玻璃棒蘸取少量溶液涂在湿润的pH试纸上,与标准比色卡对比
A.A B.B C.C D.D
7.(2分)向一定质量的CuSO 溶液中滴加NaOH溶液一段时间后,改为滴加稀盐酸,所
4
得沉淀质量随加入试剂总体积的变化趋势如图所示。下列有关说法不正确的是( )
A.b点时所加试剂一定是稀盐酸
B.加入试剂总体积为V 时,溶液中不存在NaOH
1
C.c点时溶液中的溶质都是盐
D.a点时溶液中一定不存在Cu2+
二、填空及简答题(共7小题,计31分,化学方程式2分,其余每空1分)
8.(3分)陕西名小吃肉丸糊辣汤的制作原料有:牛肉、淀粉、土豆、胡萝卜、豆角及调
料等。
(1)上述原料中富含蛋白质的是 。
(2)淀粉溶液遇碘水能变蓝色,这是淀粉的 (填“物理”“化学”)性质。
(3)在远处就能闻到胡辣汤的香味,说明分子 。
9.(3分)电影《流浪地球》开创了中国科幻电影的新里程。描写了太阳在因老化形成
“氦闪”而将毁灭地球的情况下,人类是如何应对一系列生存危机的。
(1)画出氦原子的结构示意图 。
(2)当地球即将撞向木星时,木星表面的氢气与地球表面的大气混合,救援人员利用
点燃混合气体时产生的巨大冲击力将地球推离木星,写出此反应的化学方程式 。
10.(4分)如图是对某固体物质的溶液在一定温度下,进行恒温蒸发操作的实验记录,
请回答:
(1)乙中的溶液为 (填“饱和”或“不饱和”)溶液。(2)该固体物质在当时温度下的溶解度为 。
(3)甲、乙、丙、丁中溶液溶质质量分数的大小关系是 。
(4)给丁中的溶液升高温度时,固体逐渐消失,说明该物质的溶解度随温度升高而
(填“增大”或“减小”)。
11.(4分)学习金属的化学性质时,小亮同学将一称重后的铜片伸入盛有AgNO 溶液的
3
烧杯中,待溶液颜色变蓝后,取出铜片直接称量,发现其质量增加了ag。
请回答:
(1)写出上述反应的化学方程式 。
(2)取出铜片后,烧杯内溶液质量减少了 g。
(3)小建同学将一定量的铁粉加入取出铜片后的溶液中,充分振荡后过滤,向滤渣中
加入稀硫酸,有气泡生成,则可推断,滤液中的溶质是 。
12.(5分)工业上用电解饱和食盐水的方法制得的烧碱中常含有一定量的NaCl.为测定
某烧碱样品的纯度,同学们设计了如下方案。
加水溶解
方案一:称取m g烧碱样品 → 测定消耗稀盐酸的质量。
滴加a%稀盐酸
加水溶解
方案二:称取m g烧碱样品 → 测定生成沉淀的质量。
滴加过量b%FeCl溶液
3
请回答:
(1)方案一中,发生反应的化学方程式为 。
(2)方案一中,为减少误差,最好选择下列方法中的 (填字母)来判断反应恰
好完全进行。
A.向样品溶液中滴加2~3滴无色酚酞溶液,根据溶液颜色变化判断。
B.测定过程中,边滴加稀盐酸边用pH试纸频繁测定混合液的pH
C.向样品溶液中滴加2~3滴紫色石蕊溶液,根据溶液颜色变化判断。
(3)判断方案二中FeCl 溶液过量的化学方法是 。
3
(4)小李同学可将方案二中的FeCl 溶液换成稀硝酸和 (填化学式)溶液,也
3
能达到实验目的。
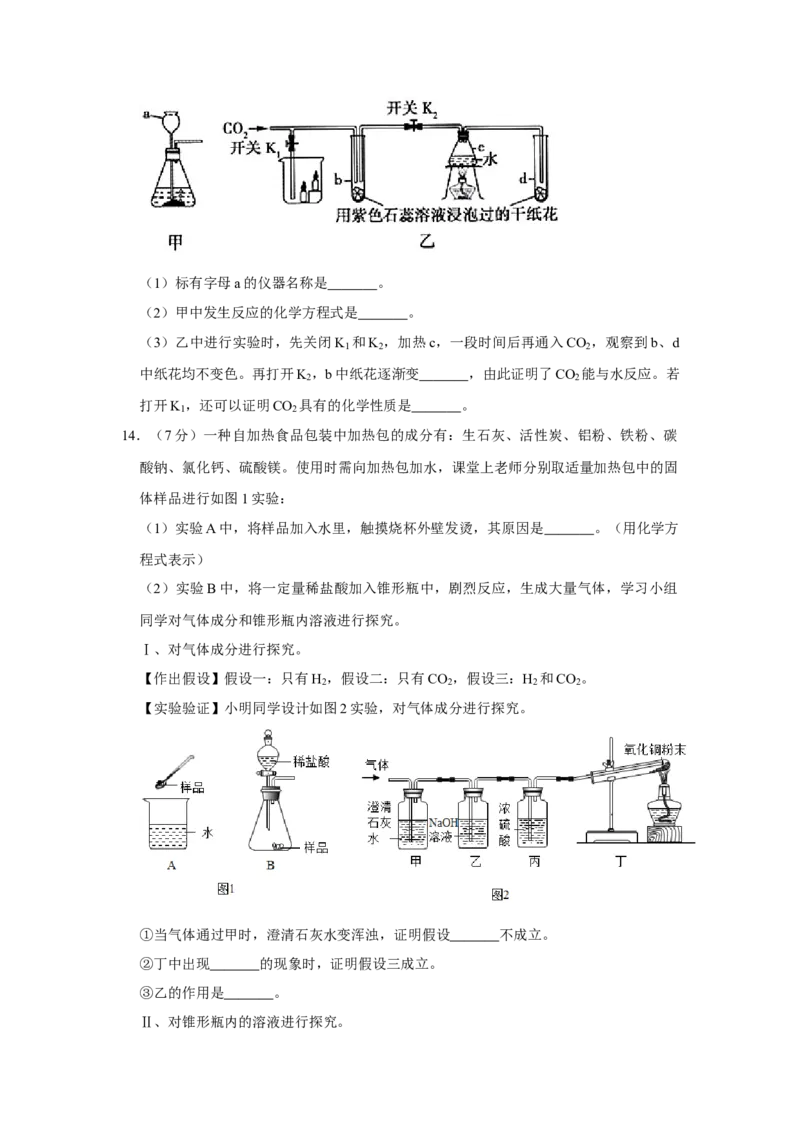
13.(5分)如图甲、乙是实验室制备CO 和某同学设计的验证CO 性质的实验装置图。
2 2(1)标有字母a的仪器名称是 。
(2)甲中发生反应的化学方程式是 。
(3)乙中进行实验时,先关闭K 和K ,加热c,一段时间后再通入CO ,观察到b、d
1 2 2
中纸花均不变色。再打开K ,b中纸花逐渐变 ,由此证明了CO 能与水反应。若
2 2
打开K ,还可以证明CO 具有的化学性质是 。
1 2
14.(7分)一种自加热食品包装中加热包的成分有:生石灰、活性炭、铝粉、铁粉、碳
酸钠、氯化钙、硫酸镁。使用时需向加热包加水,课堂上老师分别取适量加热包中的固
体样品进行如图1实验:
(1)实验A中,将样品加入水里,触摸烧杯外壁发烫,其原因是 。(用化学方
程式表示)
(2)实验B中,将一定量稀盐酸加入锥形瓶中,剧烈反应,生成大量气体,学习小组
同学对气体成分和锥形瓶内溶液进行探究。
Ⅰ、对气体成分进行探究。
【作出假设】假设一:只有H ,假设二:只有CO ,假设三:H 和CO 。
2 2 2 2
【实验验证】小明同学设计如图2实验,对气体成分进行探究。
①当气体通过甲时,澄清石灰水变浑浊,证明假设 不成立。
②丁中出现 的现象时,证明假设三成立。
③乙的作用是 。
Ⅱ、对锥形瓶内的溶液进行探究。实验后,小萍同学取少量锥形瓶内的溶液于试管中,向其中滴加NaOH溶液,开始一段
时间无沉淀生成,其原因是锥形瓶内的溶液中存在 。
【总结反思】通过以上探究,小林同学做了如下的反思归纳:
a.加热包应密封防潮保存
b.向用过的加热包内的固体中,加入过量稀盐酸后过滤,可以回收活性炭
c.能与水混合放出热量的物质均可用作加热包中的发热材料
你认为其中不正确的是 (填字母)
四.计算与分析题)(5分)
15.(5分)化学兴趣小组为测定某铜锌合金中成分金属的含量,称取10g样品放入烧杯
中,向其中加入 100g稀硫酸,恰好完全反应后。测得烧杯内所有物质的总质量为
109.8g。
请完成下列分析及计算:
(1)反应中共生成气体 g。
(2)计算合金中铜的质量分数。