文档内容
第二章 海水中的重要元素—钠和氯
第三节 物质的量 课时作业
第四课时 配制一定的物质的量浓度的溶液
基础达标
1.下列仪器中,通常不能用作反应容器的是( )
①容量瓶 ②烧杯 ③锥形瓶 ④量筒
A.①②④ B.②③ C.①④ D.③④
2.下列叙述正确的是( )
A.容量瓶用蒸馏水洗净后,可不经干燥直接用于配制溶液
B.用分液的方法分离水和酒精的混合物
C.配制1 L 0.1 mol·L-1的NaCl溶液时可用托盘天平称量5.85 g NaCl固体
D.用胶头滴管滴加液体时,为防止液滴飞溅,胶头滴管尖嘴紧贴试管内壁
3.实验室需用 450mL0.1mol•L-1 硫酸铜溶液,下列有关该溶液的配制说法正确的是(
)
A.用天平称取 12.5g 胆矾
B.应选用 450mL 容量瓶配制溶液
C.溶解胆矾的烧杯需用水洗涤2~3次,并将洗涤液丢弃
D.定容时,眼睛盯着胶头滴管
4.用氢氧化钠固体配制1.0 mol·L-1的溶液220 mL,下列说法正确的是( )
A.需先称取氢氧化钠固体8.8 g
B.氢氧化钠在烧杯中溶解后,要立即转移至容量瓶
C.溶液转移到容量瓶后,烧杯及玻璃棒用蒸馏水洗涤 2~3次,并将洗涤液转移至容
量瓶
D.定容后将溶液振荡摇匀,静置时发现液面低于刻度线,于是又加水至刻度线
的
5.实验室中需0.5 mol·L-1 NaCO 溶液950 mL,下图为配制该溶液 示意图。
2 3如下情况中使所配溶液浓度偏高的有( )
A.步骤①称量的NaCO·10H O失去部分结晶
2 3 2
B.在步骤③中不慎有少量液体流到容量瓶外
C.没有进行步骤④和⑤
D.某同学在步骤⑥观察液面时仰视
6.用36.5%的浓盐酸(ρ=1.2 g·cm-3)配制1 mol·L-1的稀盐酸100 mL,配制过程需要
用到哪些仪器,且先后顺序正确的是( )
①100 mL量筒 ②10 mL量筒 ③50 mL烧杯 ④托盘天平
⑤100 mL容量瓶 ⑥胶头滴管 ⑦玻璃棒
A.①⑥③⑤⑥⑦ B.②⑥③⑦⑤⑥
C.③⑤⑦⑥① D.④③⑦⑤⑥
7.配制一定物质的量浓度的氢氧化钾溶液时,导致浓度偏低的原因可能是( )
A.用敞口容器称量氢氧化钾且时间过长
B.配制前先向容量瓶中加入少量蒸馏水
C.容量瓶盛过氢氧化钾溶液,使用前未洗涤
D.溶解后快速转移到容量瓶,然后加足量蒸馏水,定容
8.配制500 mL 0.1 mol·L-1的NaCl溶液,下列说法或操作正确的是( )
A.准确称量2.9 g NaCl固体溶于500 mL蒸馏水
B.用托盘天平准确称量干燥的NaCl固体2.925 g
C.在500 mL容量瓶中溶解氯化钠固体,然后加蒸馏水至刻度线
D.准确称量2.9 g混有KCl的NaCl固体,其他操作均正确,配好后的溶液中c(Cl-)偏
低
9.在溶液的配制过程中会引起浓度偏高的是( )
A.配制500 mL 0.1 mol·L-1的硫酸铜溶液,用托盘天平称取胆矾8.0 g
B.配制NaOH溶液时,NaOH固体放在烧杯中称量时间过长
C.定容时,仰视刻度线
D.配制NaOH溶液时,将称量好的NaOH固体放入小烧杯中溶解,未经冷却立即转
移到容量瓶中并定容
10.实验室需要480mL0.2mol·L-1的氢氧化钠溶液,下列说法正确的是( )
A.用托盘天平称取3.8gNaOH固体
B.若其他操作正确,将NaOH固体放在烧杯中溶解后,立即转移至容量瓶中定容,
所得溶质物质的量浓度偏大
C.若其他操作正确,定容摇匀后,溶液凹液面最低点低于刻度线,用胶头滴管加水
至刻度线,所得溶质物质的量浓度偏大D.用0.8mol·L-112mLNaOH溶液稀释成480mL即可
能力提升
11.配制一定物质的量浓度的溶液是一个重要的定量实验,下列有关说法正确的是(
)
A.容量瓶用蒸馏水洗净后,必须干燥才能用于配制溶液
B.配制1 L 0.1 mol·L-1的NaCl溶液时,用托盘天平称量5.85 g NaCl固体
C.配制一定物质的量浓度的溶液时,定容时仰视刻度线会导致所配溶液浓度偏高
D.用浓盐酸配制稀盐酸,量取浓盐酸时仰视量筒的刻度线会导致所配溶液浓度偏高
12.为了配制100mL 1mol•L﹣1的NaOH溶液,其中有下列几个操作:①NaOH固体放
在纸上进行称量②选刚用蒸馏水洗净的100mL容量瓶进行配制③NaOH在烧杯里刚好完全
溶解,立即把溶液转移到容量瓶中④用蒸馏水洗涤烧杯内壁和玻璃棒2次,洗涤液也均转
入容量瓶中⑤使蒸馏水沿玻璃棒注入容量瓶,直到溶液的凹液面恰好与刻度线相切.其中
错误的是( )
A.①②③ B.③④⑤ C.②③⑤ D.①③⑤
13.下列目的能达到的是( )
A.将58.5 g NaCl溶于1 L水中可得1 mol·L-1的NaCl溶液
B.将标准状况下22.4 L HCl溶于1 L水中可得1 mol·L-1盐酸
C.将25.0 g胆矾(CuSO ·5H O)溶于水后配成100 mL溶液所得溶液浓度为1 mol·L-1
4 2
D.将78 g Na O 溶于水,配成1 L溶液可得到浓度为1 mol·L-1的溶液
2 2
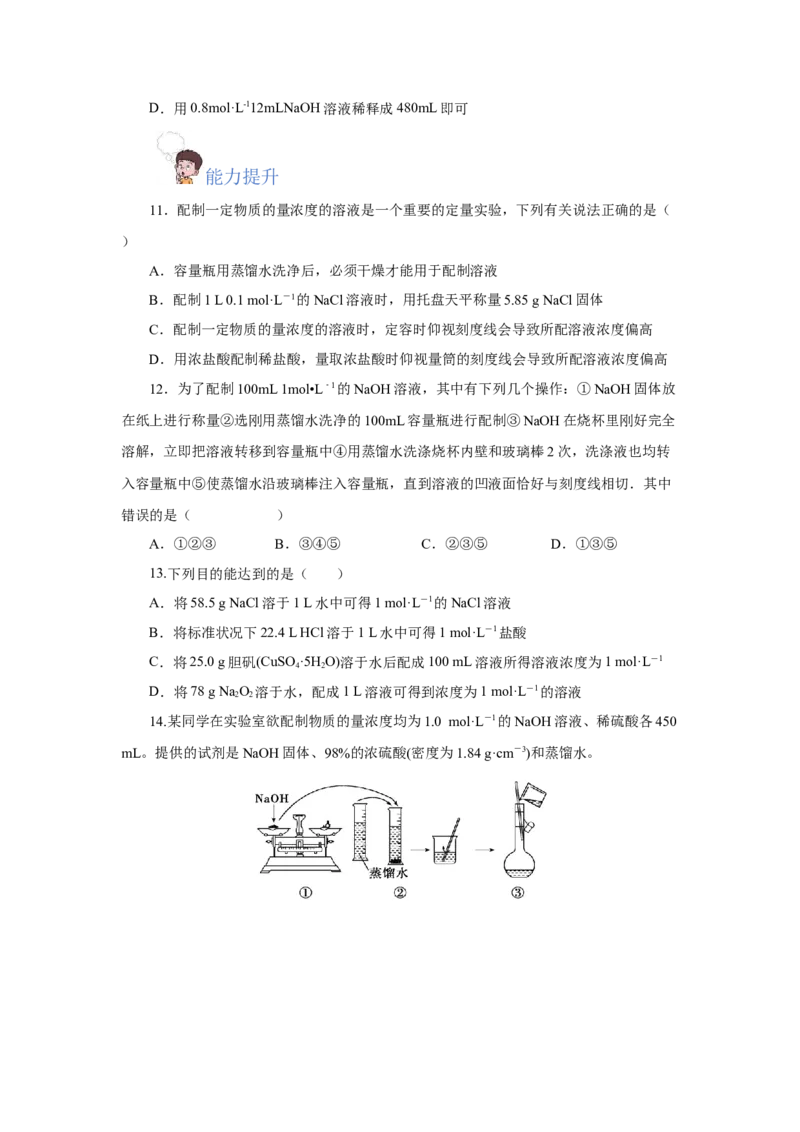
14.某同学在实验室欲配制物质的量浓度均为1.0 mol·L-1的NaOH溶液、稀硫酸各450
mL。提供的试剂是NaOH固体、98%的浓硫酸(密度为1.84 g·cm-3)和蒸馏水。(1)请你观察图示,判断其中不正确的操作有_______________(填序号)。
(2)应用托盘天平称量NaOH固体_________g,应用量筒量取浓硫酸________mL。
(3)浓硫酸用于配制稀硫酸时,需先进行稀释,稀释浓硫酸的方法是
___________________________
____________________________________________________________________________。
(4)在配制上述溶液的实验中,下列操作引起结果偏低的有_________(填字母)。
A.该学生在量取浓硫酸时,俯视刻度线
B.称量NaOH固体时,将砝码和药品的位置颠倒
C.稀释浓硫酸后没有冷却至室温就立即完成后面的配制操作
D.在烧杯中溶解搅拌时,溅出少量溶液
E.没有用蒸馏水洗涤烧杯2~3次
F.将量取浓硫酸的量筒洗涤2~3次,并全部转移至容量瓶中
G.容量瓶中原来存有少量蒸馏水
H.用胶头滴管加水定容时俯视刻度线
直击高考
15.下列有关实验原理或操作正确的是( )
A.用20 mL量筒量取15 mL酒精,加水5 mL,配制质量分数为75%酒精溶液
B.在200 mL某硫酸盐溶液中,含有1.5N 个硫酸根离子,同时含有N 个金属离子,
A A
则该硫酸盐的物质的量浓度为2.5 mol·L-1
C.实验中需用2.0 mol·L-1的NaCO 溶液950 mL,配制时应选用的容量瓶的规格和
2 3
称取NaCO 的质量分别为950 mL、201.4 g
2 3
D.实验室配制500 mL 0.2 mol·L-1的硫酸亚铁溶液,其操作是:用天平称15.2 g绿矾
(FeSO ·7H O),放入小烧杯中加水溶解,转移到500 mL容量瓶,洗涤、稀释、定容、摇匀
4 2
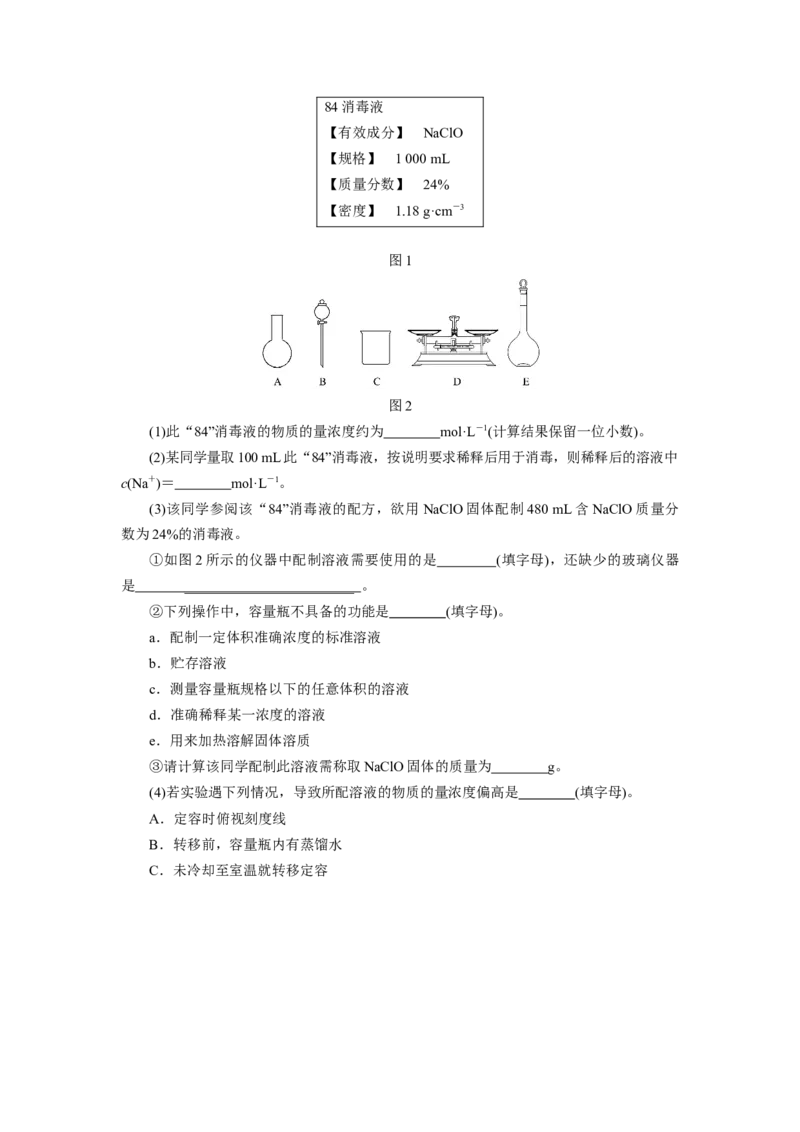
16.“84”消毒液是一种以NaClO为主的高效消毒剂,被广泛用于宾馆、旅游、医
院、食品加工行业、家庭等的卫生消毒,某“84”消毒液瓶体部分标签如图 1所示,该
“84”消毒液通常稀释100倍(体积之比)后使用,请回答下列问题:84消毒液
【有效成分】 NaClO
【规格】 1 000 mL
【质量分数】 24%
【密度】 1.18 g·cm-3
图1
图2
(1)此“84”消毒液的物质的量浓度约为 mol·L-1(计算结果保留一位小数)。
(2)某同学量取100 mL此“84”消毒液,按说明要求稀释后用于消毒,则稀释后的溶液中
c(Na+)= mol·L-1。
(3)该同学参阅该“84”消毒液的配方,欲用NaClO固体配制480 mL含NaClO质量分
数为24%的消毒液。
①如图2所示的仪器中配制溶液需要使用的是 (填字母),还缺少的玻璃仪器
是 _______________________ _ 。
②下列操作中,容量瓶不具备的功能是 (填字母)。
a.配制一定体积准确浓度的标准溶液
b.贮存溶液
c.测量容量瓶规格以下的任意体积的溶液
d.准确稀释某一浓度的溶液
e.用来加热溶解固体溶质
③请计算该同学配制此溶液需称取NaClO固体的质量为 g。
(4)若实验遇下列情况,导致所配溶液的物质的量浓度偏高是 (填字母)。
A.定容时俯视刻度线
B.转移前,容量瓶内有蒸馏水
C.未冷却至室温就转移定容