文档内容
第三节 分子结构与物质的性质
一、共价键的极性
1.键的极性和分子的极性
(1)键的极性
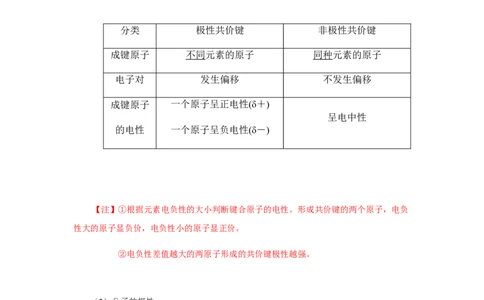
分类 极性共价键 非极性共价键
成键原子 不同元素的原子 同种元素的原子
电子对 发生偏移 不发生偏移
成键原子 一个原子呈正电性(δ+)
呈电中性
的电性 一个原子呈负电性(δ-)
【注】①根据元素电负性的大小判断键合原子的电性。形成共价键的两个原子,电负
性大的原子显负价,电负性小的原子显正价。
②电负性差值越大的两原子形成的共价键极性越强。
(2)分子的极性
分子有极性分子和非极性分子。分子的极性与分子的空间结构及分子中
键的极性有关。(3) 键的极性与分子极性之间的关系
①只含非极性键的分子一定是非极性分子(O 除外)。
3
②含有极性键的分子,如果分子中各个键的极性的向量和等于零,则为非
极性分子,否则为极性分子。
③极性分子中一定有极性键,非极性分子中不一定含有非极性键。例如
CH 是非极性分子,只含有极性键。含有非极性键的分子不一定为非极性分子
4
如H O 是含有非极性键的极性分子。
2 2
例如:
(4)分子极性的判断方法
(1)只含有非极性键的双原子分子或多原子分子大多是非极性分子。如 O 、
2
H 、P 、C 。
2 4 60
(2)含有极性键的双原子分子都是极性分子。如HCl、HF、HBr。
(3)含有极性键的多原子分子,空间结构对称的是非极性分子;空间结构不
对称的是极性分子。(4)判断AB 型分子极性的经验规律:
n
①若中心原子A的化合价的绝对值等于该元素所在的主族序数,则为非极
性分子;若不等,则为极性分子。
②若中心原子有孤电子对,则为极性分子;若无孤电子对,则为非极性分
子。
如CS 、BF 、SO 、CH 为非极性分子;H S、SO 、NH 、PCl 为极性分子。
2 3 3 4 2 2 3 3
【注】①一般情况下,单质分子为非极性分子,但O 是V形分子,其空间结构
3
不对称,故O 为极性分子。
3
②H O 的结构式为H—O—O—H,其空间结构如图所示,是不对称的,
2 2
为极性分子。
③只含极性键的分子不一定是极性分子(如CH );极性分子不一定含
4
有极性键(如CH OH);含有非极性键的分子不一定是非极性分子(如
3
H O )。
2 2
例1.下列有关分子的叙述中正确的是( )
A.以非极性键结合起来的双原子分子一定是非极性分子
B.以极性键结合起来的分子一定是极性分子
C.非极性分子只能是双原子单质分子
D.非极性分子中一定含有非极性共价键
【答案】A [对于抽象的选择题可用举反例法以具体的物质判断正误。A
项正确,如O 、H 、N 等;B项错误,以极性键结合起来的分子不一定是极性
2 2 2分子,若分子的空间结构对称,正电中心和负电中心重合,就是非极性分子,
如CH 、CO 、CCl 、CS 等;C项错误,非极性分子不一定是双原子单质分子,
4 2 4 2
如CH 等;D项错误,非极性分子中不一定含有非极性键,如CH 、CO 等
4 4 2
。]
例2.PH 又称磷化氢,在常温下是一种无色、有大蒜气味的气体,电石气
3
的杂质中常含有它。它的结构与 NH 分子结构相似。以下关于PH 的叙述中正
3 3
确的是( )
A.PH 是非极性分子
3
B.PH 分子中有未成键的电子对
3
C.PH 是一种强氧化剂
3
D.PH 分子中的P—H是非极性键
3
【答案】 B [PH 与NH 分子的结构相似,因此在P原子的最外层有一对
3 3
孤电子对未成键。P—H是由不同种原子形成的共价键,属于极性键。根据 PH
3
的分子结构可知该分子的正电中心和负电中心不重合,故分子有极性。PH 中P
3
呈-3价,具有很强的还原性。]
2.键的极性对化学性质的影响
(1)键的极性对有机酸的酸性大小的影响
羧酸的酸性可用pK 的大小来衡量,pK 越小,酸性越强。羧酸的酸性大小
a a
与其分子的组成和结构有关,如下表所示。
羧酸 pK
a
丙酸(C H COOH) 4.88
2 5
乙酸(CH COOH) 4.76
3
甲酸(HCOOH) 3.75氯乙酸(CH ClCOOH) 2.86
2
二氯乙酸(CHCl COOH) 1.29
2
三氯乙酸(CCl COOH) 0.65
3
三氟乙酸(CF COOH) 0.23
3
结论:①烃基(R—)是推电子基团,烃基越长推电子效应越大,使羧基中
的 烃 基 的 极 性 越 小 , 羧 酸 的 酸 性 越 弱 。 所 以 , 酸 性 HCOOH
>CH COOH>CH CH COOH。
3 3 2
②与羧基(—COOH)相连的C—X(X为卤素原子)的极性越大,
羧酸的酸性越大;C—X 的数量越多,羧酸的酸性越大,如酸性:
CF COOH>CCl COOH>CH COOH;CCl COOH>CHCl COOH>CH ClCOOH。
3 3 3 3 2 2
二、范德华力
1.分子间的作用力——范德华力
(1)概念:物质的分子之间存在着相互作用力,把这类分子间作用力称为范
德华力。
(2)特征:
①)范德华力广泛存在于分子之间,由分子构成的液态和固态物质,范德
华力存在于相邻的分子之间;由分子构成的气态物质,只有分子相互接近时才
存在范德华力。
②范德华力很弱,比化学键的键能小1~2个数量级。
③范德华力无方向性和饱和性。只要分子周围空间允许,分子总是尽可
能多地吸引其他分子。
(3)影响因素:
①一般来说,组成和性质相似的物质,相对分子质量越大,范德华力越大;
②相对分子质量相同或相近时,分子的极性越大,范德华力也越大。如
CO为极性分子,N 为非极性分子,范德华力:CO>N 。
2 2
③分子组成相同但结构不同的物质,分子的对称性越强,范德华力越小,
如 对二甲苯< 间二甲苯 < 邻二甲苯。
(4)范德华力对物质性质的影响
范德华力主要影响物质的熔点、沸点、溶解度等物理性质。范德华力越大,
物质的熔沸点越高。如:F 固态的密度。
(5)氢键对物质电离性质的影响:如邻苯二甲酸的电离平衡常数K 与对苯二
a1
甲酸的电离平衡常数K 相差较大。
a1四、溶解性
1.相似相溶规律
非极性溶质一般能溶于非极性溶剂,极性溶质一般能溶于极性溶剂。如蔗
糖和氨易溶于水,难溶于四氯化碳;而萘和碘却易溶于四氯化碳,难溶于水。
【注】CO、NO 等极性分子均难溶于水,不少盐类(如 AgCl、PbSO 、
4
BaSO 等)也难溶于水,H 、N 难溶于水也难溶于苯等。
4 2 2
2.影响物质溶解性的因素
(1)外界因素:主要有温度、压强等。
①温度:一般,温度越高,固体物质的溶解度越大。(Ca(OH) 、气
2
体除外)。
②压强:一般,压强越大,气体溶解度越大。
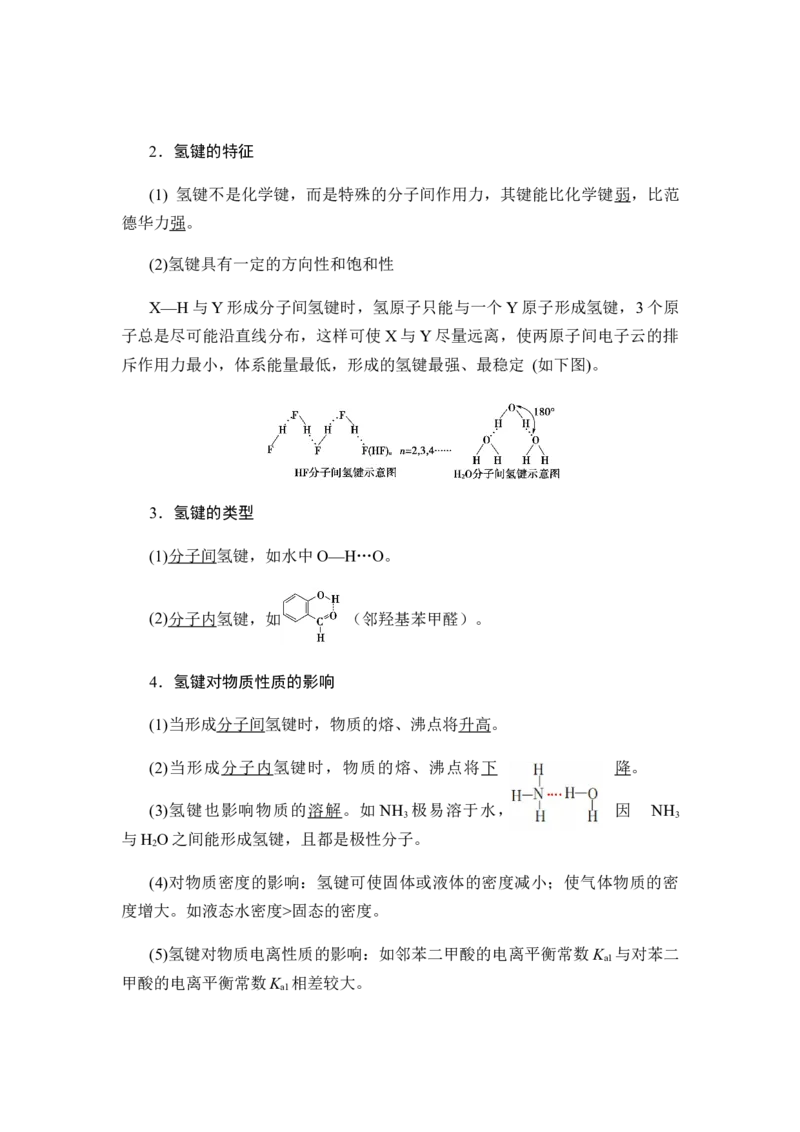
(2)氢键:溶剂和溶质之间的氢键作用力越大,溶解性越好。
(3)分子结构的相似性:溶质和溶剂的分子结构相似程度越大,其溶解性越
大。如乙醇与水互溶,而戊醇在水中的溶解度明显减小。
(4)溶质是否与水反应:溶质与水发生反应,溶质的溶解度会增大。如SO
2
与水反应生成的H SO 可溶于水,故SO 的溶解度增大。
2 3 2
五、分子的手性
1.手性异构体
具有完全相同的组成和原子排列的一对分子,如同左手与右手一样互为镜
像,却在三维空间里不能叠合,互称手性异构体(或对映异构体)。
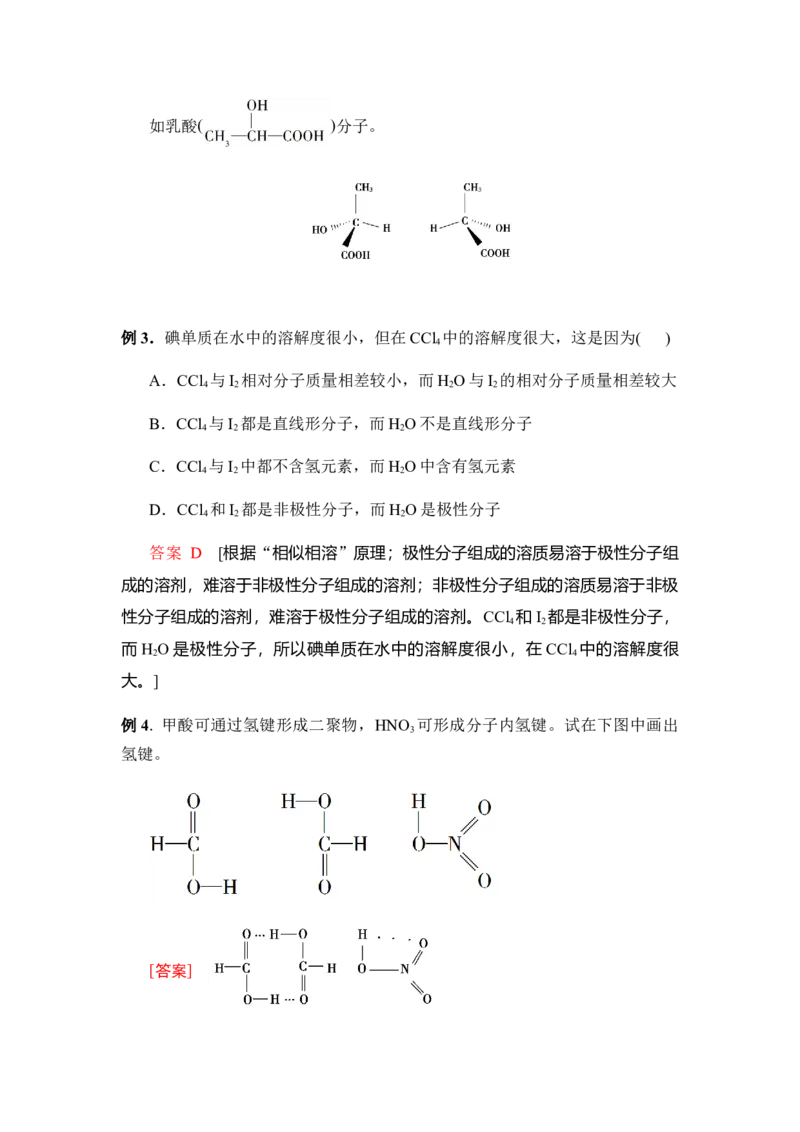
2.手性分子
有手性异构体的分子叫做手性分子。如乳酸( )分子。
例3.碘单质在水中的溶解度很小,但在CCl 中的溶解度很大,这是因为( )
4
A.CCl 与I 相对分子质量相差较小,而H O与I 的相对分子质量相差较大
4 2 2 2
B.CCl 与I 都是直线形分子,而H O不是直线形分子
4 2 2
C.CCl 与I 中都不含氢元素,而H O中含有氢元素
4 2 2
D.CCl 和I 都是非极性分子,而H O是极性分子
4 2 2
答案 D [根据“相似相溶”原理;极性分子组成的溶质易溶于极性分子组
成的溶剂,难溶于非极性分子组成的溶剂;非极性分子组成的溶质易溶于非极
性分子组成的溶剂,难溶于极性分子组成的溶剂。CCl 和I 都是非极性分子,
4 2
而H O是极性分子,所以碘单质在水中的溶解度很小,在 CCl 中的溶解度很
2 4
大。]
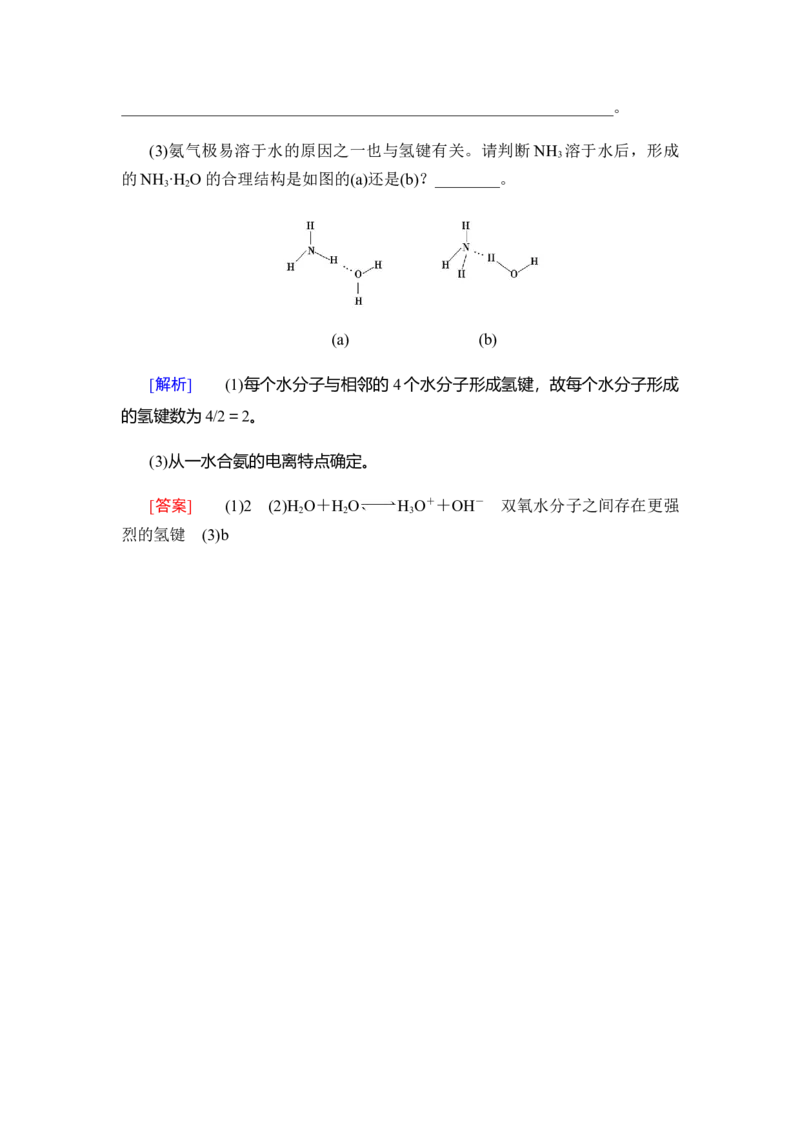
例4. 甲酸可通过氢键形成二聚物,HNO 可形成分子内氢键。试在下图中画出
3
氢键。
[答案]【总结】范德华力、氢键、化学键的比较
范德华力 氢键 共价键
已经与电负性很强的
原子形成共价键的氢 原子间通过共用电
物质分子之间普遍存
概念 原子与另一个电负性 子对所形成的相互
在的一种作用力
很强的原子之间的静 作用
电作用
作用
分子 H与N、O、F 原子
粒子
特征 无方向性和饱和性 有方向性和饱和性 有方向性和饱和性
强度 共价键>氢键>范德华力
①随分子极性的增大
成键原子半径和
而增大 对于
影响
共用电子对数
强度
②组成和结构相似的 X—H…Y,X、Y的电负
目。键长越短,
的因
分子构成的物质,相 性越大,Y原子的半径越
键能越大,共价
素
对分子质量越大,范 小,作用越强
键越稳定
德华力越大
对物 ①影响物质的熔点、 ①分子间氢键的存在,使 共价键键能越
质性 沸点、溶解度等物理 物质的熔、沸点升高,在 大,分子稳定性性质
水中的溶解度增大。如
②组成和结构相似的
熔、沸点:H O>H S
质的 2 2
物质,随相对分子质
越强
影响
量的增大,物质的 ②分子内存在氢键时,降
熔、沸点升高。如 低物质的熔、沸点
CF