文档内容
2.4 化学反应的调控
题组一 工业上合成氨
1(2021·内蒙古·包头市第四中学高二期中)工业合成氨的反应为:
,该反应在一定条件下的密闭容器中进行。下列说法正确的是
A.达到平衡时,反应速率:
B.当 、 、 的浓度比为1:3:2时,说明反应达到平衡
C.使用催化剂可同时加快正、逆反应速率,提高生产效率
D.若在密闭容器加入1 mol 和过量的 充分反应,放出热量92.4 kJ
【答案】C
【解析】A.化学平衡是动态平衡,达到平衡时,正反应速率和逆反应速率相等,但不等于0,故A错误;
B.N、H、NH 的浓度之比为1:3:2不能说明正逆反应速率相等,无法判断反应是否达到平衡,故B
2 2 3
错误;
C.合成氨反应使用催化剂,可同时加快正、逆反应速率,可提高单位时间内氨气的产率,提高生产效率,
故C正确;
D.合成氨反应是可逆反应,可逆反应不可能完全反应,则在密闭容器加入1 mol氮气和过量的氢气充分反
应,反应放出热量小于92.4 kJ,故D错误;
故选C。
2.工业上利用反应 合成氨。一定条件下,该反应体系中 的浓度随时间的变
化关系如图所示:5h后,下列有关描述中,不正确的是
A. 的浓度不再发生变化 B.正、逆反应速率均为零
C.反应处于动态平衡 D.反应达到限度
【答案】B
【解析】A.由图示可知,5h后,反应达到平衡状态,各物质浓度不变, 的浓度不再发生变化,A正
确;
B.可逆反应的平衡状态为动态平衡,平衡时正逆反应速率相等,但不等于零,B错误;
C.可逆反应的平衡状态为动态平衡,平衡时正逆反应速率相等,C正确;
D.当可逆反应达到平衡状态时,反应达到限度,D正确;
答案选B。
3.工业上利用反应 合成氨。该反应为放热反应,下列有关描述中,不正确的是
A.反应中断裂 的化学键要吸收能量 B.反应中形成 的化学键要释放能量
C.反应物的总能量比生成物的高 D.化合反应都是放热反应
【答案】D
【解析】A.旧键断裂吸收能量,则反应中断裂 的化学键要吸收能量,A正确;
B.新键形成释放能量,反应中形成 的化学键要释放能量,B正确;
C.该反应为放热反应,则反应物的总能量比生成物的高,C正确;
D.化合反应不一定是放热反应,如CO 和C的化合反应,是吸热反应,D错误;
2
故选:D。
4.工业合成氨反应为: ,该反应若在密闭容器中进行,下列有关说法正确的是
A.减压可以提高NH 产量
3
B.使用催化剂可加快反应速率
C.升高温度可以实现N 的完全转化
2
D.平衡时NH 的物质的量是N 的两倍
3 2
【答案】B
【解析】A.减小压强,平衡向气体系数和增大的方向移动,减小压强 平衡逆向移动,所以减压可以降低NH 产量,故A错误;
3
B.催化剂能降低反应活化能,提高反应速率,使用催化剂可加快 反应速率,故
B正确;
C. 是可逆反应,可逆反应中反应物不可能完全转化为生成物,故C错误;
D. 平衡时各物质浓度不变,但NH 的物质的量不一定是N 的两倍,故D错误;
3 2
选B。
5.(2022·云南·昆明一中高二期末)合成氨反应为:N(g)+3H(g) 2NH (g) H=-92.4kJ·mol-1。下
2 2 3
△
列说法正确的是
A.合成氨反应在任何温度下都能自发
B.1molN 与过量H 充分反应放热92.4kJ
2 2
C.合成氨实际生产中选择高压和低温
D.将氨液化分离,可促进平衡正移及循环利用氮气和氢气
【答案】D
【解析】A.合成氨时放热且熵减的反应,根据∆G=∆H-T∆S<0能自发可知,该反应低温下能自发,A错
误;
B.该反应为可逆反应,不能完全进行,因此1molN 与过量H 充分反应放热小于92.4kJ,B错误;
2 2
C.为了加快反应速率,实际生产中选择高压(10-20MPa)和高温(400℃-500℃),C错误;
D.氨气易液化,液化分离后生成物减少,平衡正向移动,没有液化的H 和N 可以继续放入反应器中反应,
2 2
循环利用,D正确;
故选D。
6.完成下列问题。
(1)工业合成氨的反应为 。设在容积为2.0L的密闭容器中充入0.60mol
和1.60mol ,反应在一定条件下达到平衡时, 的物质的量分数( 的物质的量与反应体系中总
的物质的量之比)为 ,试计算:①该条件下 平衡转化率为_______, 的物质的量分数为_______(小数点后保留一位)。
②该条件下 的平衡转化率_______(小数点后保留一位)。
③该条件下反应 的平衡常数为_______。
(2)已知:H—H键的键能为 ,H—N键的键能为 , 键的键能为 ,
则 与 反应生成 的热化学方程式为_______。
(3)已知 。蒸发1mol 需要吸收的能量为44kJ,
其他相关数据如下表所示:
1mol分子中的化学键断裂时需
a b z d
要吸收的能量/kJ
表中z的大小用x、a、b、d表示为_______。
(4)常温常压下,1.5g火箭燃料二甲基肼( )完全燃烧放出50kJ热量,则二甲基肼的燃
烧热为_______。
【答案】(1) 75% 28.6% 66.7% 0.005
(2)
(3)
(4)
【解析】(1)由三段式可知: 达到平衡时, 的物质的量分数(
的物质的量与反应体系中总的物质的量之比)为 ,则 ,x=0.4mol;①该条件下 平衡转化率为 , 的物质的量分数为 。②该条件下
的平衡转化率 。③反应后氮气、氢气、氨气的物质的浓度分别为
、 、 ,则该条件下反应
的平衡常数为 ,反应 的平
衡常数为 ;
(2)反应焓变=反应物键能总和-生成物键能总和;则 与 反应生成 的热化学方程式:
;
(3)蒸发1mol 需要吸收的能量为44kJ,则蒸发6mol 需要吸收的能量为264kJ,反应焓变=
反应物键能总和-生成物键能总和;则-x+264=4a+5b-4z-6d,z= ;
(4)燃烧热是在101 kPa时,1 mol物质完全燃烧生成稳定的氧化物时所放出的热量;1.5g
的物质的量为 ,则1mol 完全燃烧放出
。
7.某学习小组在实验室用 和 模拟工业合成氨。某温度下,在容积恒定为2.0L的密闭容器中充入
和 ,一段时间后反应达到平衡状态。
(1)已知在该条件下, 与 反应生成 ,每转移 电子放出 的热量,则该反应的热化学方
程式为_______。
(2)一定条件下,能说明该反应达到平衡状态的是_______(填标号)。A. 的物质的量不再改变 B.反应停止进行
C. 、 和 的反应速率之比为1∶3∶2 D.混合气体总压强不再改变
(3)反应过程中的实验数据如下表所示:
0 1 2 4 6
0 0.24 0.36 0.40 0.40
① 内用 表示的平均反应速率为_______。
②平衡时 的物质的量浓度为_______。
【答案】(1)
(2)AD
(3)
【解析】(1) 与 反应生成 ,每转移 电子生成1molNH ,即生成1mol NH 放出 的
3 3
热量,则该反应的热化学方程式为 。
(2)A.反应达到平衡状态,各物质浓度不再改变, 的物质的量不再改变,说明反应达到平衡状态,
故选A; B.反应达到平衡状态,正逆反应速率相等但不等于0,反应没有停止,故B错误;C.任意
时刻,反应速率比等于系数比, 、 和 的反应速率之比为1∶3∶2,反应不一定平衡,故不选
C;D.反应前后气体总物质的量不同,容器体积不变,压强是变量,混合气体总压强不再改变,反应一定
达到平衡状态,故选D;选AD。
(3)① 内生成0.4molNH ,则消耗0.2molN,用 表示的平均反应速率为
3 2
。②平衡时生成0.4molNH ,则消耗0.6molH, 的物质的量浓度为
3 2
。
8.氮及其化合物在生产、生活中有着重要作用。请回答下列问题:(1)工业合成氨的反应N(g)+3H(g) 2NH (g)是一个可逆反应,反应条件是高温、高压,并且需要合适
2 2 3
的催化剂。已知断裂1mol相应化学键需要的能量如下:
化学
H-H N-H N≡N
键
能量 436kJ 391kJ 946kJ
若反应生成lmolNH (g),可_______(填“吸收”或“放出”)热量_______kJ;实验室模拟工业合成氨时,
3
在容积为2L的密闭容器内,反应经过10分钟后,生成10mol氨气,则用氮气表示的化学反应速率是
_______mol·L-1·min-1。
(2)汽车尾气中含有的NO是造成城市空气污染的主要因素之一,通过NO传感器可监测汽车尾气中NO含
量,其工作原理如图所示:
NiO电极为_______(填“正极”或“负极”)。Pt电极上发生的电极反应式为_______。当电路中有1mol电
子发生转移时,消耗NO的体积为_______L(标准状况下)。
(3)一种新型催化剂能使NO和CO发生反应2CO+2NO N+2CO 。为验证温度和催化剂的比表面积对
2 2
化学反应速率的影响规律,某同学设计了如下三组实验。
实验编
T(°C) NO初始浓度(mol/L) CO初始浓度(mol/L) 催化剂的比表面积(m2/g)
号
I 280 1.20×10-3 5.80×10-3 82
II 280 1.20×10-3 b 124
III 350 a 5.80×10-3 82
①a=_______。
②能验证温度对化学反应速率影响规律的实验是_______(填实验编号)。
③恒温恒容条件下,不能说明该反应已达到平衡状态的是_______(填序号)。
a.容器内的压强保持不变
b.容器内各气体的物质的量之比为2:2:1:2c.v (CO)=v (NO)
逆 2 正
d.容器内混合气体密度不再改变
【答案】(1) 放出 46 0.25
(2) 负极 11.2
(3) 1.20×10-3 I、III bd
【解析】(1)焓变=反应物总键能-生成物总键能,N(g)+3H(g) 2NH (g)
2 2 3
,则生成1molNH 放出46KJ的能量;在容积为2L的密闭容器内,反
3
应经过10分钟后,生成10mol氨气,则反应消耗5molN ,则用氮气表示的化学反应速率是
2
mol·L-1·min-1。
(2)根据图示,NiO电极NO生成NO ,N元素化合价升高,发生氧化反应,NiO电极为负极。氧气在Pt
2
电极得电子生成氧离子,电极反应式为 。负极反应为 ,当电路中有1mol
电子发生转移时,消耗0.5molNO,标准状况下的体积为11.2L。
(3)①验证温度和催化剂的比表面积对化学反应速率的影响规律,根据控制变量法,反应物浓度必须相
等,所以a=1.20×10-3。②根据“控制变量法”,能验证温度对化学反应速率影响规律的实验,只能温度是
变量,所以I、III是能验证温度对化学反应速率影响规律。③a.反应前后气体系数和不同,压强是变量,
容器内的压强保持不变,反应一定达到平衡状态,故a不符题意;B.反应达到平衡状态,各物质浓度不
变,容器内各气体的物质的量之比为2:2:1:2,不能判断是否发生改变,反应不一定平衡,故b符合题
意;C.反应达到平衡状态,正逆反应速率比等于系数比,v (CO)=v (NO)一定达到平衡状态,故c不符
逆 2 正
题意;D.反应前后气体总质量不变、容器体积不变,密度是恒量,若容器内混合气体密度不再改变,反
应不一定达到平衡状态,故d符合题意;选bd。
9.(2022·辽宁·营口市第二高级中学)合成氨生产技术的创立开辟了人工固氮的途径,对化学工业技术也
产生了重大影响。合成氨工业中原料气N 可以从空气中分离得到,H 可用甲烷或焦炭与水蒸气反应制得。
2 2
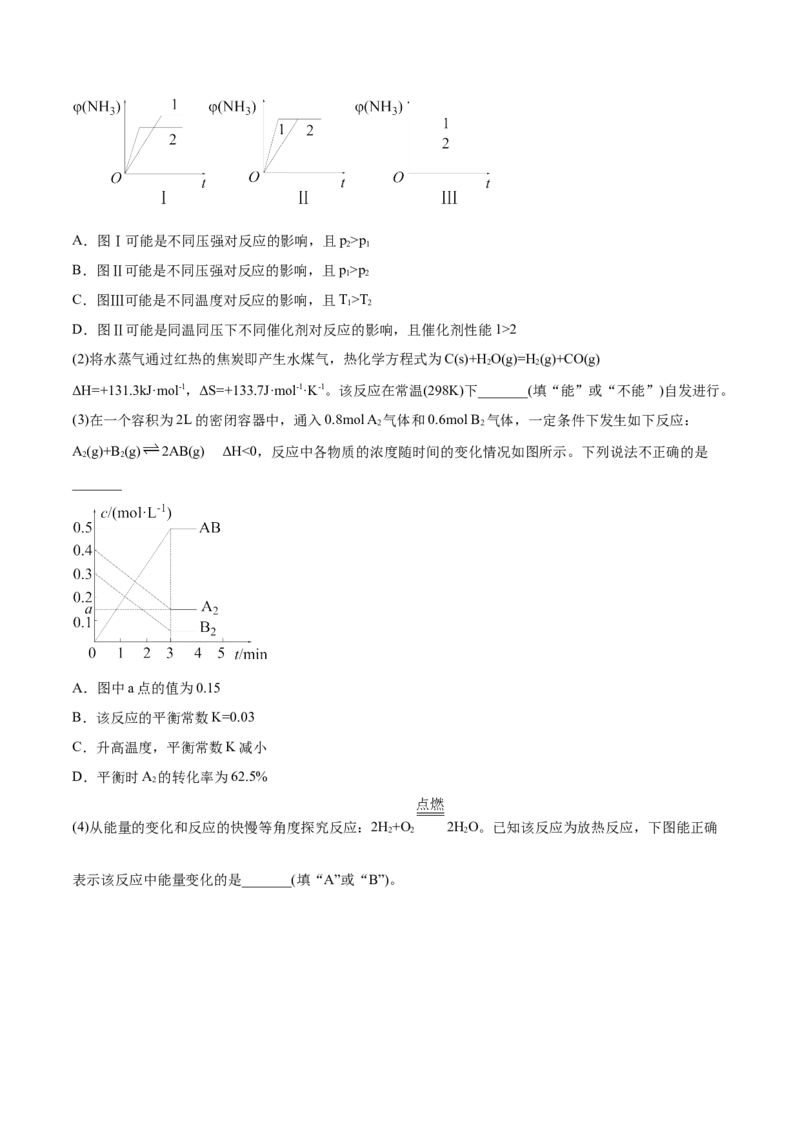
(1)在三个相同容器中各充入1mol N 和3mol H,在不同条件下反应达到平衡,氨的体积分数随时间变化的
2 2
曲线如图所示。下列说法中正确的是_______(填字母)。A.图Ⅰ可能是不同压强对反应的影响,且p>p
2 1
B.图Ⅱ可能是不同压强对反应的影响,且p>p
1 2
C.图Ⅲ可能是不同温度对反应的影响,且T>T
1 2
D.图Ⅱ可能是同温同压下不同催化剂对反应的影响,且催化剂性能1>2
(2)将水蒸气通过红热的焦炭即产生水煤气,热化学方程式为C(s)+HO(g)=H (g)+CO(g)
2 2
ΔH=+131.3kJ·mol-1,ΔS=+133.7J·mol-1·K-1。该反应在常温(298K)下_______(填“能”或“不能”)自发进行。
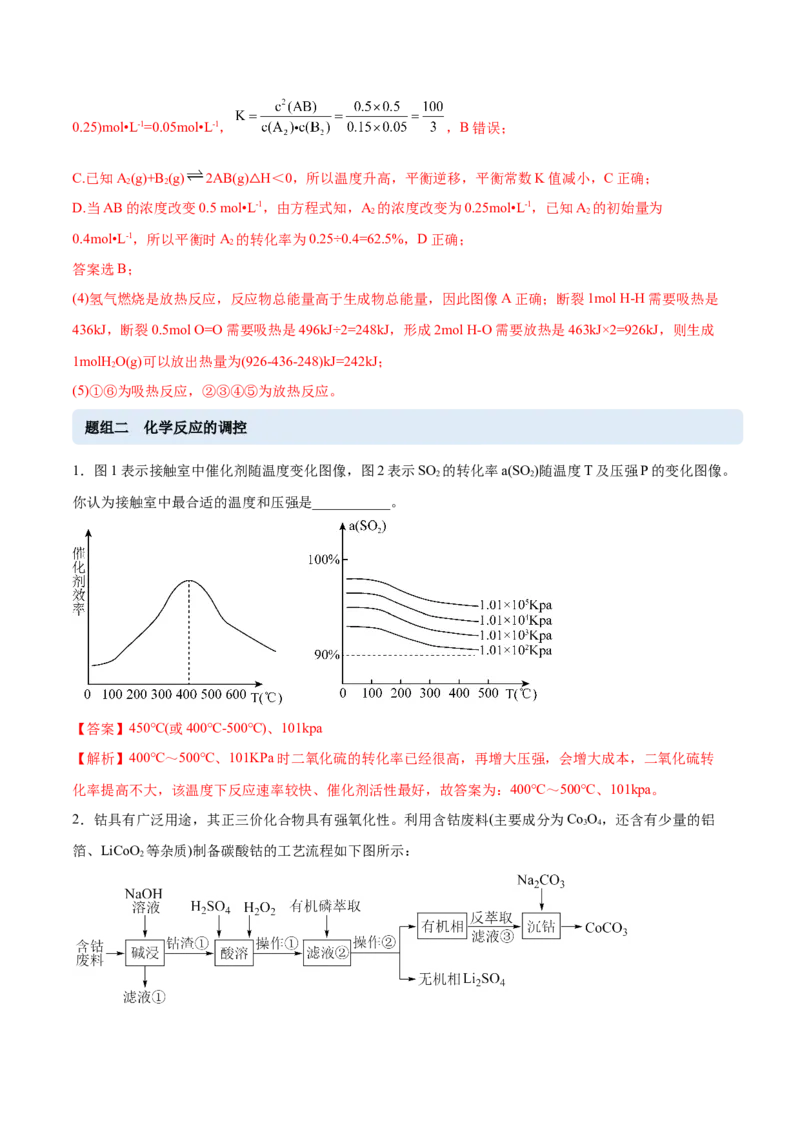
(3)在一个容积为2L的密闭容器中,通入0.8mol A 气体和0.6mol B 气体,一定条件下发生如下反应:
2 2
A(g)+B (g) 2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示。下列说法不正确的是
2 2
_______
A.图中a点的值为0.15
B.该反应的平衡常数K=0.03
C.升高温度,平衡常数K减小
D.平衡时A 的转化率为62.5%
2
(4)从能量的变化和反应的快慢等角度探究反应:2H+O 2HO。已知该反应为放热反应,下图能正确
2 2 2
表示该反应中能量变化的是_______(填“A”或“B”)。从断键和成键的角度分析上述反应中能量的变化。化学键的键能如下表:
化学键 H—H O=O H-O
键能/(kJ·mol-1) 436 496 463
则生成1mol水可以放出热量_______kJ。
(5)以下反应:①木炭与水制备水煤气;②氯酸钾分解;③炸药爆炸;④酸与碱的中和反应;⑤生石灰与水
作用制熟石灰;⑥Ba(OH) ·8H O与NH Cl反应。其中属于放热反应的有_______(填序号)。
2 2 4
【答案】(1)D
(2)不能
(3)B
(4) A 242
(5)②③④⑤
【解析】(1)A.根据先拐先平数值大知压强:p>p,增大压强平衡正向移动导致氨气体积分数增大,图像
2 1
不符合,故A错误;
B.根据先拐先平数值大知压强:p>p,增大压强平衡正向移动导致氨气体积分数增大,图像不符合,故B
1 2
错误;
C.根据先拐先平数值大知温度:T>T,升高温度平衡逆向进行,氨气体积分数减小,图像不符合,故C
1 2
错误;
D.催化剂只改变化学反应速率不影响平衡移动,所以只改变反应达到平衡时间不改变氨气体积分数,图像
符合,故D正确;
答案选D;
(2)如果△G= H-T S<0,反应能自发进行,该反应在常温(298K)下△G= H-T S=131.3kJ/
mol-298×133△.7J/mo△l=91457.4J/mol>0,不能自发进行; △ △
(3)A.当AB的浓度改变0.5 mol•L-1,由方程式知,A 的浓度改变为0.25mol•L-1,所以a=(0.4-
2
0.25)mol•L-1=0.15mol•L-1,即图中a点的值为0.15,A正确;
B.当AB的浓度改变0.5 mol•L-1,由方程式知,B 的浓度改变为0.25mol•L-1,所以平衡时B 的浓度为=(0.3-
2 20.25)mol•L-1=0.05mol•L-1, ,B错误;
C.已知A(g)+B (g) 2AB(g) H<0,所以温度升高,平衡逆移,平衡常数K值减小,C正确;
2 2
D.当AB的浓度改变0.5 mol•L△-1,由方程式知,A
2
的浓度改变为0.25mol•L-1,已知A
2
的初始量为
0.4mol•L-1,所以平衡时A 的转化率为0.25÷0.4=62.5%,D正确;
2
答案选B;
(4)氢气燃烧是放热反应,反应物总能量高于生成物总能量,因此图像A正确;断裂1mol H-H需要吸热是
436kJ,断裂0.5mol O=O需要吸热是496kJ÷2=248kJ,形成2mol H-O需要放热是463kJ×2=926kJ,则生成
1molH O(g)可以放出热量为(926-436-248)kJ=242kJ;
2
(5)①⑥为吸热反应,②③④⑤为放热反应。
题组二 化学反应的调控
1.图1表示接触室中催化剂随温度变化图像,图2表示SO 的转化率a(SO )随温度T及压强P的变化图像。
2 2
你认为接触室中最合适的温度和压强是___________。
【答案】450℃(或400℃-500℃)、101kpa
【解析】400℃~500℃、101KPa时二氧化硫的转化率已经很高,再增大压强,会增大成本,二氧化硫转
化率提高不大,该温度下反应速率较快、催化剂活性最好,故答案为:400℃~500℃、101kpa。
2.钴具有广泛用途,其正三价化合物具有强氧化性。利用含钴废料(主要成分为Co O,还含有少量的铝
3 4
箔、LiCoO 等杂质)制备碳酸钴的工艺流程如下图所示:
2(1)“碱浸”过程中,可以加快反应速率和提高原料利用率的方法是__________(任写两点)。
(2)“滤液①”主要成分是__________;“操作②”的分离方法是__________。
(3)“酸溶”时,Co、Li元素的浸出率随温度的变化如图所示:
“酸溶”的适宜温度是__________;“酸溶”时有无色气体产生,该气体为__________;若用NaSO 代
2 2 3
替HO 则有两种硫酸盐生成,写出NaSO 在“酸溶”时发生的化学方程式:__________。
2 2 2 2 3
【答案】(1)升高温度、粉碎废料、适当增大NaOH溶液的浓度等(任写两点)
(2) NaAlO 萃取分液或分液
2
(3) 80℃或80℃左右 O 4Co O+Na SO+11H SO =12CoSO+Na SO +11H O
2 3 4 2 2 3 2 4 4 2 4 2
【解析】“碱浸”过程中,Co O 和LiCoO 不与碱反应存在于滤渣中,Al在碱性溶液中发生反应生成
3 4 2
NaAlO ,滤液①主要成分为NaAlO ,滤渣中加入硫酸和过氧化氢发生反应使滤渣溶解,过滤后加入有机
2 2
磷萃取,得到有机相和无机相,有机相反萃取后加入NaCO 沉钴,得到CoCO,以此解答。
2 3 3
(1)“碱浸”过程中可以加快反应速率和提高原料利用率的方法是升高温度、粉碎矿石、适当增加NaOH的
浓度等,故答案为:升高温度、粉碎废料或适当增大NaOH溶液的浓度等;
(2)由分析知,滤液①主要成分为NaAlO ;操作②为萃取分液或分液,故答案为:NaAlO ;萃取分液或分
2 2
液;
(3)由图可知,当温度过高时,钴元素的浸出率降低,则酸浸的适宜温度是80℃;由分析知,“酸溶”时
HO 的作用为还原剂,则产生的气体为O;若用NaSO 代替HO,根据题意知,生成CoSO 和NaSO ,
2 2 2 2 2 3 2 2 4 2 4
结合得失电子守恒、元素守恒配平的化学方程式为4Co O+Na SO+11H SO =12CoSO+Na SO +11H O,故
3 4 2 2 3 2 4 4 2 4 2
答案为:80℃;O;4Co O+Na SO+11H SO =12CoSO+Na SO +11H O。
2 3 4 2 2 3 2 4 4 2 4 2
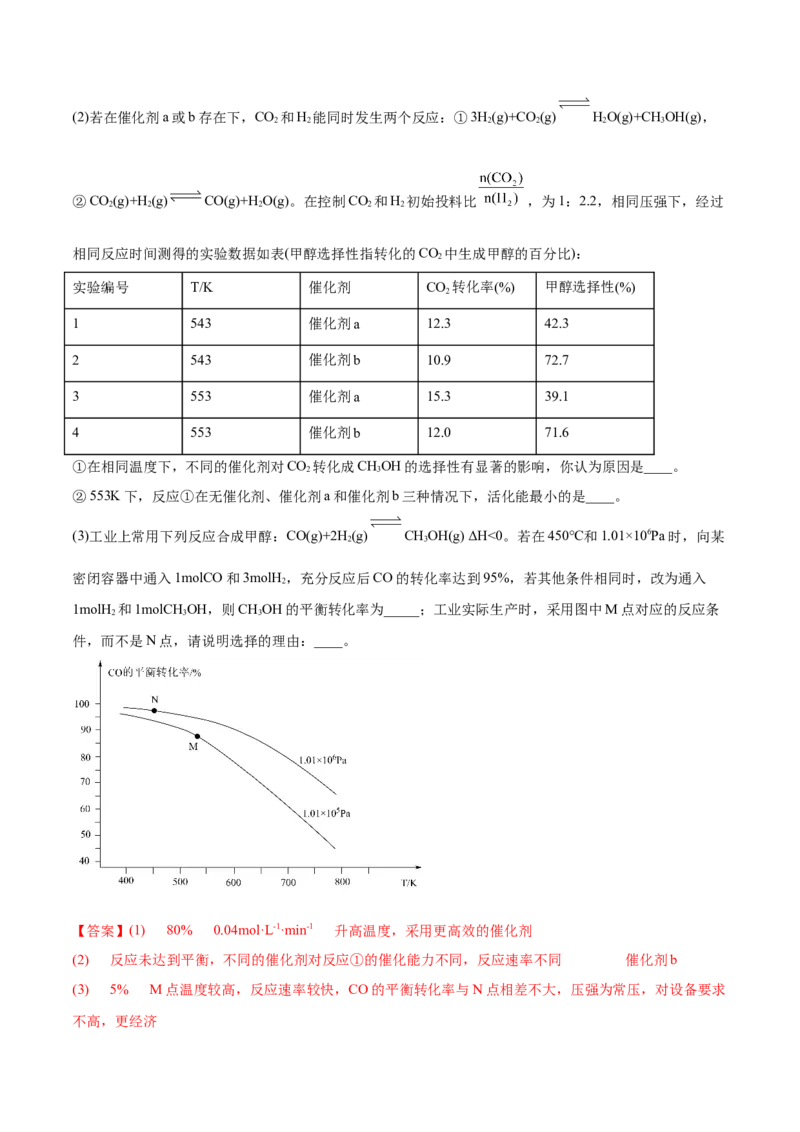
3.甲醇是一种重要的有机化工原料,在工业上有着重要的用途。
(1)二氧化碳催化加氢制甲醇反应的化学方程式为3H(g)+CO (g) HO(g)+CHOH(g)。在2L恒容密闭容
2 2 2 3
器中加入4molH 和1molCO 在一定条件下发生上述反应,10min时剩余1.6molH,此时CO 的转化率为
2 2 2 2
____,用CHOH表示10min内的化学反应速率为____,增加该反应中活化分子百分数的方法有____(答两
3
点)。(2)若在催化剂a或b存在下,CO 和H 能同时发生两个反应:①3H(g)+CO (g) HO(g)+CHOH(g),
2 2 2 2 2 3
②CO(g)+H(g) CO(g)+HO(g)。在控制CO 和H 初始投料比 ,为1:2.2,相同压强下,经过
2 2 2 2 2
相同反应时间测得的实验数据如表(甲醇选择性指转化的CO 中生成甲醇的百分比):
2
实验编号 T/K 催化剂 CO 转化率(%) 甲醇选择性(%)
2
1 543 催化剂a 12.3 42.3
2 543 催化剂b 10.9 72.7
3 553 催化剂a 15.3 39.1
4 553 催化剂b 12.0 71.6
①在相同温度下,不同的催化剂对CO 转化成CHOH的选择性有显著的影响,你认为原因是____。
2 3
②553K下,反应①在无催化剂、催化剂a和催化剂b三种情况下,活化能最小的是____。
(3)工业上常用下列反应合成甲醇:CO(g)+2H(g) CHOH(g) ΔH<0。若在450℃和1.01×106Pa时,向某
2 3
密闭容器中通入1molCO和3molH ,充分反应后CO的转化率达到95%,若其他条件相同时,改为通入
2
1molH 和1molCH OH,则CHOH的平衡转化率为_____;工业实际生产时,采用图中M点对应的反应条
2 3 3
件,而不是N点,请说明选择的理由:____。
【答案】(1) 80% 0.04mol·L-1·min-1 升高温度,采用更高效的催化剂
(2) 反应未达到平衡,不同的催化剂对反应①的催化能力不同,反应速率不同 催化剂b
(3) 5% M点温度较高,反应速率较快,CO的平衡转化率与N点相差不大,压强为常压,对设备要求
不高,更经济【解析】(1)10min时剩余1.6molH,该时间段消耗H 的物质的量为(4mol-1.6mol)=2.4mol,消耗CO 的物
2 2 2
质的量为 =0.8mol,CO 的转化率为 ×100%=80%;v(CHOH)= =0.04mol/(L·min);升
2 3
高温度和使用更高效的催化剂,均会提高活化分子的百分数,加快反应速率;故答案为80%;0.04mol/
(L·min);升高温度,使用更高效的催化剂;
(2)①从表格中数据分析,在相同的温度下,不同的催化剂,相同的反应时间内CO 的转化率不同,说明此
2
时反应未达到平衡,不同的催化剂对反应①的催化能力不同,反应速率不同,因而对甲醇的选择性有影响;
故答案为反应未达到平衡,不同的催化剂对反应①的催化能力不同,反应速率不同;
②由实验3、4可知,4中甲醇选择性高,则相同温度下,催化剂b对CO 转化成CHOH有较高的选择性,
2 3
对应的活化能最小;故答案为催化剂b;
(3)通入1molH 和1molCH OH与通入1molCO和3molH 达到的平衡为等效平衡,正向CO的平衡转化率为
2 3 2
95%,则逆向甲醇的平衡转化率为5%。相对于N点而言,M点温度在500~600K之间,温度较高,反应速
率较快,CO的平衡转化率与N点相差不大,且常压对设备和动力要求低,更经济;故答案为5%;M点温
度较高,反应速率较快,CO的平衡转化率与N点相差不大,压强为常压,对设备要求不高,更经济。
4.近年来,我国大力加强温室气体 氢化合成甲醇技术的工业化量产研究,实现可持续发展。在合适
的催化剂作用下,二氧化碳可催化加氢制甲醇。
(1)已知:①
②
则反应③ _______ 。
(2)若将物质的量之比为1∶3的 (g)和 (g)充入容积为1.0 L的恒容密闭容器中发生反应③,不同压强
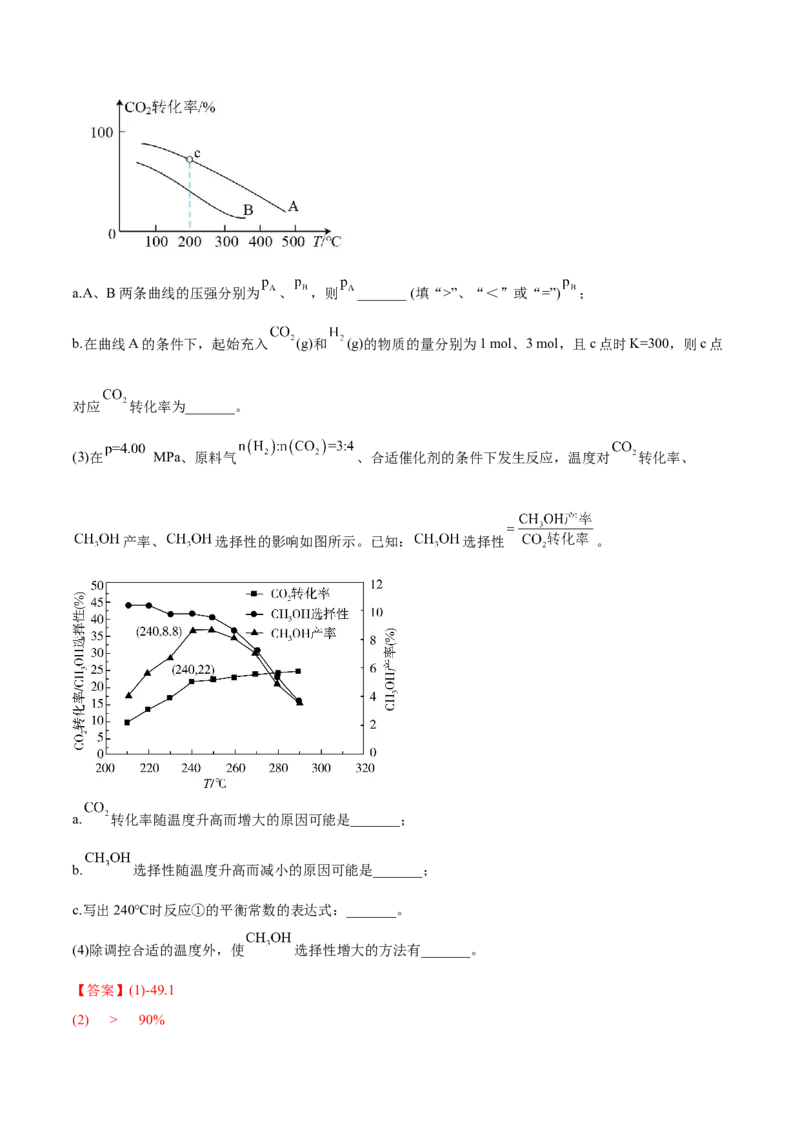
下 转化率随温度的变化关系如图所示。a.A、B两条曲线的压强分别为 、 ,则 _______ (填“>”、“<”或“=”) ;
b.在曲线A的条件下,起始充入 (g)和 (g)的物质的量分别为1 mol、3 mol,且c点时K=300,则c点
对应 转化率为_______。
(3)在 MPa、原料气 、合适催化剂的条件下发生反应,温度对 转化率、
产率、 选择性的影响如图所示。已知: 选择性 。
a. 转化率随温度升高而增大的原因可能是_______;
b. 选择性随温度升高而减小的原因可能是_______;
c.写出240℃时反应①的平衡常数的表达式:_______。
(4)除调控合适的温度外,使 选择性增大的方法有_______。
【答案】(1)-49.1
(2) > 90%(3) 反应①为吸热反应,温度升高不但能加快反应速率,而且有利于该反应正向进行 反应
②(或反应③)为放热反应,而反应①为吸热反应,所以温度升高不利于 的合成,但有利于CO的生
成,所以 产率降低
(4)增大压强或使用更高效的催化剂
【解析】(1)反应③=反应①+反应②,则ΔH=ΔH+ΔH=+41.4 kJmol−1+(-90.5kJmol−1)=-49.1kJmol−1。
3 1 2
(2)a.反应③是气体体积减小的反应,同一温度下,增大压强,⋅平衡正向移动,⋅ CO
2
转化率升⋅高,则p
A
>
p ;
B
b.在曲线A的条件下,起始充入CO(g)和H(g)的物质的量分别为1mol、3mol,则CO(g)和H(g)的起始
2 2 2 2
浓度分别为1mol/L、3mol/L,设c点时,CO 的转化浓度为x mol/L,则H、CHOH、HO的转化浓度分别
2 2 3 2
为3x mol/L、x mol/L、x mol/L,则c点时CO、H、CHOH、HO的浓度分别为(1-x)mol/L、(3-3x)mol/L、
2 2 3 2
x mol/L、x mol/L,K= =300,则 =300,解得x=0.9,则c点对
应CO 转化率为 =90%。
2
(3)a.反应①为吸热反应,温度升高不但能加快反应速率,而且有利于该反应正向进行,故CO 转化率随
2
温度升高而增大;
b.反应②(或反应③)为放热反应,而反应①为吸热反应,所以温度升高不利于CHOH的合成,但有利于
3
CO的生成,所以CHOH产率降低,CHOH选择性减小;
3 3
c.反应①的平衡常数的表达式为K= 。
(4)反应②(或反应③)是气体体积减小的反应,反应①是气体体积不变的反应,增大压强,反应①的平衡
不移动,反应②(或反应③)的平衡正向移动,CHOH产率增大,CHOH选择性增大;使用更高效的催
3 3
化剂,加快反应②(或反应③)的速率,使CHOH产率增大,从而使CHOH选择性增大;综上所述,除
3 3
调控合适的温度外,使CHOH选择性增大的方法有增大压强或使用更高效的催化剂。
3
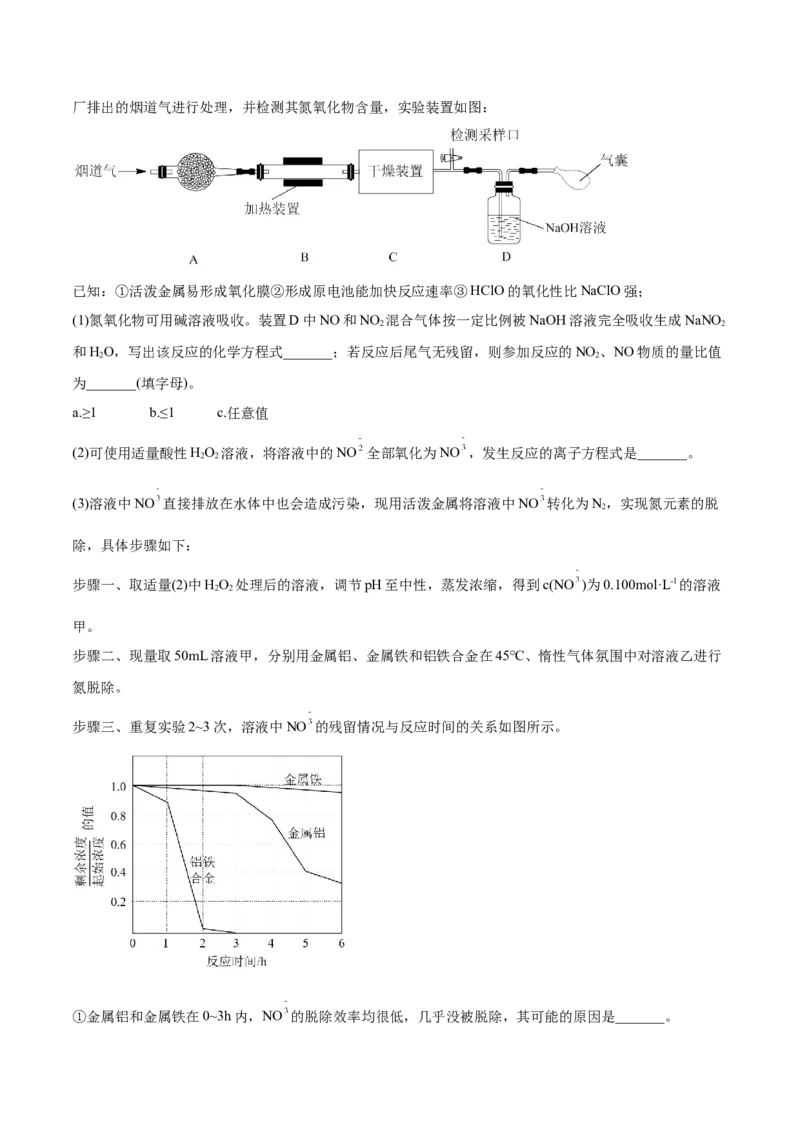
5.某处工厂排出的烟道气中含氮氧化物(主要为NO、NO )、粉尘和少量水蒸气。课外兴趣活动小组对该工
2厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图:
已知:①活泼金属易形成氧化膜②形成原电池能加快反应速率③HClO的氧化性比NaClO强;
(1)氮氧化物可用碱溶液吸收。装置D中NO和NO 混合气体按一定比例被NaOH溶液完全吸收生成NaNO
2 2
和HO,写出该反应的化学方程式_______;若反应后尾气无残留,则参加反应的NO 、NO物质的量比值
2 2
为_______(填字母)。
a.≥1 b.≤1 c.任意值
(2)可使用适量酸性HO 溶液,将溶液中的NO 全部氧化为NO ,发生反应的离子方程式是_______。
2 2
(3)溶液中NO 直接排放在水体中也会造成污染,现用活泼金属将溶液中NO 转化为N,实现氮元素的脱
2
除,具体步骤如下:
步骤一、取适量(2)中HO 处理后的溶液,调节pH至中性,蒸发浓缩,得到c(NO )为0.100mol·L-1的溶液
2 2
甲。
步骤二、现量取50mL溶液甲,分别用金属铝、金属铁和铝铁合金在45℃、惰性气体氛围中对溶液乙进行
氮脱除。
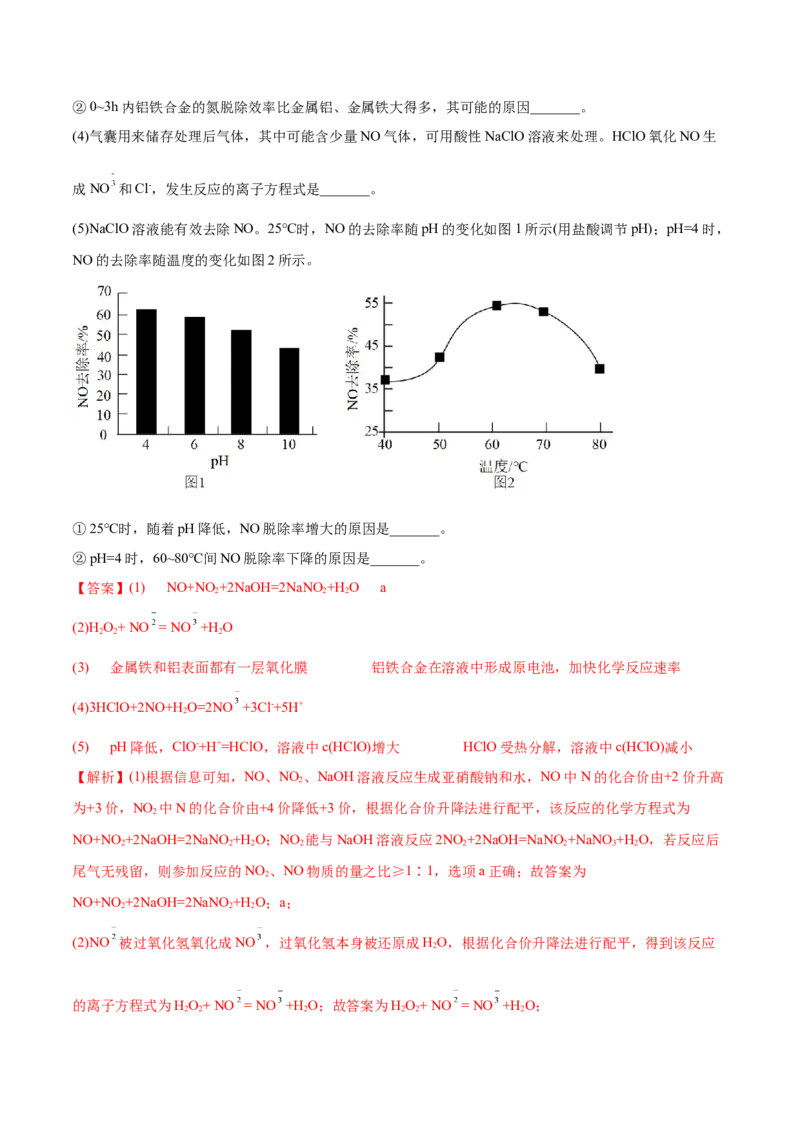
步骤三、重复实验2~3次,溶液中NO 的残留情况与反应时间的关系如图所示。
①金属铝和金属铁在0~3h内,NO 的脱除效率均很低,几乎没被脱除,其可能的原因是_______。②0~3h内铝铁合金的氮脱除效率比金属铝、金属铁大得多,其可能的原因_______。
(4)气囊用来储存处理后气体,其中可能含少量NO气体,可用酸性NaClO溶液来处理。HClO氧化NO生
成NO 和Cl-,发生反应的离子方程式是_______。
(5)NaClO溶液能有效去除NO。25℃时,NO的去除率随pH的变化如图1所示(用盐酸调节pH);pH=4时,
NO的去除率随温度的变化如图2所示。
①25℃时,随着pH降低,NO脱除率增大的原因是_______。
②pH=4时,60~80℃间NO脱除率下降的原因是_______。
【答案】(1) NO+NO +2NaOH=2NaNO +H O a
2 2 2
(2)H O+ NO = NO +H O
2 2 2
(3) 金属铁和铝表面都有一层氧化膜 铝铁合金在溶液中形成原电池,加快化学反应速率
(4)3HClO+2NO+H O=2NO +3Cl-+5H+
2
(5) pH降低,ClO-+H+=HClO,溶液中c(HClO)增大 HClO受热分解,溶液中c(HClO)减小
【解析】(1)根据信息可知,NO、NO 、NaOH溶液反应生成亚硝酸钠和水,NO中N的化合价由+2价升高
2
为+3价,NO 中N的化合价由+4价降低+3价,根据化合价升降法进行配平,该反应的化学方程式为
2
NO+NO +2NaOH=2NaNO +H O;NO 能与NaOH溶液反应2NO +2NaOH=NaNO +NaNO +H O,若反应后
2 2 2 2 2 2 3 2
尾气无残留,则参加反应的NO 、NO物质的量之比≥1∶1,选项a正确;故答案为
2
NO+NO +2NaOH=2NaNO +H O;a;
2 2 2
(2)NO 被过氧化氢氧化成NO ,过氧化氢本身被还原成HO,根据化合价升降法进行配平,得到该反应
2
的离子方程式为HO+ NO = NO +H O;故答案为HO+ NO = NO +H O;
2 2 2 2 2 2(3)①金属铝和金属铁在0~3h,NO 脱除效率较低,几乎没有被脱除,根据题中所给信息,活泼金属易形
成氧化膜,金属铝和金属铁表面有一层致密氧化薄膜,这层致密氧化薄膜阻碍反应的进行,故答案为金属
铁和铝表面都有一层氧化膜;
②铝铁合金中铝和铁的活动性不同,可以构成原电池,根据题中信息可知,形成原电池能加快反应速率;
故答案为铝铁合金在溶液中形成原电池,加快化学反应速率;
(4)HClO具有强氧化性,可将NO氧化成NO ,本身被还原成Cl-,N元素的化合价由+2价升高为+5价,
Cl元素化合价由+1降低为-1价,利用化合价升降法进行配平,反应的离子方程式为
3HClO+2NO+H O=2NO +3Cl-+5H+;故答案为3HClO+2NO+H O=2NO +3Cl-+5H+;
2 2
(5)①根据题中信息,HClO的氧化性比NaClO强, pH降低,即c(H+)增大,产生较多的HClO,氧化性增
强,NO的去除率增大;故答案为pH降低,ClO-+H+=HClO,溶液中c(HClO)增大;
②HClO受热易分解,温度太高,造成HClO分解,溶液中c(HClO)减小,去除率降低,故答案为HClO受
热分解,溶液中c(HClO)减小。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育