文档内容
2020-2021学年下学期期末测试卷01
高一化学·全解全析
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16
B B B B C A C B A B D B C A C B
1.B
【详解】
A.生产水泥以黏土和石灰石为主要原料,生成玻璃的原料为纯碱、石灰石和石英,均用到石灰石,故A
正确;
B.高温结构陶瓷属于新型无机非金属材料,不属于传统的硅酸盐材料,故B错误;
C.二氧化硅具有良好的光学特性,是制造光缆的主要原料,故C正确;
D.硅属于半导体材料,可以用于制造芯片,则手机芯片的主要成分是晶体硅,故D正确;
故选B。
2.B
【详解】
A.NO 排放会导致形成硝酸型酸雨,降低NO 排放可以减少硝酸型酸雨的形成,故A正确;
x x
B.由图可知,储存过程中NO被氧化为NO ,方程式为:2NO+O=2NO ,故B错误;
2 2 2
C.由图可知,还原过程中Ba(NO )→N,N元素化合价从+5价降低了0价,故消耗1mol Ba(NO ) 转移
3 2 2 3 2
的电子数为10mol,即10N ,故C正确;
A
D.根据图示储存和还原过程中,通过BaO和Ba(NO ) 的相互转化实现NO 的储存和还原,故D正确。
3 2 x
故选B。
3.B
【详解】
A.NH HCO 溶液中加入过量的NaOH溶液中铵根离子和碳酸氢根离子均反应:NH +HCO +2OH-=
4 3
NH ·HO+CO +HO,A错误;
3 2 2
B.氢氧化钠溶液中通入少量SO 生成亚硫酸钠和水:SO +2OH-=SO +HO,B正确;
2 2 2
C.浓盐酸与铁屑反应生成亚铁离子:Fe+2H+=Fe2++H↑,C错误;
2
D.FeO与稀硝酸发生氧化还原反应:3FeO+NO +10H+=NO↑+3Fe3++5HO,D错误;
2答案选B。
4.B
【分析】
和Cl 反应的产物之一为 ,S元素的化合价升高,则Cl元素的化合价降低,结合氧化还原反应
2
中的概念及规律来解答。
【详解】
A.因Cl元素的化合价降低,所以氧化剂是Cl,故A错误;
2
B. 在强酸性条件下发生反应生成能使品红褪色的物质二氧化硫,同时还有单质硫和水生成,故B
正确;
C.每生成l mol ,则转移(6-2)×l mol=4mol电子,可脱去2mol Cl,故C错误;
2
D.SO 具有还原性,可用作抗氧化剂,因此在一定范围内能用于食品加工工业,故D错误;
2
故选B。
5.C
【详解】
A.实验室用HO 分解制O,加入MnO 后,二氧化锰其催化作用,反应速率明显加快,A正确;
2 2 2 2
B.由于反应2SO +O 2SO 是可逆反应,所以SO 不能全部转化为SO ,B正确;
2 2 3 2 3
C.2SO +O 2SO 反应中,增加O 用量,提高二氧化硫的转化率,但由于是可逆反应,SO 不可能全部
2 2 3 2 2
转化为SO ,C错误;
3
D.实验室用碳酸钙和盐酸反应制CO,用碳酸钙粉末可以增大反应物的接触面积,因此比用块状碳酸钙
2
反应要快,D正确;
答案选C。
6.A
【详解】
A.反应至6 min时,生成氧气 ,消耗 HO,故反应至6 min时,
2 2
,故A错误;B.反应物浓度越大反应速率越大,随着反应进行,HO 的浓度逐渐减小,反应速率逐渐减小,即6min后
2 2
浓度减小,反应速率逐渐减慢,故B正确;
C.因为 ,0~6min产生的氧气的物质的量n(O )=0.001mol,
2
n(H O)=2n(O )=0.002mol, ,故C正确;
2 2 2
D.因为 ,0~6min产生的氧气的物质的量n(O )=0.001mol,
2
n(H O)=2n(O)=0.002mol,其分解率= ,故D正确;
2 2 2
故答案为A。
7.C
【分析】
A 极逐渐变细,说明是原电池的负极,B 极逐渐变粗,说明是原电池正极。
【详解】
A.A 是 Zn、B 是 Cu、C 为稀硫酸,则B极会产生气泡,质量不会增加,故A不符合题意;
B.A 是 Cu、B 是 Zn、C 为稀硫酸,则B质量减少,A上产生气泡,故B不符合题意;
C.A 是 Fe、B 是 Ag、C 为 AgNO 溶液,则A极质量减少,B极质量增加,故C符合题意;
3
D.A 是 Ag、B 是 Fe、C 为 AgNO 溶液,则B极质量减少,A极质量增加,故D不符合题意。
3
综上所述,答案为C。
8.B
【详解】
A.容器绝热,而反应进行过程中一定会有热量的变化,所以当温度不再变化时说明正逆反应速率相等,
反应达到平衡,A不符合题意;
B.无论是否平衡,同一方向同一时段内,用N、H、NH 表示反应速率的比均为1:3:2,所以不能说明
2 2 3
反应平衡,B符合题意;
C.该反应中反应物和生成物均为气体,则气体总质量始终不变,但反应前后气体系数之和不相等,即气
体总物质的量会变,所以未平衡时平均相对分子质量会变,当其不变时说明反应达到平衡,C不符合题意;D.有生成3molH 的同时,生成2molNH 说明正逆反应速率相等,反应达到平衡,D不符合题意;
2 3
综上所述答案为B。
9.A
【详解】
A.1molCH (g)含有4molC-H,断裂1molCH (g)吸收的热量为4×440kJ=1760kJ,但是形成氢气分子的过程
4 4
中还会放出热量,故整个甲烷的裂解反应吸收的能量小于1760kJ,故A错误;
B.由图可知,步骤①中反应物总能量小于生成物总能量,该步骤为吸热反应;步骤②、③中反应物的总
能量都大于生成物的总能量,则两个步骤均为放热反应,故B正确;
C.碳在催化剂表面沉积,能够阻碍反应物与催化剂接触,催化剂使用一段时间后失活的原因可能是碳在
催化剂表面沉积,故C正确;
D.催化剂只能改变反应的历程,不能改变反应的热效应,因此使用该催化剂反应吸收的能量不变,故D
正确;
故选A。
10.B
【详解】
A.立方烷的分子式为C H,A错误;
8 8
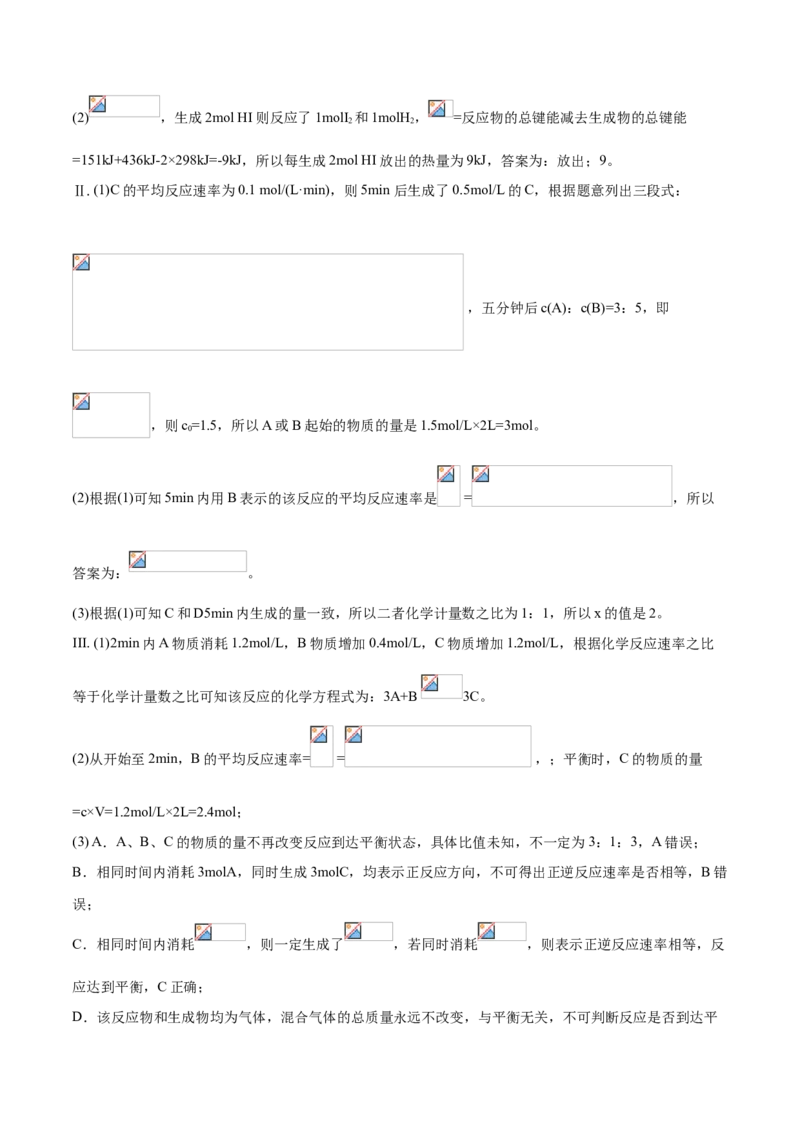
B.立方烷的所有的氢原子的化学环境相同,故立方烷的一氯代物有一种;立方烷的二氯代物有三种,如
图所示: 、 、 ;B正确;
C.1mol立方烷和Cl 发生取代反应,最多会生成8mol HCl,C错误;
2
D.立方烷不含不饱和键,不能使酸性KMnO 溶液褪色,D错误;
4
故选B。
11.D
【详解】A.只有烷烃的通式为C H ,则符合通式C H 的烃一定都是烷烃,分子中均只含单键,故A正确;
n 2n+2 n 2n+2
B.CH 为正四面体经过,正四面体的二元取代物不存在同分异构体,所以CH 的二氯代物只有一种,故B
4 4
正确;
C.烷烃的通式为C H ,含碳量越高,完全燃烧生成的二氧化碳越多,因此等质量的烷烃完全燃烧,生
n 2n+2
成CO 的量随着分子中碳的质量分数的增大而变大,故C正确;
2
D.烷烃分子结构中碳原子形成四个单键,每个碳原子形成的都是四面体结构,相邻的三个碳原子成V型,
不可能在同一条直线上,故D错误;
故选D。
12.B
【分析】
短周期元素W、X、Y、Z的原子序数依次增大,元素W是制备一种高效电池的重要材料,W是Li元素,
X的一种核素在考古时常用来鉴定一些文物的年代,X为C元素,元素Y是地壳中含量最丰富的金属元素,
Y是Al元素,Z原子的最外层电子数是其电子层数的2倍,Z是S元素。据此分析。
【详解】
A.由分析可知,化合物XZ 为CS。由CS 的结构式S=C=S可知,各原子均满足8电子的稳定结构,A
2 2 2
项正确;
B.X为C元素,Z是S元素,题中已知酸性:HSO >HCO,但HSO 不是S元素的最高价氧化物对应
2 3 2 3 2 3
的水化物,所以不能说明S的非金属性强于C,B项错误;
C.Li属于碱金属元素,和Na性质相近,常温下可以和水反应,在加热时也可以和CO 反应,所以Li着
2
火时,不能用二氧化碳灭火器扑灭,C项正确;
D.Y是Al元素,Al(OH) 能与HCl反应,故可以用于治疗胃酸过多。D项正确;
3
答案选B。
13.C
【详解】
A.发生取代反应生成的HCl溶于氯化钠溶液后,能使氯化钠的溶解度降低,故能使饱和氯化钠溶液中有
晶体析出,A错误;
B.甲烷与氯气在光照条件下发生取代反应,反应产物有一氯甲烷、二氯甲烷、三氯甲烷和四氯化碳四种
卤代烃,同时还有氯化氢生成,故甲烷和Cl 反应后的产物不止4种,B错误;
2
C. 氯气不断消耗,反应产物中二氯甲烷、三氯甲烷和四氯化碳呈液态,且不溶于水中,因此反应过程中
试管内黄绿色逐渐消失,试管壁上有油珠产生,C正确;
D. 生成的一氯甲烷及HCl为气体, HCl溶于水而一氯甲烷不溶,故此反应中气体的物质的量减少,导致液面上升,但液体不能充满整个试管, D错误;
答案选C。
14.A
【详解】
A.乙醇与金属钠反应时,反应产生CHCHONa和H,断裂醇分子中的O-H键,即化学键①断裂,A正
3 2 2
确;
B.乙醇具有还原性,可以被酸性KMnO 溶液氧化而使溶液的紫色褪色,B错误;
4
C.乙醇中含有C、H、O三种元素,属于烃的衍生物,不属于烃,C错误;
D.酯化反应实质是酸脱羟基醇脱氢,故乙醇发生酯化反应时,化学键①断裂,D错误;
故合理选项是A。
15.C
【详解】
A.减少二氧化碳向大气的排放,有利于降低大气中二氧化碳的浓度,从而减少温室效应的产生,缓解全
球变暖,延缓南北极冰川的熔化,减少极端天气发生的频率,A正确;
B.风电、光伏发电、生物质发电等行业健康有序发展,可减少含碳物质的燃烧,从而减少二氧化碳向大
气的排放,降低大气中二氧化碳的浓度,B正确;
C.农村居民燃烧农作物秸秆,会增大二氧化碳气体的排放,从而增加大气中温室气体的浓度,导致地球
的变暖,C错误;
D.大力发展电动汽车、氢燃料电池汽车等新能源汽车,可减少含碳燃料的使用,从而降低大气中二氧化
碳的浓度,D正确;
故选C。
16.B
【详解】
A.一般来说,合金熔点低于其成分金属的熔点,硬度比成分金属大,A正确;
B.人类使用最早的合金,是易于从自然界取得、性质不太活泼的金属混合物,青铜是人类使用最早的合
金,B不正确;
C.钠钾合金常温下呈液态,是原子反应堆的导热剂,C正确;
D.目前世界上使用量最大的合金是铁碳合金,D正确;
故选B。17.I.(1)HSO (2分) (2)2CaO+2SO+O 2CaSO(2分) (3)C(1分)
2 4 2 2 4
II.(1)做制冷剂、做化肥、做生产纯碱的原料、做生产硝酸的原料等(1分)
(2)2NH Cl+Ca(OH) CaCl +2NH↑+2H O(2分)
4 2 2 3 2
【详解】
I.根据转化关系分析,若A是淡黄色固体,C、D是氧化物,C是造成酸雨的主要物质,故A为单质硫,
C为SO ,硫与氢气反应生成硫化氢,硫化氢在氧气中燃烧生成二氧化硫,故B为HS;
2 2
(1)二氧化硫被氧气氧化为三氧化硫,三氧化硫与水反应生成硫酸;或二氧化硫与水反应生成亚硫酸,亚硫
酸被氧气氧化为硫酸;结合以上分析可知,酸雨的形成过程中,SO 最终转化为HSO ;
2 2 4
(2)二氧化硫与氧化钙反应生成亚硫酸钙,亚硫酸钙又被氧气氧化为硫酸钙,硫元素为+6价,为最高正价,
反应的化学方程式为:2CaO+2SO+O 2CaSO;
2 2 4
(3)二氧化硫与水反应生成亚硫酸,易被氧化为硫酸,雨水酸性增强,则由二氧化硫形成的雨水的主要成分
是硫酸,把工厂烟囱造高,在已酸化的土壤中加入石灰等措施不能从源头上有效地防止酸雨的形成,少用
煤做燃料、燃料脱硫、开发新的能源等措施可以减少二氧化硫气体的排放,从而减小酸雨的形成,故选
C;
II.根据转化关系分析,若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染,则C、D分别为
NO、NO ,B为氨气,氨气发生催化氧化生成NO,氮气与氢气在一定条件下反应生成氨气,氮气与氧气
2
放电条件下生成NO,所以A为氮气;
(1)液氨气化时从周围环境吸收热量,可以做制冷剂;氨气与酸反应生成铵盐,可以做化肥;氨气、二氧化
碳、氯化钠和水混合后生成小苏打,加热后生成苏打;氨气发生催化氧化生成一氧化氮,一氧化氮氧化为
二氧化氮,二氧化氮与水反应生成硝酸等;结合以上分析可知,氨气在生产生活中有广泛的用途,可以做
制冷剂、做化肥、做生产纯碱的原料、做生产硝酸的原料等;
(2)实验室常用氯化铵与熟石灰混合加热生成氯化钙、氨气和水,反应的化学方程式:2NH Cl+Ca(OH)
4 2
CaCl +2NH↑+2H O。
2 3 2
18.(1)除去氮气中的氧气(1分) 增大反应物接触面积,加快反应速率,提高原料利用率(1分)(2)6mol(2分)
(3)硝酸(2分)
(4)洗涤后的滤出液呈中性 (2分)
(5)abd (2分)
(6) (2分)
【分析】
净化后的N 在氮化炉中与粉碎的硅在1200~1400℃反应生成氮化硅;该方法制取的氮化硅中混有少量
2
Cu,可以用硝酸酸洗除去杂质铜,再用蒸馏水水洗、后处理得到较纯净的氮化硅,据此分析解答。
【详解】
(1)Cu能与氧气反应,可以除去氮气中含有的少量氧气;将硅块粉碎,可以增大反应物接触面积,加快反
应速率,提高原料利用率,故答案为:除去氮气中的氧气;增大反应物接触面积,加快反应速率,提高原
料利用率;
(2) 的物质的量为 =0.5mol,在氮化炉中氮气和硅反应生成氮化硅,Si由0价升高为+4
价,则生成0.5mol氮化硅转移电子的物质的量为0.5mol×3×4=6mol,故答案为:6mol;
(3) 该方法制取的氮化硅中混有少量Cu,氮化硅能与HF酸反应,盐酸、稀硫酸均不与Cu反应,氮化硅中
混有铜粉,为除去混有的Cu,可选择硝酸,Cu与硝酸反应,而氮化硅与硝酸不反应,故答案为:硝酸;
(4)氮化硅不溶于水、不溶于酸(HF酸除外),若氮化硅产品用水洗干净,则洗涤后的滤出液呈中性,故答案
为:洗涤后的滤出液呈中性;
(5)氮化硅硬度大、熔点高可以用来制作坩埚;硬度大可以用作新型结构陶瓷,但一般不用作建筑陶瓷;熔
点高、化学性质稳定可制作耐高温轴承,切削刀具等,故答案为:abd:
(6)四氯化硅和氮气在氢气的气氛保护下,加强热发生反应,可得较高纯度的氮化硅以及氯化氢。
19.(除标明外,每空1分)Ⅰ.(1)A (2)放出 9
Ⅱ.(1)3mol (2) (3)2
III.(1)3A+B 3C (2) 2.4mol(2分) (3)CE (4)BD
【详解】
Ⅰ.(1)键能越大的同类物质越稳定,HCl的键能在三者中最大,所以HCl更稳定,答案选A。(2) ,生成2mol HI则反应了1molI 和1molH , =反应物的总键能减去生成物的总键能
2 2
=151kJ+436kJ-2×298kJ=-9kJ,所以每生成2mol HI放出的热量为9kJ,答案为:放出;9。
Ⅱ.(1)C的平均反应速率为0.1 mol/(L·min),则5min 后生成了0.5mol/L的C,根据题意列出三段式:
,五分钟后c(A):c(B)=3:5,即
,则c=1.5,所以A或B起始的物质的量是1.5mol/L×2L=3mol。
0
(2)根据(1)可知5min内用B表示的该反应的平均反应速率是 = ,所以
答案为: 。
(3)根据(1)可知C和D5min内生成的量一致,所以二者化学计量数之比为1:1,所以x的值是2。
III. (1)2min内A物质消耗1.2mol/L,B物质增加0.4mol/L,C物质增加1.2mol/L,根据化学反应速率之比
等于化学计量数之比可知该反应的化学方程式为:3A+B 3C。
(2)从开始至2min,B的平均反应速率= = ,;平衡时,C的物质的量
=c×V=1.2mol/L×2L=2.4mol;
(3) A.A、B、C的物质的量不再改变反应到达平衡状态,具体比值未知,不一定为3:1:3,A错误;
B.相同时间内消耗3molA,同时生成3molC,均表示正反应方向,不可得出正逆反应速率是否相等,B错
误;
C.相同时间内消耗 ,则一定生成了 ,若同时消耗 ,则表示正逆反应速率相等,反
应达到平衡,C正确;
D.该反应物和生成物均为气体,混合气体的总质量永远不改变,与平衡无关,不可判断反应是否到达平衡,D错误;
E.B的体积分数不再发生变化,反应达到平衡,E正确;
答案选CE。
(4) A.加催化剂可能加快反应速率,A错误;
B.降低温度,反应速率减小,B正确;
C.容积不变,充入A,A物质浓度增大,反应速率加快,C错误;
D.容积不变,从容器中分离出A,A物质浓度减小,反应速率减小,D正确;
答案选BD。
方程式为3SiCl +2N +6H Si N+12HCl,故答案为:3SiCl +2N +6H Si N+12HCl。
4 2 2 3 4 4 2 2 3 4
20.(1)过滤(1分) (2)A(2分) (3)坩埚(1分)
(4) (2分)
(5)萃取(1分) 分液(1分) 乙醇和水互溶,不出现分层现象 (2分)
【详解】
(1)过滤法适合分离固体和液体,除去粗盐中难溶性杂质,实验室常用的分离操作是过滤;
(2)除去粗盐中可溶性杂质,加入氯化钡后再加碳酸钠,可以除去钙离子和钡离子,所以加入试剂的顺序是
NaOH、BaCl 、NaCO,选A;
2 2 3
(3)根据图示,仪器A名称是坩埚;
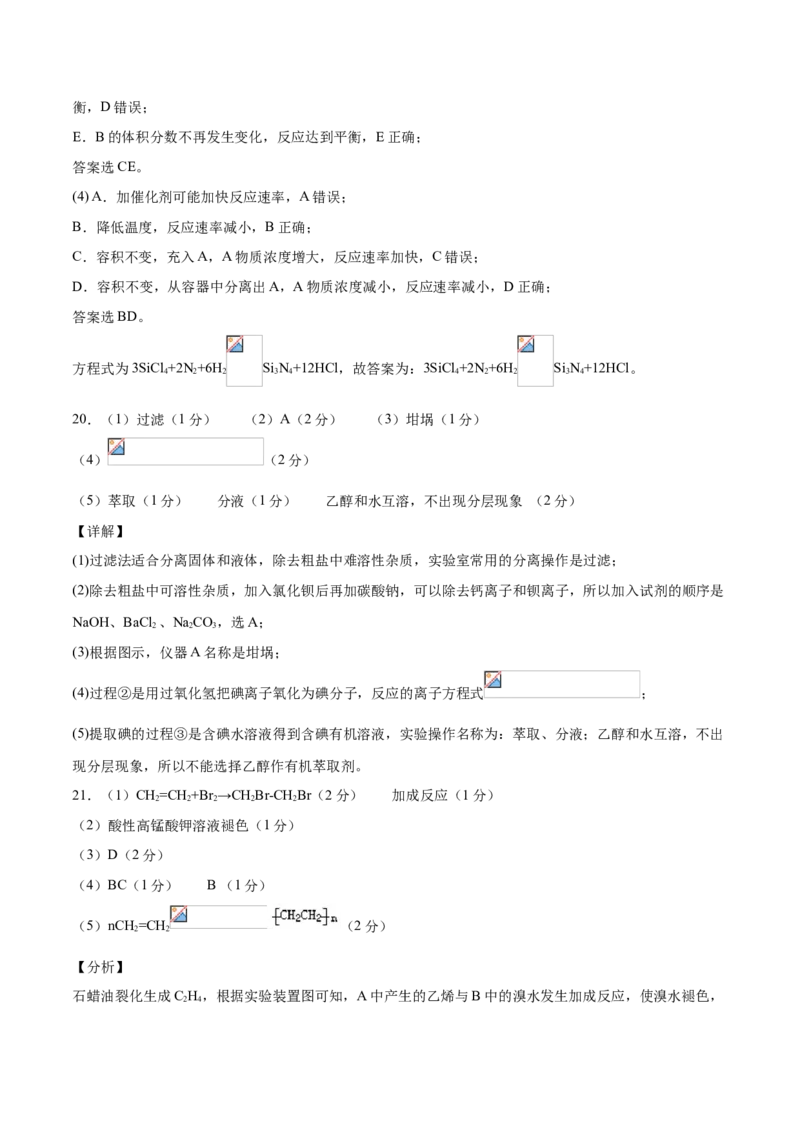
(4)过程②是用过氧化氢把碘离子氧化为碘分子,反应的离子方程式 ;
(5)提取碘的过程③是含碘水溶液得到含碘有机溶液,实验操作名称为:萃取、分液;乙醇和水互溶,不出
现分层现象,所以不能选择乙醇作有机萃取剂。
21.(1)CH=CH +Br →CHBr-CH Br(2分) 加成反应(1分)
2 2 2 2 2
(2)酸性高锰酸钾溶液褪色(1分)
(3)D(2分)
(4)BC(1分) B (1分)
(5)nCH=CH (2分)
2 2
【分析】
石蜡油裂化生成C H,根据实验装置图可知,A中产生的乙烯与B中的溴水发生加成反应,使溴水褪色,
2 4在C中乙烯被高锰酸钾溶液氧化生成二氧化碳,溶液褪色,生成的二气氧化碳在D中与澄清石灰水反应,
石灰水变浑浊,装置最后多余的乙烯可以用排水法收集,据此分析解答。
【详解】
(1)乙烯含有碳碳双键,能够与溴发生加成反应:CH=CH +Br →CHBr-CH Br,使溴水褪色,故答案为:
2 2 2 3 3
CH=CH +Br →CHBr-CH Br;加成反应;
2 2 2 3 3
(2)乙烯含有碳碳双键,能够被酸性高锰酸钾溶液氧化,使高锰酸钾溶液褪色,故答案为:酸性高锰酸钾溶
液褪色;
(3)乙烯与酸性高锰酸钾溶液反应产生二氧化碳,二氧化碳能够与氢氧化钙反应,反应的离子方程式为Ca2+
+2OH-+CO =CaCO ↓+H O,生成碳酸钙沉淀,D中装有澄清的石灰水,可根据D中的澄清石灰水变浑浊判
2 3 2
断该资料是否真实,故答案为:D。
(4)A.甲烷、乙烯不溶于水,且常温下都不与水反应,不能用于除杂和鉴别甲烷、乙烯;
B.乙烯含有C=C双键,能与溴水发生加成反应生成1,2-二溴乙烷液体,溴水褪色,甲烷与溴水不反应,
可用溴水除去甲烷中混有的乙烯,并且可用于鉴别甲烷、乙烯;
C.甲烷与酸性高锰酸钾溶液不反应,但是乙烯能够被酸性高锰酸钾溶液氧化生成二氧化碳气体,高锰酸
钾溶液褪色,可用于鉴别甲烷、乙烯,有新的杂质生成,不能用于除杂;
D.甲烷、乙烯都不溶于氢氧化钠溶液,不能用来除杂和鉴别甲烷、乙烯;
综上,检验甲烷和乙烯的方法是BC,除去甲烷中乙烯的方法是B,故答案为:BC;B;
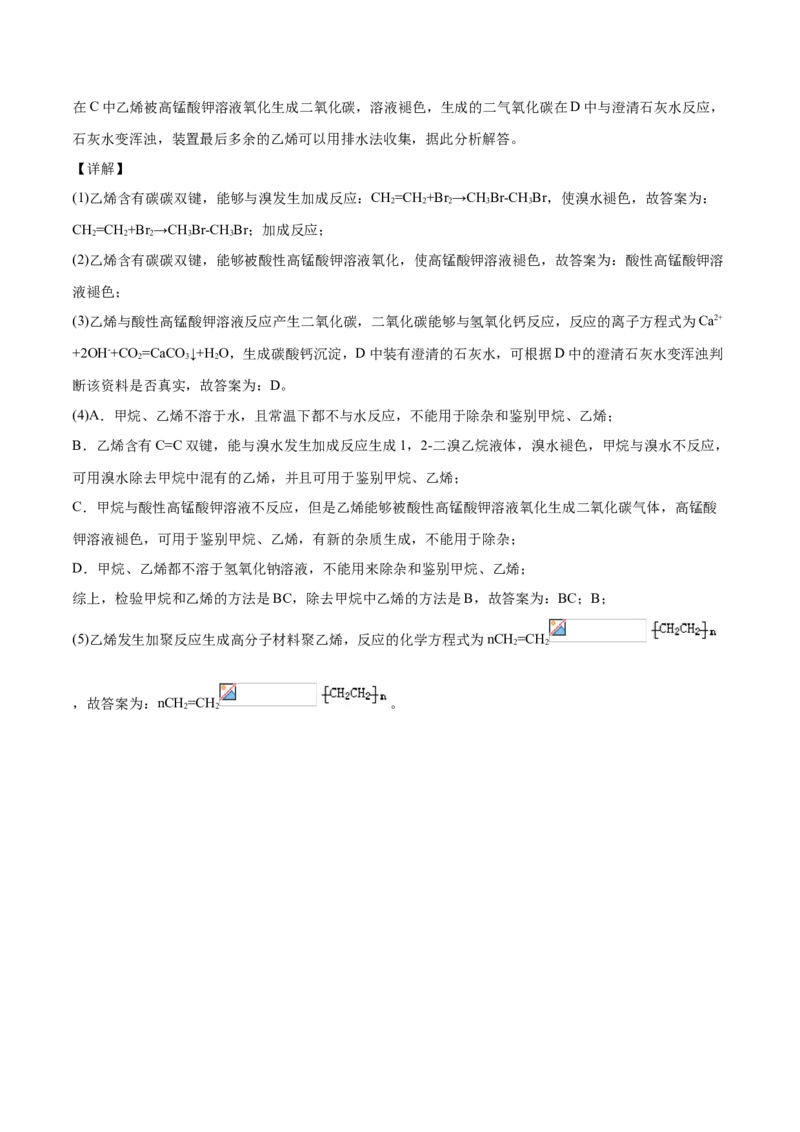
(5)乙烯发生加聚反应生成高分子材料聚乙烯,反应的化学方程式为nCH=CH
2 2
,故答案为:nCH=CH 。
2 2