文档内容
2.4 化学反应的调控
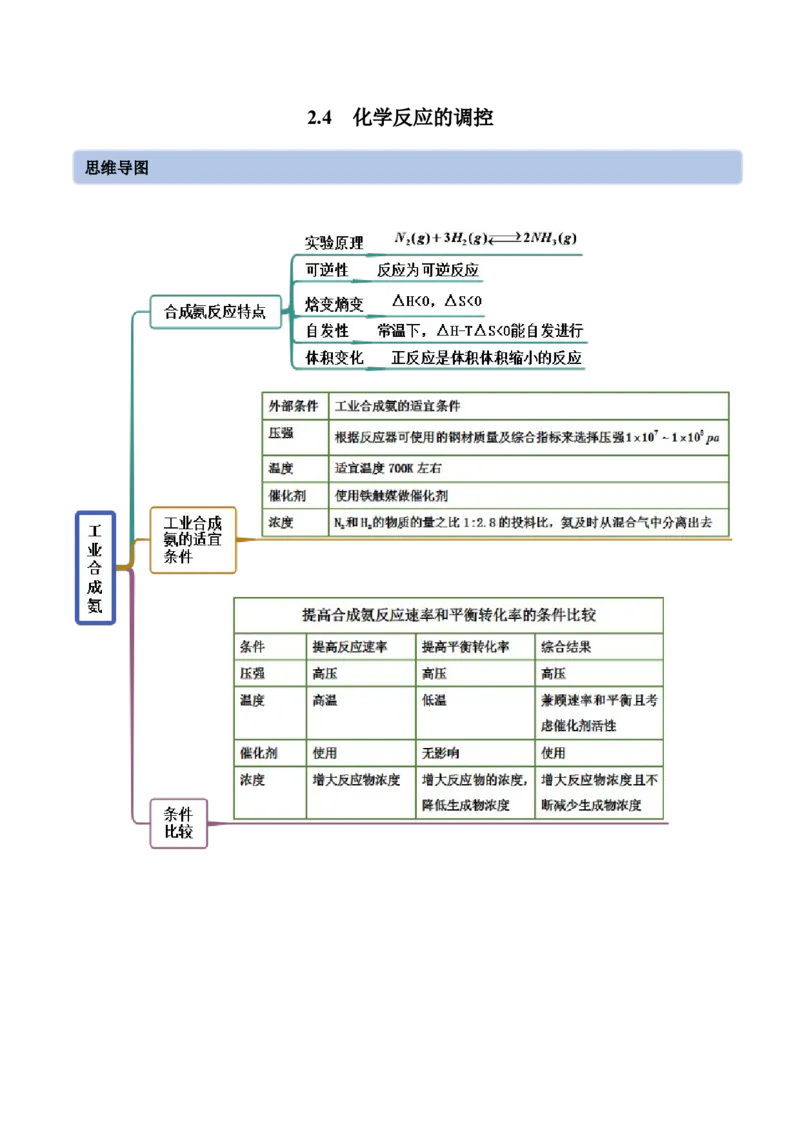
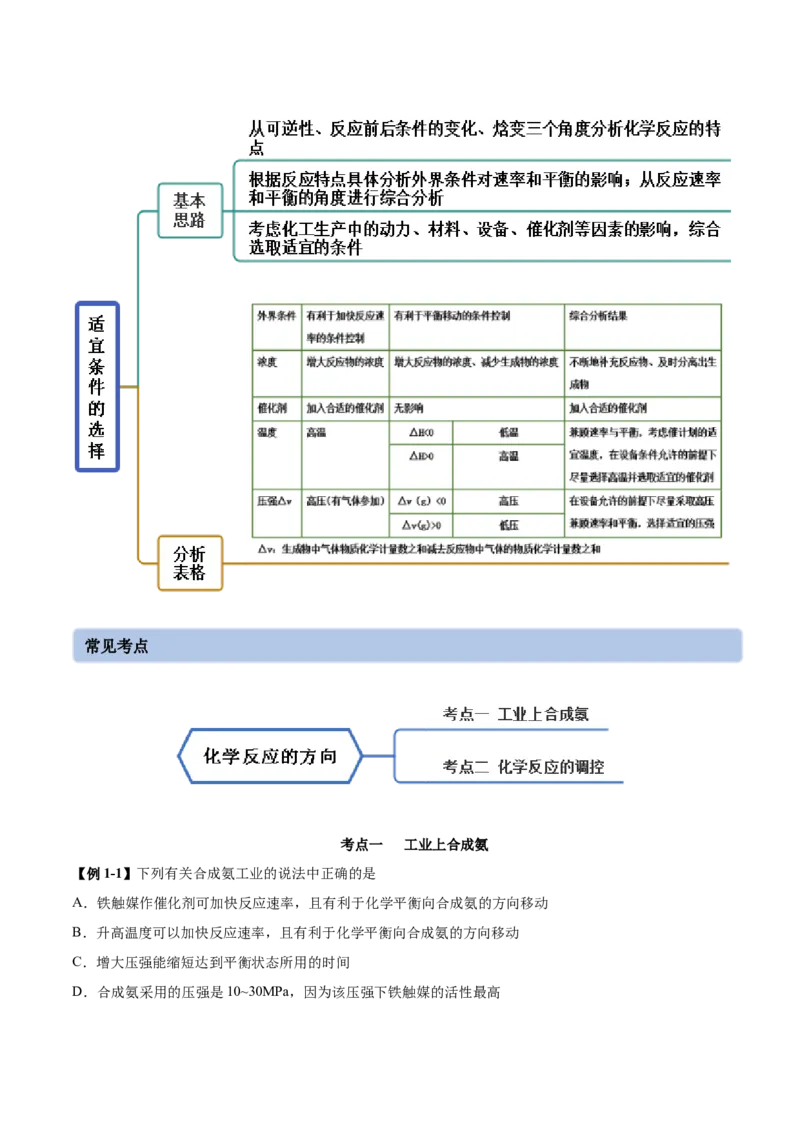
思维导图常见考点
考点一 工业上合成氨
【例1-1】下列有关合成氨工业的说法中正确的是
A.铁触媒作催化剂可加快反应速率,且有利于化学平衡向合成氨的方向移动
B.升高温度可以加快反应速率,且有利于化学平衡向合成氨的方向移动
C.增大压强能缩短达到平衡状态所用的时间
D.合成氨采用的压强是10~30MPa,因为该压强下铁触媒的活性最高【例1-2】工业合成氨是重要的人工固氮途径,它为农作物的生长提供了必需的氮元素,更为炸药、农药、
染料等的生产提供了原料。工业合成氨的化学方程式为 。恒温下,将
与 的混合气体通入一个固定容积的密闭容器中,模拟工业合成氨。回答下列问题:
(1)工业合成氨的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达
到平衡状态的是_______(填标号)。
A. B.
C. D.
(2)若反应进行到某时刻t时, , ,经过计算 _______。
(3)反应达平衡时,混合气体的体积为716.8L(标准状况下),其中 的含量(体积分数)为25%,平衡时
的物质的量为_______。
(4)原混合气体中, _______。
【一隅三反】
1.在合成氨工业中,为增加NH 的日产量,下列操作与平衡移动无关的是
3
A.不断将氨分离出来
B.使用催化剂
C.采用500℃左右的高温而不是700℃的高温
D.采用2×107~5×107Pa的压强
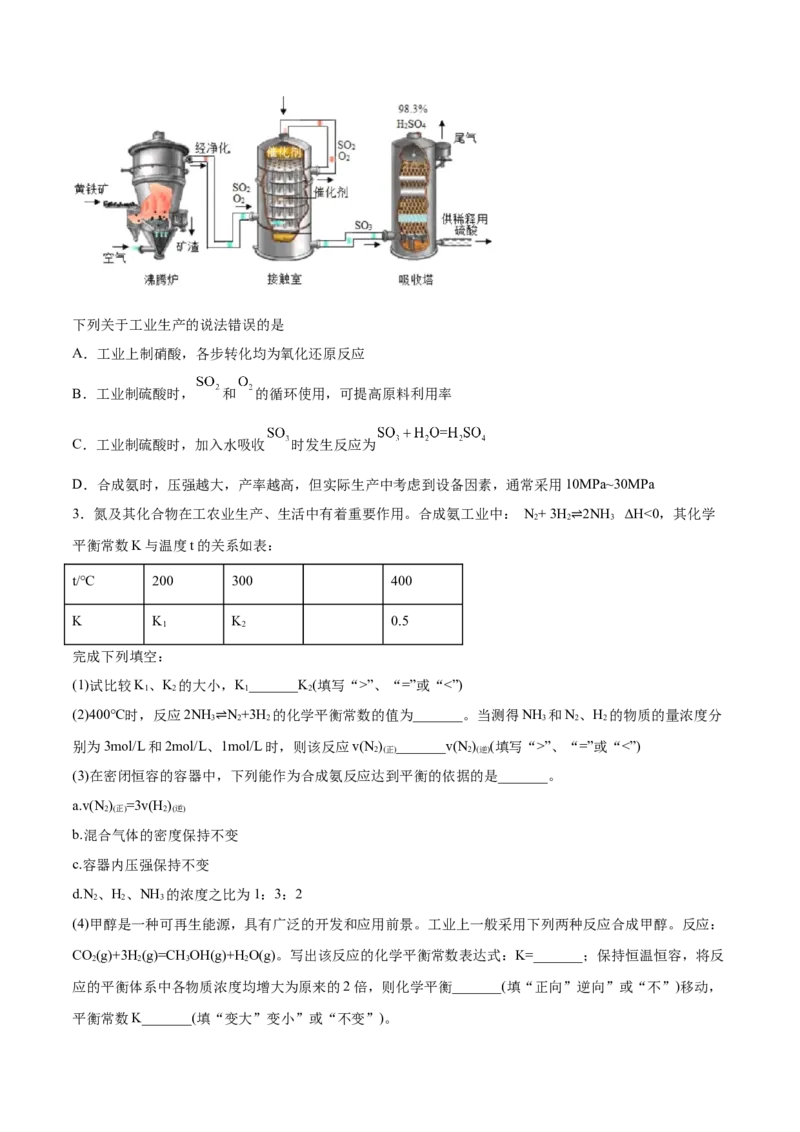
2.硫酸、硝酸工业和合成氨是重要的化学工业,如图是利用黄铁矿生产硫酸的工艺流程图。下列关于工业生产的说法错误的是
A.工业上制硝酸,各步转化均为氧化还原反应
B.工业制硫酸时, 和 的循环使用,可提高原料利用率
C.工业制硫酸时,加入水吸收 时发生反应为
D.合成氨时,压强越大,产率越高,但实际生产中考虑到设备因素,通常采用10MPa~30MPa
3.氮及其化合物在工农业生产、生活中有着重要作用。合成氨工业中: N+ 3H 2NH ΔH<0,其化学
2 2 3
平衡常数K与温度t的关系如表: ⇌
t/℃ 200 300 400
K K K 0.5
1 2
完成下列填空:
(1)试比较K、K 的大小,K_______K(填写“>”、“=”或“<”)
1 2 1 2
(2)400℃时,反应2NH N+3H 的化学平衡常数的值为_______。当测得NH 和N、H 的物质的量浓度分
3 2 2 3 2 2
别为3mol/L和2mol/L、⇌1mol/L时,则该反应v(N ) _______v(N ) (填写“>”、“=”或“<”)
2 (正) 2 (逆)
(3)在密闭恒容的容器中,下列能作为合成氨反应达到平衡的依据的是_______。
a.v(N ) =3v(H )
2 (正) 2 (逆)
b.混合气体的密度保持不变
c.容器内压强保持不变
d.N 、H、NH 的浓度之比为1:3:2
2 2 3
(4)甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列两种反应合成甲醇。反应:
CO(g)+3H(g)=CH OH(g)+H O(g)。写出该反应的化学平衡常数表达式:K=_______;保持恒温恒容,将反
2 2 3 2
应的平衡体系中各物质浓度均增大为原来的2倍,则化学平衡_______(填“正向”逆向”或“不”)移动,
平衡常数K_______(填“变大”变小”或“不变”)。考点二 化学反应的调控
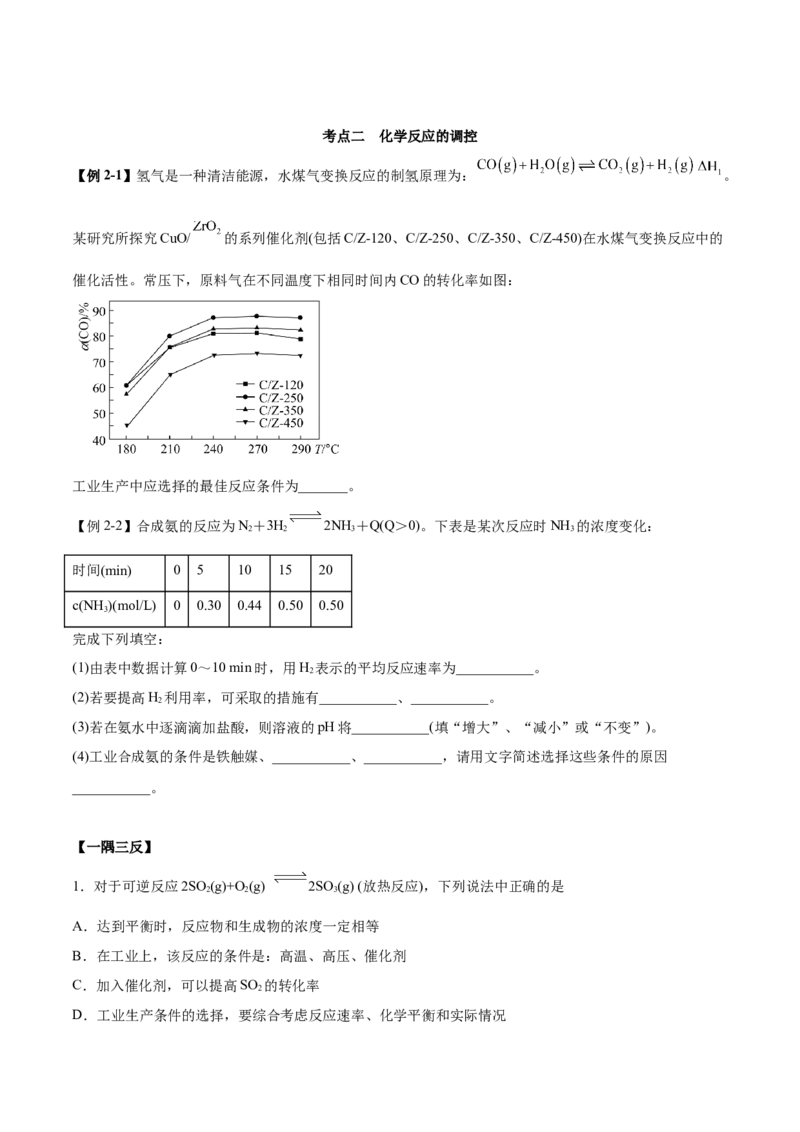
【例2-1】氢气是一种清洁能源,水煤气变换反应的制氢原理为: 。
某研究所探究CuO/ 的系列催化剂(包括C/Z-120、C/Z-250、C/Z-350、C/Z-450)在水煤气变换反应中的
催化活性。常压下,原料气在不同温度下相同时间内CO的转化率如图:
工业生产中应选择的最佳反应条件为_______。
【例2-2】合成氨的反应为N+3H 2NH +Q(Q>0)。下表是某次反应时NH 的浓度变化:
2 2 3 3
时间(min) 0 5 10 15 20
c(NH )(mol/L) 0 0.30 0.44 0.50 0.50
3
完成下列填空:
(1)由表中数据计算0~10 min时,用H 表示的平均反应速率为___________。
2
(2)若要提高H 利用率,可采取的措施有___________、___________。
2
(3)若在氨水中逐滴滴加盐酸,则溶液的pH将___________(填“增大”、“减小”或“不变”)。
(4)工业合成氨的条件是铁触媒、___________、___________,请用文字简述选择这些条件的原因
___________。
【一隅三反】
1.对于可逆反应2SO (g)+O(g) 2SO (g) (放热反应),下列说法中正确的是
2 2 3
A.达到平衡时,反应物和生成物的浓度一定相等
B.在工业上,该反应的条件是:高温、高压、催化剂
C.加入催化剂,可以提高SO 的转化率
2
D.工业生产条件的选择,要综合考虑反应速率、化学平衡和实际情况2.(2022·云南·丘北县第一中学校高二开学考试)有平衡体系:CO(g)+2H(g) CHOH(g)(正反应为放热
2 3
反应),为了增加甲醇的产量,提高生产效益,应采取的正确措施是
A.高温、高压 B.适宜的温度、高压、催化剂
C.低温、低压 D.高温、高压、催化剂
3.硫化钴铜矿主要成分有CoS、CuS、CuFeS、FeS,还含有少量Mg、Ca等元素。一种热活化硫酸浸出
2 2
工艺实现了钴和铜的高效回收利用,并较好解决了焙烧过程中二氧化硫的溢出问题。工艺流程如图所示:
回答下列问题:
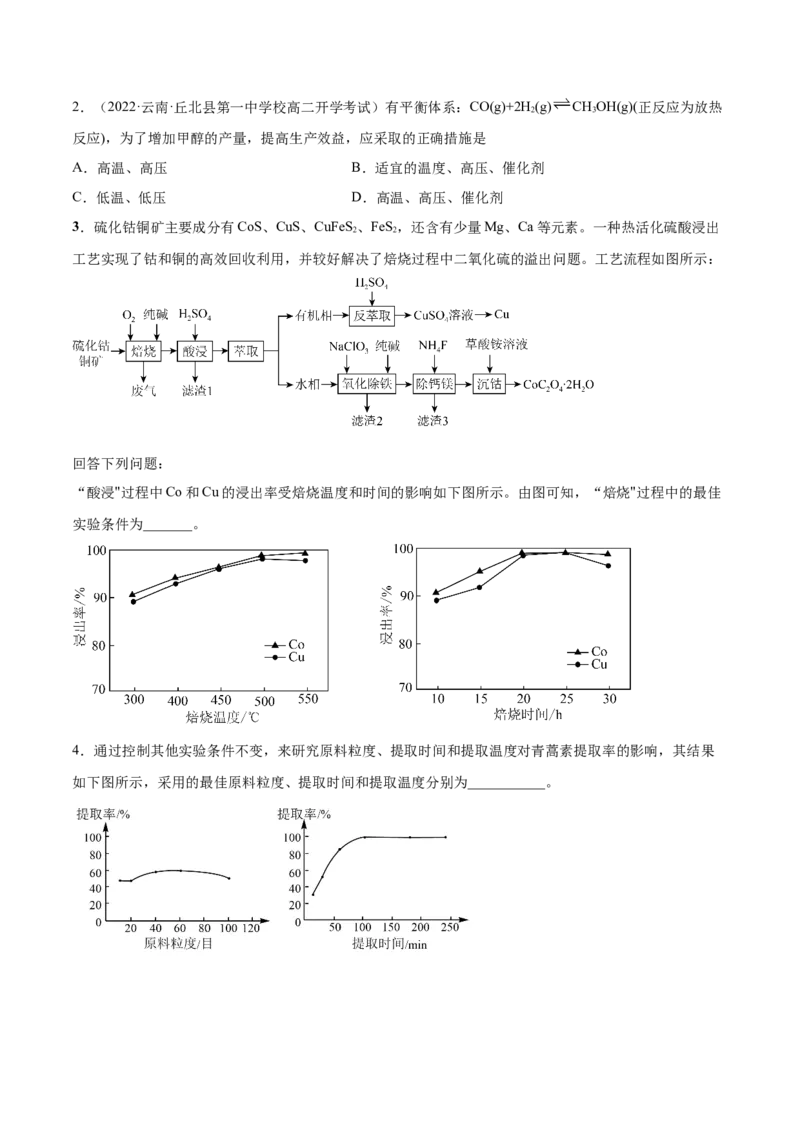
“酸浸"过程中Co和Cu的浸出率受焙烧温度和时间的影响如下图所示。由图可知,“焙烧"过程中的最佳
实验条件为_______。
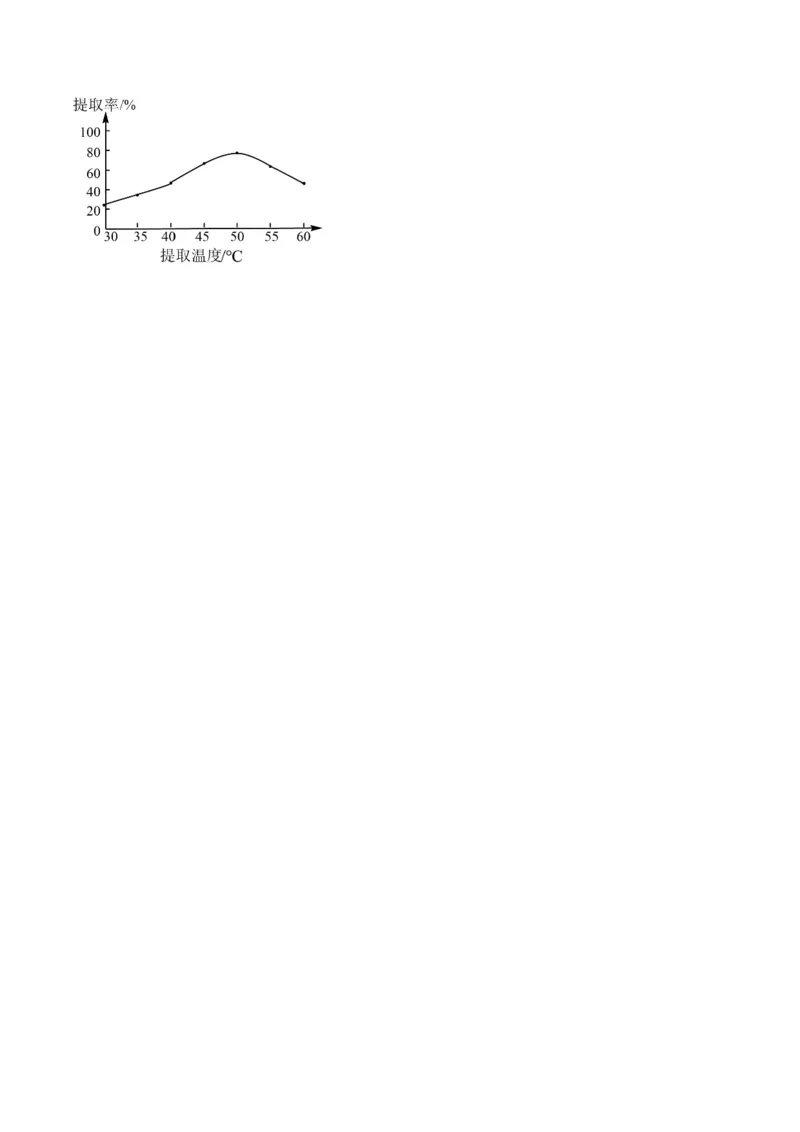
4.通过控制其他实验条件不变,来研究原料粒度、提取时间和提取温度对青蒿素提取率的影响,其结果
如下图所示,采用的最佳原料粒度、提取时间和提取温度分别为___________。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育