文档内容
单元素养评价(五)(第五章)
(90分钟 100分)
【合格性考试】(60分钟 70分)
一、选择题(本题包括14小题,每小题3分,共42分)
1.(2019·全国卷Ⅰ)陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性
质与化学有着密切的关系。下列说法错误的是 ( )
A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁
B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成
C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐
D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点
【解析】选A。氧化铁是红色的,俗称铁红,所以瓷器的青色不来自氧化铁。
2.(2019·泰州高一检测)下列物质中不能用化合反应的方法制得的是
( )
①SiO ②H SiO ③Na O ④Al(OH) ⑤FeCl
2 2 3 2 2 3 3
⑥CaSiO
3
A.①③⑤ B.②④⑥
C.②⑤ D.②④【解析】选D。①Si+O SiO ;③2Na+O Na O ;⑤2Fe+3Cl 2FeCl ;⑥CaO+SiO
2 2 2 2 2 2 3 2
CaSiO ;②无法通过化合反应来制备;④一般用铝盐和氨水反应来制备,但不属
3
于化合反应。
3.氮、氧、硫、氯是四种重要的非金属元素,下列有关说法中正确的是
( )
A.NO在加热条件下才能与空气中的氧气反应
B.氮、硫的最高价氧化物对应水化物的溶液均具有很强的氧化性
C.Cl 不与硫化钠溶液反应
2
D.四种元素的单质中化学性质最稳定的是N ,其次是硫
2
【解析】选D。NO在常温下即可与空气中的O 反应,A错误;稀硫酸的氧化性较
2
弱,B错误;Cl 与硫化钠溶液反应生成S和NaCl,C错误。
2
4.由下列实验事实得出的结论正确的是 ( )
A.由SiO 不能与水反应生成H SiO 可知,SiO 不是酸性氧化物
2 2 3 2
B.由SiO +2C Si+2CO↑,可知碳的非金属性大于硅
2
C.CO 通入Na SiO 溶液产生白色沉淀,可知酸性H CO >H SiO
2 2 3 2 3 2 3
D.SiO 可与NaOH溶液反应,也可与氢氟酸反应,可知SiO 为两性氧化物
2 2【解析】选C。SiO 是酸性氧化物,A项错误;反应SiO +2C Si+2CO↑不能说明碳
2 2
的非金属性比硅强,该反应能发生是因为生成CO气体,它的放出促进了反应进行,
B项错误;CO 通入Na SiO 溶液中生成H SiO 沉淀,符合强酸制弱酸的规律,证明
2 2 3 2 3
酸性H CO >H SiO ,C项正确;D项中SiO 除氢氟酸外不能与其他的酸反应,SiO 为
2 3 2 3 2 2
酸性氧化物,不具有两性,D项错误。
5.二氧化硫是中国允许使用的还原性漂白剂。对食品有漂白和对植物性食品内
的氧化酶有强烈的抑制作用。中国规定可用于葡萄酒和果酒,最大使用量
0.25 g·kg-1,残留量不得超过0.05 g·kg-1。
下列说法正确的是 ( )
A.因为SO 具有漂白性,所以它能使品红溶液、溴水、酸性KMnO 溶液、石蕊溶液
2 4
褪色
B.能使品红溶液褪色的不一定是SO
2
C.SO 、漂白粉、活性炭、Na O 都能使红墨水褪色,其原理相同
2 2 2
D.SO 和Cl 混合使用,将会有更强的漂白能力
2 2【解析】选B。A选项不正确,SO 使溴水、酸性KMnO 溶液褪色是因为SO 具有还原
2 4 2
性,能使品红溶液褪色是因为SO 有漂白性,SO 不能使酸碱指示剂褪色。B选项正
2 2
确,因为能使品红溶液褪色的物质很多,不仅仅是SO 。C选项不正确,因为这些漂
2
白剂的漂白原理不相同,SO 漂白属于加合型,活性炭漂白属于吸附型,漂白粉、
2
Na O 漂白属于氧化型。D选项不正确,SO 和Cl 混合会发生反应SO +Cl +2H O
2 2 2 2 2 2 2
H SO +2HCl,失去漂白能力。
2 4
【补偿训练】
(2019·南昌高一检测)下列叙述正确的是 ( )
A.H O 、SO 、氯水、过氧化钠、臭氧、活性炭都有漂白性,其原理相同
2 2 2
B.将SO 通入BaCl 溶液可生成BaSO 溶液
2 2 4
C.检验SO 中含有CO 的方法是通过澄清的石灰水
2 2
D.向含有BaCl 和NaOH的混合溶液中通入少量的CO 气体,有白色沉淀生成
2 2
【解析】选D。H O 、氯水、过氧化钠和臭氧因具有强氧化性而具有漂白性,SO 因能
2 2 2
和有色物质化合而具有漂白性,活性炭因具有吸附性而具有漂白性,A错误;SO
2
和BaCl 溶液不反应,B错误;SO 和CO 均能使澄清石灰水变浑浊,C错误。
2 2 2
6.下列关于氮及其化合物的说法错误的是 ( )A.N 化学性质稳定,是因为分子内氮氮三键很强
2
B.NO、NO 均为大气污染气体,在大气中可稳定存在
2
C.可用浓盐酸检测输送NH 的管道是否发生泄漏
3
D.HNO 具有强氧化性,可溶解铜、银等不活泼金属
3
【解析】选B。N 分子中存在氮氮三键,化学性质比较稳定,故A正确;NO、NO 均为
2 2
大气污染气体,其中NO遇氧气可以与之反应生成NO ,故B错误; 浓盐酸易挥发,
2
与氨气反应生成氯化铵,可以看到白烟,可用浓盐酸检测输送NH 的管道是否发
3
生泄漏,故C正确;HNO 具有强氧化性,可以与铜和银反应,所以可溶解铜、银等不
3
活泼金属,故D正确。
【补偿训练】
下列有关NH 的实验或结论正确的是 ( )
3
A.NH 溶于水形成的溶液呈碱性,故NH 属于一元碱
3 3
B.将湿润的红色石蕊试纸伸入集气瓶内,试纸变蓝则证明NH 已收集满
3
C.将少量浓氨水滴入装有碱石灰的烧瓶中,可快速获得NH
3
D.将NH HCO 热分解后的产物通过硅胶干燥管,可收集到干燥纯净的NH
4 3 3
【解析】选C。NH 溶于水显碱性是因为NH 与水反应生成的NH ·H O属于一元碱,
3 3 3 2
而NH 本身不是碱,A错误;检验NH 是否集满容器,应将湿润的红色石蕊试纸接近
3 3瓶口而不是伸入瓶内,B错误;NH HCO 热分解后的产物中含有NH 、H O、CO 三种成
4 3 3 2 2
分,硅胶只能吸收H O而不能除去CO ,故D错误。
2 2
7.(2019·珠海高一检测)下列说法错误的是 ( )
A.在稀硫酸中加入铜粉,铜粉不溶解,再加入Cu(NO ) 固体,铜粉就会溶解
3 2
B.某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性
C.白纸上滴加浓硫酸后变黑体现了浓硫酸的吸水性
D.HNO →NO→NO ,以上各步变化均能通过一步反应完成
3 2
【解析】选C。在稀硫酸中加入铜粉,再加入Cu(NO ) 固体,硝酸根离子在酸性环境
3 2
下具有强的氧化性,能够氧化铜,所以铜粉会溶解,故A正确;某气体能使湿润的
红色石蕊试纸变蓝,该气体的水溶液一定显碱性,故B正确;白纸上滴加浓硫酸后
变黑体现了浓硫酸的脱水性,故C错误;稀硝酸与铜反应生成一氧化氮,一氧化氮
与氧气反应生成二氧化氮,都能通过一步反应实现,故D正确。
8.(2019·聊城高一检测)下列说法正确的是 ( )
A.浓硝酸在光照条件下变黄,说明浓硝酸不稳定,生成的有色产物能溶于浓硝酸
B.在KI-淀粉溶液中通入氯气,溶液变蓝,说明氯气能与淀粉发生显色反应
C.在某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成,说明溶液中含SD.将铜片放入浓硫酸中,无明显实验现象,说明铜在冷的浓硫酸中发生钝化
【解析】选A。A项,浓硝酸光照下发生分解生成NO ,NO 溶于浓硝酸中使浓硝酸呈
2 2
黄色;B项,Cl 氧化I-生成I ,淀粉遇I 变蓝色;C项,溶液中若存在Ag+或S ,
2 2 2
也会产生相同的实验现象;D项,常温时,Cu与浓硫酸不发生反应。
9.(2019·邯郸高一检测)氯气和二氧化硫都用于物质的漂白。
将按等物质的量的SO 和Cl 混合后的气体溶解于适量的蒸馏水中,再滴入含有
2 2
品红和Ba(NO ) 的混合溶液,则实验现象是 ( )
3 2
①品红溶液很快褪色 ②品红溶液不褪色
③有白色沉淀生成 ④溶液仍然透明
A.仅①和④ B.仅①和③
C.仅②和③ D.仅②和④
【解析】选C。SO 和Cl 混合后发生反应:SO +Cl +2H O 2HCl+H SO ,所以品红溶
2 2 2 2 2 2 4
液不褪色,硫酸和Ba(NO ) 溶液生成硫酸钡沉淀。
3 2
【补偿训练】将SO 通入BaCl 溶液至饱和,未见沉淀生成,继续通入另一种气体,仍无沉
2 2
淀,则通入的气体可能是 ( )
A.CO B.NH
2 3
C.SO D.Cl
3 2
【解析】选A。NH 、SO 、Cl 分别与溶有SO 的水溶液反应生成(NH ) SO 或H SO ,再
3 3 2 2 4 2 3 2 4
与BaCl 溶液反应生成白色沉淀;而CO 不与溶有SO 的水溶液反应,也不与BaCl
2 2 2 2
溶液反应,无沉淀生成。
10.(2019·长沙高一检测)下列由相关实验现象所推出的结论正确的是
( )
A.Cl 、SO 均能使品红溶液褪色,说明二者均有氧化性
2 2
B.向溶液中滴加酸化的Ba(NO ) 溶液出现白色沉淀,说明该溶液中一定有S
3 2
C.Fe与稀HNO 、稀H SO 反应均有气泡产生,说明Fe与两种酸均发生置换反应
3 2 4
D.分别充满HCl、NH 的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水
3
【解析】选D。SO 使品红溶液褪色是由于SO 能与有色物质化合生成无色物质,不
2 2
能说明其具有氧化性,选项A错误;当溶液中含有S 时,加入酸化的Ba(NO )
3 2
溶液也会出现白色沉淀,选项B错误;Fe与稀硝酸反应生成的气体为NO,该反应不是置换反应,选项C错误;HCl、NH 极易溶于水,分别充满HCl、NH 的烧瓶倒置
3 3
于水中,气体溶解,液面迅速上升,选项D正确。
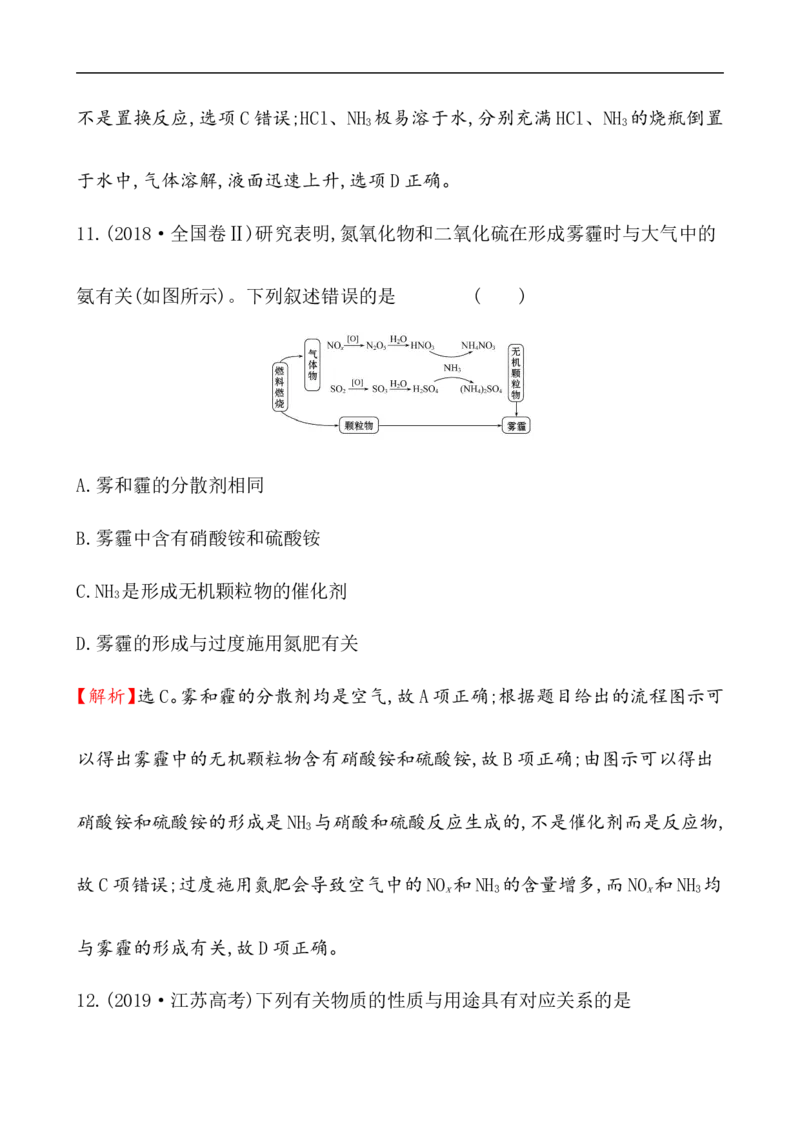
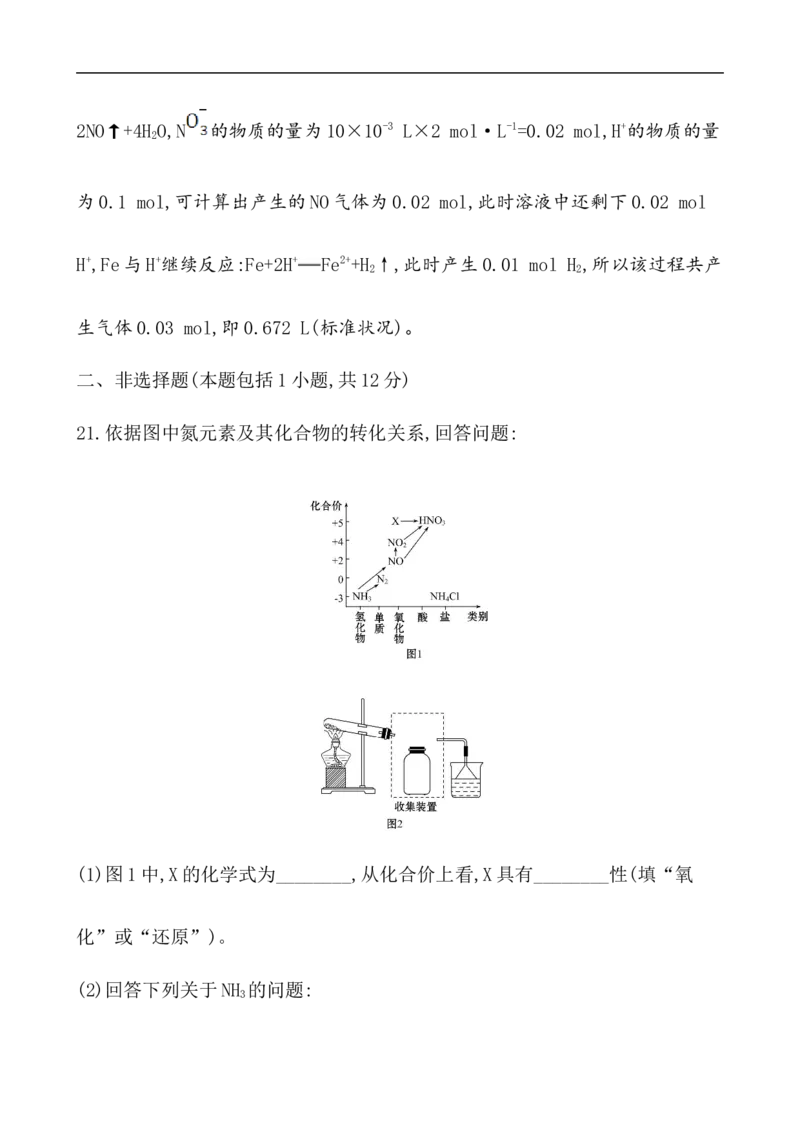
11.(2018·全国卷Ⅱ)研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的
氨有关(如图所示)。下列叙述错误的是 ( )
A.雾和霾的分散剂相同
B.雾霾中含有硝酸铵和硫酸铵
C.NH 是形成无机颗粒物的催化剂
3
D.雾霾的形成与过度施用氮肥有关
【解析】选C。雾和霾的分散剂均是空气,故A项正确;根据题目给出的流程图示可
以得出雾霾中的无机颗粒物含有硝酸铵和硫酸铵,故B项正确;由图示可以得出
硝酸铵和硫酸铵的形成是NH 与硝酸和硫酸反应生成的,不是催化剂而是反应物,
3
故C项错误;过度施用氮肥会导致空气中的NO 和NH 的含量增多,而NO 和NH 均
x 3 x 3
与雾霾的形成有关,故D项正确。
12.(2019·江苏高考)下列有关物质的性质与用途具有对应关系的是( )
A.NH HCO 受热易分解,可用作化肥
4 3
B.稀硫酸具有酸性,可用于除去铁锈
C.SO 具有氧化性,可用于纸浆漂白
2
D.Al O 具有两性,可用于电解冶炼铝
2 3
【解析】选B。A项,NH HCO 中含有氮元素,可以用作化肥,不是因为其受热分解,错
4 3
误;B项,铁锈的主要成分为Fe O ,加入稀硫酸可以除去Fe O 是运用了稀硫酸的
2 3 2 3
酸性,正确;C项,SO 漂白纸浆是运用了SO 的漂白性,不是其氧化性,错误;D项,
2 2
电解Al O 获得铝,不是因为Al O 具有两性,错误。
2 3 2 3
13.硫酸能在金星的上层大气中找到。硫酸在金星大气中较高较冷的地区为液体,
厚厚的、离星球表面约45~70公里的硫酸云层覆盖整个星球表面。大气不断地
释放出酸雨。
下列叙述正确的是 ( )A.浓硫酸是一种干燥剂,能够干燥氢气、氧气、氨气等气体,但不能干燥有较强还
原性的HI、H S等气体
2
B.浓硫酸与单质硫反应的方程式为2H SO (浓)+S 3SO ↑+2H O,在此反应中,浓
2 4 2 2
硫酸既表现了其强氧化性又表现了其酸性
C.把足量铜粉投入只含2 mol H SO 的浓硫酸中,得到气体体积标准状况下为
2 4
22.4 L
D.常温下能够用铁、铝等容器盛放浓H SO ,是因为浓H SO 的强氧化性使其钝化
2 4 2 4
【解析】选D。A项浓硫酸具有吸水性,但由于其具有强氧化性和酸性,故不能用来
干燥具有还原性的气体和碱性气体(NH )。B项金属与浓硫酸反应时,生成相应的
3
盐和SO ,此时浓硫酸显酸性和强氧化性,而与S、C等非金属单质作用时,由于没
2
有盐生成,故只显强氧化性。C项Cu与浓H SO 反应时,浓H SO 浓度逐渐降低,当
2 4 2 4
降到一定程度变为稀H SO 时,反应自行停止,故产生的SO 在标准状况下不足
2 4 2
22.4 L。
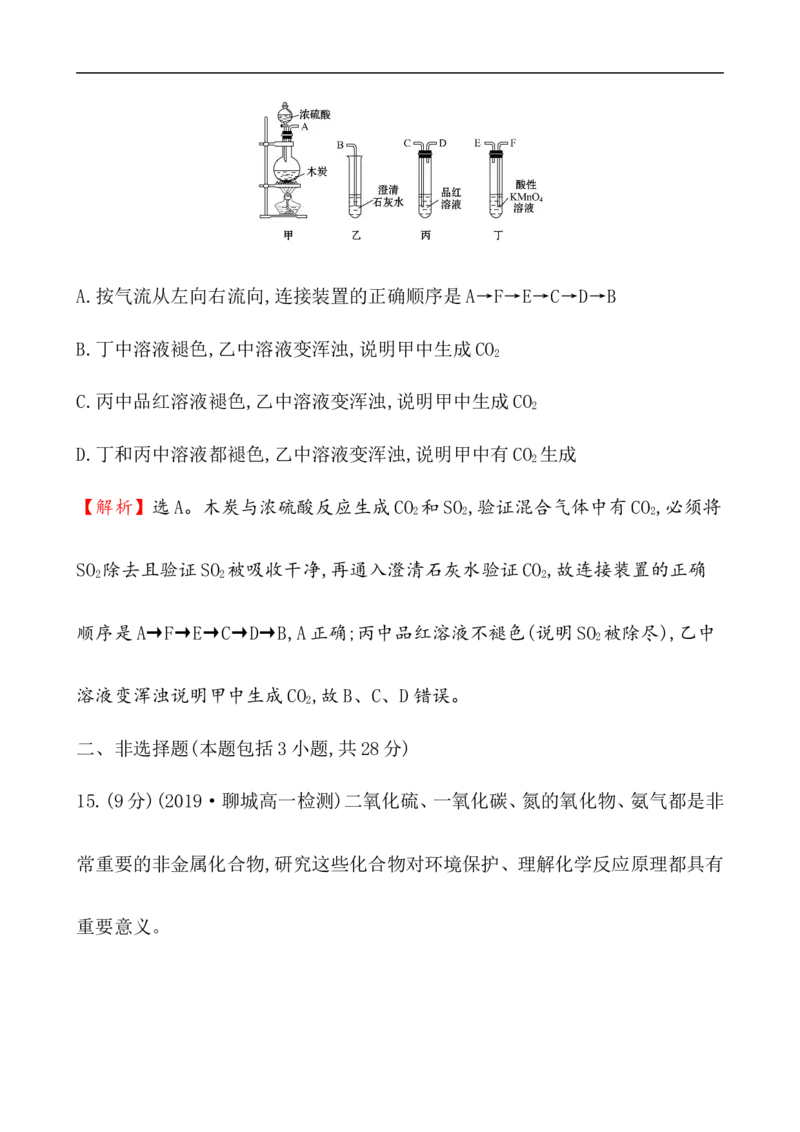
14.(2019·威海高一检测)选用如图所示仪器中的两个或几个(内含物质)组装
成实验装置,以验证木炭可被浓硫酸氧化成CO ,下列说法正确的是
2
( )A.按气流从左向右流向,连接装置的正确顺序是A→F→E→C→D→B
B.丁中溶液褪色,乙中溶液变浑浊,说明甲中生成CO
2
C.丙中品红溶液褪色,乙中溶液变浑浊,说明甲中生成CO
2
D.丁和丙中溶液都褪色,乙中溶液变浑浊,说明甲中有CO 生成
2
【解析】选A。木炭与浓硫酸反应生成CO 和SO ,验证混合气体中有CO ,必须将
2 2 2
SO 除去且验证SO 被吸收干净,再通入澄清石灰水验证CO ,故连接装置的正确
2 2 2
顺序是A→F→E→C→D→B,A正确;丙中品红溶液不褪色(说明SO 被除尽),乙中
2
溶液变浑浊说明甲中生成CO ,故B、C、D错误。
2
二、非选择题(本题包括3小题,共28分)
15.(9分)(2019·聊城高一检测)二氧化硫、一氧化碳、氮的氧化物、氨气都是非
常重要的非金属化合物,研究这些化合物对环境保护、理解化学反应原理都具有
重要意义。(1)二氧化氮与一定量空气混合通入水中能被水完全吸收,反应的化学方程式为
_________________。
若该反应有aN 个电子转移,则参加反应的二氧化氮的物质的量为________
A
__________________。
(2)下列除去大气污染物的化学方程式不正确的是________。
A.汽车尾气经催化剂作用:CO+NO NO +C
2
B.石灰乳吸收硫酸厂尾气:SO +Ca(OH) CaSO +H O
2 2 3 2
C.燃烧法除去尾气中硫化氢:2H S+3O 2SO +2H O
2 2 2 2
D.氨气与一氧化氮在一定条件下反应:4NH +6NO 5N +6H O
3 2 2
(3)大多数非金属氧化物能被氢氧化钠溶液吸收。例如NaOH+SO
2
NaHSO ,2NaOH+SO Na SO +H O,2NO +2NaOH NaNO +NaNO +H O,NO+
3 2 2 3 2 2 3 2 2
NO +2NaOH 2NaNO + H O,NO不溶于氢氧化钠溶液或水。
2 2 2
①同种反应物,其反应产物与浓度、温度、反应物相对量等因素有关。影响二氧化
硫与氢氧化钠反应产物的因素与下列反应相同的是________。
A.木炭与氧气反应 B.硫与氧气反应
C.钠与氧气反应 D.铜与硝酸溶液反应②某NO与NO 混合气体通入氢氧化钠溶液被完全吸收,推测混合气体中气体组
2
成V(NO )∶V(NO)________。
2
【解析】(1)二氧化氮与氧气在水中反应生成硝酸:4NO +O +2H O 4HNO ,1 mol
2 2 2 3
NO 反应转移1 mol电子,所以转移a mol电子消耗a mol二氧化氮。(2)A项,产
2
物应为二氧化碳和氮气;B项正确;C项,硫化氢燃烧生成大气污染物二氧化硫,应
用碱溶液吸收H S,错误;D项,生成N 无污染,正确。(3)①氢氧化钠与二氧化硫
2 2
之间相对量不同,产物不同。A项,碳与氧气反应,氧气不足时生成CO,符合题
意;B项,只生成SO ;C项,钠与氧气反应的产物受温度影响;D项,硝酸浓度不同,
2
产物不同。②由题意可知,二氧化氮体积大于或等于一氧化氮时,能被完全吸收。
答案:(1)4NO +O +2H O 4HNO a mol
2 2 2 3
(2)AC (3)①A ②≥1
16.(9分)氮的氧化物和硫的氧化物是导致酸雨的物质。
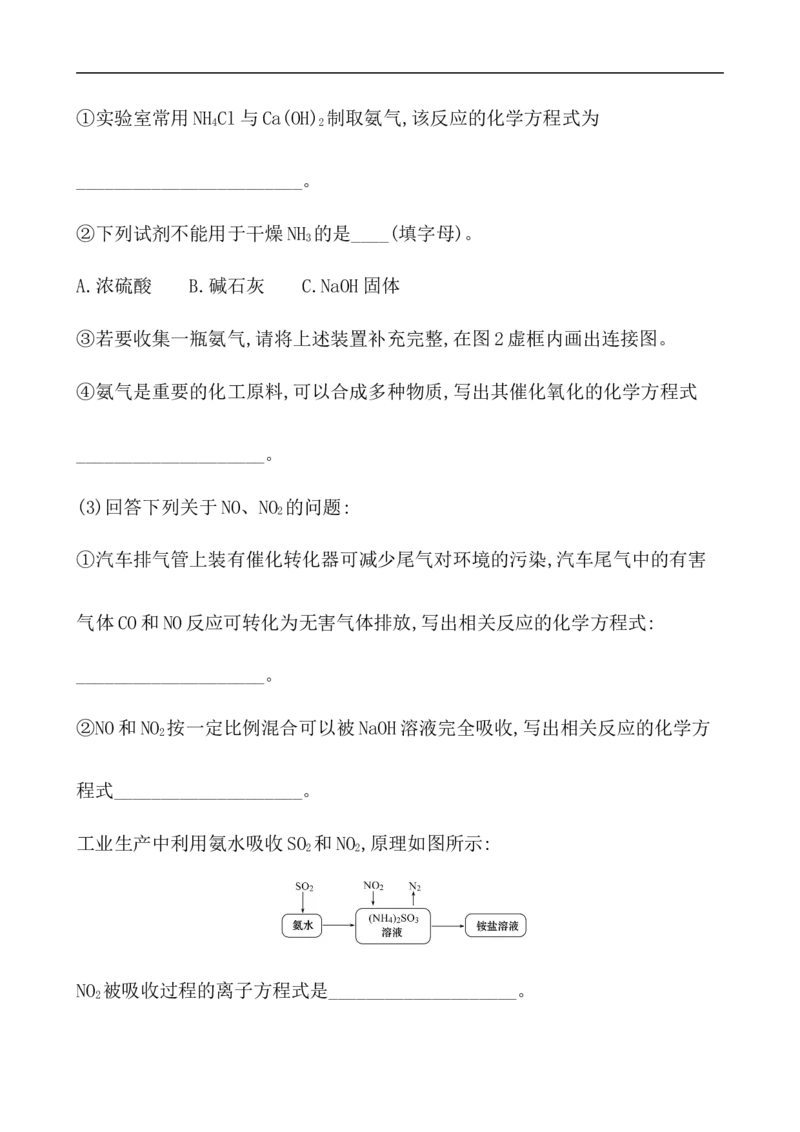
(1)形成酸雨的原理之一可简单表示如图:
请回答下列问题:
①酸雨的pH________(填“>”“<”或“=”)5.6;②D物质的化学式为________;
③反应b的化学方程式为____________________。
(2)在一定条件下氨气亦可用来将氮氧化物转化为无污染的物质,写出氨气和二
氧化氮在一定条件下反应生成氮气和水的化学方程式:_______________,
反应中氧化剂是__________________________。
【解析】(1)①酸雨的pH<5.6;②含硫燃料燃烧生成A是二氧化硫,二氧化硫溶于
水生成D是亚硫酸,化学式为H SO ;③反应b是二氧化硫被氧气氧化为三氧化硫,
2 3
反应的化学方程式为2SO +O 2SO 。(2)氨气和二氧化氮在一定条件下反应
2 2 3
生成氮气和水的化学方程式为6NO +8NH 7N +12H O,二氧化氮中氮元素化
2 3 2 2
合价降低,得到电子,所以反应中氧化剂是NO 。
2
答案:(1)①< ②H SO
2 3
③2SO +O 2SO
2 2 3
(2)6NO +8NH 7N +12H O NO
2 3 2 2 2
17.(10分)(2019·烟台高一检测)为了测定实验室长期存放的Na SO 固体的纯
2 3
度,准确称取W g固体样品,配成250 mL溶液。设计了以下两种实验方案:方案Ⅰ:取25.00 mL上述溶液,加入过量的盐酸酸化的BaCl 溶液,过滤、洗涤和
2
干燥沉淀,称得沉淀的质量为m g。
1
方案Ⅱ:取25.00 mL上述溶液,加入过量的盐酸酸化的Ba(NO ) 溶液,过滤、洗涤
3 2
和干燥沉淀,称重,其质量为m g。
2
(1)配制250 mL Na SO 溶液时,必须用到的实验仪器有烧杯、玻璃棒、胶头滴管、
2 3
药匙和______、____________________。
(2)写出Na SO 固体氧化变质的化学方程式:____________________。
2 3
(3)方案Ⅰ加入过量的盐酸酸化的BaCl 溶液,目的是__________________
2
____________________。
(4)方案Ⅰ中,若滤液浑浊,将导致测定结果________(选填“偏高”或“偏
低”)。
(5)若操作正确,则m________m(选填“>”“<”或“=”)。原因是_______
1 2
___________________________________。
【解析】(1)配制250 mL Na SO 溶液时,必须用到的实验仪器有烧杯、玻璃棒、胶
2 3
头滴管、药匙、托盘天平和250 mL的容量瓶。
(2)Na SO 固体被氧化为Na SO 。
2 3 2 4(3)方案Ⅰ加入过量的盐酸酸化的BaCl 溶液,目的是使S 充分转化为气体,
2
使S 完全沉淀。
(4)若滤液浑浊,证明滤液中含有BaSO ,所称量的BaSO 减少,造成Na SO 的纯度
4 4 2 3
偏高。
(5)若操作正确,则m