文档内容
第 2 课时 酚
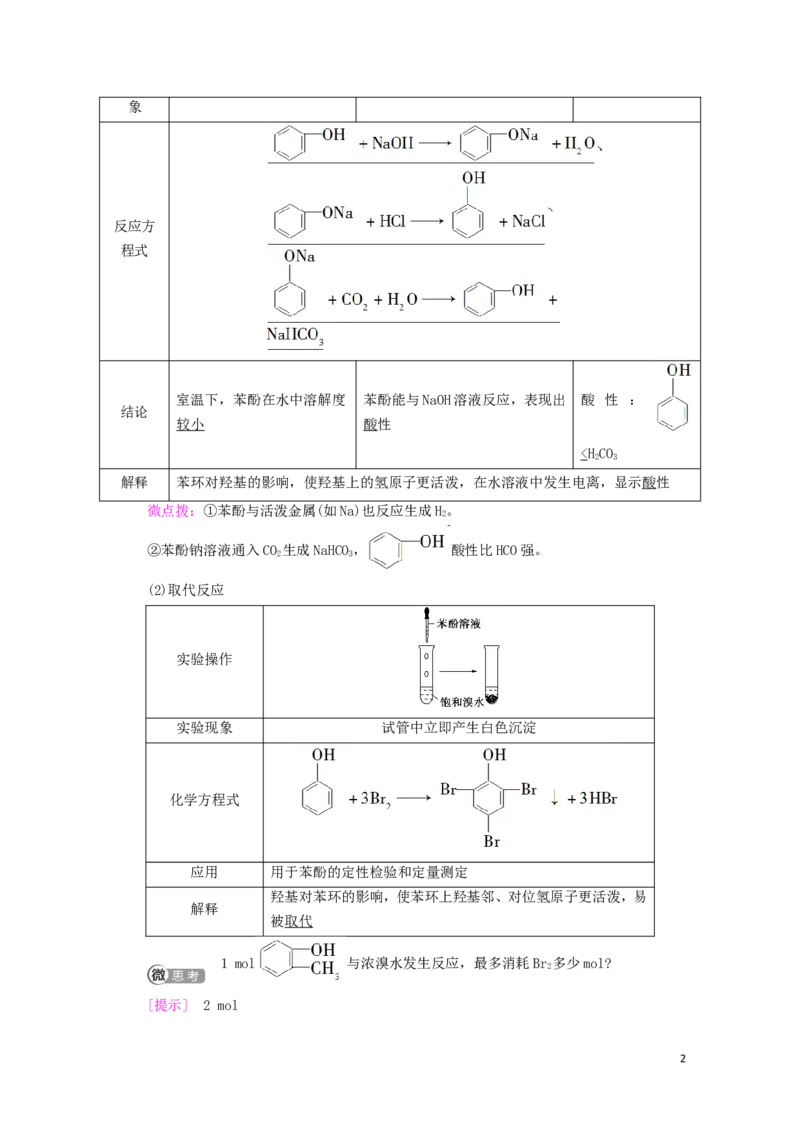
发 展 目 标 体 系 构 建
1.结合代表物苯酚了解酚的结构,理解
酚的性质及应用培养“微观探析与变化
观念”的核心素养。
2.根据苯酚的化学性质,理解有机物中
基团之间的相互影响,培养“证据推理
与模型认知”的核心素养。
一、苯酚的组成、结构与物理性质
1.组成与结构
苯酚是一元酚,是酚类化合物最简单的,分子式为CHO,结构可表示为 或
6 6
,官能团为 羟基 (—OH )。
2.物理性质
(1)纯净的苯酚是无色晶体,有特殊气味,易被空气氧化呈粉红色。
(2)苯酚室温下在水中的溶解度为9.2 g,当温度高于65 ℃时能与水混溶,苯酚易溶于有
机溶剂。
(3)苯酚有毒,对皮肤有腐蚀性,如不慎沾到皮肤上,应立即用乙醇冲洗,再用水冲洗。
二、苯酚的化学性质及应用
1.化学性质
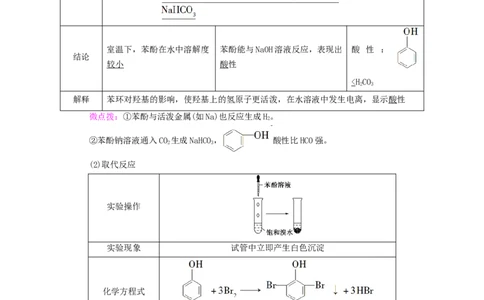
(1)酸性——弱酸性,俗称石炭酸
实验步
骤
实验现 得到浑浊液体 液体变澄清 液体变浑浊
1象
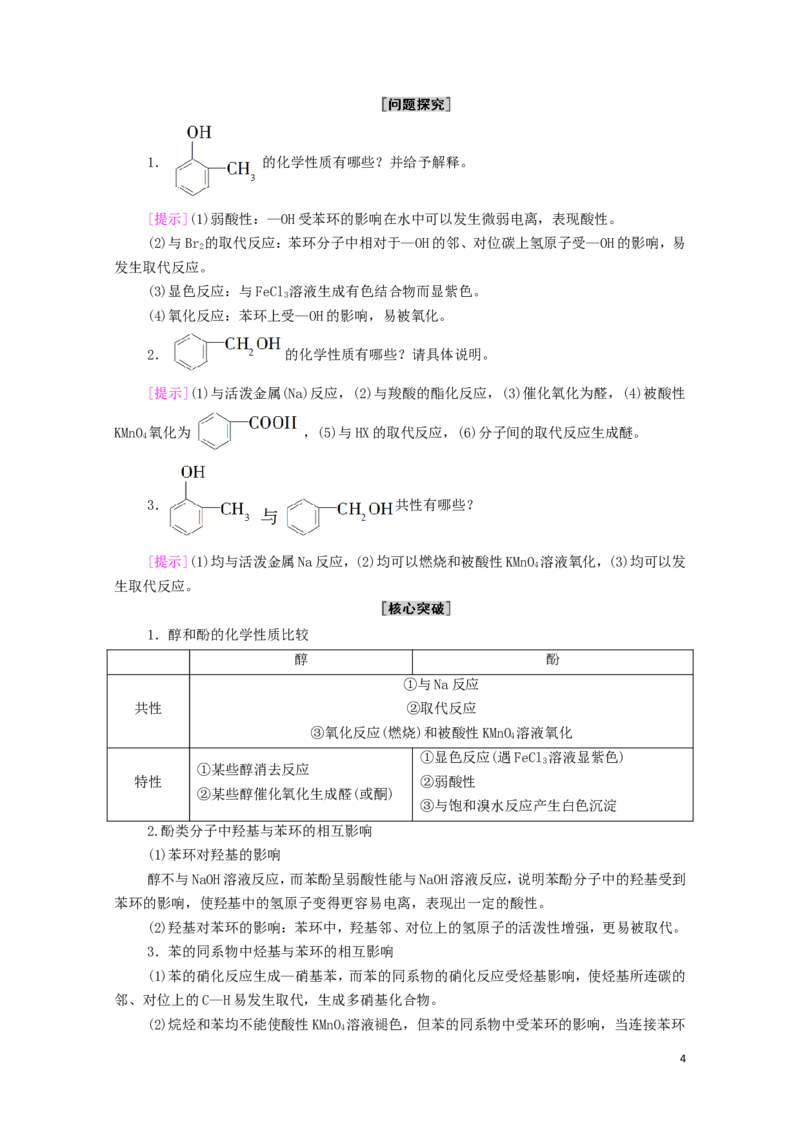
反应方
程式
室温下,苯酚在水中溶解度 苯酚能与NaOH溶液反应,表现出 酸 性 :
结论
较小 酸性
HCO,下列化学方程式正确的是( )
2 3 6 5
A.2CHONa+HO+CO―→2CHOH+NaCO
6 5 2 2 6 5 2 3
B.CHOH+NaHCO―→CHONa+HO+CO↑
6 5 3 6 5 2 2
C.2CHOH+NaCO―→2CHONa+HO+CO↑
6 5 2 3 6 5 2 2
D.CHOH+NaCO―→CHONa+NaHCO
6 5 2 3 6 5 3
D [酸性强弱顺序为HCO >CHOH>HCO,所以CHONa能与CO 、HO反应生成NaHCO 和
2 3 6 5 6 5 2 2 3
CHOH,化学方程式为CHONa+HO+CO―→CHOH+NaHCO,A错误;酸性:HCO>CHOH,因此
6 5 6 5 2 2 6 5 3 2 3 6 5
CHOH与NaHCO 不反应,B错误;酸性:HCO >CHOH>HCO,所以CHOH能与NaCO 反应生成
6 5 3 2 3 6 5 6 5 2 3
CHONa和NaHCO,化学方程式为CHOH+NaCO―→CHONa+NaHCO,C错误、D正确。]
6 5 3 6 5 2 3 6 5 3
4.下列四种有机化合物均含有多个官能团,其结构简式如下所示,下列有关说法中正确
的是( )
7A.①属于酚类,可与NaHCO 溶液反应产生CO
3 2
B.②属于酚类,能使FeCl 溶液显紫色
3
C.1 mol③最多能与3 mol Br 发生苯环上的取代反应
2
D.④可以发生消去反应
D [A项有机物属于酚类,具有一定的酸性,但是酸性比碳酸弱,故其不能与NaHCO 溶液
3
反应产生CO,错误;B项有机物分子中没有酚羟基,故其不属于酚类,不能使FeCl 溶液显紫色,
2 3
错误;C项有机物苯环上只有2个氢原子,且处于酚羟基邻位,故1 mol③最多能与2 mol Br
2
发生苯环上的取代反应,错误;D项有机物分子中羟基所连碳原子的邻位碳原子上有H原子,故
其可以发生消去反应,正确。 ]
5.(素养题)含苯酚的工业废水必须处理达标后才能排放,苯酚含量在1 g·L-1以上的工
业废水应回收苯酚。某研究性学习小组设计下列流程,探究废水中苯酚的回收方法。
――→――→――→
(1)可用________为试剂检验水样中是否含有苯酚。
(2)操作Ⅰ的名称为________,试剂a为________。
(3)通入CO 发生反应生成苯酚的化学方程式为
2
_______________________________________________________
_____________________________________________________。
[解析](1)苯酚遇氯化铁溶液发生显色反应,苯酚与浓溴水反应生成白色沉淀,则可选择
的检验试剂为FeCl 溶液或浓溴水。
3
(2)由分离流程可知,加苯是为了萃取苯酚,操作I为萃取,然后分液得到有机层;苯酚与
NaOH反应生成的苯酚钠易溶于水,则试剂a为NaOH溶液。
(3)苯酚钠与二氧化碳、水反应生成苯酚、碳酸氢钠,该化学方程式为
[答案] (1)FeCl 溶液或浓溴水 (2)萃取(或萃取、分液) NaOH 溶液 (3)
3
8+NaHCO
3
9