文档内容
第1课时 醇
发 展 目 标 体 系 构 建
1.结合醇的代表物了解醇的
分类、组成和结构,理解醇的
性质,培养“宏观辨别与微
观探析”的核心素养。
2.以乙醇为代表物,从化学
键的变化理解醇的取代、消
去、氧化反应的原理及转化
关系。培养“变化观念与证
据推理”的核心素养。
一、醇的分类、组成与物理性质
1.醇与酚的定义
(1)醇是指羟基与饱和碳原子相连的化合物。如 1丙醇 CHCHCHOH,苯甲醇
3 2 2
, 可命名为 3 甲基 2 戊醇 。
(2)酚是指羟基与苯环直接相连而形成的化合物。如苯酚 。
微点拨:醇的命名步骤:①选主链:含—OH的最长碳链,称“某醇”;②编号码:从离羟基
最近的一端的碳原子依次编号;③写名称:醇的名称前用阿拉伯数字标出羟基位置,用汉字数
字标出羟基个数。如 命名为1,2丙二醇。
2.醇的分类与组成
按羟基数目分为一元醇、二元醇和多元醇,其中饱和一元醇的分子通式为CH OH。乙二
n 2n+1
1醇 和 丙 三 醇 的 分 子 式 分 别 为 CHO 、 CHO , 结 构 简 式 分 别 为 、
2 6 2 3 8 3
。
3.醇的物理性质
(1)甲醇、乙二醇与丙三醇(又叫甘油)及应用
甲醇(CHOH)是无色、具有挥发性的液体,易溶于水,沸点为65 ℃。甲醇有毒,误服会损伤
3
视神经,甚至致人死亡。甲醇广泛应用于化工生产,也可作为车用燃料。乙二醇和丙三醇都是无
色、黏稠的液体,都易溶于水和乙醇,是重要的化工原料。
(2)溶解性:①醇在水中的溶解度随着分子中碳原子数的增加而降低,原因是极性的—OH
在分子中所占的比例逐渐减少。羟基越多,溶解度越大。
②醇的溶解度大于含有相同碳原子数烃类的溶解度,原因是醇分子中的羟基属于极性基
团且能与水形成氢键。
(3)熔沸点:①随分子中碳原子数的增多,熔沸点逐渐升高。
②醇的沸点远远高于相对分子质量相近的烃、卤代烃等的沸点,原因是醇分子之间形成了
氢键(醇分子中羟基的氧原子与另一醇分子中羟基的氢原子间存在着氢键)。
微点拨:多元醇分子中存在多个羟基,彼此形成分子间氢键的概率增加,分子间作用力增
强,故碳原子数相同的醇,随着羟基数的增多,其沸点逐渐升高;此外,与水分子间形成氢键的
概率也增大,从而使多元醇具有易溶于水的性质。
二、醇的化学性质(以乙醇为例)
醇的化学性质主要由羟基官能团决定。在醇分子中由于氧原子吸引电子能力比氢原子和
碳原子强,使 O—H 和 C—O 的电子对都向氧原子偏移,使 O—H 和 C—O 易断裂,即
。
1.置换反应
与活泼金属(如Na)发生置换反应,其反应方程式为
2CHCH O H + 2Na→2C HCH ON a + H↑,反应时乙醇分子断裂的化学键为O—H。
3 2 3 2 2
2.取代反应
(1)酯化反应:与乙酸发生反应的方程式为
。
(2)与氢卤酸反应
与HBr反应的化学方程式为
CH O H + HB r ――→ CH —B r + HO,反应时,乙醇分子断裂的键为C—O。
2 5 2 5 2
(3)分子间脱水生成醚
乙醇在浓硫酸作用下加热至 140 ℃时,生成乙醚,其反应方程式为 CHCH OH +
3 2
CHCH O H ――→ C HCH—O—CHCH + HO。
3 2 3 2 2 3 2
2注意:①乙醚是一种无色、易挥发的液体,沸点34.5 ℃,有特殊气味,具有麻醉作用。乙醚
微溶于水,易溶于有机溶剂,它本身是一种优良溶剂,能溶解多种有机物。
②醚的官能团叫醚键,表示为 ,醚的结构可用R—O—R′表示,R、R′
都是烃基,可以相同也可以不同。
3.消去反应
乙 醇 在 浓 硫 酸 的 作 用 下 , 加 热 至 170_℃ 时 生 成 乙 烯 , 反 应 方 程 式 为
CHCH O H ――→ C H = = = C H ↑ + HO,浓硫酸的作用是催化剂和脱水剂。反应时乙醇分子断的键是
3 2 2 2 2
C—H 与C—O。
4.氧化反应
(1)实例:
②乙醇被酸性重铬酸钾(KCrO)溶液氧化的过程为
2 2 7
(2)有机反应中的氧化、还原反应
①有机物分子中失去氢原子或加入氧原子的反应叫氧化反应。如乙醇在氧化剂的作用下
失去氢原子转化为乙醛,乙醛在氧化剂的作用下加入氧原子转化为乙酸。
②有机物分子中加入氢原子或失去氧原子的反应叫还原反应。如烯烃与H 的加成反应,
2
也属于还原反应。
1.判断正误(对的在括号内打“√”,错的在括号内打“×”。)
(1)烃分子中的氢原子被羟基取代而生成的羟基化合物一定为醇。
( )
(2)醇的熔沸点高于相应烃的熔沸点,是因醇分子间形成氢键。
( )
(3)乙醇发生酯化反应时,乙醇断裂的键是C—O键。
( )
(4)乙醇生成醚的反应属于消去反应。
3( )
[答案] (1)× (2)√ (3)× (4)×
2.下列物质不是醇类的是( )
[答案] C
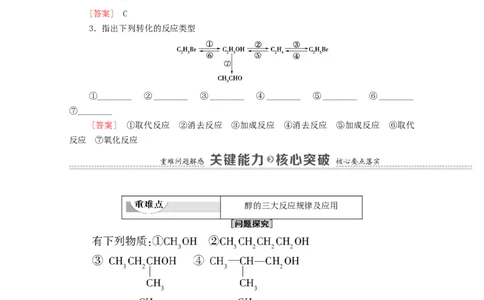
3.指出下列转化的反应类型
①________ ②________ ③________ ④________ ⑤________ ⑥________
⑦________
[答案] ①取代反应 ②消去反应 ③加成反应 ④消去反应 ⑤加成反应 ⑥取代
反应 ⑦氧化反应
醇的三大反应规律及应用
(1)上述物质能与HX发生取代反应有________(填序号)。
(2)上述物质能发生消去反应的有________。
(3)上述物质能发生催化氧化的有________,其中生成醛的有________生成酮的有
________。
4[提示](1)①②③④⑤⑥
(2)②③④⑤
(3)①②③④⑥ ①②④⑥ ③
1.醇的取代反应规律
醇分子中,—OH或—OH上的氢原子在一定条件下可被其他原子或原子团取代,如醇与羧
酸的酯化反应、醇分子间脱水及与HX的取代反应。
2.醇的消去反应规律
(1)醇分子中,连有—OH的碳原子的相邻碳原子上连有氢原子时,才能发生消去反应而形
成不饱和键。
(2)若醇分子中与—OH相连的碳原子无相邻碳原子或其相邻碳原子上无氢原子,则不能
发生消去反应。如CHOH、(CH)CCHOH不能发生消去反应生成烯烃。
3 3 3 2
3.醇的催化氧化规律
醇能否被氧化以及被氧化的产物的类别,取决于与羟基相连的碳原子上的氢原子的个数,
具体分析如下:
1.有关下列两种物质的说法正确的是( )
5A.二者都能发生消去反应
B.二者都能在Cu作催化剂条件下发生催化氧化反应
C.相同物质的量的①和②分别与足量Na反应,产生H 的量:①>②
2
D.二者在一定条件下可与乙酸、氢溴酸发生取代反应
D [由两种物质的结构简式可知,①中与羟基相连的碳原子的邻位碳原子上没有氢原子,
不能发生消去反应;②中与羟基相连的碳原子上没有氢原子,不能被催化氧化;相同物质的量
的①和②分别与足量Na反应时,产生H 的量相等。]
2
2.将浓硫酸和分子式为CHO、CHO的醇的混合物共热,所得到的有机产物最多有( )
2 6 3 8
A.5种 B.6种
C.7种 D.8种
D [本题考查醇在浓硫酸作用下的脱水反应。分子式为CHO的醇为乙醇,满足分子式为
2 6
CHO的醇的结构共有2种,即正丙醇和异丙醇;醇发生的脱水反应有两种类型,即分子内脱水
3 8
和分子间脱水。乙醇分子内脱水所得有机产物是乙烯,正丙醇和异丙醇分子内脱水所得有机产
物都是丙烯,故分子内脱水所得有机产物有2种;而分子间脱水既要考虑同种物质分子间脱水
又要考虑不同种物质分子间脱水,同种物质分子间脱水所得有机产物有3种,不同种物质分子
间脱水所得有机产物有3种,故所得有机产物最多有8种。]
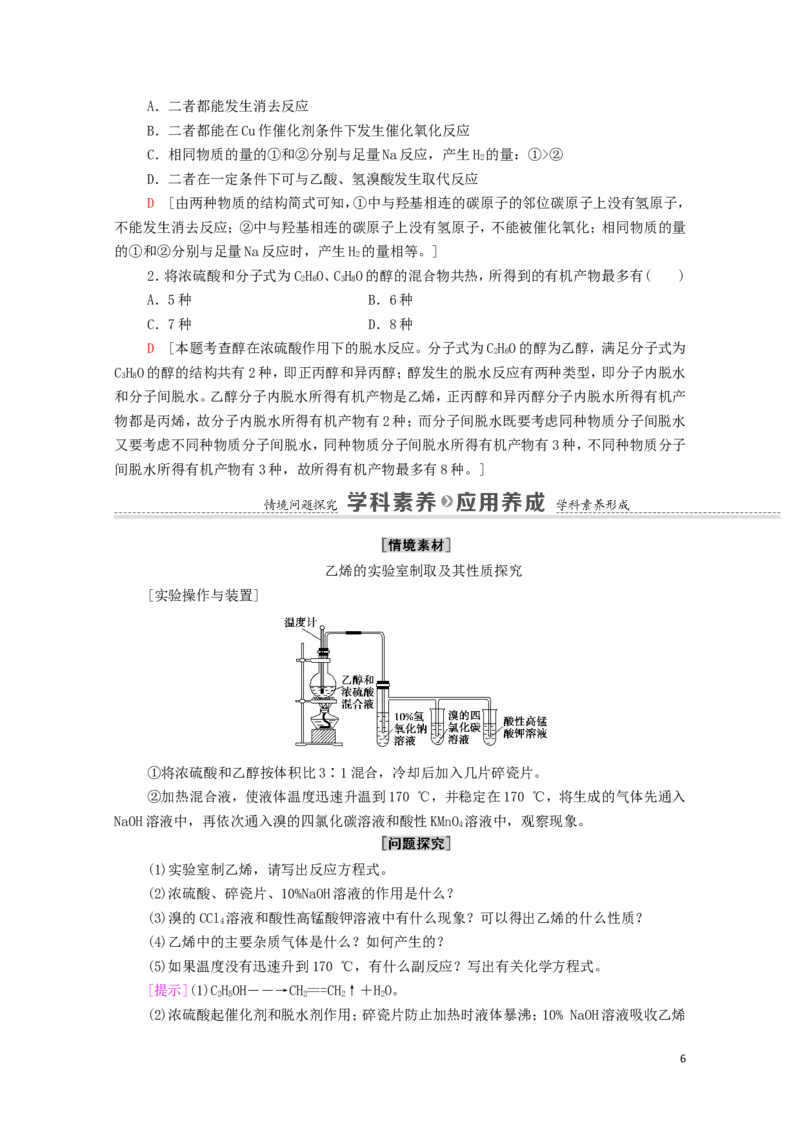
乙烯的实验室制取及其性质探究
[实验操作与装置]
①将浓硫酸和乙醇按体积比3∶1混合,冷却后加入几片碎瓷片。
②加热混合液,使液体温度迅速升温到170 ℃,并稳定在170 ℃,将生成的气体先通入
NaOH溶液中,再依次通入溴的四氯化碳溶液和酸性KMnO 溶液中,观察现象。
4
(1)实验室制乙烯,请写出反应方程式。
(2)浓硫酸、碎瓷片、10%NaOH溶液的作用是什么?
(3)溴的CCl 溶液和酸性高锰酸钾溶液中有什么现象?可以得出乙烯的什么性质?
4
(4)乙烯中的主要杂质气体是什么?如何产生的?
(5)如果温度没有迅速升到170 ℃,有什么副反应?写出有关化学方程式。
[提示](1)CHOH――→CH===CH↑+HO。
2 5 2 2 2
(2)浓硫酸起催化剂和脱水剂作用;碎瓷片防止加热时液体暴沸;10% NaOH溶液吸收乙烯
6中杂质气体SO 和乙醇,防止干扰验证乙烯的性质。
2
(3)二者均褪色,分别说明乙烯能发生加成反应和氧化反应。
(4)SO,浓HSO 被还原生成的。
2 2 4
(5)CHOH+CHOH――→CHOCH+HO。
2 5 2 5 2 5 2 5 2
通过本实验探究,了解乙烯的制法和乙烯的性质,培养学生“科学探究”与“科学
态度”的核心素养。
1.下列物质中既属于芳香族化合物又属于醇的是( )
[答案] B
2.结合下表数据分析,下列说法不合理的是 ( )
物质 分子式 沸点/℃ 溶解性
乙醇 CHO 78.5 与水以任意比混溶
2 6
乙二醇 CHO 197.3 与水和乙醇以任意比混溶
2 6 2
A.二者的溶解性与其在水中能够形成氢键有关
B.可以采用蒸馏的方法将二者进行分离
C.丙三醇的沸点应该高于乙二醇的沸点
D.二者组成和结构相似,互为同系物
D [乙醇和乙二醇都能与水分子形成氢键,均能与水以任意比混溶,A项正确;二者的沸
点相差较大,可用蒸馏法进行分离,B项正确;丙三醇分子中羟基数目多,分子间可形成更多氢
键,其沸点高于乙二醇,C项正确;二者分子中所含羟基数不同,不互为同系物,D项错误。]
3.以下四种有机化合物分子式均为CH O:
4 10
其中既能发生消去反应生成相应的烯烃,又能氧化生成相应醛的是 ( )
7A.①和② B.只有②
C.②和③ D.③和④
C [①能发生消去反应,能发生催化氧化反应,但生成物不是醛;②既能发生消去反应,
又能催化氧化生成醛;③既能发生消去反应,又能发生催化氧化生成醛;④能发生消去反应,但
不能发生催化氧化反应。]
4.将一定量的饱和一元醇平均分成两份,将其中一份完全燃烧,消耗28.8 g氧气,在另
一份中加入过量金属钠,产生2.24 L(标准状况)H,则该醇为 ( )
2
A.乙醇 B.丙醇
C.丁醇 D.甲醇
B [设饱和一元醇的分子式为CH OH。由题意知:
n 2n+1
2CH OH+2Na―→2CH ONa+H↑
n 2n+1 n 2n+1 2
2 1
0.2 mol 0.1 mol
CH OH+nO――→nCO+(n+1)HO
n 2n+1 2 2 2
1 n
0.2 mol 0.9 mol
则n×0.2=0.9,n=3,即该饱和一元醇为CHOH(丙醇)。]
3 7
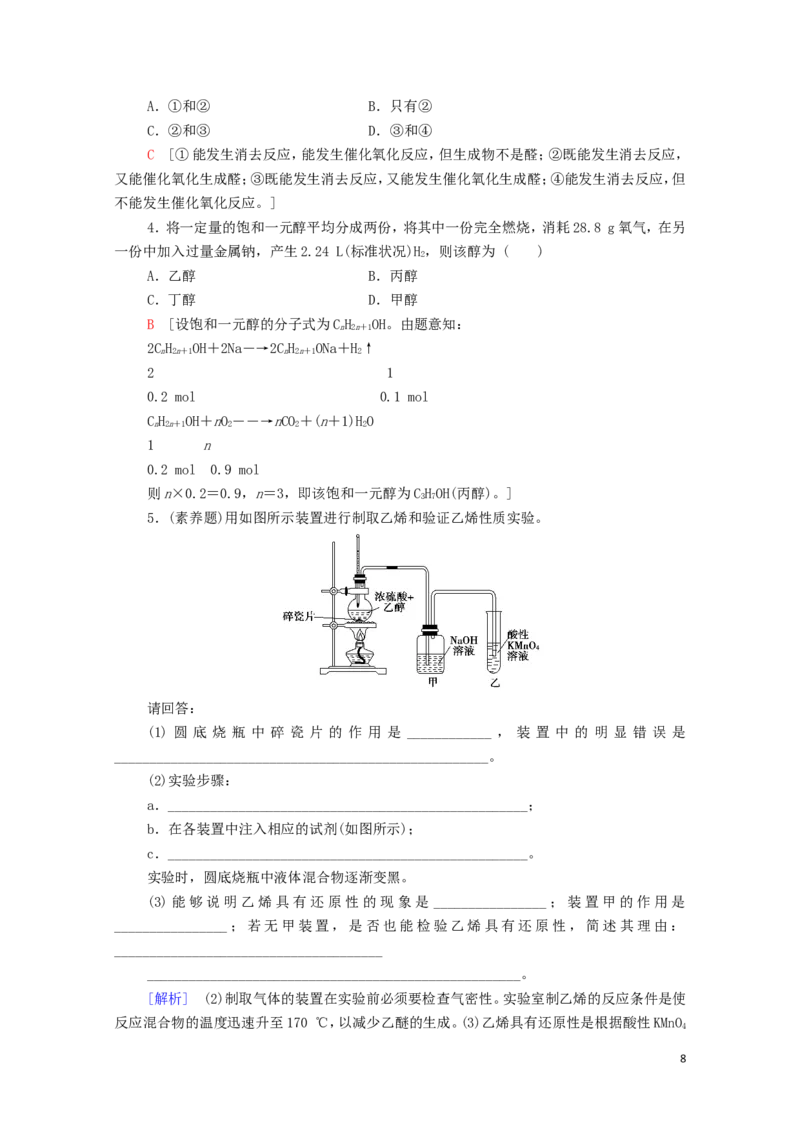
5.(素养题)用如图所示装置进行制取乙烯和验证乙烯性质实验。
请回答:
(1) 圆 底 烧 瓶 中 碎 瓷 片 的 作 用 是 ____________ , 装 置 中 的 明 显 错 误 是
_____________________________________________________。
(2)实验步骤:
a.___________________________________________________;
b.在各装置中注入相应的试剂(如图所示);
c.___________________________________________________。
实验时,圆底烧瓶中液体混合物逐渐变黑。
(3)能够说明乙烯具有还原性的现象是 ________________;装置甲的作用是
________________;若无甲装置,是否也能检验乙烯具有还原性,简述其理由:
______________________________________
_____________________________________________________。
[解析] (2)制取气体的装置在实验前必须要检查气密性。实验室制乙烯的反应条件是使
反应混合物的温度迅速升至170 ℃,以减少乙醚的生成。(3)乙烯具有还原性是根据酸性KMnO
4
8溶液褪色来判断的。圆底烧瓶中混合物变黑,说明生成了C,联想浓硫酸具有强氧化性,推出在
乙烯中混有还原性气体SO,同时还有挥发出的乙醇蒸气,由于SO、乙醇也会使酸性KMnO 溶液
2 2 4
褪色,会干扰乙烯的还原性验证实验,所以检验乙烯的还原性前必须除去SO 和乙醇。
2
[答案] (1)防止暴沸 温度计水银球没有插入反应液中央
(2)组装仪器,检查装置的气密性 加热,使温度迅速升到170 ℃
(3)乙中酸性KMnO 溶液褪色 除去乙烯中混有的SO、CO、乙醇蒸气等杂质 不能,SO、
4 2 2 2
乙醇具有还原性,也可以使酸性KMnO 溶液褪色
4
9