文档内容
《金属晶体与离子晶体》第二课时 教学设计
课题 《金属晶体与离 单元 3 学科 化学 年级 高二
子晶体》
本章内容比较系统地介绍了晶体结构与性质,内容比较丰富。第三章作
为选修性必修2结尾章,与前两章一起构成“原子、分子、晶体的结构与性
质”三位一体的物质结构与性质模块的基本内容。本节教学内容是人教版高中
化学选择性必修第二册第三章《晶体结构与性质》第三节《金属晶体与离子晶
教材
体》第二课时。
分析
本节安排了“离子晶体”这部分内容。学生通过学习这部分知识,能辨识
常见的离子晶体,能从微观角度理解离子键对离子晶体性质的影响,能从宏观
角度解释离子晶体性质的差异。通过对离子晶体模型的认识,理解离子晶体的
结构特点,预测其性质。
宏观辨识与微观探析:能辨识常见的离子晶体,能从微观角度理解离子键
对离子晶体性质的影响,能从宏观角度解释离子晶体性质的差异。
教学
目标
与核 证据推理与模型认知:通过对离子晶体模型的认识,理解离子晶体的结构
心素 特点,预测其性质。
养
重点 离子晶体
难点教学过程
教学环节 教师活动 学生活动 设计意图
导入新课 思考:下列晶体构成微粒有什么共同点? 思考 通过思
微粒之间存在哪种相同的作用力? 考,引发
学生兴
趣,提高
学生学习
积极性。
讲授新课 第三节 金属晶体与离子晶体
第二课时 离子晶体
一、离子晶体
1.定义
由阳离子与阴离子相互作用而形成的晶体,叫离子
晶体。
2.构成微粒
阴阳离子。
3.微粒间作用
离子键——阴阳离子之间的静电作用。
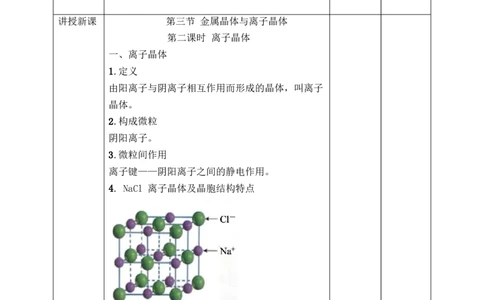
4. NaCl 离子晶体及晶胞结构特点
能辨识常
见的离子
Cl-数 = 8×1/8 + 6×1/2 = 4
晶体,能
Na+数 = 12×1/4 + 1 = 4 从微观角
度理解离
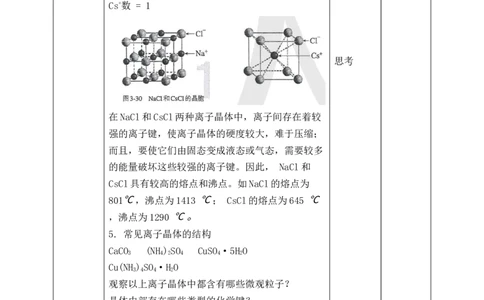
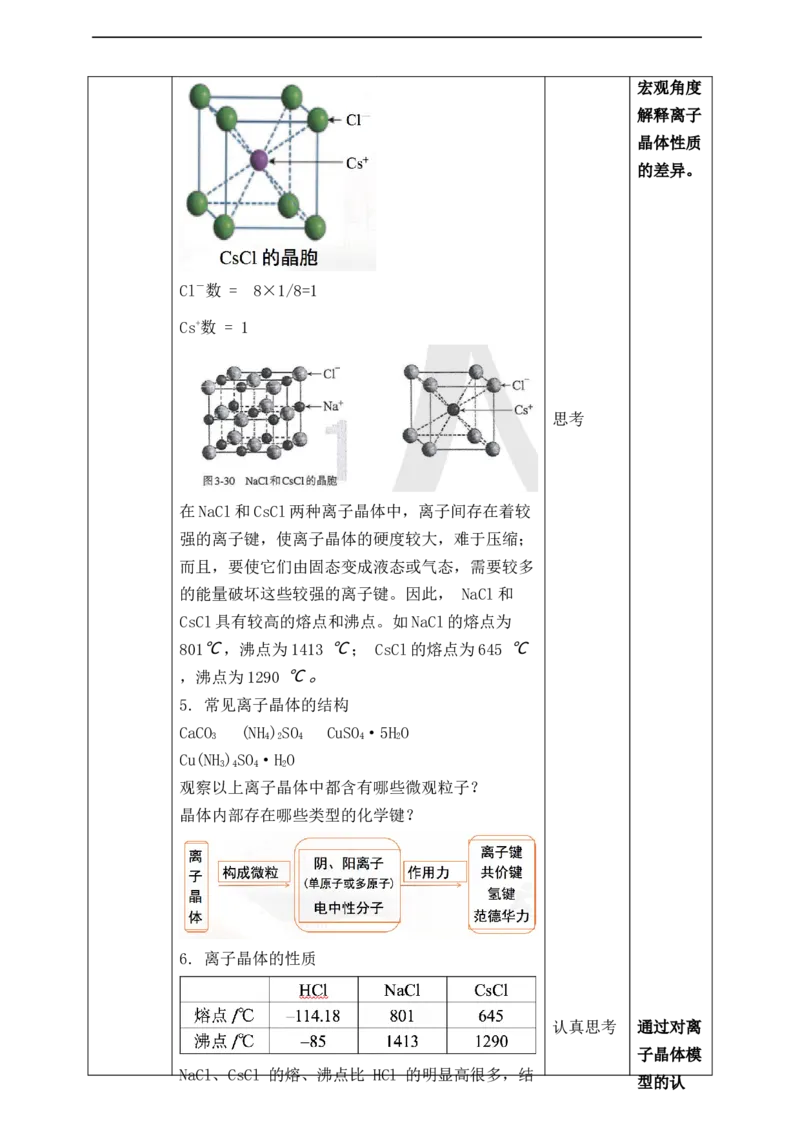
思考:CsCl 离子晶体的晶胞特点会怎样呢?
子键对离
子晶体性
质的影
响,能从宏观角度
解释离子
晶体性质
的差异。
Cl-数 = 8×1/8=1
Cs+数 = 1
思考
在NaCl和CsCl两种离子晶体中,离子间存在着较
强的离子键,使离子晶体的硬度较大,难于压缩;
而且,要使它们由固态变成液态或气态,需要较多
的能量破坏这些较强的离子键。因此, NaCl和
CsCl具有较高的熔点和沸点。如NaCl的熔点为
801℃,沸点为1413 ℃; CsCl的熔点为645 ℃
,沸点为1290 ℃。
5. 常见离子晶体的结构
CaCO (NH ) SO CuSO ·5H O
3 4 2 4 4 2
Cu(NH ) SO ·H O
3 4 4 2
观察以上离子晶体中都含有哪些微观粒子?
晶体内部存在哪些类型的化学键?
6. 离子晶体的性质
认真思考 通过对离
子晶体模
NaCl、CsCl 的熔、沸点比 HCl 的明显高很多,结
型的认