文档内容
第五章《化工生产中的重要非金属元素》教学设计
第二节 氮及其化合物
第三课时 硝酸 酸雨及防治
课题: 5.2.3 硝酸 酸雨及防治 课时 1 授课年级 高一
结合真实情境中的应用实例或通过实验探究,了解氮及其重要化合物的主要性质,认识这
课标 些物质在生产中的应用和对生态环境的影响。结合实例认识金属、非金属及其化合物的多样
要求 性,了解通过化学反应可以探索物质性质、实现物质转化,认识物质及其转化在自然资源综合
利用和环境保护中的重要价值。
本节是人教版(2019版)必修第二册第五章第二节氮及其化合物的内容。本节内容主要包
括:氮及氮的固定、一氧化氮和二氧化氮、氨和铵盐、硝酸、酸雨及其防治。教材编排思路与
上一节相似,首先介绍氮元素在元素周期表中的位置、氮的原子结构知识,应用前一节掌握的
研究非金属单质性质的基本思路预测氮的化学性质,渗透条件对化学反应的影响,引出自然界
中氮循环及氮的固定对人类生存的重要意义。之后,根据物质类别研究氮的化合物,包括一氧
化氮、二氧化氮、硝酸、氨和铵盐的化学性质。以工业合成氨、工业制硝酸的生产原理为载
体,应用氧化还原反应原理,设计含氮化合物的转化,使学生认识到从一种原料转化成多种产
品,路径之一是通过氧化还原反应改变主要元素的化合价,提升“变化观念”等学科核心素
养。教材设置铵根离子的检验、实验室制取氨的实验活动,让学生根据氨、铵根离子的性质和
反应,选择合适的试剂,设计检验或者制取物质的方案,提升其科学探究的能力。最后,教材
编入“酸雨及其防治”内容以及“测定雨水的pH”的研究与实践活动,综合运用硫和氮及其化
教材
合物的相关知识,寻求证据参与社会性议题的讨论,分析硫酸工业、合成氨工业对社会发展的
分析 价值和对环境的影响,有意识地渗透资源合理利用和环境保护的意识。
本节教学情景素材非常丰富,如:“雷雨发庄稼”;氮的循环与氮的固定;工业合成氨、
工业制硫酸(或硝酸);氮肥的生产与合理使用;氯气、氨气等泄漏的处理;酸雨的成因与防
治;汽车尾气的处理等。教学内容共安排三个课时:第一课时为氮气与氮的固定,一氧化氮和
二氧化氮,第二课时为氨和铵盐,第三课时为硝酸和酸雨及防治。
本课时为第三课时的内容,主要包括硝酸和酸雨及防治两部分。硝酸的主要包括 硝酸的
物理性质、化学性质、用途等知识。其中硝酸的强氧化性既时本课时的教学难点,也时本节教
学的难点,教学时可通过浓硝酸、浓硫酸分别与铜发生反应的比较加深理解,帮助记忆,突破
难点。最后教材通过二氧化硫和二氧化氮对大气的污染,给自然环境、人类的正常生活和工农
业生产带来的危害,介绍了酸雨的定义、形成及防治环境污染的方法等知识,通过“研究与实
践”栏目介绍了酸雨的测定方法等。
1.通过实验探究、讨论交流,了解硝酸的主要性质—酸性、不稳定性和强氧化性,并能从
氧化还原反应角度分析反应原理,认识硝酸浓度不同其氧化性强弱不同、还原产物不同,知道
教学 硝酸是重要的化工原料。
目标 2.通过阅读思考、查阅资料,从含氮物质的性质及转化的视角,了解酸雨的概念,知道酸
雨形成的主要原因是二氧化氮和二氧化硫进入大气,酸雨会严重危害环境及防治方法,增强环
境保护意识,培养社会责任感。
教学 重点:硝酸的不稳定性和强氧化性
重、 难点:硝酸的强氧化性原理及应用
难点
科学探究与创新意识:通过对浓、稀硝酸与铜反应的实验探究,强化学生能对观察记录的
核心 实验信息进行加工并获得结论,通过交流实验探究的成果,提出进 一步探究或改进实验的设
素养 想,培养创新能力。
证据推理与模型认知:通过学习硝酸的性质及原子守恒法、电子守恒法的分析应用,认识硝酸的强氧化性与浓度、反应条件、反应速率、还原产物等的关系,促进知识的系统化和结构
化,初步形成氮及其化合物的转化认知模型。
科学态度与社会责任:通过学习酸雨的形成原因和防治,关注与化学有关的社会热点问
题,认识环境保护和资源合理开发的重要性,树立可持续发展意识和绿色化学观念,勇于承担
责任,积极参与有关化学问题的社会决策。
学情 硝酸已熟悉酸的通性,浓硫酸具有强氧化性,部分含氮物质(如单质、氧化物、氢化物、
铵盐等)的性质及转化关系,有一定的实验设计和实验探究能力。但对氮及其化合物的认识还
分析 缺乏系统性和规律性,对硝酸强氧化性的原理分析及应用可能存在一定困难。
教学过程
教学 设计意
教学活动
环节 图
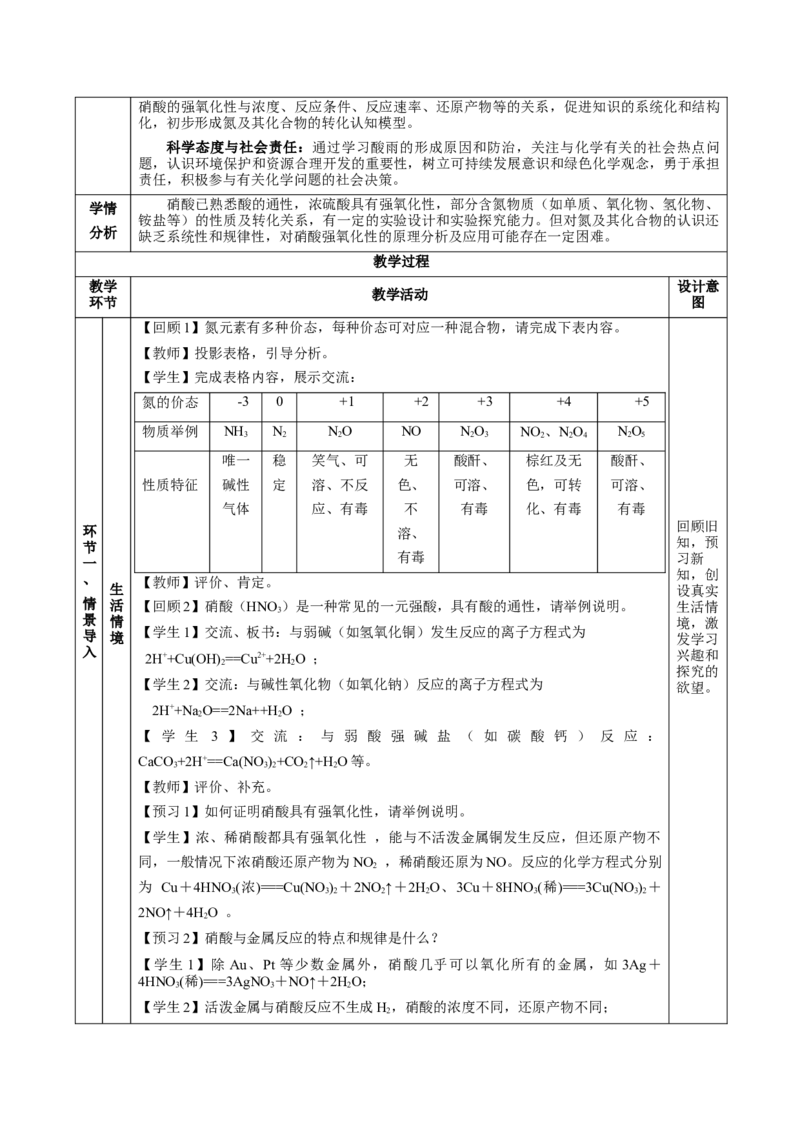
【回顾1】氮元素有多种价态,每种价态可对应一种混合物,请完成下表内容。
【教师】投影表格,引导分析。
【学生】完成表格内容,展示交流:
氮的价态 -3 0 +1 +2 +3 +4 +5
物质举例 NH N NO NO NO NO 、NO NO
3 2 2 2 3 2 2 4 2 5
唯一 稳 笑气、可 无 酸酐、 棕红及无 酸酐、
性质特征 碱性 定 溶、不反 色、 可溶、 色,可转 可溶、
气体 应、有毒 不 有毒 化、有毒 有毒
回顾旧
环 溶、
知,预
节
有毒 习新
一
知,创
、 【教师】评价、肯定。
生 设真实
情 活 【回顾2】硝酸(HNO)是一种常见的一元强酸,具有酸的通性,请举例说明。 生活情
3
景 情 境,激
导 境 【学生1】交流、板书:与弱碱(如氢氧化铜)发生反应的离子方程式为 发学习
入 2H++Cu(OH) ==Cu2++2H O ; 兴趣和
2 2
探究的
【学生2】交流:与碱性氧化物(如氧化钠)反应的离子方程式为 欲望。
2H++Na O==2Na++HO ;
2 2
【 学 生 3 】 交 流 : 与 弱 酸 强 碱 盐 ( 如 碳 酸 钙 ) 反 应 :
CaCO +2H+==Ca(NO )+CO ↑+H O等。
3 3 2 2 2
【教师】评价、补充。
【预习1】如何证明硝酸具有强氧化性,请举例说明。
【学生】浓、稀硝酸都具有强氧化性 ,能与不活泼金属铜发生反应,但还原产物不
同,一般情况下浓硝酸还原产物为NO ,稀硝酸还原为NO。反应的化学方程式分别
2
为 Cu+4HNO(浓)===Cu(NO) +2NO ↑+2HO、3Cu+8HNO(稀)===3Cu(NO) +
3 3 2 2 2 3 3 2
2NO↑+4HO 。
2
【预习2】硝酸与金属反应的特点和规律是什么?
【学生 1】除 Au、Pt 等少数金属外,硝酸几乎可以氧化所有的金属,如 3Ag+
4HNO(稀)===3AgNO +NO↑+2HO;
3 3 2
【学生2】活泼金属与硝酸反应不生成H,硝酸的浓度不同,还原产物不同;
2NO NO、N、NH NO 等NO
2 2 2 4 3
【教师】评价、强调:常温下浓硝酸能使Fe、Al钝化,加热时反应。
【导入】2023年2月14日,美国亚利桑那州图森市高速公路一卡车侧翻,引发危险
物质硝酸泄漏,产生大量红棕色烟雾,现场可闻到刺鼻的气味。消防人员运来纯碱进
行处理,以防止其扩散造成更大危害。(见PPT视频)
【过渡】硝酸是中学常见三大强酸之一,除具有酸的通性外,还具有一些特殊的性
质。
【问题1】观察浓、稀HNO 样品,阅读教材P15页内容,思考总结硝酸具有哪些物
3 在教师
理性质?
的引导
【教师】展示硝酸样品,打开瓶塞,引导观 察。 下认识
硝酸的
【学生】纯硝酸是无色(久置可能呈黄色)、 易挥发(沸点83℃)、有
物理性
刺激性气味的液体,密度比水大,能以任意比 溶解于水。。
质。
【学生2】一元强酸,具有腐蚀性,使用时须注意防护何通风。
联系酸
【教师】评价、强调:质量分数为69%的硝酸为浓硝酸,质量分数为98%以上的硝酸 的通
为发烟硝酸。因此浓硝酸为混合物。 性,推
测硝酸
【问题2】讨论:阅读教材P15页内容,结合所学知识,思考硝酸具有哪些化学性
的性
质,培
质?
养证据
【学生】板书、交流:酸的通性:HNO 3 ===H+ + NO 3 ― 。如与碱(如NaOH)反应:H 推理于
++OH-===H O;与碱性氧化物(如NaO)反应:2H++NaO===2Na++HO;与弱酸 模型认
2 2 2 2
盐(如CaCO ):CaCO +2H+===Ca2++CO↑+HO。 知的化
3 3 2 2
学核心
【教师】评价、追问:久置的硝酸为什么呈黄色?浓硝酸应如何保存?
素养。
【学生1】浓硝酸具有不稳定性,见光或受热易分解:4HNO=====4NO ↑+O↑+
3 2 2
2HO。
2
生成的红棕色气体NO 溶于浓硝酸使浓硝酸呈黄色。
2
【学生2】实验室常将浓硝酸保存在棕色细口试剂瓶中,并放置在
阴凉处。
检测与
【教师】评价、强调:我们学过的氯水以及常见的AgNO 、AgCl
3
评价,
等均用棕色试剂瓶保存,它们的共同特点是见光易分解,因此,我们可推测HNO 具 发现问
3
活
题,调
动 有不稳定性。
控课
环 一 【教师】追问:除上述性质外,硝酸还具有哪些性质呢? 堂,提
节 、 高教学
二 硝 【学生】强氧化性:如浓硝酸、稀硝酸与铜反应的化学方程式分别为:Cu+ 的实效
、 酸 4HNO(浓)===Cu(NO) +2NO ↑+2HO、3Cu+8HNO(稀)===3Cu(NO) +2NO↑+ 性。
硝 的 3 3 2 2 2 3 3 2
酸 性 4HO;与非金属(碳)的反应:C+4HNO(浓)====CO↑+4NO ↑+2HO。
2 3 2 2 2
质
氧 【对应练习1】下列关于硝酸的说法不正确的是( )
A.浓硝酸是一种易挥发的液体混合物
B.浓硝酸在空气中敞口放置,因吸收水蒸气而浓度减小
C.浓硝酸不稳定,易分解生成二氧化氮、氧气和水
D.常温下,浓硝酸常保存在棕色试剂瓶中
【答案】B【解析】浓硝酸是一种易挥发的液体混合物,在空气中敞口放置,其浓度会不断减
小;浓硝酸不具有吸水性,浓硝酸不稳定,见光易分解生成二氧化氮、氧气和水,所
以浓硝酸常保存在棕色试剂瓶中。
【对应练习1】下列反应中硝酸既能表现出酸性又表现出氧化性的是( )
A.能使紫色石蕊溶液变为红色
B.与铜反应放出一氧化氮气体,生成硝酸铜
C.与碳酸钠反应放出二氧化碳气体,生成硝酸钠
D.与单质硫混合共热时生成硫酸和二氧化氮
【答案】B
【解析】A.硝酸使紫色石蕊溶液变为红色,只表现酸性,A不符合题意;B.硝酸
与铜反应生成硝酸铜、一氧化氮和水,既表现其强氧化性又表现其酸性,B符合题
意;C.与碳酸钠反应放出二氧化碳气体,表现的是硝酸的酸性,C不符合题意;
D.硝酸与单质硫混合共热时生成硫酸和二氧化氮,表现的是硝酸的强氧化性,D不
符合题意;综上所述答案为B。
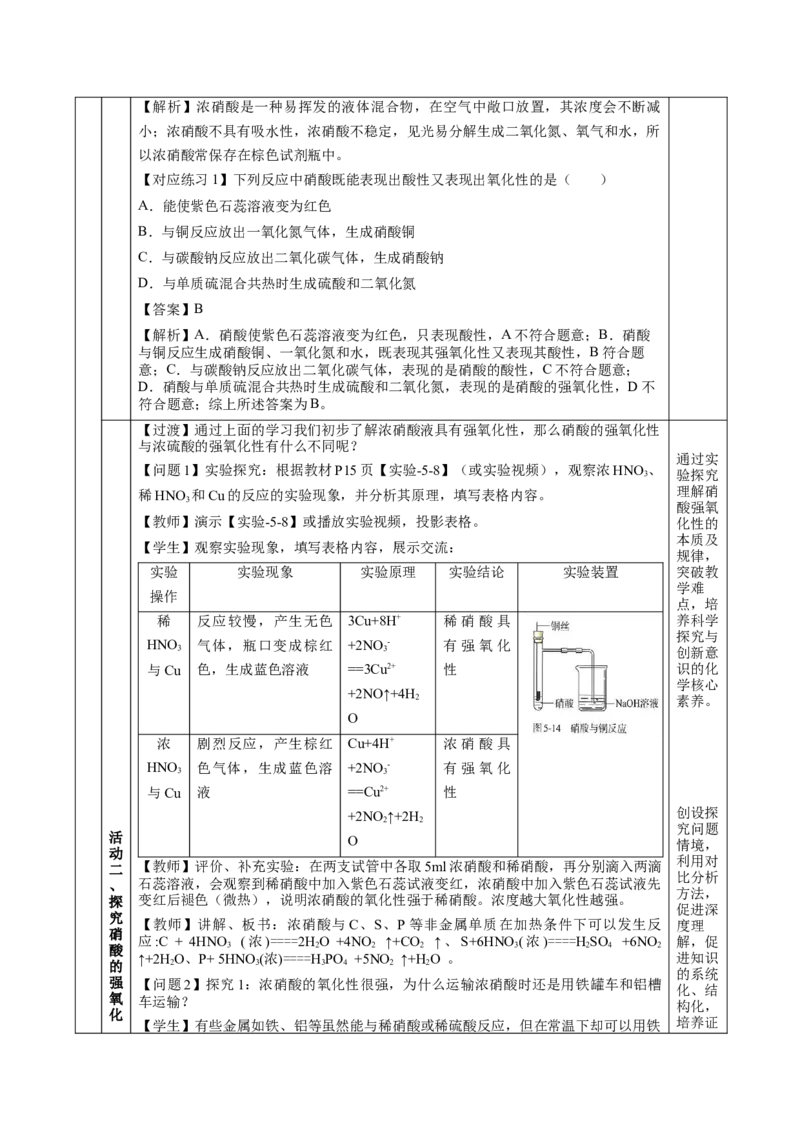
【过渡】通过上面的学习我们初步了解浓硝酸液具有强氧化性,那么硝酸的强氧化性
与浓硫酸的强氧化性有什么不同呢?
通过实
【问题1】实验探究:根据教材P15页【实验-5-8】(或实验视频),观察浓HNO
3
、
验探究
理解硝
稀HNO 和Cu的反应的实验现象,并分析其原理,填写表格内容。
3
酸强氧
【教师】演示【实验-5-8】或播放实验视频,投影表格。 化性的
本质及
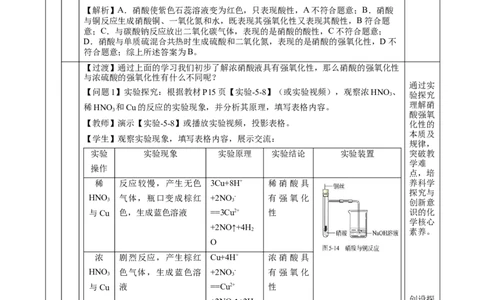
【学生】观察实验现象,填写表格内容,展示交流:
规律,
实验 实验现象 实验原理 实验结论 实验装置 突破教
学难
操作
点,培
稀 反应较慢,产生无色 3Cu+8H+ 稀硝酸具 养科学
探究与
HNO 气体,瓶口变成棕红 +2NO- 有强氧化
3 3 创新意
与Cu 色,生成蓝色溶液 ==3Cu2+ 性 识的化
学核心
+2NO↑+4H
2 素养。
O
浓 剧烈反应,产生棕红 Cu+4H+ 浓硝酸具
HNO 色气体,生成蓝色溶 +2NO- 有强氧化
3 3
与Cu 液 ==Cu2+ 性
创设探
+2NO↑+2H
2 2
究问题
活
O 情境,
动
利用对
二 【教师】评价、补充实验:在两支试管中各取5ml浓硝酸和稀硝酸,再分别滴入两滴
比分析
、 石蕊溶液,会观察到稀硝酸中加入紫色石蕊试液变红,浓硝酸中加入紫色石蕊试液先
方法,
探 变红后褪色(微热),说明浓硝酸的氧化性强于稀硝酸。浓度越大氧化性越强。
促进深
究
【教师】讲解、板书:浓硝酸与C、S、P等非金属单质在加热条件下可以发生反 度理
硝
应:C + 4HNO (浓)====2HO +4NO ↑+CO ↑、S+6HNO (浓)====HSO +6NO 解,促
酸 3 2 2 2 3 2 4 2
↑+2H O、P+ 5HNO(浓)====HPO +5NO ↑+H O 。 进知识
的 2 3 3 4 2 2
的系统
强 【问题2】探究1:浓硝酸的氧化性很强,为什么运输浓硝酸时还是用铁罐车和铝槽
化、结
氧 车运输?
构化,
化
【学生】有些金属如铁、铝等虽然能与稀硝酸或稀硫酸反应,但在常温下却可以用铁 培养证性 或铝制容器来盛装浓硝酸或浓硫酸。这是因为常温下,铁、铝的表面被浓硝酸或浓硫 据推理
酸氧化,生成了一层致密的氧化物薄膜,这层薄膜阻止了酸与内层金属的进一步反应 与模型
(又叫钝化)。 认知的
化学核
【教师】评价、强调:钝化不是没有反应,二是反应很快停止。且当加热时,铁、铝
心素
会与浓硝酸或浓硫酸发生反应。
养。
【问题2】探究2:结合P教材102页“资料卡片”,回答“王水”的组成及性质,
归纳总结硝酸与金属反应的特点和规律是什么?
【学生1】浓硝酸和浓盐酸按1:3的体积比配制成的的混和溶液叫“王水”。王水的
氧化能力比硝酸强,不溶于硝酸的金(Au)和铂(Pt),可以溶解在王水中。
【学生 2】除 Au、Pt 等少数金属外,硝酸几乎可以氧化所有的金属,如 3Ag+
4HNO(稀)===3AgNO +NO↑+2HO;
3 3 2
【学生3】活泼金属与硝酸反应不生成H ,硝酸的浓度不同,还原产物不同。且浓硝
2
酸一般还原产物为 NO ,稀硝酸一般还原产物为 NO,极稀硝酸可为 NO、N 、
2 2 2
NH NO 等。
4 3
【学生4】常温下浓硝酸能使Fe、Al钝化,加热时反应。
【教师】评价、追问:与铜反应时,硝酸和硫酸有何不同? 学以致
用,了
【学生1】浓、稀硝酸均具有强氧化性,而浓硫酸具有强氧化性,稀硫酸不具有强氧
解硝酸
化性。
的用途
【学生2】不管是浓硝酸还是稀硝酸与铜反应均不需要加热,而浓硫酸与铜反应需要 及工业
制法,
加热,稀硫酸与铜不反应。
培养社
【问题2】探究3:少量铁粉或过量铁粉与稀硝酸反应的产物是什么?并写出化学方 会责任
感。
程式。
【学生】稀硝酸也具有强氧化性,只能将Fe氧化成Fe3+,但若铁粉过量,会发生反
应:Fe+2Fe3+==3Fe2+,所以少量铁粉或过量铁粉与稀硝酸反应的化学方程式分别为:
Fe ( 少 ) +4HNO ( 稀 )==Fe(NO )+NO↑+2HO 、 3Fe ( 多 )
3 3 3 2
+8HNO(稀)==3Fe(NO )+2NO↑+4HO。
3 3 2 2
【教师】评价、强调:NO ―在酸性条件下,就相当于硝酸溶液,具有强氧化性,因
3
此,在强酸性条件下NO ―与Fe2+不能大量共存,而在弱酸性或碱性条件下 NO ―与
3 3
Fe2+就可以大量共存。
【问题3】阅读教材P16页“思考与讨论”内容,回答硝酸有哪些用途?工业上如何
制硝酸?
【学生】硝酸是重要的化工原料,用于制化肥、农药、炸药、染料等。
【教师】评价、投影工业制硝酸流程:
化学方程式:N+3H 2NH ,N 发生还原反应。
2 2 3 2
4NH +5O=====4NO+6HO,NH 发生氧化反应。
3 2 2 3
2NO+O===2NO,NO发生氧化反应。 检测与
2 2
评价,
3NO 2 +H 2 O===2HNO 3 +NO,NO 2 既发生氧化反应,又发生还原反应。 发现问
题,调
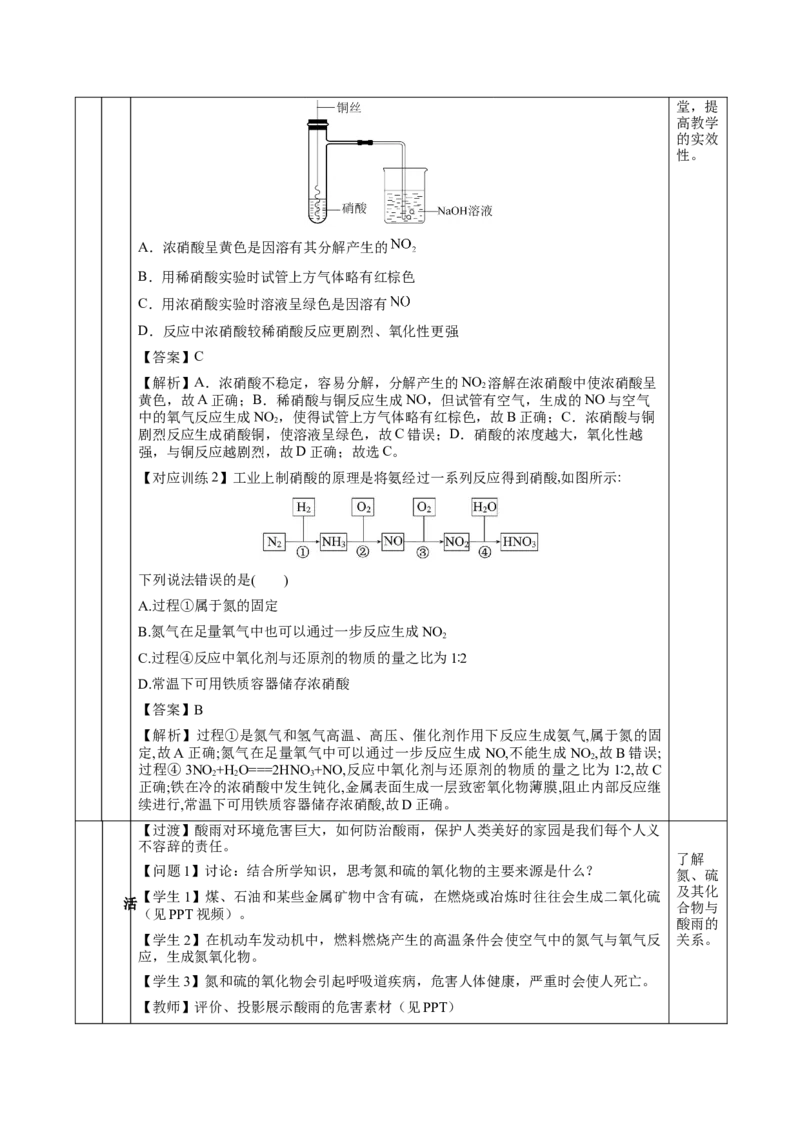
【对应训练1】硝酸与铜反应实验装置如图所示,下列有关叙述不正确的是( )
控课堂,提
高教学
的实效
性。
A.浓硝酸呈黄色是因溶有其分解产生的
B.用稀硝酸实验时试管上方气体略有红棕色
C.用浓硝酸实验时溶液呈绿色是因溶有
D.反应中浓硝酸较稀硝酸反应更剧烈、氧化性更强
【答案】C
【解析】A.浓硝酸不稳定,容易分解,分解产生的NO 溶解在浓硝酸中使浓硝酸呈
2
黄色,故A正确;B.稀硝酸与铜反应生成NO,但试管有空气,生成的NO与空气
中的氧气反应生成NO ,使得试管上方气体略有红棕色,故B正确;C.浓硝酸与铜
2
剧烈反应生成硝酸铜,使溶液呈绿色,故C错误;D.硝酸的浓度越大,氧化性越
强,与铜反应越剧烈,故D正确;故选C。
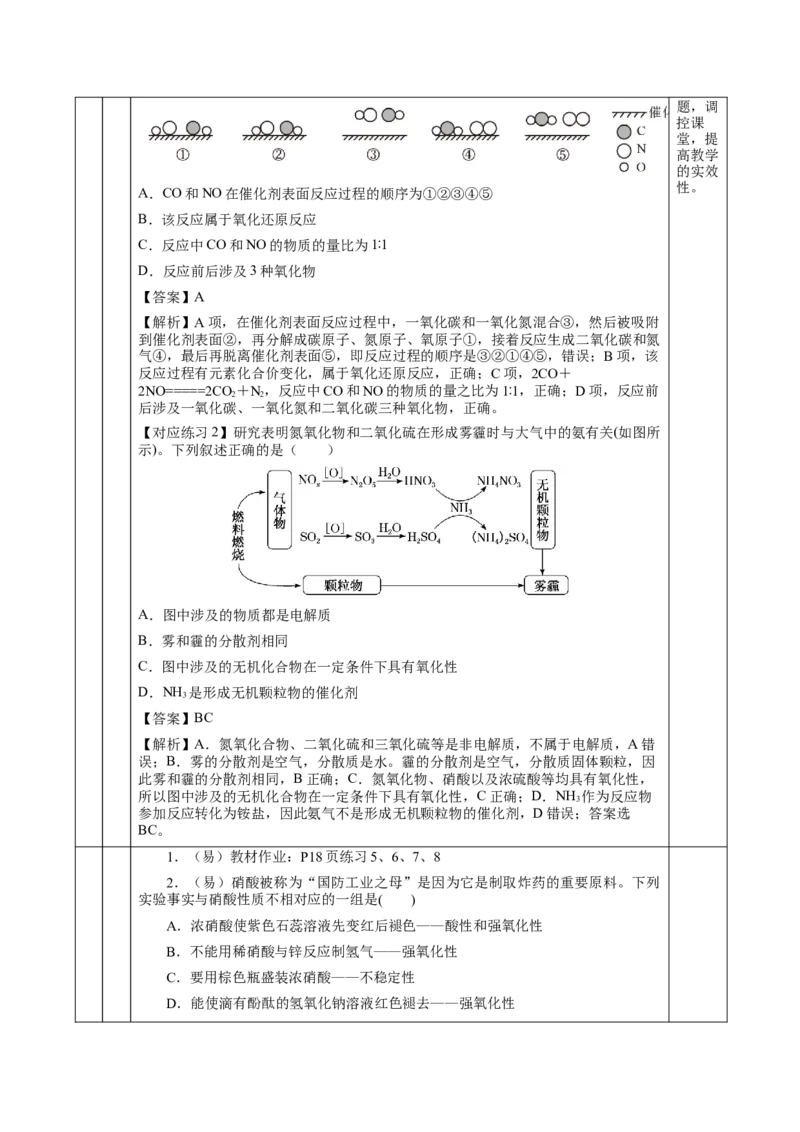
【对应训练2】工业上制硝酸的原理是将氨经过一系列反应得到硝酸,如图所示:
下列说法错误的是( )
A.过程①属于氮的固定
B.氮气在足量氧气中也可以通过一步反应生成NO
2
C.过程④反应中氧化剂与还原剂的物质的量之比为1∶2
D.常温下可用铁质容器储存浓硝酸
【答案】B
【解析】过程①是氮气和氢气高温、高压、催化剂作用下反应生成氨气,属于氮的固
定,故A正确;氮气在足量氧气中可以通过一步反应生成NO,不能生成NO ,故B错误;
2
过程④3NO +H O===2HNO+NO,反应中氧化剂与还原剂的物质的量之比为1∶2,故C
2 2 3
正确;铁在冷的浓硝酸中发生钝化,金属表面生成一层致密氧化物薄膜,阻止内部反应继
续进行,常温下可用铁质容器储存浓硝酸,故D正确。
【过渡】酸雨对环境危害巨大,如何防治酸雨,保护人类美好的家园是我们每个人义
不容辞的责任。
了解
【问题1】讨论:结合所学知识,思考氮和硫的氧化物的主要来源是什么?
氮、硫
及其化
【学生1】煤、石油和某些金属矿物中含有硫,在燃烧或冶炼时往往会生成二氧化硫
活
合物与
(见PPT视频)。
酸雨的
【学生2】在机动车发动机中,燃料燃烧产生的高温条件会使空气中的氮气与氧气反 关系。
应,生成氮氧化物。
【学生3】氮和硫的氧化物会引起呼吸道疾病,危害人体健康,严重时会使人死亡。
【教师】评价、投影展示酸雨的危害素材(见PPT)进一步
了解酸
雨的概
【问题2】观察教材P16页图5-51,思考酸雨的定义、形成原因及类型分别是什么?
念及形
成原
因,为
制定酸
雨的防
治方法
提供依
据。
活
【教师】投影图片、引导分析。
环 活
节 【学生1】定义:主要指 pH小于5.6 的雨水,其主要是含有硫酸和硝酸。
动
三
、 一 【学生2】成因:二氧化硫、氮氧化物以及它们在大气中发生反应后的生成物溶于雨
酸 、 水会形成酸雨。
雨
酸
及
防 雨
治
的 【教师】投影硫酸型酸雨:
形 【学生】板书:S→SO →SO →HSO :
2 3 2 4
成 【教师】投影硝酸型酸雨:NO →HNO:汽车尾气→NO――→NO ――→HNO
2 3 2 3
【对应练习1】下列关于氮及其化合物的说法错误的是( )
A. N 化学性质稳定,是因为分子内氮氮三键很强
2
B. NO、NO 均为大气污染气体,在大气中可稳定存在
2
C. 可用浓盐酸检测输送NH 的管道是否发生泄漏
3
D. HNO 具有强氧化性,可溶解铜、银等不活泼金属 检测与
3
评价,
【答案】B
发现问
【解析】A.N 分子中存在氮氮三键,氮氮三键很强不易断裂,N 化学性质比较稳 题,调
2 2
控课
定,故A正确;B.NO、NO 均为大气污染气体,其中NO遇氧气可以与之反应生成
2 堂,提
NO
2
,故B错误;C.浓盐酸易挥发,与氨气反应生成氯化铵,可以看到白烟,可用
高教学
浓盐酸检测输送N H 的管道是否发生泄漏,故C正确;D.HNO 具有强氧化性,可 的实效
3 3
以与铜和银反应,能溶解铜、银等不活泼金属,故D正确。 性。
【对应练习2】酸雨被称为“天堂的眼泪”,会造成水土酸性化、建筑物加速腐蚀等
危害。下列说法正确的是( )
A.酸雨不会对动植物产生任何影响
B.使用新型能源不会对酸雨的防治产生效果
C.酸雨指的是pH小于7的雨水
D.NO 和SO 的过度排放是形成酸雨的主要原因
2 2【答案】D
【解析】A.酸雨中含有硫酸和硝酸,因此酸雨会造成水土酸性化、建筑物加速腐
蚀、污染水源,危害人体健康,使农作物和植物的生长遭到破坏,故A错误;B.使
用新型能源,可以减少污染物的排放,有利于酸雨的防治,故B错误;C.pH小于
5.6的雨水为酸雨,故C错误;D.人类超量排放的NO 和SO ,是形成酸雨的主要原
2 2
因,故D正确;故选D。
活【过渡】正常雨水由于溶解了CO,其pH约为5.6,而酸雨的pH小于5.6,酸雨对人 了解酸
2
类生产、生活会造成很多危害。 雨的危
害,拓
【问题1】阅读教材P16页有关内容,回答酸雨有哪些危害?
展学生
【学生1】对人体的直接危害首先是它的刺激性,其次是它会形成硫酸雾和硫酸盐 知识
雾,其毒性比SO 大,能浸入人的肺部,引起肺水肿等疾病而使人致死。 面,关
2
注与化
【学生2】引起河流、湖泊的水体酸化,严重影响水生动物生长。 学有关
的社会
【学生3】破坏土壤、植被、森林。
热点问
【学生4】腐蚀金属、油漆、皮革、纺织品及建筑材料等。 题。
【学生5】渗入地下,可引起地下水酸化,酸化后的地下水中铝、铜、锌、镉等对人 认识环
体有害金属元素的含量会偏高。(图片见PPT) 境保护
活 和资源
【教师】评价、补充。 合理开
活
发的重
【问题2】讨论:结合教材P17页“研究与实践”栏目,回答如何测定雨水的pH及
动 要性,
防治酸雨?
深刻理
二
【教师】设问:雨水的pH测定方法是什么? 解 化
、 学、技
【学生1】下雨时用容器直接收集一些雨水作为样品,静置,以蒸馏水或自来水作为
术、社
酸 参照,观察并比较它们的外观;
会和环
雨 【学生2】用pH试纸(或pH计)测量雨水和蒸馏水的酸度并记录; 境之间
的相互
的 【教师】评价、强调:有条件的话,可连续取样并测定一段时间(如一周)内本地雨
关系,
危
水、地表水或自来水的pH,将得到的数据列表或作图,确定你所在地区本时间段内
培养勇
雨水等的平均酸度。 于承担
害
责任,
【教师】设问:有哪些防治酸雨的方法?
及 积极参
【学生1】调整能源结构,积极开发新能源。 与有关
防
化学问
【学生2】对煤(其中含硫为0.3%-5%)进行处理,如选洗加工、综合开发、在煤中加
治 题的社
入适量的生石灰、对排放的烟进行处理等。
会决策
【学生3】种植能够吸收SO 的有关树木(如臭椿、垂柳、柳杉)等。 的责任
2
意识。
【学生4】加强工厂废气的回收处理。
【学生5】改进汽车尾气的处理技术,控制尾气排放。
【教师】评价、
【对应练习1】目前,汽车尾气系统中均安装了催化转化器(含有催化剂),在催化剂
作用下,尾气中CO和NO发生反应,其微观过程如图所示。下列说法错误的是(
)
检测与
评价,
发现问题,调
控课
堂,提
高教学
的实效
性。
A.CO和NO在催化剂表面反应过程的顺序为①②③④⑤
B.该反应属于氧化还原反应
C.反应中CO和NO的物质的量比为1∶1
D.反应前后涉及3种氧化物
【答案】A
【解析】A项,在催化剂表面反应过程中,一氧化碳和一氧化氮混合③,然后被吸附
到催化剂表面②,再分解成碳原子、氮原子、氧原子①,接着反应生成二氧化碳和氮
气④,最后再脱离催化剂表面⑤,即反应过程的顺序是③②①④⑤,错误;B项,该
反应过程有元素化合价变化,属于氧化还原反应,正确;C项,2CO+
2NO=====2CO+N,反应中CO和NO的物质的量之比为1∶1,正确;D项,反应前
2 2
后涉及一氧化碳、一氧化氮和二氧化碳三种氧化物,正确。
【对应练习2】研究表明氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如图所
示)。下列叙述正确的是( )
A.图中涉及的物质都是电解质
B.雾和霾的分散剂相同
C.图中涉及的无机化合物在一定条件下具有氧化性
D.NH 是形成无机颗粒物的催化剂
3
【答案】BC
【解析】A.氮氧化合物、二氧化硫和三氧化硫等是非电解质,不属于电解质,A错
误;B.雾的分散剂是空气,分散质是水。霾的分散剂是空气,分散质固体颗粒,因
此雾和霾的分散剂相同,B正确;C.氮氧化物、硝酸以及浓硫酸等均具有氧化性,
所以图中涉及的无机化合物在一定条件下具有氧化性,C正确;D.NH 作为反应物
3
参加反应转化为铵盐,因此氨气不是形成无机颗粒物的催化剂,D错误;答案选
BC。
1.(易)教材作业:P18页练习5、6、7、8
2.(易)硝酸被称为“国防工业之母”是因为它是制取炸药的重要原料。下列
实验事实与硝酸性质不相对应的一组是( )
A.浓硝酸使紫色石蕊溶液先变红后褪色——酸性和强氧化性
B.不能用稀硝酸与锌反应制氢气——强氧化性
C.要用棕色瓶盛装浓硝酸——不稳定性
D.能使滴有酚酞的氢氧化钠溶液红色褪去——强氧化性【答案】D
【解析】D项中“滴有酚酞的氢氧化钠溶液红色褪去”,其褪色的原因可能是因
为硝酸的强氧化性把酚酞氧化而褪色,但也有可能是硝酸与氢氧化钠发生中和反应,
究竟是哪个原因,还需要实验验证,D项不准确。
3.(易)下列关于硝酸的说法中正确的是( )
A.硝酸和活泼金属反应生成氢气和相应的硝酸盐
B.硝酸的浓度越大,其氧化性越强
C.稀硝酸可溶解Fe(OH) 生成Fe(NO ) 和水
2 3 2
D.王水是浓硝酸和浓盐酸体积比为3∶1的混合物,能溶解金和铂
【答案】B
【解析】A.硝酸和活泼金属反应生成一氧化氮或二氧化氮气体和相应的硝酸
盐,A错误;B.硝酸的浓度越大,其氧化性越强,B正确;C.稀硝酸可溶解
Fe(OH) 生成Fe(NO ) 和水,C错误;D.王水是浓硝酸和浓盐酸体积比为1∶3的混合
2 3 3
物,能溶解金和铂,D错误;故选B。 及时巩
固、消
4.(中)在通风橱中进行下列实验:
化所
学,促
进对必
步骤 备知识
掌握,
评价教
学效
Fe表面产生大量无色气泡,液 Fe表面产生少量红棕色气泡
果,为
现象
面上方变为红棕色 后,迅速停止 后期优
环 化教学
节 下列说法中不正确的是( ) 方案提
四 供依
A.Ⅰ中气体有无色变红棕色的化学方程式为2NO+O===2NO
、 2 2 据。
课 B.Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
后
作
巩
C.对比Ⅰ、Ⅱ中现象,说明稀HNO
3
的氧化性强于浓HNO
3
业
固
设 D.红棕色气体的成分是NO
2
计
【答案】C
【解析】Ⅰ中由于稀硝酸有强的氧化性,与铁发生氧化还原反应,硝酸得到电子
被还原变为NO,气体为无色,当遇到空气时,发生反应:2NO+O===2NO ,气体
2 2
变为红棕色的NO ,A正确;在Ⅱ中浓硝酸有强的氧化性,在室温下遇铁、铝会使金
2
属表面氧化产生一层氧化物薄膜,对内层金属起保护作用,从而防止金属的进一步反
应,即发生钝化现象,因此不能进一步反应,这恰好说明浓硝酸的氧化性比稀硝酸
强,B正确;C错误。
5.(中)C、N、S的氧化物中许多是工业上重要的化工原料,但是当它们分散
到空气中时,会带来很多环境问题。下列有关这些元素的氧化物说法不正确的是(
)
A. 开发太阳能、水能、风能、氢能等有利于减少这些氧化物的产生
B. 这些氧化物使雨水的pH<7,我们把pH<7的雨水称之为酸雨
C. N的氧化物是造成光化学烟雾的主要原因
D. 温室效应与二氧化碳的排放有着直接的关系【答案】B
【解析】A.传统能源会产生C、N、S的氧化物,会带来很多环境问题,太阳
能、水能、风能、氢能为清洁能源,有利于减少这些元素的氧化物的产生,故A正
确;B.正常雨水中溶解二氧化碳气体,pH约为5.6,pH<5.6的雨水才称之为酸雨,
故B错误;C.N的氧化物是造成光化学烟雾的主要原因,故C正确;D.二氧化碳的排
放是引起温室效应的主要原因,故D正确。故选B。
6.(中)下列由废铜屑与浓硝酸反应制取NO 和Cu(NO ) 溶液的实验原理与装
2 3 2
置能达到实验目的的是( )
A.用装置甲制取NO B.用装置乙干燥NO
2 2
C.用装置丙收集NO D.用装置丁过滤得到Cu(NO )
2 3 2
溶液
【答案】D
【解析】A项,浓硝酸具有挥发性,挥发出的硝酸及生成的NO 会从长颈漏斗口
2
下端逸出,所以不能用装置甲制取二氧化氮,错误;B项,二氧化氮能与碱石灰反
应,所以不能用装置乙干燥二氧化氮,错误;C项,二氧化氮能与水反应生成硝酸和
一氧化氮,所以不能用装置丙收集二氧化氮,错误;D项,用装置丁过滤可以分离不
溶于水的铜和溶于水的硝酸铜得到硝酸铜溶液,正确。
7.(难)我国清代《本草纲目拾遗》中记叙无机药物335种,其中“强水”条
目下写道:“性最烈,能蚀五金……其水甚强,五金八石皆能穿第,惟玻璃可盛。”
这里的“强水”是指硝酸,下列有关硝酸的相关描述中正确的是( )
A.浓硝酸保存于无色试剂瓶中
B.向装有Fe(NO ) 溶液的试管中加入稀硫酸,可在试管口观察到红棕色气体
3 2
C.常温下,浓硝酸可以用铝制容器储存,说明浓硝酸与铝不反应
D.稀HNO 与金属反应时,可被还原为更低价态,说明稀HNO 氧化性强于浓
3 3
HNO
3
【答案】B
【解析】A项,浓硝酸见光会分解,要保存在棕色试剂瓶中,错误;B项,酸性
溶液中硝酸根离子有强氧化性,与亚铁离子发生氧化还原反应生成一氧化氮,一氧化
氮在试管口与氧气反应生成二氧化氮,可在试管口观察到红棕色气体,正确;C项,
常温下,铝与浓硝酸发生钝化,所以浓硝酸可以用铝制容器储存,错误;D项,与金
属反应时,稀硝酸被还原为一氧化氮,反应较慢,浓硝酸被还原为二氧化氮,反应较
快,所以稀硝酸的氧化性比浓硝酸弱,错误。
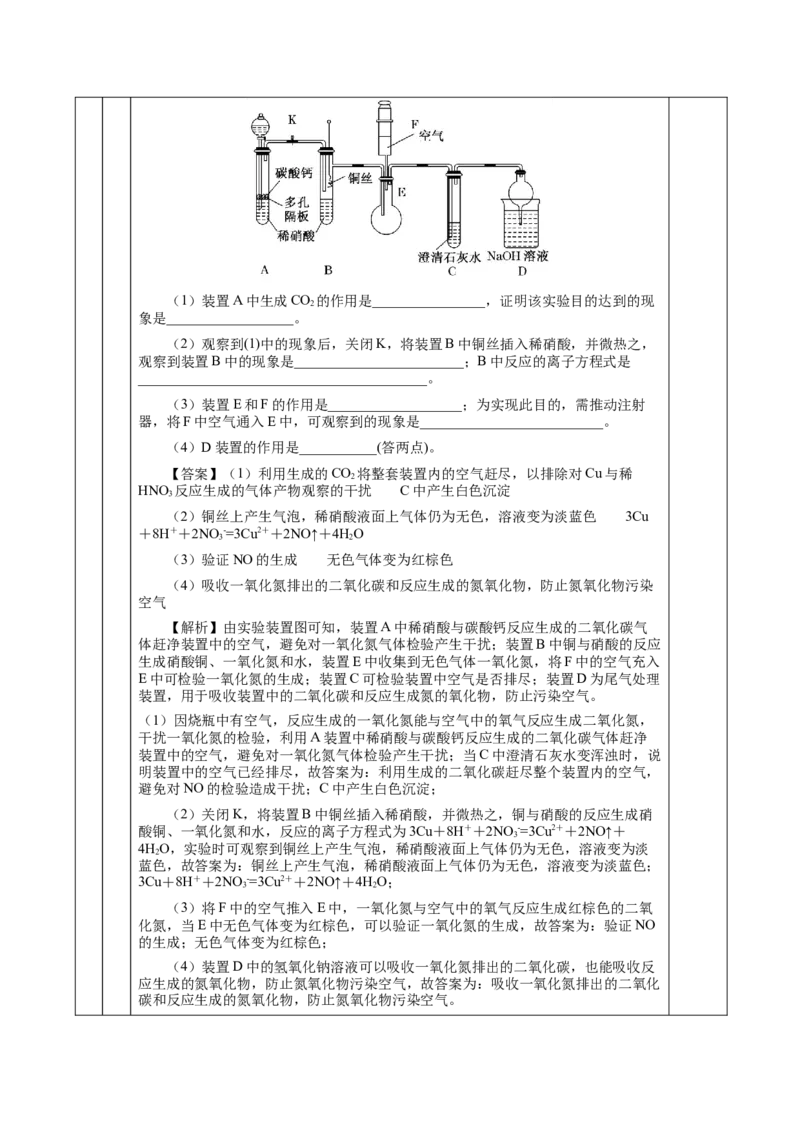
8.(中) 某校课外活动小组为了探究铜与稀硝酸反应产生的是NO气体,设计了
如下实验。实验装置如图所示:(1)装置A中生成CO 的作用是________________,证明该实验目的达到的现
2
象是__________________。
(2)观察到(1)中的现象后,关闭K,将装置B中铜丝插入稀硝酸,并微热之,
观察到装置B中的现象是________________________;B中反应的离子方程式是
_________________________________________。
(3)装置E和F的作用是___________________;为实现此目的,需推动注射
器,将F中空气通入E中,可观察到的现象是__________________________。
(4)D装置的作用是___________(答两点)。
【答案】(1)利用生成的CO 将整套装置内的空气赶尽,以排除对Cu与稀
2
HNO 反应生成的气体产物观察的干扰 C中产生白色沉淀
3
(2)铜丝上产生气泡,稀硝酸液面上气体仍为无色,溶液变为淡蓝色 3Cu
+8H++2NO -=3Cu2++2NO↑+4HO
3 2
(3)验证NO的生成 无色气体变为红棕色
(4)吸收一氧化氮排出的二氧化碳和反应生成的氮氧化物,防止氮氧化物污染
空气
【解析】由实验装置图可知,装置A中稀硝酸与碳酸钙反应生成的二氧化碳气
体赶净装置中的空气,避免对一氧化氮气体检验产生干扰;装置B中铜与硝酸的反应
生成硝酸铜、一氧化氮和水,装置E中收集到无色气体一氧化氮,将F中的空气充入
E中可检验一氧化氮的生成;装置C可检验装置中空气是否排尽;装置D为尾气处理
装置,用于吸收装置中的二氧化碳和反应生成氮的氧化物,防止污染空气。
(1)因烧瓶中有空气,反应生成的一氧化氮能与空气中的氧气反应生成二氧化氮,
干扰一氧化氮的检验,利用A装置中稀硝酸与碳酸钙反应生成的二氧化碳气体赶净
装置中的空气,避免对一氧化氮气体检验产生干扰;当C中澄清石灰水变浑浊时,说
明装置中的空气已经排尽,故答案为:利用生成的二氧化碳赶尽整个装置内的空气,
避免对NO的检验造成干扰;C中产生白色沉淀;
(2)关闭K,将装置B中铜丝插入稀硝酸,并微热之,铜与硝酸的反应生成硝
酸铜、一氧化氮和水,反应的离子方程式为3Cu+8H++2NO -=3Cu2++2NO↑+
3
4HO,实验时可观察到铜丝上产生气泡,稀硝酸液面上气体仍为无色,溶液变为淡
2
蓝色,故答案为:铜丝上产生气泡,稀硝酸液面上气体仍为无色,溶液变为淡蓝色;
3Cu+8H++2NO -=3Cu2++2NO↑+4HO;
3 2
(3)将F中的空气推入E中,一氧化氮与空气中的氧气反应生成红棕色的二氧
化氮,当E中无色气体变为红棕色,可以验证一氧化氮的生成,故答案为:验证NO
的生成;无色气体变为红棕色;
(4)装置D中的氢氧化钠溶液可以吸收一氧化氮排出的二氧化碳,也能吸收反
应生成的氮氧化物,防止氮氧化物污染空气,故答案为:吸收一氧化氮排出的二氧化
碳和反应生成的氮氧化物,防止氮氧化物污染空气。课堂
总结
第二节 氮及其化合物
第三课时 硝酸 酸雨及防治
一、硝酸
1、硝酸的性质
物理性质:纯硝酸是无色(久置可能呈黄色)、易挥发、有刺激性气味的液体,密度比水
大,能以任意比溶解于水,一元强酸。
化学性质:
酸的通性:HNO=== H+ + NO ―
3 3
不稳定性:4HNO=====4NO ↑+O↑+2HO
3 2 2 2
板书
强氧化性:与不活泼金属反应
设计
2.探究硝酸的强氧化性
Cu+4HNO(浓)===Cu(NO)+2NO ↑+2HO
3 3 2 2 2
3Cu+8HNO(稀)===3Cu(NO)+2NO↑+4HO;
3 3 2 2
C+4HNO(浓)====CO↑+4NO ↑+2HO。
3 2 2 2
二、酸雨及防治
1、酸雨的形成
2、酸雨的危害及防治
本课时的重点是硝酸的性质,学生阅读教材的基础上,通过观察浓、稀硝酸样品,了解硝
酸的物理性质。通过设凝、实验探究认识硝酸的不稳定性和强氧化性,得出硝酸的保存方法。
再通过创设问题情境,利用对比分析方法,在教师的引导下,学生充分讨论交流,认识浓、稀
硝酸与金属和非金属反应原理、反应产物的特殊性及规律,培养学生科学探究与创新意识、证
教学
据推理与模型认知的化学核心素养。最后通过视频素材、教材素材等了解酸雨的概念、成因及
反思 防治等,培养学生科学态度与社会责任的化学核心素养。