文档内容
第五章 化学生产中的重要非金属元素
第二节 氮及其化合物
第三课时 硝酸 酸雨及防治
【学习目标】1.通过实验探究、讨论交流,了解硝酸的主要性质—酸性、不稳定性和强氧化性,并能
从氧化还原反应角度分析反应原理,认识硝酸浓度不同其氧化性强弱不同、还原产物不同,知道硝酸是重
要的化工原料。
2.通过阅读思考、查阅资料,从含氮物质的性质及转化的视角,了解酸雨的概念,知道酸雨形成的主
要原因是二氧化氮和二氧化硫进入大气,酸雨会严重危害环境及防治方法,增强环境保护意识,培养社会
责任感。
【学习重点】硝酸的不稳定性和强氧化性
【学习难点】硝酸的强氧化性原理及应用
【课前预习】
旧知回顾:1.氮元素有多种价态,每种价态可对应一种混合物,请完成下表内容。
【答案要点】
氮的价态 -3 0 +1 +2 +3 +4 +5
物质举例 NH N NO NO NO NO 、NO NO
3 2 2 2 3 2 2 4 2 5
唯一碱 稳 笑气、可 无色、 酸酐、可 棕红及无色, 酸酐、
性质特征 性气体 定 溶、不反 不溶、 溶、有毒 可转化、有毒 可溶、
应、有毒 有毒 有毒
2. 硝酸(HNO)是一种常见的一元强酸,具有酸的通性,请举例说明。
3
【答案要点】与弱碱(如氢氧化铜)发生反应的离子方程式为 2H++Cu(OH) ==Cu2++2H O ;与碱性氧
2 2
化物(如氧化钠)反应的离子方程式为 2H++Na O==2Na++H O ;与弱酸强碱盐(如碳酸钙)反应:
2 2
CaCO +2H+==Ca(NO )+CO ↑+H O等。
3 3 2 2 2
新知预习:1.如何证明硝酸具有强氧化性,请举例说明。
【答案要点】浓、稀硝酸都具有强氧化性 ,能与不活泼金属铜发生反应,但还原产物不同,一般情
况下浓硝酸还原产物为NO ,稀硝酸还原为NO。反应的化学方程式分别为 Cu+4HNO(浓)===Cu(NO)
2 3 3 2
+2NO ↑+2HO、3Cu+8HNO(稀)===3Cu(NO)+2NO↑+4HO 。
2 2 3 3 2 2
2.硝酸与金属反应的特点和规律是什么?
【答案要点】①除 Au、Pt 等少数金属外,硝酸几乎可以氧化所有的金属,如 3Ag+
4HNO(稀)===3AgNO +NO↑+2HO;
3 3 2
②活泼金属与硝酸反应不生成H,硝酸的浓度不同,还原产物不同;
2
NO NO、N、NH NO 等NO
2 2 2 4 3
③常温下浓硝酸能使Fe、Al钝化,加热时反应。
【课中探究】情景导入:2023年2月14日,美国亚利桑那州图森市高速公路一卡车侧翻,引发危险物质硝酸泄
漏,产生大量红棕色烟雾,现场可闻到刺鼻的气味。消防人员运来纯碱进行处理,以防止其扩散造成更大
危害。
(见PPT视频)
一、硝酸
活动一、硝酸的性质
任务一、观察浓、稀HNO 样品,阅读教材P15页内容,思考总结硝酸具有哪些物理性质?
3
【答案要点】①纯硝酸是无色(久置可能呈黄色)、易挥发(沸点83℃)、有刺激性气味的液体,密
度(1.5027 g/cm3)比水大,能以任意比溶解于水。
②一元强酸,具有腐蚀性,使用时须注意防护何通风。
【注意】质量分数为69%的硝酸为浓硝酸,质量分数为98%以上的硝酸为发烟硝酸。因此浓硝酸为混
合物。
任务二、讨论交流:阅读教材P15页内容,结合所学知识,思考硝酸具有哪些化学性质?
【答案要点】①酸的通性:HNO=== H+ + NO ― 。如与碱(如NaOH)反应:H++OH-===H O;与碱
3 3 2
性氧化物(如NaO)反应:2H++NaO===2Na++HO;与弱酸盐(如CaCO ):CaCO +2H+===Ca2++CO↑
2 2 2 3 3 2
+HO。
2
②不稳定性:浓硝酸见光或受热易分解,化学方程式为4HNO=====4NO ↑+O↑+2HO。
3 2 2 2
【注意】a.长期存放的浓硝酸呈黄色是因为其分解生成的NO 溶于硝酸中,实验室常将浓硝酸保存在
2
棕色细口试剂瓶中,并放置在阴凉处。
b.我们学过的氯水以及常见的AgNO、AgCl等均用棕色试剂瓶保存,它们的共同特点
3
是见光易分解,因此,我们可推测HNO 具有不稳定性。
3
③强氧化性:如浓硝酸、稀硝酸与铜反应的化学方程式分别为:Cu+4HNO(浓)===Cu(NO) +2NO ↑+
3 3 2 2
2HO、3Cu+8HNO(稀)===3Cu(NO) +2NO↑+4HO;与非金属(碳)的反应:C+4HNO(浓)=====CO↑+
2 3 3 2 2 3 2
4NO ↑+2HO。
2 2
【对应练习】1.下列关于硝酸的说法不正确的是( )
A.浓硝酸是一种易挥发的液体混合物
B.浓硝酸在空气中敞口放置,因吸收水蒸气而浓度减小
C.浓硝酸不稳定,易分解生成二氧化氮、氧气和水
D.常温下,浓硝酸常保存在棕色试剂瓶中
【答案】B
【解析】浓硝酸是一种易挥发的液体混合物,在空气中敞口放置,其浓度会不断减小;浓硝酸不具有
吸水性,浓硝酸不稳定,见光易分解生成二氧化氮、氧气和水,所以浓硝酸常保存在棕色试剂瓶中。
2.下列反应中硝酸既能表现出酸性又表现出氧化性的是( )A.能使紫色石蕊溶液变为红色
B.与铜反应放出一氧化氮气体,生成硝酸铜
C.与碳酸钠反应放出二氧化碳气体,生成硝酸钠
D.与单质硫混合共热时生成硫酸和二氧化氮
【答案】B
【解析】A.硝酸使紫色石蕊溶液变为红色,只表现酸性,A不符合题意;B.硝酸与铜反应生成硝酸
铜、一氧化氮和水,既表现其强氧化性又表现其酸性,B符合题意;C.与碳酸钠反应放出二氧化碳气
体,表现的是硝酸的酸性,C不符合题意;D.硝酸与单质硫混合共热时生成硫酸和二氧化氮,表现的是
硝酸的强氧化性,D不符合题意;综上所述答案为B。
活动二、探究硝酸的强氧化性
任务一、实验探究:根据教材P15页【实验-5-8】(或实验视频),观察浓HNO 、稀HNO 和Cu的
3 3
反应的实验现象,并分析其原理,填写表格内容。
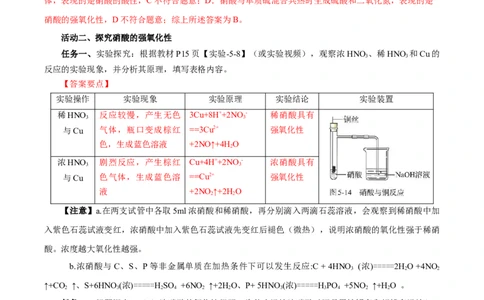
【答案要点】
实验操作 实验现象 实验原理 实验结论 实验装置
稀HNO 反应较慢,产生无色 3Cu+8H++2NO- 稀硝酸具有
3 3
与Cu 气体,瓶口变成棕红 ==3Cu2+ 强氧化性
色,生成蓝色溶液 +2NO↑+4HO
2
浓HNO 剧烈反应,产生棕红 Cu+4H++2NO- 浓硝酸具有
3 3
与Cu 色气体,生成蓝色溶 ==Cu2+ 强氧化性
液 +2NO↑+2H O
2 2
【注意】a.在两支试管中各取5ml浓硝酸和稀硝酸,再分别滴入两滴石蕊溶液,会观察到稀硝酸中加
入紫色石蕊试液变红,浓硝酸中加入紫色石蕊试液先变红后褪色(微热),说明浓硝酸的氧化性强于稀硝
酸。浓度越大氧化性越强。
b.浓硝酸与C、S、P等非金属单质在加热条件下可以发生反应:C + 4HNO (浓)=====2HO +4NO
3 2 2
↑+CO ↑、S+6HNO (浓)=====HSO +6NO ↑+2H O、P+ 5HNO(浓)=====HPO +5NO ↑+H O 。
2 3 2 4 2 2 3 3 4 2 2
任务二、问题探究:(1)浓硝酸的氧化性很强,为什么运输浓硝酸时还是用铁罐车和铝槽车运输?
【答案要点】有些金属如铁、铝等虽然能与稀硝酸或稀硫酸反应,但在常温下却可以用铁或铝制容器
来盛装浓硝酸或浓硫酸。这是因为常温下,铁、铝的表面被浓硝酸或浓硫酸氧化,生成了一层致密的氧化
物薄膜,这层薄膜阻止了酸与内层金属的进一步反应(又叫钝化)。当加热时,铁、铝会与浓硝酸或浓硫
酸发生反应。
(2)结合P教材102页“资料卡片”,回答“王水”的组成及性质,归纳总结硝酸与金属反应的特点
和规律是什么?【答案要点】①浓硝酸和浓盐酸按1:3的体积比配制成的的混和溶液叫“王水”。王水的氧化能力比
硝酸强,不溶于硝酸的金(Au)和铂(Pt),可以溶解在王水中。
②除Au、Pt等少数金属外,硝酸几乎可以氧化所有的金属,如 3Ag+4HNO(稀)===3AgNO +NO↑+
3 3
2HO;
2
③活泼金属与硝酸反应不生成H ,硝酸的浓度不同,还原产物不同。且浓硝酸一般还原产物为NO ,
2 2
稀硝酸一般还原产物为NO,极稀硝酸可为NO、N、NH NO 等。
2 2 4 3
④常温下浓硝酸能使Fe、Al钝化,加热时反应。
(3)少量铁粉或过量铁粉与稀硝酸反应的产物是什么?并写出化学方程式。
【答案要点】稀硝酸也具有强氧化性,只能将Fe氧化成Fe3+,但若铁粉过量,会发生反应:
Fe+2Fe3+==3Fe2+,所以少量铁粉或过量铁粉与稀硝酸反应的化学方程式分别为:
Fe +4HNO (稀)==Fe(NO )+NO↑+2HO、3Fe +8HNO(稀)==3Fe(NO )+2NO↑+4HO。
(少量) 3 3 3 2 (过量) 3 3 2 2
【注意】NO ―在酸性条件下,就相当于硝酸溶液,具有强氧化性,因此,在强酸性条件下NO ―与
3 3
Fe2+不能大量共存,而在弱酸性或碱性条件下NO ―与Fe2+就可以大量共存。
3
任务三、阅读教材P16页“思考与讨论”内容,回答硝酸有哪些用途?工业上如何制硝酸?
【答案要点】①硝酸是重要的化工原料,用于制化肥、农药、炸药、染料等。
②工业制硝酸流程:
化学方程式:N+3H 2NH ,N 发生还原反应。
2 2 3 2
4NH +5O=====4NO+6HO,NH 发生氧化反应。
3 2 2 3
2NO+O===2NO,NO发生氧化反应。
2 2
3NO +HO===2HNO +NO,NO 既发生氧化反应,又发生还原反应。
2 2 3 2
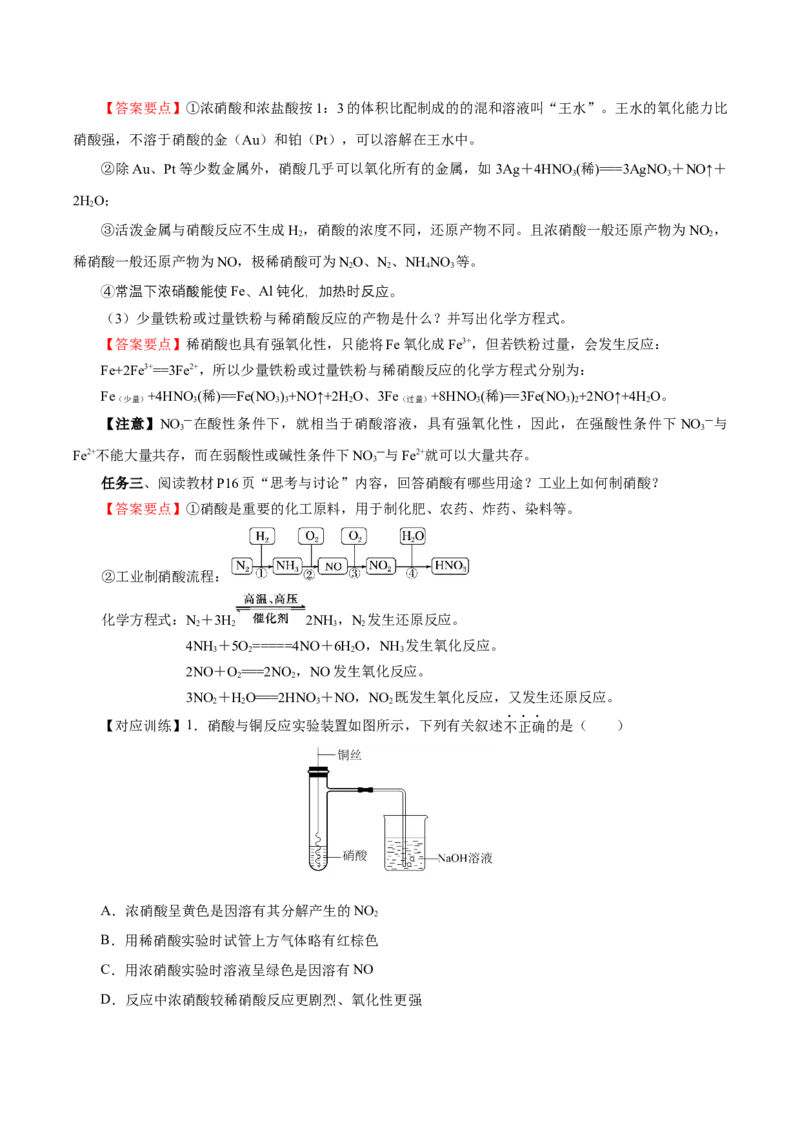
【对应训练】1.硝酸与铜反应实验装置如图所示,下列有关叙述不正确的是( )
A.浓硝酸呈黄色是因溶有其分解产生的NO
2
B.用稀硝酸实验时试管上方气体略有红棕色
C.用浓硝酸实验时溶液呈绿色是因溶有NO
D.反应中浓硝酸较稀硝酸反应更剧烈、氧化性更强【答案】C
【解析】A.浓硝酸不稳定,容易分解,分解产生的NO 溶解在浓硝酸中使浓硝酸呈黄色,故A正
2
确;B.稀硝酸与铜反应生成NO,但试管有空气,生成的NO与空气中的氧气反应生成NO ,使得试管上
2
方气体略有红棕色,故B正确;C.浓硝酸与铜剧烈反应生成硝酸铜,使溶液呈绿色,故C错误;D.硝
酸的浓度越大,氧化性越强,与铜反应越剧烈,故D正确;故选C。
2.工业上制硝酸的原理是将氨经过一系列反应得到硝酸,如图所示:
下列说法错误的是( )
A.过程①属于氮的固定
B.氮气在足量氧气中也可以通过一步反应生成NO
2
C.过程④反应中氧化剂与还原剂的物质的量之比为1∶2
D.常温下可用铁质容器储存浓硝酸
【答案】B
【解析】过程①是氮气和氢气高温、高压、催化剂作用下反应生成氨气,属于氮的固定,故A正确;氮气
在足量氧气中可以通过一步反应生成NO,不能生成NO ,故B错误; 过程④3NO +H O===2HNO+NO,反应
2 2 2 3
中氧化剂与还原剂的物质的量之比为1∶2,故C正确;铁在冷的浓硝酸中发生钝化,金属表面生成一层致密氧化
物薄膜,阻止内部反应继续进行,常温下可用铁质容器储存浓硝酸,故D正确。
二、酸雨及防治
活动一、酸雨的形成
任务一、讨论交流:结合所学知识,思考氮和硫的氧化物的主要来源是什么?
【答案要点】①煤、石油和某些金属矿物中含有硫,在燃烧或冶炼时往往会生成二氧化硫(见PPT视
频)。
②在机动车发动机中,燃料燃烧产生的高温条件会使空气中的氮气与氧气反应,生成氮氧化物。
③氮和硫的氧化物会引起呼吸道疾病,危害人体健康,严重时会使人死亡。任务二、观察教材P16页图5-51,思考酸雨的定义、形成原因及类型分别是什么?
【答案要点】①定义:主要指 pH小于5.6 的雨水,其主要是含有硫酸和硝酸。
②成因:二氧化硫、氮氧化物以及它们在大气中发生反应后的生成物溶于雨水会形成酸雨。正常雨水
由于溶解了CO,其pH约为5.6,而酸雨的pH小于5.6。
2
③类型:硫酸型酸雨:S→SO →SO →HSO :
2 3 2 4
硝酸型酸雨:NO →HNO:汽车尾气→NO――→NO ――→HNO
2 3 2 3
【对应练习】1.下列关于氮及其化合物的说法错误的是( )
A. N 化学性质稳定,是因为分子内氮氮三键很强
2
B. NO、NO 均为大气污染气体,在大气中可稳定存在
2
C. 可用浓盐酸检测输送NH 的管道是否发生泄漏
3
D. HNO 具有强氧化性,可溶解铜、银等不活泼金属
3
【答案】B
【解析】A.N 分子中存在氮氮三键,氮氮三键很强不易断裂,N 化学性质比较稳定,故A正确;B.
2 2
NO、NO 均为大气污染气体,其中NO遇氧气可以与之反应生成NO ,故B错误;C.浓盐酸易挥发,与
2 2
氨气反应生成氯化铵,可以看到白烟,可用浓盐酸检测输送N H 的管道是否发生泄漏,故 C正确;D.
3
HNO 具有强氧化性,可以与铜和银反应,能溶解铜、银等不活泼金属,故D正确。
3
2.酸雨被称为“天堂的眼泪”,会造成水土酸性化、建筑物加速腐蚀等危害。下列说法正确的是
( )
A.酸雨不会对动植物产生任何影响
B.使用新型能源不会对酸雨的防治产生效果
C.酸雨指的是pH小于7的雨水
D.NO 和SO 的过度排放是形成酸雨的主要原因
2 2
【答案】D
【解析】A.酸雨中含有硫酸和硝酸,因此酸雨会造成水土酸性化、建筑物加速腐蚀、污染水源,危
害人体健康,使农作物和植物的生长遭到破坏,故A错误;B.使用新型能源,可以减少污染物的排放,有利于酸雨的防治,故B错误;C.pH小于5.6的雨水为酸雨,故C错误;D.人类超量排放的NO 和
2
SO ,是形成酸雨的主要原因,故D正确;故选D。
2
活动二、酸雨的危害及防治
任务一、阅读教材P16页有关内容,回答酸雨有哪些危害?
【答案要点】①对人体的直接危害首先是它的刺激性,其次是它会形成硫酸雾和硫酸盐雾,其毒性比
SO 大,能浸入人的肺部,引起肺水肿等疾病而使人致死。
2
②引起河流、湖泊的水体酸化,严重影响水生动物生长。
③破坏土壤、植被、森林。
④腐蚀金属、油漆、皮革、纺织品及建筑材料等。
⑤渗入地下,可引起地下水酸化,酸化后的地下水中铝、铜、锌、镉等对人体有害金属元素的含量会
偏高。(图片见PPT)
任务二、讨论交流:结合教材P17页“研究与实践”栏目,回答如何测定雨水的pH及防治酸雨?
【答案要点】(1)雨水的pH测定:
①下雨时用容器直接收集一些雨水作为样品,静置,以蒸馏水或自来水作为参照,观察并比较它们的
外观;
②用pH试纸(或pH计)测量雨水和蒸馏水的酸度并记录;
③有条件的话,可连续取样并测定一段时间(如一周)内本地雨水、地表水或自来水的 pH,将得到
的数据列表或作图,确定你所在地区本时间段内雨水等的平均酸度。
(2)防治酸雨的方法:
①调整能源结构,积极开发新能源。
②对煤(其中含硫为0.3%-5%)进行处理,如选洗加工、综合开发、在煤中加入适量的生石灰、对排放
的烟进行处理等。
③种植能够吸收SO 的有关树木(如臭椿、垂柳、柳杉)等。
2
④加强工厂废气的回收处理。
⑤改进汽车尾气的处理技术,控制尾气排放。
【对应练习】1.目前,汽车尾气系统中均安装了催化转化器(含有催化剂),在催化剂作用下,尾气中
CO和NO发生反应,其微观过程如图所示。下列说法错误的是( )
A.CO和NO在催化剂表面反应过程的顺序为①②③④⑤
B.该反应属于氧化还原反应C.反应中CO和NO的物质的量比为1∶1
D.反应前后涉及3种氧化物
【答案】A
【解析】A项,在催化剂表面反应过程中,一氧化碳和一氧化氮混合③,然后被吸附到催化剂表面
②,再分解成碳原子、氮原子、氧原子①,接着反应生成二氧化碳和氮气④,最后再脱离催化剂表面⑤,
即反应过程的顺序是③②①④⑤,错误;B项,该反应过程有元素化合价变化,属于氧化还原反应,正
确;C项,2CO+2NO=====2CO+N,反应中CO和NO的物质的量之比为1∶1,正确;D项,反应前后
2 2
涉及一氧化碳、一氧化氮和二氧化碳三种氧化物,正确。
2.研究表明氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如图所示)。下列叙述正确的是(
)
A.图中涉及的物质都是电解质
B.雾和霾的分散剂相同
C.图中涉及的无机化合物在一定条件下具有氧化性
D.NH 是形成无机颗粒物的催化剂
3
【答案】BC
【解析】A.氮氧化合物、二氧化硫和三氧化硫等是非电解质,不属于电解质,A错误;B.雾的分散
剂是空气,分散质是水。霾的分散剂是空气,分散质固体颗粒,因此雾和霾的分散剂相同,B正确;C.
氮氧化物、硝酸以及浓硫酸等均具有氧化性,所以图中涉及的无机化合物在一定条件下具有氧化性,C正
确;D.NH 作为反应物参加反应转化为铵盐,因此氨气不是形成无机颗粒物的催化剂,D错误;答案选
3
BC。
【课后巩固】1.(易)教材作业:P18页练习5、6、7、8
2.(易)硝酸被称为“国防工业之母”是因为它是制取炸药的重要原料。下列实验事实与硝酸性质
不相对应的一组是( )
A.浓硝酸使紫色石蕊溶液先变红后褪色——酸性和强氧化性
B.不能用稀硝酸与锌反应制氢气——强氧化性
C.要用棕色瓶盛装浓硝酸——不稳定性D.能使滴有酚酞的氢氧化钠溶液红色褪去——强氧化性
【答案】D
【解析】D项中“滴有酚酞的氢氧化钠溶液红色褪去”,其褪色的原因可能是因为硝酸的强氧化性把
酚酞氧化而褪色,但也有可能是硝酸与氢氧化钠发生中和反应,究竟是哪个原因,还需要实验验证,D项
不准确。
3.(易)下列关于硝酸的说法中正确的是( )
A.硝酸和活泼金属反应生成氢气和相应的硝酸盐
B.硝酸的浓度越大,其氧化性越强
C.稀硝酸可溶解Fe(OH) 生成Fe(NO ) 和水
2 3 2
D.王水是浓硝酸和浓盐酸体积比为3∶1的混合物,能溶解金和铂
【答案】B
【解析】A.硝酸和活泼金属反应生成一氧化氮或二氧化氮气体和相应的硝酸盐,A错误;B.硝酸的
浓度越大,其氧化性越强,B正确;C.稀硝酸可溶解Fe(OH) 生成Fe(NO ) 和水,C错误;D.王水是浓
2 3 3
硝酸和浓盐酸体积比为1∶3的混合物,能溶解金和铂,D错误;故选B。
4.(中)在通风橱中进行下列实验:
步骤
Fe表面产生大量无色气 Fe表面产生少量红棕色气
现象
泡,液面上方变为红棕色 泡后,迅速停止
下列说法中不正确的是( )
A.Ⅰ中气体有无色变红棕色的化学方程式为2NO+O===2NO
2 2
B.Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C.对比Ⅰ、Ⅱ中现象,说明稀HNO 的氧化性强于浓HNO
3 3
D.红棕色气体的成分是NO
2
【答案】C
【解析】Ⅰ中由于稀硝酸有强的氧化性,与铁发生氧化还原反应,硝酸得到电子被还原变为 NO,气
体为无色,当遇到空气时,发生反应:2NO+O===2NO ,气体变为红棕色的NO ,A正确;在Ⅱ中浓硝
2 2 2
酸有强的氧化性,在室温下遇铁、铝会使金属表面氧化产生一层氧化物薄膜,对内层金属起保护作用,从
而防止金属的进一步反应,即发生钝化现象,因此不能进一步反应,这恰好说明浓硝酸的氧化性比稀硝酸
强,B正确;C错误。5.(中)C、N、S的氧化物中许多是工业上重要的化工原料,但是当它们分散到空气中时,会带来很
多环境问题。下列有关这些元素的氧化物说法不正确的是( )
A. 开发太阳能、水能、风能、氢能等有利于减少这些氧化物的产生
B. 这些氧化物使雨水的pH<7,我们把pH<7的雨水称之为酸雨
C. N的氧化物是造成光化学烟雾的主要原因
D. 温室效应与二氧化碳的排放有着直接的关系
【答案】B
【解析】A.传统能源会产生C、N、S的氧化物,会带来很多环境问题,太阳能、水能、风能、氢能
为清洁能源,有利于减少这些元素的氧化物的产生,故A正确;B.正常雨水中溶解二氧化碳气体,pH约
为5.6,pH<5.6的雨水才称之为酸雨,故B错误;C.N的氧化物是造成光化学烟雾的主要原因,故C正
确;D.二氧化碳的排放是引起温室效应的主要原因,故D正确。故选B。
6.(中)下列由废铜屑与浓硝酸反应制取NO 和Cu(NO ) 溶液的实验原理与装置能达到实验目的的
2 3 2
是( )
A.用装置甲制取NO B.用装置乙干燥NO
2 2
C.用装置丙收集NO D.用装置丁过滤得到Cu(NO ) 溶液
2 3 2
【答案】D
【解析】A项,浓硝酸具有挥发性,挥发出的硝酸及生成的NO 会从长颈漏斗口下端逸出,所以不能
2
用装置甲制取二氧化氮,错误;B项,二氧化氮能与碱石灰反应,所以不能用装置乙干燥二氧化氮,错
误;C项,二氧化氮能与水反应生成硝酸和一氧化氮,所以不能用装置丙收集二氧化氮,错误;D项,用
装置丁过滤可以分离不溶于水的铜和溶于水的硝酸铜得到硝酸铜溶液,正确。
7.(难)我国清代《本草纲目拾遗》中记叙无机药物335种,其中“强水”条目下写道:“性最烈,
能蚀五金……其水甚强,五金八石皆能穿第,惟玻璃可盛。”这里的“强水”是指硝酸,下列有关硝酸的
相关描述中正确的是( )
A.浓硝酸保存于无色试剂瓶中
B.向装有Fe(NO ) 溶液的试管中加入稀硫酸,可在试管口观察到红棕色气体
3 2
C.常温下,浓硝酸可以用铝制容器储存,说明浓硝酸与铝不反应
D.稀HNO 与金属反应时,可被还原为更低价态,说明稀HNO 氧化性强于浓HNO
3 3 3【答案】B
【解析】A项,浓硝酸见光会分解,要保存在棕色试剂瓶中,错误;B项,酸性溶液中硝酸根离子有
强氧化性,与亚铁离子发生氧化还原反应生成一氧化氮,一氧化氮在试管口与氧气反应生成二氧化氮,可
在试管口观察到红棕色气体,正确;C项,常温下,铝与浓硝酸发生钝化,所以浓硝酸可以用铝制容器储
存,错误;D项,与金属反应时,稀硝酸被还原为一氧化氮,反应较慢,浓硝酸被还原为二氧化氮,反应
较快,所以稀硝酸的氧化性比浓硝酸弱,错误。
8.(中) 某校课外活动小组为了探究铜与稀硝酸反应产生的是NO气体,设计了如下实验。实验装置
如图所示:
(1)装置A中生成CO 的作用是________________,证明该实验目的达到的现象是
2
__________________。
(2)观察到(1)中的现象后,关闭K,将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的现
象是________________________;B中反应的离子方程式是
_________________________________________。
(3)装置E和F的作用是___________________;为实现此目的,需推动注射器,将F中空气通入E
中,可观察到的现象是__________________________。
(4)D装置的作用是___________(答两点)。
【答案】(1)利用生成的CO 将整套装置内的空气赶尽,以排除对Cu与稀HNO 反应生成的气体产
2 3
物观察的干扰 C中产生白色沉淀
(2)铜丝上产生气泡,稀硝酸液面上气体仍为无色,溶液变为淡蓝色 3Cu+8H++2NO -=3Cu2+
3
+2NO↑+4HO
2
(3)验证NO的生成 无色气体变为红棕色
(4)吸收一氧化氮排出的二氧化碳和反应生成的氮氧化物,防止氮氧化物污染空气
【解析】由实验装置图可知,装置A中稀硝酸与碳酸钙反应生成的二氧化碳气体赶净装置中的空气,
避免对一氧化氮气体检验产生干扰;装置B中铜与硝酸的反应生成硝酸铜、一氧化氮和水,装置E中收集到无色气体一氧化氮,将F中的空气充入E中可检验一氧化氮的生成;装置C可检验装置中空气是否排
尽;装置D为尾气处理装置,用于吸收装置中的二氧化碳和反应生成氮的氧化物,防止污染空气。
(1)因烧瓶中有空气,反应生成的一氧化氮能与空气中的氧气反应生成二氧化氮,干扰一氧化氮的检
验,利用A装置中稀硝酸与碳酸钙反应生成的二氧化碳气体赶净装置中的空气,避免对一氧化氮气体检验
产生干扰;当C中澄清石灰水变浑浊时,说明装置中的空气已经排尽,故答案为:利用生成的二氧化碳赶
尽整个装置内的空气,避免对NO的检验造成干扰;C中产生白色沉淀;
(2)关闭K,将装置B中铜丝插入稀硝酸,并微热之,铜与硝酸的反应生成硝酸铜、一氧化氮和
水,反应的离子方程式为3Cu+8H++2NO -=3Cu2++2NO↑+4HO,实验时可观察到铜丝上产生气泡,稀
3 2
硝酸液面上气体仍为无色,溶液变为淡蓝色,故答案为:铜丝上产生气泡,稀硝酸液面上气体仍为无色,
溶液变为淡蓝色;3Cu+8H++2NO -=3Cu2++2NO↑+4HO;
3 2
(3)将F中的空气推入E中,一氧化氮与空气中的氧气反应生成红棕色的二氧化氮,当E中无色气
体变为红棕色,可以验证一氧化氮的生成,故答案为:验证NO的生成;无色气体变为红棕色;
(4)装置D中的氢氧化钠溶液可以吸收一氧化氮排出的二氧化碳,也能吸收反应生成的氮氧化物,
防止氮氧化物污染空气,故答案为:吸收一氧化氮排出的二氧化碳和反应生成的氮氧化物,防止氮氧化物
污染空气。