文档内容
《原子结构与性质》基础过关单元检测
学校:___________姓名:___________班级:___________考号:___________
一、单选题(16小题,每小题3分,共48分)
1.下列有关原子轨道的叙述中正确的是
A.硅原子的2s轨道能量较3p轨道高
B.锂原子的2s轨道与5s轨道均为球形
C.p能级的原子轨道呈哑铃形,随着能层序数的增加,p能级原子轨道数也在增多
D.第四能层最多可容纳16个电子
2.下列关于能层和能级的说法正确的是
A.原子核外每能层最多可容纳的电子数为n2
B.能层序数较大的能级,能量不一定较高
C.同一原子中,1s、2s、3s电子的能量逐渐减小
D.同一原子中,2p、3p、4p能容纳的电子数逐渐增多
3.下列各项叙述错误的是
A.若硫原子核外电子排布图为 ,则违反了泡利原理
B.若21号Sc元素的基态原子电子排布式为 ,则违反了构造原理
C.铍原子的核外电子排布图为 ,符合洪特规则和泡利原理
D.原子的电子排布式由 能释放特定能量产生发射光谱
4.下列叙述正确的是
A.基态铝原子核外有三个单电子 B.铜原子的外围电子排布式是:3d94s2
C.[Ar]3d24s2是基态钛原子的电子排布 D.铬原子的电子排布式是:
1s22s22p63s23p64s13d5
5.下列关于元素周期表与原子结构的说法正确的是
A.所有的非金属元素都分布在p区
B.金属性: ,因此第一电离能:
C.价电子排布式为 的元素位于第四周期第VIII族
D.最外层电子数均为2的两种元素一定位于同一族
6.下列有关元素周期表的说法正确的是
A.按照核外电子排布,可把元素周期表划分为s、 p、d、 f四个区
B.元素周期表中,氟元素的电负性最大,第一电离能也最大
C.元素周期表的各个周期总是从ns能级开始,以mp能级结束
D.元素周期表中,从第IIIB族到第IIB族的10个纵列的元素全都是金属元素7.元素性质呈周期性变化的决定因素是
A.元素原子的核外电子排布呈周期性变化 B.元素相对原子质量依次递增
C.元素原子半径大小呈周期性变化 D.元素的最高正化合价呈周期性变化
8.同周期元素X、Y、Z,已知它们的最高价氧化物对应水化物的酸性强弱顺序是:
,则下列各判断中正确的是
A.原子半径:X>Y>Z
B.非金属性:X>Y>Z
C.气态氢化物的稳定性:
D.原子序数:Z>Y>X
9.硒(Se)的原子序数为34,与氧、硫同主族,下列说法正确的是
A.硒的最高价是+6价,所以只有一种氧化物SeO
3
B.HSe的热稳定性比HS差,还原性比HS弱
2 2 2
C.氧、硫、硒三种元素的电负性递减
D.原子序数为33的元素是砷(As),则砷原子的第一电离能小于硒原子的第一电离能
10.下列关于Na、Mg、C、N、O、Cl元素及其化合物的说法正确的是
A.原子半径:r(O)>r(N)>r(C)
B.N的非金属性比C的弱
C.NaOH的碱性比Mg(OH) 的强
2
D.Cl形成的最高价氧化物对应的水化物是HClO
3
11.短周期主族元素X、Y、Z、W的原子序数依次增大,其中X是地壳中含量最多的元素,
X原子的电子数与Y、Z、W原子的最外层电子数之和相等。Y、Z原子的最外层电子数之
和与W的最外层电子数相等,且X、Y可形成两种常见的离子化合物,且晶体中的阴阳离
子个数比均为1∶2,下列说法不正确的是
A.工业上通常采用电解法制备Y和Z的单质
B.W和X形成的物质 是酸性氧化物,能与水反应生成W的最高价含氧酸
C.与水反应的剧烈程度:Y>Z
D.简单离子半径大小:X>Y>Z
12.已知 N 是阿伏加德罗常数的值,下列说法错误的是
A
A.3 g 3He 含有的中子数为 1N
A
B.22.4L(标准状况)氮气中含有 7 N 个中子
A
C.1 mol K Cr O 被还原为 Cr3+转移的电子数为 6 N
2 2 7 A
D.48 g 正丁烷和 10 g 异丁烷的混合物中共价键数目为 13 N
A
13.d轨道中电子排布成 而不是排布成 其最
直接的根据是
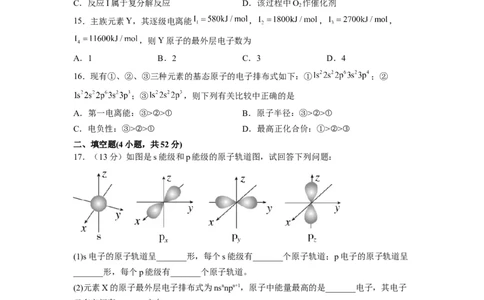
A.洪特规则 B.泡利不相容原理 C.能量最低原则 D.能量守恒原理14.大气中氮氧化物和碳氢化合物受紫外线
作用可产生二次污染物光化学烟雾,其中某些反应过程如图所示。下列说法正确的是
A.丙烯发生氧化反应生成甲醛和乙醛 B.O 和O 互为同位素
2 3
C.反应I属于复分解反应 D.该过程中O 作催化剂
2
15.主族元素Y,其逐级电离能 , , ,
,则Y原子的最外层电子数为
A.1 B.2 C.3 D.4
16.现有①、②、③三种元素的基态原子的电子排布式如下:① ;②
;③ ,则下列有关比较中正确的是
A.第一电离能:③>②>① B.原子半径:③>②>①
C.电负性:③>②>① D.最高正化合价:①>②>③
二、填空题(4小题,共52分)
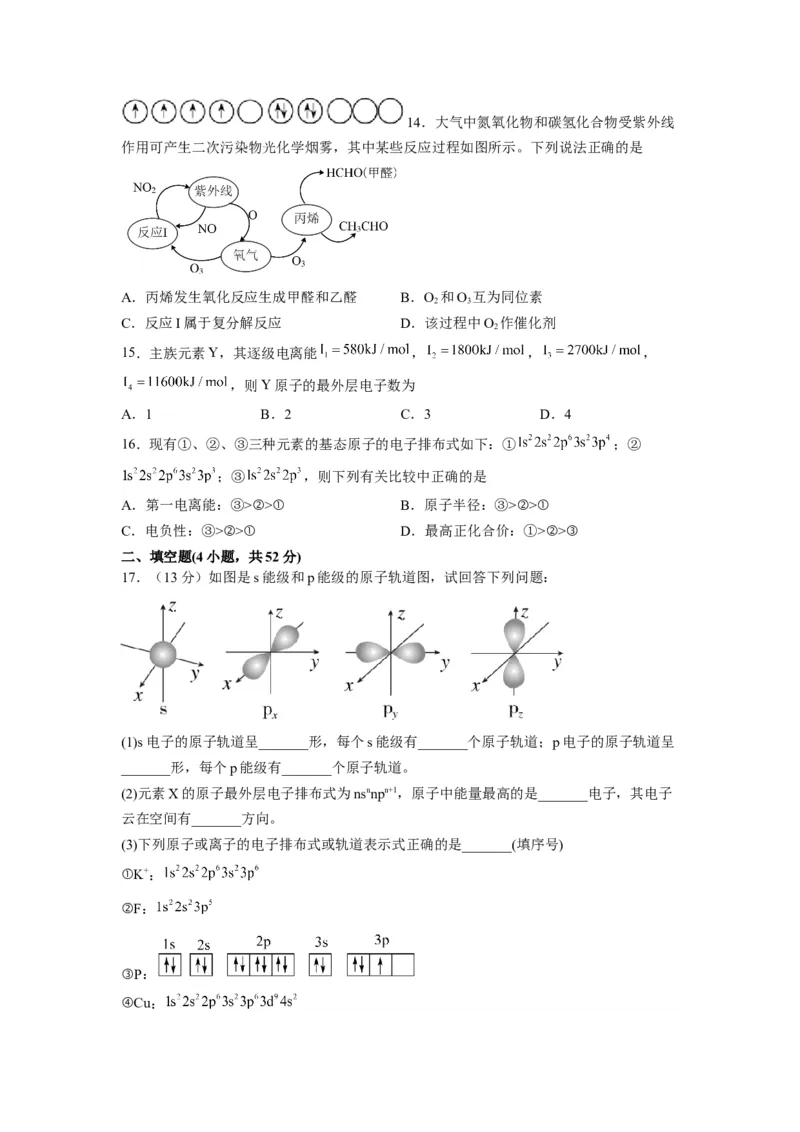
17.(13分)如图是s能级和p能级的原子轨道图,试回答下列问题:
(1)s电子的原子轨道呈_______形,每个s能级有_______个原子轨道;p电子的原子轨道呈
_______形,每个p能级有_______个原子轨道。
(2)元素X的原子最外层电子排布式为nsnnpn+1,原子中能量最高的是_______电子,其电子
云在空间有_______方向。
(3)下列原子或离子的电子排布式或轨道表示式正确的是_______(填序号)
①K+:
②F:
③P:
④Cu:⑤Fe2+:
⑥Mg:
⑦O:
18.(13分)根据原子核外电子排布规则,回答下列问题:
(1)基态N原子中,核外电子占据的最高能层的符号是____________,占据该能层电子的电
子云轮廓图形状为____________。
(2)写出基态 Cr原子的价电子排布式:____________;
24
(3)写出基态N的原子核外电子排布图:____________;
(4)若将基态 Si的电子排布式写成1s22s22p63s33p1,则它违背了____________;
14
(5)Fe3+比Fe2+的稳定性更___________(填“强”或“弱”),从结构上分析原因是
____________;
(6)元素被科学家称之为人体微量元素中的“防癌之王”,其原子的价层电子排布式为
4s24p4,该元素的名称是___________。
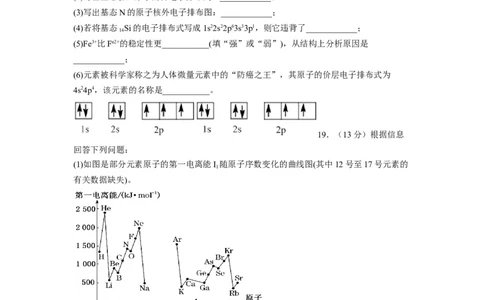
19.(13分)根据信息
回答下列问题:
(1)如图是部分元素原子的第一电离能I 随原子序数变化的曲线图(其中12号至17号元素的
1
有关数据缺失)。
①认真分析图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离
能的大小范围为___________<Al<___________(填元素符号);
②图中Ge元素中未成对电子有___________个;
③图中的C和N可以形成分子(CN) ,该分子中键与键之间的夹角为180°,并有对称性,
2
分子中每个原子最外层均满足8电子稳定结构,其结构式为___________,1个分子中含有
___________个π键。
(2)已知元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出部分元素的电负性:
元素 Al B Be C Cl F Li
电负
2.0 1.5 2.5 3.0 4.0 1.0
性
元素 Mg N Na O P S Si
电负
1.2 3.0 0.9 3.5 2.1 2.5 1.8
性
已知:两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于
1.7时,形成共价键。
①通过分析电负性值变化规律,确定Al元素电负性值的最小范围____;
②判断下列物质是离子化合物还是共价化合物:
A.LiN B.PCl C.MgCl D.SiC
3 3 2
I.属于离子化合物的是____;II.属于共价化合物的是____;
20.(13分)如表是元素周期表的一部分。表中所列的字母分别代表一种化学元素:
(1)I的最高化合价为____;K的元素名称为____。
(2)基态时G元素原子的电子排布式___,J元素原子的外围电子排布式___。
(3)下列对比正确的是___。
a.原子半径H>G>B>A b.第一电离能E>D>C>B
c.电负性A>H>G>Q d.最高价氧化物的水化物酸性B>A>H>G
(4)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙述不正
确的是____。
a.L位于元素周期表中第5周期ⅠA族,属于s区元素
b. O位于元素周期表中第7周期ⅧB族,属于d区元素
c.M的外围电子排布式为6s1,属于ds区元素
d.H所在族的外围电子排布式为ns2np2,属于p区元素(5)元素B和C的气态氢化物热稳定性较强的是____(填化学式)。倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育