文档内容
第一章 物质及其变化
单元检测
一、选择题(本题包括16小题,每小题3分,共48分,每小题只有一个选项符合题意。)
1.科学家在《自然》杂志上报告,他们用DNA制造出了一种臂长只有7纳米的纳米级镊子,以便能够
镊起分子或原子并对它们随意组合。下列分散系中的分散质的粒子直径与纳米级镊子具有相同数量级的
是( )
A.溶液 B.悬浊液 C.乳浊液 D.胶体
【答案】D
【解析】胶体的分散质的粒子直径与纳米级镊子具有相同的数量级。
2.下列说法正确的是
①只含有一种元素的物质一定是纯净物
②生石灰作干燥剂时发生化学变化
③ 与 反应生成 和NO,故 是酸性氧化物
④碱性氧化物一定是金属氧化物
⑤用鸡蛋壳膜和蒸馏水除去淀粉胶体中的食盐不涉及化学变化
⑥两种盐反应一定生成两种新盐
A.①③⑥ B.①②③④⑥ C.②④⑤ D.②④⑥
【答案】C
【解析】①只含有一种元素的物质不一定是纯净物,如氧气和臭氧的混合物,①错误;
②生石灰作干燥剂时,与水发生反应生成氢氧化钙,是化学变化,②正确;
③与碱反应生成盐和水的氧化物称为酸性氧化物,大部分酸性氧化物能与水化合成酸, 与 反应
生成 和NO,不符合酸性氧化物的定义,③错误;
④碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物,如Mn O 是酸性氧化物,④正确;
2 7
⑤鸡蛋壳膜是半透膜,用鸡蛋壳膜和蒸馏水除去淀粉胶体中的食盐的过程为渗析,是物理变化,⑤正确;
⑥两种盐反应不一定生成两种新盐,如 ,⑥错误;
综上所述,②④⑤正确,C满足题意;
答案选C。
3.周杰伦在歌曲《青花瓷》中唱到“帘外芭蕉惹骤雨,门环惹铜绿”,其中的“铜绿”即是铜锈,它的
化学成分是Cu (OH) CO (碱式碳酸铜)。铜在潮湿的空气中生锈的化学反应为:
2 2 3
2Cu+O +CO +H O=Cu (OH) CO 。下列有关该反应的说法正确的是( )
2 2 2 2 2 3
A.该反应不是氧化还原反应
B.该反应中氧元素和碳元素化合价发生变化,所以是氧化还原反应
C.该反应中铜得电子,O 失电子,所以是氧化还原反应
2
D.该反应是氧化还原反应,变价的只有两种元素
【答案】D
【解析】
学科网(北京)股份有限公司在反应2Cu+O +CO +H O=Cu (OH) CO 中,铜元素的化合价由0价变成+2价,失去电子,被氧化,氧元素
2 2 2 2 2 3
的化合价由0价变成-2价,得到电子,被还原,其余元素的化合价都没有发生变化,据此分析解答。
A.在该反应中,铜元素的化合价由0价变成+2价,失去电子,被氧化,氧元素的化合价由0价变成-2价,
得到电子被还原,故该反应属于氧化还原反应,故A错误;
B.该反应中氧元素和铜元素化合价发生变化,碳元素化合价没有发生变化,是氧化还原反应,故B错误
C.根据分析,该反应中铜失电子,O 得电子,故C错误;
2
D.该反应是氧化还原反应,化合价发生改变的只有铜、氧两种元素,故D正确;
答案选D。
4.下列逻辑关系图示中正确的是( )
A B C D
【答案】D
【解析】
解答本题的关键是理解物质的分类标准,根据分散质粒子直径的大小将分散系分为溶液、胶体和浊液,
而气溶胶属于胶体的一种,故A错误;氧化还原反应与吸热反应和放热反应的分类标准不同,故B错误;
钾盐与钠盐是根据盐中的阳离子进行分类的,碳酸盐是根据盐中阴离子进行分类的,故C错误。
答案:D
5.下列电离方程式中正确的是
A.HNO =H++N5++3O2 B.Ca(OH) =Ca2++(OH-)
3 2 2
C.AlCl =Al+3+3Cl D.Al (SO ) =2Al3++3SO
3 2 4 3
【答案】D
【解析】
A.HNO 是一元强酸,完全电离,电离方程式应该为:HNO =H++NO ,A错误;
3 3
B.Ca(OH) 是二元强碱,电离方程式应该为:Ca(OH) =Ca2++2OH-,B错误;
2 2
C.AlCl 是可溶性盐,电离方程式应该为:AlCl =Al3++3Cl-,C错误;
3 3
D.Al (SO ) 是可溶性盐,电离方程式为:Al (SO ) =2Al3++3SO ,D正确;
2 4 3 2 4 3
故选D。
6.在无色透明溶液中,能大量共存的离子组是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
【答案】B
【解析】
A. 题给附加条件是无色溶液,含 的溶液一般呈蓝色,A项不符合题意;
学科网(北京)股份有限公司B. 、 、 、 离子间不反应,能大量共存,B项符合题意;
C. 是弱酸的酸式酸根离子,既能与酸反应也能与碱反应,故 和 不能大量共存,C项不符
合题意;
D. 与 能发生反应生成 沉淀,不能大量共存,D项不符合题意。
答案选B。
7.已知氮氧化物、CO都是大气污染物。“三效催化转换器”可将汽车尾气中的有毒气体(NO、CO)转化
为无污染的气体,如图为该反应的微观示意图(未配平),其中不同的球代表不同的原子。下列说法不正确
的是
A.该反应属于氧化还原反应 B.甲和丙中相同元素的化合价不相等
C.丁一定是非金属单质 D.配平后甲、乙,丙的化学计量数均为2
【答案】B
【解析】
NO、CO转化为无污染的气体,则该过程发生的反应为 ,据
此解答。
A.N、C化合价发生变化,该反应为氧化还原反应,A项正确;
B.通过化学方程式可判断甲、丙中相同的元素为O元素,O元素的化合价均为 ,B项错误;
C. 是非金属单质,C项正确;
D.由配平的化学方程式可知,D项正确。
答案选B。
8.下列反应的离子方程式书写正确的是
A.碳酸钙与盐酸反应:CO +2H+=H O+CO ↑
2 2
B.稀H SO 与铁粉反应:2Fe+6H+=2Fe3++3H ↑
2 4 2
C.氢氧化钡溶液与稀H SO 反应:Ba2++ =BaSO ↓
2 4 4
D.氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu
【答案】D
【解析】
A.碳酸钙难溶于水,应该写化学式,离子方程式应该为:CaCO +2H+=Ca2++CO ↑+H O,A错误;
3 2 2
B.稀H SO 与铁粉反应产生FeSO 、H ,离子方程式应该为:Fe+2H+=Fe2++H ↑,B错误;
2 4 4 2 2
C.二者反应除产生BaSO 沉淀外,还有H O,离子方程式应该为:Ba2++2OH-+2H++ =BaSO ↓+2H O,C
4 2 4 2
错误;
D.反应符合事实,遵循物质的拆分原则,D正确;
学科网(北京)股份有限公司故合理选项是D。
9.下图是四种基本反应类型与氧化还原反应的关系图,图中用Ⅰ~Ⅳ阴影部分表示反应所属的区域正确的是
( )。
A.粗硅提纯:Si(粗)+3HCl SiHCl +H 所属区域可能是Ⅰ或Ⅱ
3 2
B.金属钠在空气中燃烧:2Na+O NaO 所属的区域一定是Ⅲ
2 2 2
C.实验室制取氯气:4HCl(浓)+MnO MnCl +Cl↑+2H O 所属的区域可能是Ⅲ
2 2 2 2
D.土法制碱:Na CO+Ca(OH) 2NaOH+CaCO ↓ 所属的区域一定是Ⅳ
2 3 2 3
【答案】D
【解析】
A中反应属于置换反应,应该属于Ⅲ,A项错误。B中反应属于化合反应,且属于氧化还原反应,所属的区域
一定不是Ⅲ,应该属于Ⅰ或Ⅱ,B项错误。C中反应属于氧化还原反应,但不是置换反应,不可能属于Ⅲ,C项
错误。D中反应属于复分解反应,一定不是氧化还原反应,所属的区域一定是Ⅳ,D项正确。
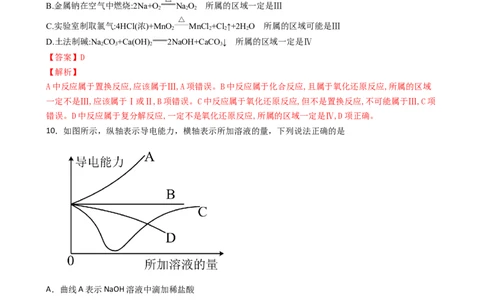
10.如图所示,纵轴表示导电能力,横轴表示所加溶液的量,下列说法正确的是
A.曲线A表示NaOH溶液中滴加稀盐酸
B.曲线B表示CH COOH溶液中滴加KOH溶液
3
C.曲线C表示Ba(OH) 溶液中滴加稀硫酸
2
D.曲线D表示Cu(OH) 悬浊液中滴加 溶液
2
【答案】C
【解析】
A.稀盐酸和NaOH溶液混合时反应生成NaCl,溶液的体积增大,溶液中离子浓度减小,溶液导电性降低,
应该用D表示,故A错误;
B.醋酸是弱电解质,醋酸中加入KOH溶液生成强电解质醋酸钾,溶液中离子浓度增大,溶液导电性增强,
应该用A表示,故B错误;
学科网(北京)股份有限公司C.氢氧化钡和稀硫酸反应生成硫酸钡沉淀和水,当二者完全反应时溶液中离子浓度最小,导电性最弱,
继续加入稀硫酸,溶液中离子浓度增大,溶液导电性增强,应该用C表示,故C正确;
D.氢氧化铜是弱电解质,溶液中离子浓度较小,加入 溶液后生成强电解质硝酸铜,离子浓度增大,
溶液导电性增强,应该用A表示,故D错误;
故选C。
11.已知I-、Fe2+、SO 、Cl-和H O 均有还原性,它们在酸性溶液中还原性的强弱顺序为,Cl-<Fe2+<H O
2 2 2 2 2
<I-<SO ,则下列反应中不可能发生的是
2
A.
B.
C.
D.
【答案】A
【解析】
A.标注元素化合价可知,反应中硫元素化合价降低,过氧化氢中氧元素化合价升高,所以根据规律判断
还原性强弱,还原剂H O 的还原性大于还原产物SO ,和题目所给条件不符,故A不可能发生;
2 2 2
B.反应中还原剂SO 的还原性大于还原产物HI,符合题给条件,故B可以发生;
2
C.反应中还原剂Fe2+的还原性大于还原产物Cl-,符合题给条件,故C可以发生;
D.反应中还原剂SO 的还原性大于还原产物Fe2+,符合题给条件,故D可以发生;
2
故选:A。
12.在酸性条件下,可发生如下反应: +2M3++4H O= +Cl-+8H+, 中M的化合价是
2
A.+4 B.+5 C.+6 D.+7
【答案】C
【解析】
根据离子反应方程式中,反应前后所带电荷数相等,即6-1=8-n-1,解得n=2,从而得出M O n-中M
2 7
的化合价为+6价,故C正确。
13.图中相连的物质间在一定条件下可以反应,“→”表示丁在一定条件下可以转化为乙。下面四组选
项中,符合图示要求的是( )
甲 乙 丙 丁
A H SO Na SO NaOH NaCl
2 4 2 4
B KCl K CO KOH HCl
2 3
学科网(北京)股份有限公司C O CO CuO C
2
D Fe CuCl Ag HCl
2
A.A B.B C.C D.D
【答案】C
【解析】
A. 甲和乙、乙和丙、丙和丁、丁和甲均不能反应,A错误;
B. 甲和乙、乙和丙、丁和甲均不能反应,B错误;
C. 甲和乙: ;乙和丙: ;丙和丁: ;甲
和丁: ,丁―→乙: ,C正确;
D. 乙与丙、丙与丁均不能反应,D错误;
故合理选项为C。
14.被称为万能还原剂的NaBH (NaBH 中H为﹣1价)能溶于水并和水反应,有如下反应
4 4
NaBH +2H O=NaBO +4H ↑,下列有关该反应的说法中,正确的是( )
4 2 2 2
A.NaBH 既是氧化剂又是还原剂
4
B.NaBH 是氧化剂,H O是还原剂
4 2
C.硼元素被氧化,氢元素被还原
D.被氧化的元素与被还原的元素质量比为1:1
【答案】D
【解析】
反应NaBH +2H O=NaBO +4H ↑中,NaBH 中H元素化合价为-1价,水中H元素化合价为+1价,二者发生
4 2 2 2 4
氧化还原反应生成H 。
2
A.NaBH 中氢元素的化合价升高,NaBH 是还原剂,故A错误;
4 4
B.NaBH 中氢元素的化合价升高,NaBH 是还原剂,水中氢元素化合价降低,水是氧化剂,故B错误;
4 4
C.NaBH 中氢元素的化合价升高,被氧化,硼元素化合价不变,故C错误;
4
D.化合价升高的元素是NaBH 中的氢元素,被氧化,水中的氢元素被还原,氧化剂和还原剂中H元素的
4
化合价变化数值相同,转移电子数相同,物质的量之比为1:1,被氧化的元素与被还原的元素质量比为
1:1,故D正确。
故选D。
15.下列氧化还原反应方程式中,电子转移方向和数目正确的是( )
学科网(北京)股份有限公司D.
【答案】D
【解析】先标出各反应前后元素的化合价,根据化合价升降、得失电子守恒进行分析。Cl 与Ca(OH) 反
2 2
应时,得、失电子数目均是2,A项错误;Cl 与FeCl 反应时,Cl 是氧化剂,得电子,FeCl 是还原剂,
2 2 2 2
失电子,B项错误;由氧化还原反应规律可知,HS与HSO 反应时,还原产物是SO,氧化产物是S,得、
2 2 4 2
失电子数目均是2,C项错误。
16.废水脱氮工艺中有一种方法是在废水中加入过量NaClO使NH 完全转化为N,该反应可表示为
2
2NH +3ClO-=N ↑+3Cl-+2H++3H O。下列说法中不正确的是( )
2 2
A.反应中氮元素被氧化,氯元素被还原
B.还原性:NH >Cl-
C.反应中每生成1个N 分子,转移6个电子
2
D.经此法处理过的废水不用再处理就可以直接排放
【答案】D
【解析】A.反应2NH +3ClO-=N ↑+3Cl-+2H++3H O中氮元素从-3价升高为0价,Cl元素从+1价降为-1
2 2
价,则氮元素被氧化,氯元素被还原,故A正确;
B.反应2NH +3ClO-=N ↑+3Cl-+2H++3H O中氮元素从-3价升高为0价,Cl元素从+1价降为-1价,则
2 2
NH 是还原剂,Cl-是还原产物,则还原性:NH >Cl-,故B正确;
C.反应2NH +3ClO-=N ↑+3Cl-+2H++3H O中氮元素从-3价升高为0价,则每生成1个N 分子,转移6
2 2 2
个电子,故C正确;
D.经反应2NH ++3ClO-═N +3Cl-+2H++3H O处理过的废水呈酸性,需要先用石灰水中和酸,则不能直接
4 2 2
排放,故D错误;
故答案为D。
学科网(北京)股份有限公司二、非选择题(本题包括4小题,共52分)
17(10分).如图所示为一“铁链”图案,某化学兴趣小组的同学在图案上分别写了 、 、 、
、 五种物质,图中相连的两种物质均可归属为一类,相交部分A、B、C、D为其相应的分类依
据代号。
(1)将分类依据代号填入相应的横线上:
①两种物质都不是电解质____;
②两种物质都是钠的化合物_____;
③两种物质都是氧化物______;
④两种物质都是盐____。
(2)用洁净的烧杯取少量蒸馏水,加热至沸腾,向烧杯中逐滴加入图中某物质的饱和溶液,继续煮沸可制
得一种红褐色胶体。
①该物质的化学式为____。
②证明有胶体生成的实验原理是__________________________________。
③向该胶体中逐滴加入稀盐酸,会发生一系列变化:
a.先产生红褐色沉淀,原因是_______________________________________________________________。
b.随后红褐色沉淀溶解,此时发生反应的离子方程式是_________________________________________。
【答案】 A C B D 丁达尔效应 胶体发生聚沉产生
沉淀。
【解析】
(1)① 和 都不是电解质,故答案为:A;
② 和 都是氧化物,故答案为:C;
③ 和 都是钠的化合物,故答案为:B;
④ 和 都是盐,故答案为: D;
(2)①将饱和 溶液加入煮沸的蒸馏水中,继续煮沸至液体呈红褐色可制得 胶体,故答案为:
FeCl ;
3
②证明有胶体生成的实验原理是丁达尔效应,故答案为:丁达尔效应;
③a.胶体遇可溶性电解质会发生聚沉,加入HCl产生沉淀的原因是 胶体发生聚沉产生
沉淀,故答案为: 胶体发生聚沉产生 沉淀;
b.氢氧化铁溶解是因为氢氧化铁和HCl反应,反应的离子方程式为 ,故答案
为: 。
18(14分).按要求填空
学科网(北京)股份有限公司(1)向CuCl 溶液中滴加NaOH溶液,现象:____________________________________________________,
2
离子方程式:_________________________________________________.
(2)向NaHCO 溶液中滴加稀硫酸,现象:
3
__________________________________________________________,离子方程式:
__________________________________________________ .
(3)铜粉(铁粉):除杂,括号内为杂质,所加试剂_________,离子方程式;___________________________。
(4)FeSO (CuSO ):除杂,括号内为杂质,所加试剂 ________,离子方程式
4 4
___________________________。
【答案】 有蓝色沉淀生成 Cu2++2OH-=Cu(OH) ↓ 生成无色无味的气体
2
+H+=CO ↑+H O 盐酸(或硫酸、或硫酸铜溶液) Fe+2H+=Fe2++H ↑(或Fe+
2 2 2
Cu2+=Fe2++Cu) 铁粉 Fe+Cu2+=Fe2++Cu
【解析】
(1)CuCl 溶液中滴加NaOH溶液,发生复分解反应,生成难溶的氢氧化铜,因此反应过程中能看到蓝色沉
2
淀生成,离子方程式为:Cu2++2OH-=Cu(OH) ↓。
2
(2)向NaHCO 溶液中滴加稀硫酸,发生复分解反应,强酸制弱酸,反应离子方程式为: +H+=
3
CO ↑+H O,反应中可观察到有无色无味的气体生成。
2 2
(3)Cu不能与盐酸、硫酸反应,而Fe可以,故可以利用盐酸或硫酸除去铜粉中的铁粉杂质,反应的离子方
程式为:Fe+2H+=Fe2++H ↑;也可以利用CuSO 溶液除去铁粉,离子方程式为:Fe+Cu2+=Fe2++Cu。
2 4
(4)除去FeSO 中的CuSO 杂质,可以将混合物溶于水后加入足量的铁粉,充分反应后过滤除去剩余的Fe粉
4 4
和生成的Cu,反应的离子方程式为:Fe+Cu2+=Fe2++Cu。
19(10分).NaNO 因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO 能发生如下反应:
2 2
2NaNO +4HI=2NO+I +2NaI+2H O。
2 2 2
(1)反应中______元素被氧化(填元素名称),_________是氧化剂(填化学式);
(2)用单线桥标出电子转移方向和数目:2NaNO +4HI=2NO+I +2NaI+2H O,________
2 2 2
(3)HI表现的性质是________。
(4)根据上述反应,鉴别NaNO 和NaCl。可选用的物质有:①水②碘化钾③淀粉溶液④白酒⑤食醋,你
2
认为必须选用的物质有________(填序号)。
(5)某厂废液中,含有2%~5%的NaNO ,直接排放会造成污染,下列试剂能使NaNO 转化为不引起二
2 2
次污染的N 的是____________。
2
A.NaCl B.NH Cl C.HNO D.浓H SO
4 3 2 4
【答案】 碘 NaNO 还原性、酸性
2
②③⑤ B
【解析】
(1)2NaNO +4HI=2NO+I +2NaI+2H O中碘元素的化合价升高,失电子,碘元素被氧化,NaNO 中氮元素的化
2 2 2 2
合价降低,所以NaNO 是氧化剂;
2
学科网(北京)股份有限公司(2)2NaNO +4HI=2NO+I +2NaI+2H O中碘元素的化合价从-1价升高到0价,失去1个电子,NaNO 中氮元
2 2 2 2
素的化合价从+3价降低到+2价,得到1个电子,根据得失电子守恒可知转移电子数是2个,所以用单线
桥标出电子转移方向和数目为 ;
(3)反应中碘元素化合价升高,被氧化,同时还有碘化钠生成,则HI在反应中的作用是还原性和酸性;
(4)淀粉、白酒与NaNO 都不反应,所以无明显现象;KI与NaNO 反应生成I 必须在酸性条件下才能反应,
2 2 2
食醋会电离出微量的氢离子,碘化钾在食醋本身带的溶剂水中电离出碘离子,亚硝酸钠电离出亚硝酸根
与钠离子,发生反应生成碘单质,I 使淀粉溶液变蓝,故答案为②③⑤;
2
(5)NaNO →N 是被还原,必须加还原剂,硝酸和浓硫酸均具有强氧化性,亚硝酸钠不能氧化氯离子,故只
2 2
能加NH Cl作还原剂,方程式为NaNO +NH Cl=NaCl+N ↑+2H O,故答案为B。
4 2 4 2 2
19.(8分)(1)按如图所示操作,充分反应后:
①Ⅰ中发生反应的离子方程式为 ;
②Ⅱ中铜丝上观察到的现象是 ;
③结合Ⅰ、Ⅱ的实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为
。
(2)将少量Cl 通入FeBr 溶液中,反应的离子方程式为2Fe2++Cl 2Fe3++2Cl-;将足量Cl 通入FeBr 溶液中,
2 2 2 2 2
反应的离子方程式为2Fe2++4Br-+3Cl 2Fe3++6Cl-+2Br 。这个事实说明具有还原性的粒子的还原性强弱
2 2
顺序为 。
【答案】(1)①Fe+Cu2+ Fe2++Cu ②紫红色铜丝上有银白色金属附着 ③Ag+>Cu2+>Fe2+
(2)Fe2+>Br->Cl-
【解析】(1)铁与CuSO 溶液发生反应Fe+Cu2+ Fe2++Cu,氧化性:Cu2+>Fe2+,Cu与AgNO 溶液发生反应
4 3
Cu+2Ag+ Cu2++2Ag,Ag附着在Cu的表面,氧化性Cu2+Cu2+>Fe2+。(2)Fe2+、Br-均具有还
原性,当通入少量Cl 时,只有Fe2+被氧化,说明还原性Fe2+>Cl-;当通入过量Cl 时,Fe2+和Br-都被氧化,说明
2 2
还原性:Fe2+>Br->Cl-。
20.(10分)Ⅰ.某无色溶液中可能含有Na+、Ba2+、Cu2+、CO 、Cl-、Mg2+中的一种或几种离子。
①向此溶液中滴加足量稀盐酸无明显现象。
②取少许①的溶液并加入少量的NaSO 溶液,有白色沉淀产生。
2 4
③取②的上层清液并加入足量的NaOH溶液,有白色沉淀产生。
则原溶液中一定含有的离子是_______,一定不含有的离子是_______。
II.酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有NaHCO 、
3
NaHSO、KH PO 、KHPO 等。已知HPO (次磷酸)与足量的NaOH反应只生成一种盐NaH PO ,HPO
4 2 4 2 4 3 2 2 2 3 2
水溶液中存在HPO 分子。
3 2
学科网(北京)股份有限公司(1)HPO 属于_______酸;NaH PO 为_______盐(填序号)
3 2 2 2
①一元酸,②二元酸,③三元酸,④强酸,⑤弱酸,⑥正盐,⑦酸式盐
(2)写出HPO 溶液与足量NaOH溶液反应的离子方程式_______。
3 2
【答案】Ba2+、Cl-、Mg2+ CO 、Cu2+ ①⑤ ⑥ HPO + OH- = H PO + H O
3 2 2 2
【解析】Ⅰ.溶液无色,则一定不含Cu2+;
向此溶液中滴加足量稀盐酸无明显现象,则一定不含CO ;
取少许①的溶液并加入少量的NaSO 溶液,有白色沉淀产生,则原溶液中一定存在Ba2+;
2 4
取②的上层清液并加入足量的NaOH溶液,有白色沉淀产生,则原溶液中一定含有Mg2+;溶液显电中性,
所以还一定有一种阴离子,则一定含有Cl-;
综上所述原溶液中一定含有的离子是Ba2+、Cl-、Mg2+,一定不含有的离子是CO 、Cu2+;
Ⅱ.(1)HPO (次磷酸)与足量的NaOH反应只生成一种盐NaH PO ,说明次磷酸为一元酸,HPO 水溶
3 2 2 2 3 2
液中存在HPO 分子,说明次磷酸为弱酸,所以HPO 属于①一元酸、⑤弱酸;NaH PO 不能和NaOH反
3 2 3 2 2 2
应,即不能电离出H+,所以为⑥正盐;
(2)HPO (次磷酸)与足量的NaOH反应只生成一种盐NaH PO ,离子方程式为HPO + OH- = H PO +
3 2 2 2 3 2 2
HO。
2
学科网(北京)股份有限公司学科网(北京)股份有限公司