文档内容
第一章 物质及其变化
第一节 物质的分类及转化
本节的重难点一共五个,下面分别进行归纳总结并有精选对点练习,一定好好
体会,耐心看完,做到事半功倍!
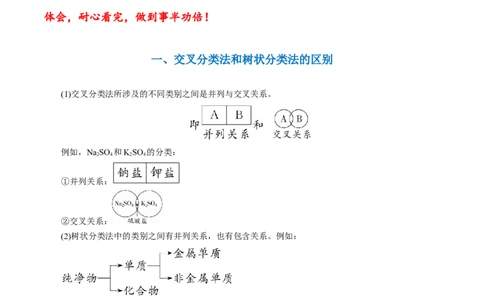
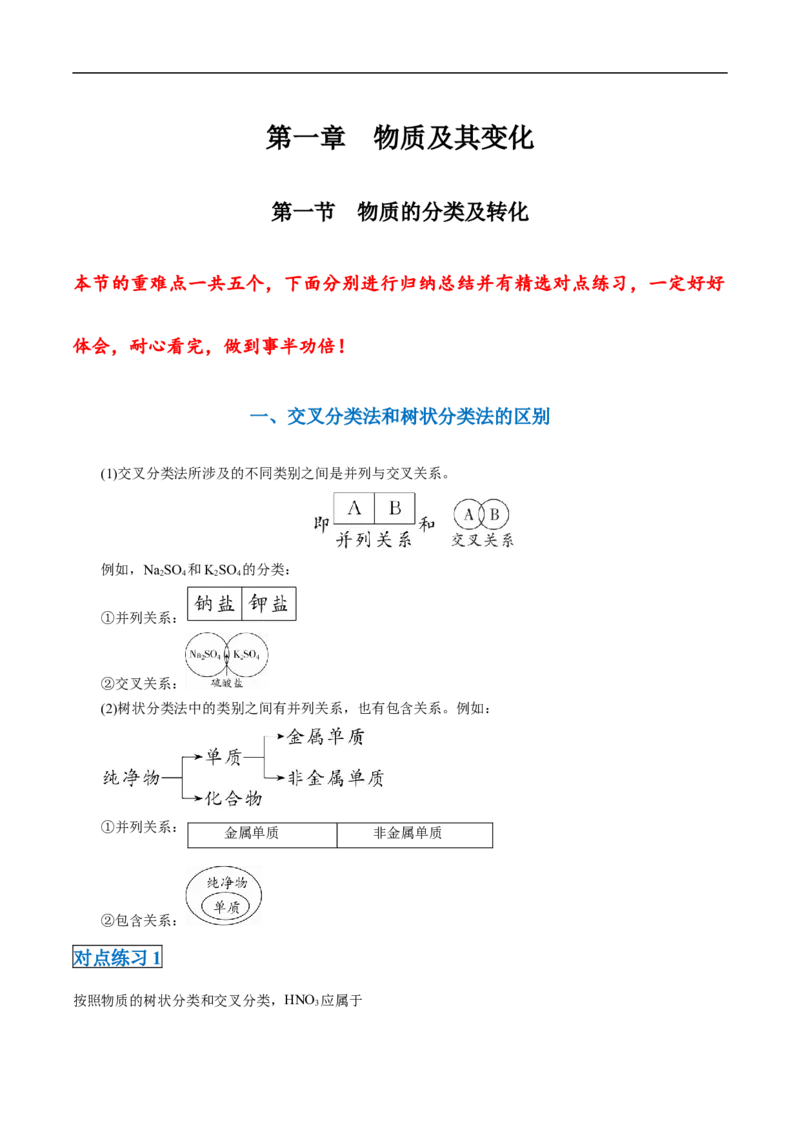
一、交叉分类法和树状分类法的区别
(1)交叉分类法所涉及的不同类别之间是并列与交叉关系。
例如,NaSO 和KSO 的分类:
2 4 2 4
①并列关系:
②交叉关系:
(2)树状分类法中的类别之间有并列关系,也有包含关系。例如:
①并列关系:
金属单质 非金属单质
②包含关系:
对点练习1
按照物质的树状分类和交叉分类,HNO 应属于
3①酸 ②氢化物 ③氧化物 ④含氧酸 ⑤难挥发性酸 ⑥强酸⑦一元酸 ⑧化合物
A.①②③④⑤⑥⑦⑧ B.①⑧
C.①④⑥⑦⑧ D.①④⑤⑥⑦
对点练习2
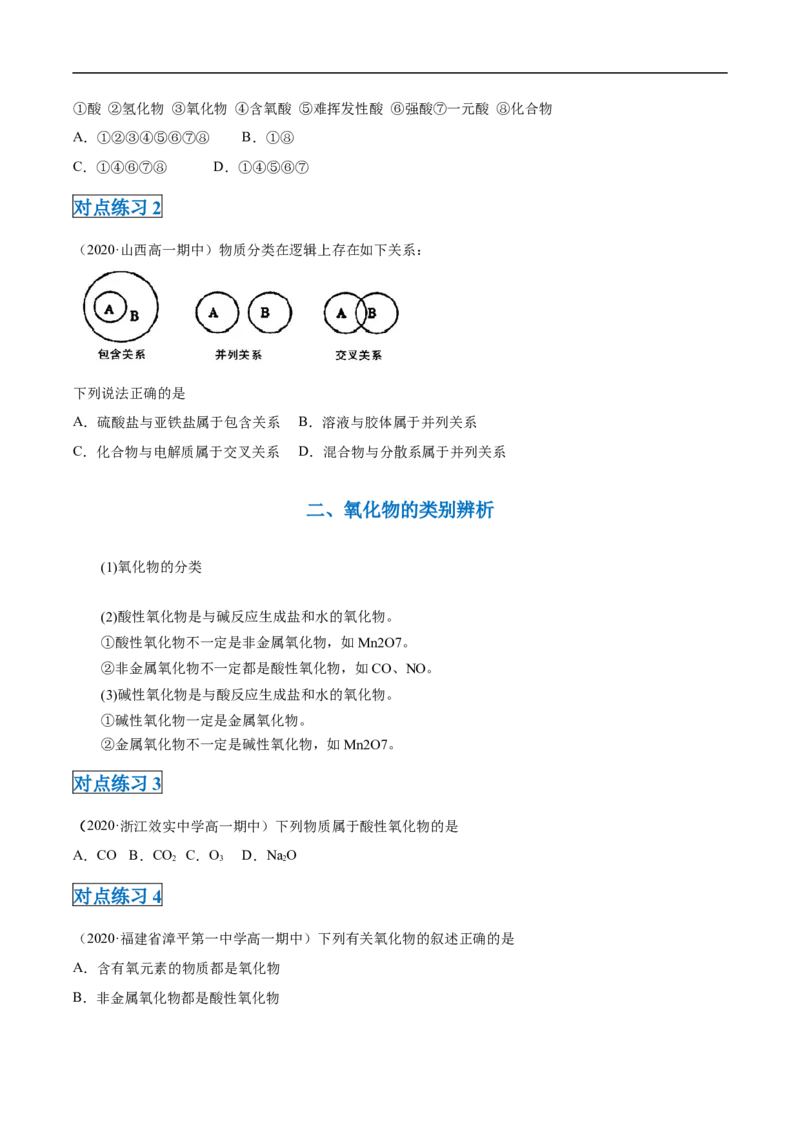
(2020·山西高一期中)物质分类在逻辑上存在如下关系:
下列说法正确的是
A.硫酸盐与亚铁盐属于包含关系 B.溶液与胶体属于并列关系
C.化合物与电解质属于交叉关系 D.混合物与分散系属于并列关系
二、氧化物的类别辨析
(1)氧化物的分类
(2)酸性氧化物是与碱反应生成盐和水的氧化物。
①酸性氧化物不一定是非金属氧化物,如Mn2O7。
②非金属氧化物不一定都是酸性氧化物,如CO、NO。
(3)碱性氧化物是与酸反应生成盐和水的氧化物。
①碱性氧化物一定是金属氧化物。
②金属氧化物不一定是碱性氧化物,如Mn2O7。
对点练习3
(2020·浙江效实中学高一期中)下列物质属于酸性氧化物的是
A.CO B.CO C.O D.NaO
2 3 2
对点练习4
(2020·福建省漳平第一中学高一期中)下列有关氧化物的叙述正确的是
A.含有氧元素的物质都是氧化物
B.非金属氧化物都是酸性氧化物C.氧化物中的氧元素不一定都显-2价
D.与水反应能生成酸(或碱)的氧化物一定是酸(或碱)性氧化物
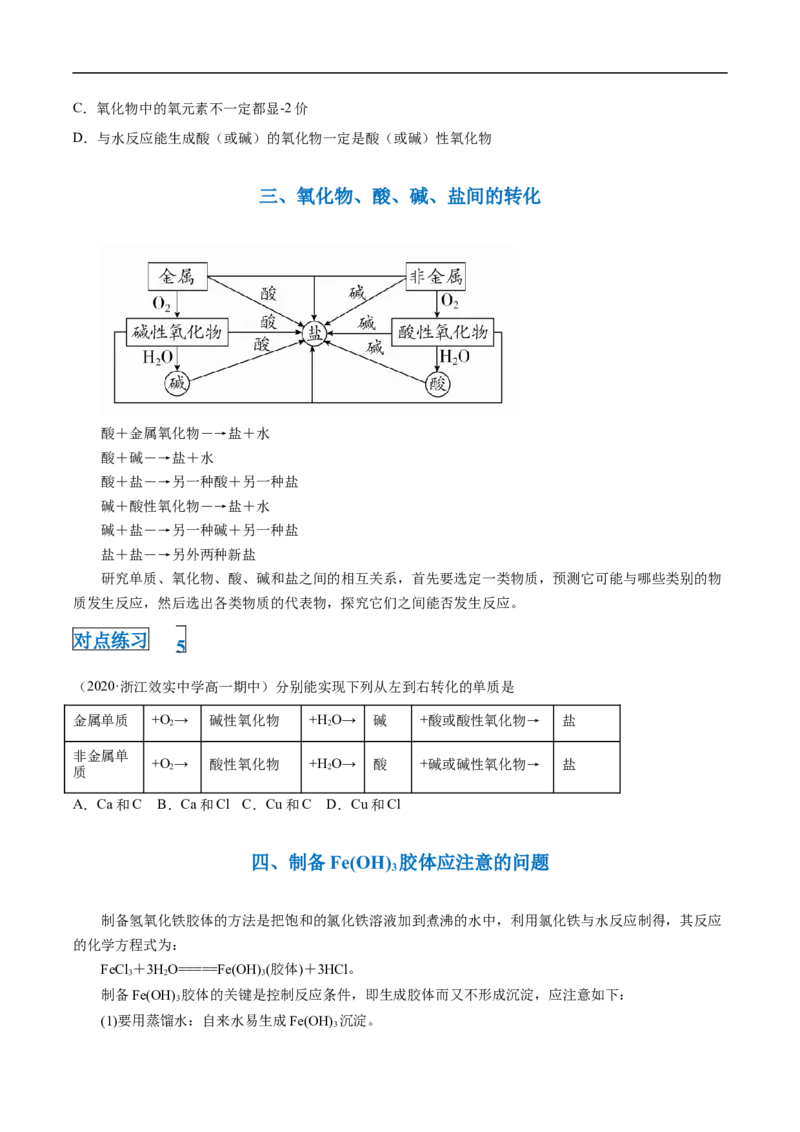
三、氧化物、酸、碱、盐间的转化
酸+金属氧化物―→盐+水
酸+碱―→盐+水
酸+盐―→另一种酸+另一种盐
碱+酸性氧化物―→盐+水
碱+盐―→另一种碱+另一种盐
盐+盐―→另外两种新盐
研究单质、氧化物、酸、碱和盐之间的相互关系,首先要选定一类物质,预测它可能与哪些类别的物
质发生反应,然后选出各类物质的代表物,探究它们之间能否发生反应。
对点练习
5
(2020·浙江效实中学高一期中)分别能实现下列从左到右转化的单质是
金属单质 +O → 碱性氧化物 +H O→ 碱 +酸或酸性氧化物→ 盐
2 2
非金属单
+O → 酸性氧化物 +H O→ 酸 +碱或碱性氧化物→ 盐
质 2 2
A.Ca和C B.Ca和Cl C.Cu和C D.Cu和Cl
四、制备Fe(OH) 胶体应注意的问题
3
制备氢氧化铁胶体的方法是把饱和的氯化铁溶液加到煮沸的水中,利用氯化铁与水反应制得,其反应
的化学方程式为:
FeCl +3HO=====Fe(OH) (胶体)+3HCl。
3 2 3
制备Fe(OH) 胶体的关键是控制反应条件,即生成胶体而又不形成沉淀,应注意如下:
3
(1)要用蒸馏水:自来水易生成Fe(OH) 沉淀。
3(2)不能把饱和FeCl 溶液直接倒入沸水中,过量的FeCl 会使Fe(OH) 胶体聚沉。
3 3 3
(3)不能搅拌:用玻璃棒搅拌会使Fe(OH) 胶体形成沉淀。
3
(4)不能长时间加热:溶液呈红褐色停止加热,长时间加热会破坏胶体形成沉淀。
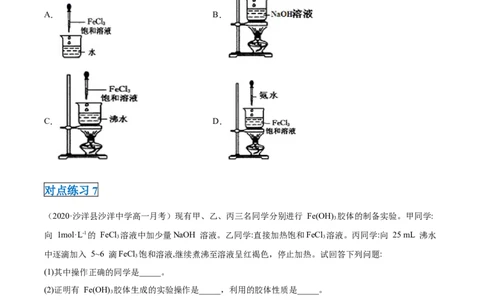
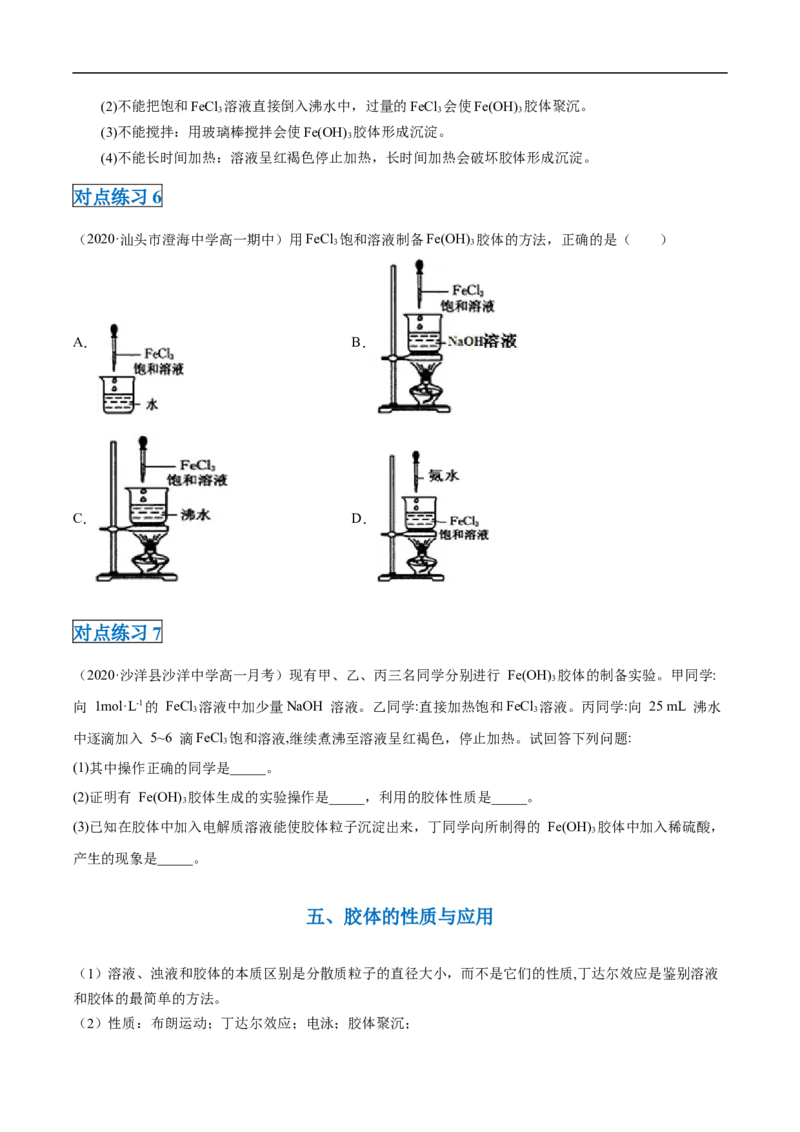
对点练习6
(2020·汕头市澄海中学高一期中)用FeCl 饱和溶液制备Fe(OH) 胶体的方法,正确的是( )
3 3
A. B.
C. D.
对点练习7
(2020·沙洋县沙洋中学高一月考)现有甲、乙、丙三名同学分别进行 Fe(OH) 胶体的制备实验。甲同学:
3
向 1mol·L-1的 FeCl 溶液中加少量NaOH 溶液。乙同学:直接加热饱和FeCl 溶液。丙同学:向 25 mL 沸水
3 3
中逐滴加入 5~6 滴FeCl 饱和溶液,继续煮沸至溶液呈红褐色,停止加热。试回答下列问题:
3
(1)其中操作正确的同学是_____。
(2)证明有 Fe(OH) 胶体生成的实验操作是_____,利用的胶体性质是_____。
3
(3)已知在胶体中加入电解质溶液能使胶体粒子沉淀出来,丁同学向所制得的 Fe(OH) 胶体中加入稀硫酸,
3
产生的现象是_____。
五、胶体的性质与应用
(1)溶液、浊液和胶体的本质区别是分散质粒子的直径大小,而不是它们的性质,丁达尔效应是鉴别溶液
和胶体的最简单的方法。
(2)性质:布朗运动;丁达尔效应;电泳;胶体聚沉;(3)胶体聚沉的方法有:①加电解质溶液;②加与胶粒带相反电荷的另一种胶体;③长时间加热等.
(4)应用:
a盐卤点豆腐
b明矾净化污水
c.FeCl 溶液用于伤口止血
3
d江河入海口形成的沙洲
e冶金厂大量烟尘用高压电除去
对点练习8
(2020·江西省宜春中学高一期中)下列叙述正确的是( )
A.分散质微粒直径的大小关系:溶液>胶体>浊液
B.胶体粒子很小,可以通过半透膜
C.往 胶体中逐滴加入稀 ,溶液时,开始时会出现沉淀,再继续逐滴加时,沉淀又会消失
D.电泳现象可证明胶体属于电解质溶液
对点练习9
下列说法正确的是
①江河入海口三角洲的形成通常与胶体的性质有关
②向Fe(OH) 胶体中加入盐酸至过量,最终出现红褐色Fe(OH) 沉淀
3 3
③用明矾处理污水是利用了胶体的性质
④光线射入密林中看到的光柱,属于胶体的性质
⑤可用渗析法分离Al(OH) 胶体和NaCl溶液
3
⑥胶体、溶液、浊液的本质区别是丁达尔效应
A.①③④⑤⑥ B.①②③④⑥
C.①③④⑤ D.①②③④⑤⑥
对点练习10
下列关于Fe(OH) 胶体的叙述中,正确的是( )
3
A.制备Fe(OH) 胶体的化学方程式是FeCl +3HO Fe(OH) ↓+3HCl
3 3 2 3
B.在制备Fe(OH) 胶体的实验中,加热煮沸时间越长,越有利于胶体的生成
3
C.Fe(OH) 胶体微粒能吸附阳离子,从而使Fe(OH) 胶体带有一定电荷
3 3
D.Fe(OH) 胶体能够吸附水中悬浮的固体颗粒并沉降,达到净水目的
3