文档内容
2016/2017 学年第一学期九年级化学
《化学方程式》单元测试题
姓名:___________ 班级:___________ 得分:_________
可能用到的相对原子质量:H—1 C—12 O—16 P—31 S—32 Fe—56
一、我会选择(本大题包括10小题,每小题2分,共20分。每小题只有一个符合题意的选项)
1.化学实验中常常出现“1+l=2”或“l+l≠2”的有趣现象。下列符合“l+l=2”的事实是( )
A.常温下,1L水与1L酒精混合后的体积等于2L
B.室温下,1g木炭在1g氧气中完全燃烧后生成2g二氧化碳
C.室温下,1g硫粉在lg氧气中完全燃烧后生成2g二氧化硫
D.室温下,1g红磷在lg氧气中完全燃烧后生成2g五氧化二磷
2.化学反应前后,下列各项中,肯定没有变化的是( )
①原子数目 ②原子种类 ③分子数目 ④分子种类 ⑤元素种类 ⑥物质总质量 ⑦物质种类
A.①②⑤⑥ B.①②③⑤ C.①②⑤⑦ D.③④⑥⑦
3.小明同学从S+O SO 中获得以下信息:①该反应反应物是硫和氧气;②反应发生条件是
2点燃 2
点燃;③反应前后元素种类和原子个数不变;④反应前后分子总数保持不变;⑤参加反应的硫和
氧气的质量比为2﹕1.其中正确的信息是( )
A.①②④⑤ B.①②③ C.④⑤ D.①②③⑤
4.三氧化铬(CrO )常用于金属镀铬。在工业上,用重铬酸钠(Na Cr O)制造三氧化铬,反应的
3 2 2 7
化学方程式:NaCr O+X=2CrO +Na SO +H O,其中X的化学式为( )
2 2 7 3 2 4 2
A.HS B.H SO C.H SO D. SO
2 2 3 2 4 2
5.在化学反应A+B=C+D中,若12 g A与一定量的B恰好完全反应,生成28 g C和2 g D,则
参加反应的B的质量为( )
A.8 g B.18 g C.28 g D.30 g
6.在化学反应MnO +4HCl(浓)=MnCl +2H O+Cl 中,同种元素的化合价在化学反应前后变化
2 2 2 2
最大的是( )
A.Mn B.Cl C.H D.O
7.氯碱工业的反应原理是电解饱和食盐水,下列物质不可能是氯碱工业产品的是( )A.H B.Cl C.Na CO D.NaOH
2 2 2 3
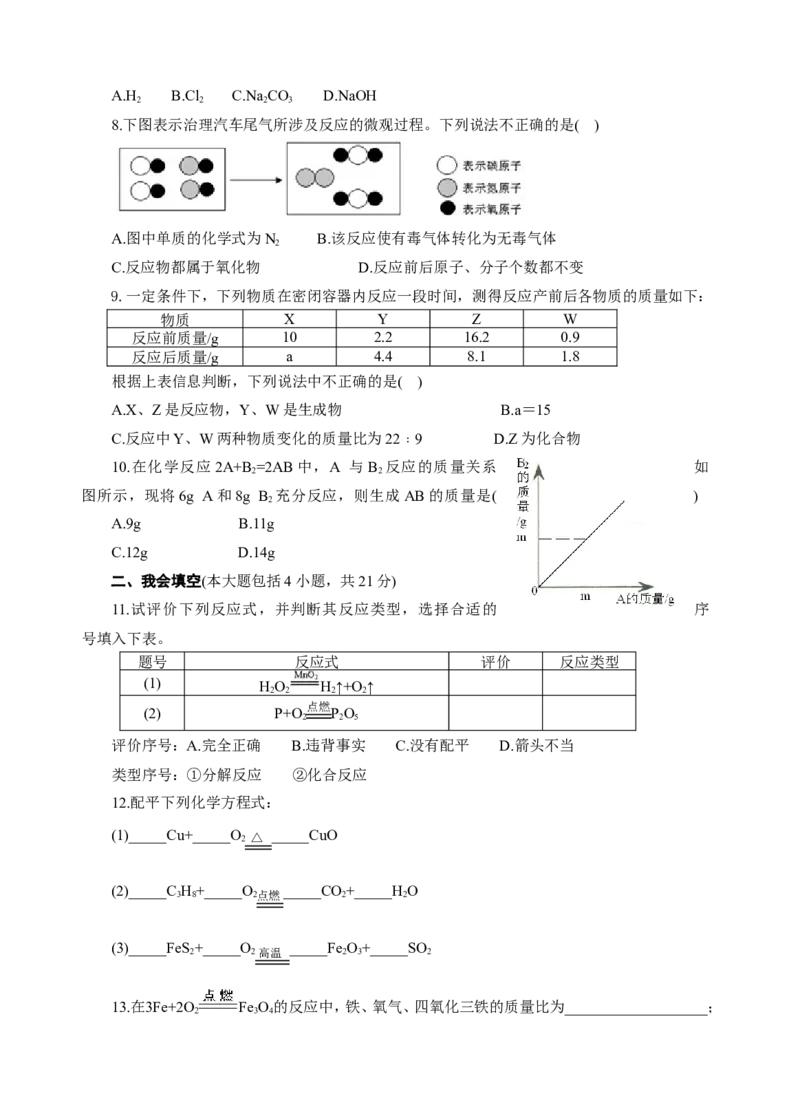
8.下图表示治理汽车尾气所涉及反应的微观过程。下列说法不正确的是( )
A.图中单质的化学式为N B.该反应使有毒气体转化为无毒气体
2
C.反应物都属于氧化物 D.反应前后原子、分子个数都不变
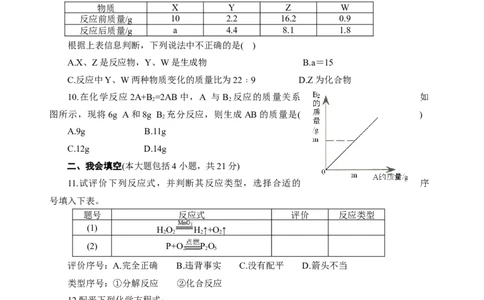
9.一定条件下,下列物质在密闭容器内反应一段时间,测得反应产前后各物质的质量如下:
物质 X Y Z W
反应前质量/g 10 2.2 16.2 0.9
反应后质量/g a 4.4 8.1 1.8
根据上表信息判断,下列说法中不正确的是( )
A.X、Z是反应物,Y、W是生成物 B.a=15
C.反应中Y、W两种物质变化的质量比为22﹕9 D.Z为化合物
10.在化学反应2A+B =2AB中,A 与B 反应的质量关系 如
2 2
图所示,现将6g A和8g B 充分反应,则生成AB的质量是( )
2
A.9g B.11g
C.12g D.14g
二、我会填空(本大题包括4小题,共21分)
11.试评价下列反应式,并判断其反应类型,选择合适的 序
号填入下表。
题号 反应式 评价 反应类型
(1) HO H↑+O ↑
2 2 2 2
点燃
(2) P+O PO
2 2 5
评价序号:A.完全正确 B.违背事实 C.没有配平 D.箭头不当
类型序号:①分解反应 ②化合反应
12.配平下列化学方程式:
(1)_____Cu+_____O 2 △ _ _ ___CuO
(2)_____C H+_____O _____CO+_____H O
3 8 2点燃 2 2
(3)_____FeS +_____O _____Fe O+_____SO
2 2高温 2 3 2
13.在3Fe+2O Fe O的反应中,铁、氧气、四氧化三铁的质量比为___________________;
2 3 4如果8.4g铁,需__________g氧气恰好完全反应,生成Fe O为__________g;如果要制取23.2g Fe O,
3 4 3 4
需Fe__________g和O__________g参加反应。
2
14.某同学把4g硫放在给定的氧气中充分燃烧,实验数据如下表所示。
第一次 第二次 第三次
O的质量(g) 3 4 6
2
生成SO 的质量(g) 6 8 8
2
回答下列问题:
(1)从以上数据说明,这三次实验中第_______次恰好完全反应;
(2)第_______次实验中硫有剩余,剩余_______g;
(3)第_______次实验中氧气有剩余,剩余_______g;
(4)这三次实验的化学反应过程中,是否有不符合质量守恒定律的?________________。
三、我会探究(本大题包括1小题,共12分)
15.对比分析是化学研究和学习的基本方法。甲、乙、丙三位同学利用图中的装置,围绕“用
称量的方法验证化学反应是否遵守质量守恒定律并分析实验条件”这一探究目的开展活动。
【实验步骤】
①如图所示,甲将白磷和反应装置、乙将装有稀盐酸的小试管和碳酸钠粉末的烧杯,分别放
在两个托盘天平上,并用砝码使天平平衡。丙对石棉网和打磨干净的镁条进行称量。
②三位同学分别利用装置进行化学反应。
③甲、乙同学在反应结束且甲的装置冷却后,将反应装置及装置内的物质放在反应前使用的
托盘天平上,观察天平是否平衡。丙同学实验结束后称量石棉网和石棉网上氧化镁的质量,比较
反应前后质量。
【实验分析】
(1)请你仿照示例,完成实验现象的记录和分析。
实验现象 化学方程式 结 论
______________________ 、
该反应遵守质
甲同学 ______________________ 、 ______________________
量守恒定律
______________________
_______________________、 该反应遵守质
乙同学 NaCO+2HCl=2NaCl+H O+CO↑
______________________ 2 3 2 2 量守恒定律
镁条剧烈燃烧,发出耀眼白
该反应不遵守
丙同学 光,放热,生成白色固体。 ______________________
质量守恒定律
反应前后称量质量不相等
(2)比较甲、丙同学的实验有许多相似之处,如生成物都属于_______(填物质的类别)。
(3)通过对上述实验的对比分析,甲、乙两位同学发现丙同学的实验现象是正确的,但结论却是错误的。在实验操作完全正确的情况下,请分析导致丙同学实验前后称量质量不相等的原因有
________________________________________________。
【实验结论】化学反应都遵守质量守恒定律。
【实验反思】(4)请从微观角度分析化学反应遵守质量守恒定律的原因是__________________
_______________________________________。
四、我会计算(本大题包括1小题,共7分)
16.新近,我国部分城市首次使用二甲醚作为公交车的燃料,有效地解决了公交车冒黑烟的问
题。二甲醚燃烧的化学方程式可表示为:C HO(二甲醚)+3O 2CO+3H O。
a b d 2点燃 2 2
请通过计算回答:
(1)a=________;b=________;d=________。
(2)23g二甲醚充分燃烧需要多少克氧气?生成多少克二氧化碳?
参 考 答 案
1.C 2.A 3.B 4.C 5.B 6.A 7.C 8.D 9.A 10.C
11.(1)B ① (2)C ②12.(1) 2 1 2 (2)1 5 3 4 (3)4 11 2 8
13.168﹕64﹕232(或21﹕8﹕29) 3.2 11.6 16.8 6.4
14.(1)二 (2)一 1 (3)三 2 (4)三次都符合
15.(1)白磷燃烧产生大量白烟,放热,气球先膨胀,后变小;天平平衡 4P+5O 2PO 烧
2点燃 2 5
杯中有大量气泡产生;天平不平衡 2Mg+O 2MgO (2)氧化物 (3)反应前未称量参加反
2点燃
应的氧气质量,反应后部分生成的氧化镁外逸,无法称量 (4)化学反应前后原子的种类没有改
变,数目没有增减,原子的质量也没有改变
16.(1)a=2 b=6 d=1 (2)48 44