文档内容
质量守恒定律
1.在化学反应A+2B C+D中,5.6 g A和7.3 g B恰好完全反应,生成12.7 g C,同时得到D的质量是
A.0.2 g B.5.6 g
C.0.4 g D.0.73 g
2.化学反应遵循质量守恒定律的原因是化学反应前后
A.分子的种类没有改变
B.分子的数目没有改变
C.原子的种类、数目和质量都没有改变
D.物质的种类没有改变
3.氧化汞受热分解生成汞和氧气的反应前后,发生改变的是
A.元素种类
B.原子种类
C.分子种类
D.原子数目
4.现将10 g A和足量的B混合加热,A和B发生化学反应,10 g A完全反应后生成8 g C和4 g D,则参加反
应的A与B的质量比是
A.1∶1 B.2∶1
C.5∶1 D.4∶1
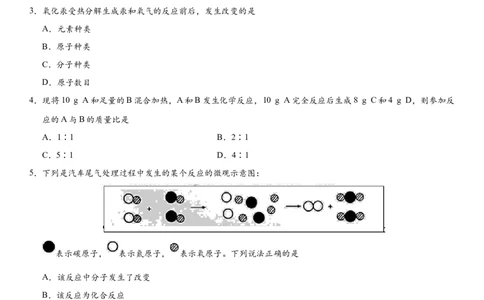
5.下列是汽车尾气处理过程中发生的某个反应的微观示意图:
表示碳原子, 表示氮原子, 表示氧原子。下列说法正确的是
A.该反应中分子发生了改变
B.该反应为化合反应
C.该反应中最后生成物全部是化合物
D.反应前后元素种类发生变化
6.FeS 常用于在接触法制硫酸过程中产生SO ,其化学方程式为4FeS+11O 2X+8SO ,则X的化学式为
2 2 2 2 2
A.FeO B.Fe O
3 4
C.Fe O D.FeSO
2 3 4
7.在化学反应A+B AB 中,A与B 反应的质量关系如图所示,现将8 g A和5 g B 充分反应,则生成AB
2 2 2 2 2
的质量是A.10 g B.13 g C.16 g D.18 g
8.在一个密闭容器内有四种物质,一定条件下充分反应后,测得反应前后各物质的质量如表,下列推理正确的是
物质 X Y Z Q
反应前质量/g 4 10 1 21
反应后质量/g 0 12 15 待测
A.反应物是X和Y,成物是Q和Z
B.参加反应的Y和Q的质量比是1∶1
C.参加反应的X与Q的质量比是1∶3
D.反应后生成15 g Z
9.天平两边各放质量相等的烧杯,分别装入等质量、等溶质质量分数的稀硫酸,此时天平平衡,将等质量的
MgCO 和NaCO 分别加入两烧杯中,充分反应后,下列说法错误的是
3 2 3
A.若天平不平衡,指针一定偏向加NaCO 的一边
2 3
B.若天平平衡,两烧杯中的酸一定完全反应
C.若反应后NaCO 有剩余,天平一定平衡
2 3
D.若天平不平衡,两种碳酸盐一定都没有剩余
10.一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示,下列
说法正确的是
A.丁是该反应的催化剂
B.参与反应的乙、丙质量比为3∶17
C.该反应的基本类型是分解反应
D.参与反应的甲、丙质量比为7∶10
11.[2017·衢州]质量守恒定律是自然界基本的规律之一。下列装置及实验(天平未画出)能用来验证质量守恒定
律的是12.[2017·扬州] 某实验过程如下:取a g锡粉置于密闭容器中,称得容器和固体的总质量为 b g,煅烧使锡粉与
O 充分反应;冷却后打开容器时发现有空气冲入,待容器内气体组成恢复到反应前,称得容器和固体的总质量
2
为c g;取出所有固体,称得固体为d g,则c等于
A.d+b+a B.d﹣b﹣a
C.d﹣b+a D.d+b﹣a
13.[2017·郴州]碳可以与浓硫酸在加热的条件下发生如下反应:C+2HSO (浓) CO↑+2X↑+2HO,其中X的
2 4 2 2
化学式为
A.O B.SO
2 3
C.SO D.HS
2 2
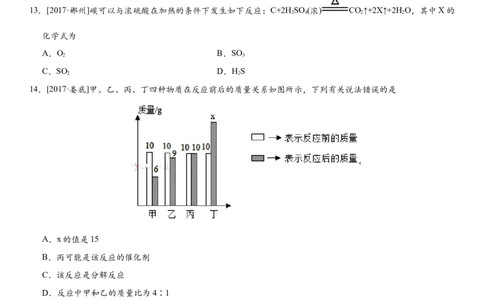
14.[2017·娄底]甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是
A.x的值是15
B.丙可能是该反应的催化剂
C.该反应是分解反应
D.反应中甲和乙的质量比为4∶1
15.[2017·铜仁]在一个密闭容器内有A、B、C、D四种物质,经过反应一段时间后,测得反应前后各物质的质量
如下表所示:
物质 甲 乙 丙 丁
反应前质量/克 34 2 5 5
反应后质量/克 0 x 5 21
以下说法正确的是
A.该反应是化合反应
B.x的值为18
C.该反应是分解反应D.丙一定是催化剂
16.[2017·淮安]质量守恒定律的发现对化学的发展作出了巨大贡献。
(1)为验证质量守恒定律,小华设计如图1所示装置进行实验。
实验时,先将装有药品的装置放在天平上,添加砝码,移动游码至天平平衡(如图 1所示),然后取下
装置,用针筒向锥形瓶中注入少量稀盐酸,反应后再将装置放置于天平上,观察到______________,从
而验证了质量守恒定律 。若将锥形瓶改为烧杯,则不能验证质量守恒定律,原因是
____________________________。
(2)某反应的微观示意图如图2所示。
①X的化学式是______________。
②根据上述微观示意图,可得出化学反应遵循质量守恒定律的本质原因是
______________________________________________________________________。
参考答案
1.【答案】A【解析】根据质量守恒定律,参加反应前各物质的质量总和等于反应后生成各物质的质量总和,设生成的 D的
质量为x,故5.6 g+7.3 g=12.7 g+x,解得:x=0.2 g。故选A。
2.【答案】C
【解析】A、如果分子的种类没有改变的话,就不属于化学变化,所以分子的种类一定变,错误;B、分子的数
目可能变,可能不变,错误;C、化学反应前后六个不变:原子的种类、数目、质量,元素种类、质量,物质
总质量,正确;D、如果物质种类没有改变的话,就不是化学变化了,所以物质的种类一定变,错误。故选
C。
3.【答案】C
【解析】化学变化的实质是分子分成原子,原子再重新组合成新分子,在反应前后,原子的种类和数目都不变。
故选C。
4.【答案】C
【解析】10 g A完全反应后生成8 g C和4 g D,由质量守恒定律可知,参加反应的B的质量为2 g,故参加
反应的A和B的质量比是10 g∶2 g=5∶1。故选C。
5.【答案】A
【解析】A、由汽车尾气处理过程可知,一氧化碳分子和一氧化氮分子发生化学变化变为氮气分子和二氧化碳分
子,故反应中分子发生了改变,正确;B、由微观示意图可知,一氧化碳和一氧化氮反应生成氮气和二氧化碳,
不属于化合反应,错误;C、根据示意图可知,生成物中有氮气生成,属于单质,错误;D、根据质量守恒定
律和反应微观示意图,化学反应前后元素种类不改变,错误。
6.【答案】C
7.【答案】A
8.【答案】C
9.【答案】D
10.【答案】B
【解析】由四种物质反应前后各物质的质量分数可知,反应前后甲的质量分数减少了70%﹣42%=28%,故甲是
反应物;同理可以通过图示确定乙的质量分数减少了14%﹣8%=6%,故乙是反应物;丙的质量分数增加了
40%﹣6%=34%,丙是生成物;丁的质量分数不变,可能作该反应的催化剂,也可能没有参加反应。A、丁的
质量分数不变,可能没有参加反应,也可能作该反应的催化剂,错误;B、参与反应的乙、丙的质量比为
6%∶34%=3∶17,正确;C、该反应的反应物为甲和乙,生成物是丙,符合“多变一”的特征,属于化合反
应,错误;D、该反应中甲、丙的质量比为28%∶34%=14∶17,错误。故选B。
11.【答案】A
【解析】A、盐酸能与硝酸银溶液反应生成氯化银白色沉淀和硝酸,能够用来验证质量守恒定律;B、水中加入
红墨水没有生成新物质,没有发生化学变化,不能用来验证质量守恒定律;C、镁带在空气中燃烧,反应后固
体质量会明显增大,因为有氧气参加,故不能直接验证质量守恒定律;D、过氧化氢溶液在二氧化锰的催化作
用下分解为水和氧气,反应物处在一个敞口容器中,生成的氧气会扩散到空气中,不能用来验证质量守恒定律故选A。
12.【答案】D
【解析】锡粉与氧气反应生成固体氧化锡,根据题意参加反应的氧气的质量为 c g﹣b g,根据质量守恒定律可知,
d g=a g+(c﹣b)g,因此c=d+b﹣a。故选D。
13.【答案】C
【解析】根据反应的化学方程式可知,反应物中碳、氢、硫、氧原子个数分别为 1、4、2、8,反应后的生成物
中碳、氢、硫、氧原子个数分别为1、4、0、4,根据反应前后原子种类、数目不变,则2X中含有2个硫原子
和4个氧原子,因此1个X分子中含有1个硫原子和2个氧原子,则物质X的化学式为SO 。故选C。
2
14.【答案】C
【解析】A、根据质量守恒定律,x=(10+10+10+10)﹣(6+9+10)=15,故说法正确;B、丙的质量在反应前后
没有变化,可能为该反应的催化剂,也可能不是,故说法正确;C、甲、乙的质量减小,为反应物,丁的质量
增加,为生成物,则此反应为化合反应,故说法错误;D、反应中甲、乙的质量比为(10﹣6)g∶(10﹣9)
g=4∶1,故说法正确。故选C。
15.【答案】C
【解析】根据质量守恒定律,反应后乙的质量为:x=34+2+5+5﹣(0+5+21)=20,故甲为反应物,乙、丁为生
成物,丙可能为催化剂,该反应为分解反应。A、甲为反应物,乙、丁为生成物,该反应为分解反应,错误;
B、x=20,错误;C、甲为反应物,乙、丁为生成物,该反应为分解反应,正确;D、丙可能是催化剂,也可能
不参加反应,错误。故选C。学&科网
16.【答案】(1)天平平衡 装置没有密闭,气体逸出
(2)①SO
2
②化学反应前后,原子质量、数目和种类不变