文档内容
专项训练(一) 酸、碱、盐综合训练
一、选择题
1.(2017·梧州)下列有关酸、碱、盐的描述错误的是( A )
A.碳酸钠俗称烧碱
B.浓硫酸有强腐蚀性
C.氢氧化镁是一种碱
D.氯化钠溶液中,钠、氯元素均以离子形式存在
2.(2017·广州)下列关于HSO 性质描述中,不属于酸的通性的是( C )
2 4
A.使紫色石蕊溶液变红
B.与NaOH发生中和反应
C.浓硫酸滴到白纸上使纸变黑
D.与Mg反应放出氢气
3.(2017·重庆B卷)小王同学往厨房的纯碱中滴加白醋,发现有气体生成。已知白醋里
含3%~5%的醋酸(CHCOOH),醋酸与盐酸的化学性质相似,下列说法不正确的是( D )
3
A.白醋里含有氢离子
B.生成的气体是二氧化碳
C.白醋能使紫色石蕊试液变红
D.白醋与纯碱的反应属于中和反应
4.(2017·宁波)有A、B两种酸碱指示剂,它们显示的颜色与溶液pH的关系如图,它们
在甲溶液和乙溶液中显示的颜色如表。下列判断错误的是( D )
溶液
甲 乙
指示剂
A 黄色 蓝色
B 无色 粉红色
A.甲溶液呈酸性
B.乙溶液的pH可能为11
C.只用A指示剂就可鉴别甲溶液、乙溶液和蒸馏水三种液体
D.在滴有A指示剂的甲溶液中不断地加入乙溶液,最后溶液一定呈绿色
5.(2017·菏泽)下列物质在水溶液中能大量共存的是( B )
A.NaCl NaCO HSO
2 3 2 4
B.CuSO KNO NaSO
4 3 2 4
C.BaCl NaOH NaCO
2 2 3
D.HCl NaSO NaOH
2 4
6.(2017·泰州)下列除去杂质(少量)的方法中正确的是( B )
选项 物质 杂质 除杂方法
A CaCO 固体 CaO 加足量稀盐酸,过滤
3
B O HO 通过浓硫酸洗气、收集
2 2
C Cu(NO) AgNO 加过量Fe粉,过滤
3 2 3溶液
D NaCl固体 KNO 配成热饱和溶液,降温结晶、过滤、洗涤、干燥
3
7.(2017·西宁)下列实验操作不能达到实验目的的是( B )
选项 实验目的 实验操作
A 鉴别NaOH和NaCl两种固体 分别加入少量水溶解
B 除去NaCl溶液中少量NaSO 先加入Ba(NO) 溶液,后过滤
2 4 3 2
C 除去H 中少量的水蒸气 将混合气体通过装有浓硫酸的洗气瓶
2
D 鉴别化肥KCl和NHCl 取样与熟石灰混合研磨,闻气味
4
8.(2017·达州)下列图象不能正确反映其对应变化关系的是( B )
A B
C D
A.向一定质量的硫酸铜和稀硫酸的混合溶液中逐滴加入氢氧化钠溶液
B.向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉
C.用等质量、等温度的过氧化氢溶液在有无催化剂条件下制氧气
D.一定质量稀盐酸中逐滴加入氢氧化钠溶液
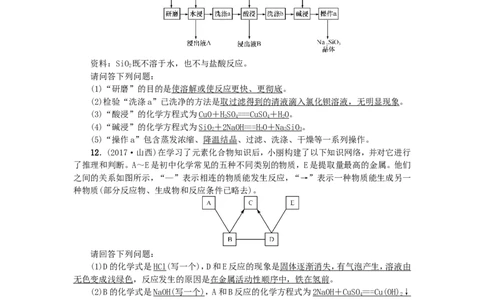
9.(2017·金华)利用饱和碳酸钠溶液与酸反应,小科同学制作了如图甲所示的简易酸
碱灭火器装置,并进行操作。操作结束后,对瓶中残留液进行如图乙所示的实验。实验现象:A
试管溶液变红色,B试管中有白色沉淀生成。则残留液中含有的溶质有( C )
A.盐酸 B.碳酸钠 C.硫酸钠 D.氯化钠
10.(2017·湖州)通过一步化学反应实现如图所示的X、Y、Z三种物质间转化,表格中X、Y、Z
对应的物质不能实现这种转化的是( B )选项 X Y Z
A CO NaCO CaCO
2 2 3 3
B CuO Cu(NO) Cu(OH)
3 2 2
C HCl BaCl NaCl
2
D Mg MgO MgCl
2
二、填空题
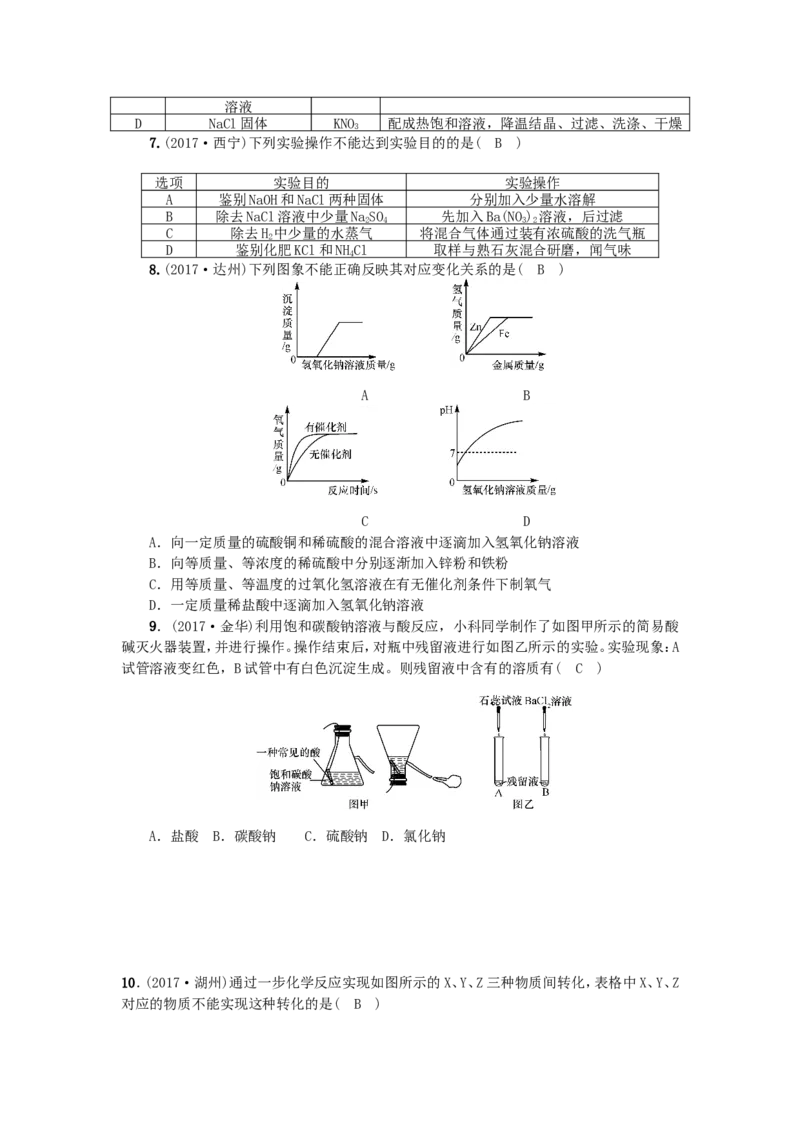
11.(2017·无锡)硅酸钠(NaSiO)是我国优先发展的精细化学品。用某种石英砂矿石
2 3
(主要成分是SiO,还含有少量的CuO、NaSO、NaCO)制备硅酸钠(NaSiO)的流程如下:
2 2 4 2 3 2 3
资料:SiO 既不溶于水,也不与盐酸反应。
2
请问答下列问题:
(1)“研磨”的目的是使溶解或使反应更快、更彻底。
(2)检验“洗涤a”已洗净的方法是取过滤得到的清液滴入氯化钡溶液,无明显现象。
(3)“酸浸”的化学方程式为 Cu O + HSO = = =CuS O + HO。
2 4 4 2
(4)“碱浸”的化学方程式为SiO + 2NaO H = = = H O + N aSiO。
2 2 2 3
(5)“操作a”包含蒸发浓缩、降温结晶、过滤、洗涤、干燥等一系列操作。
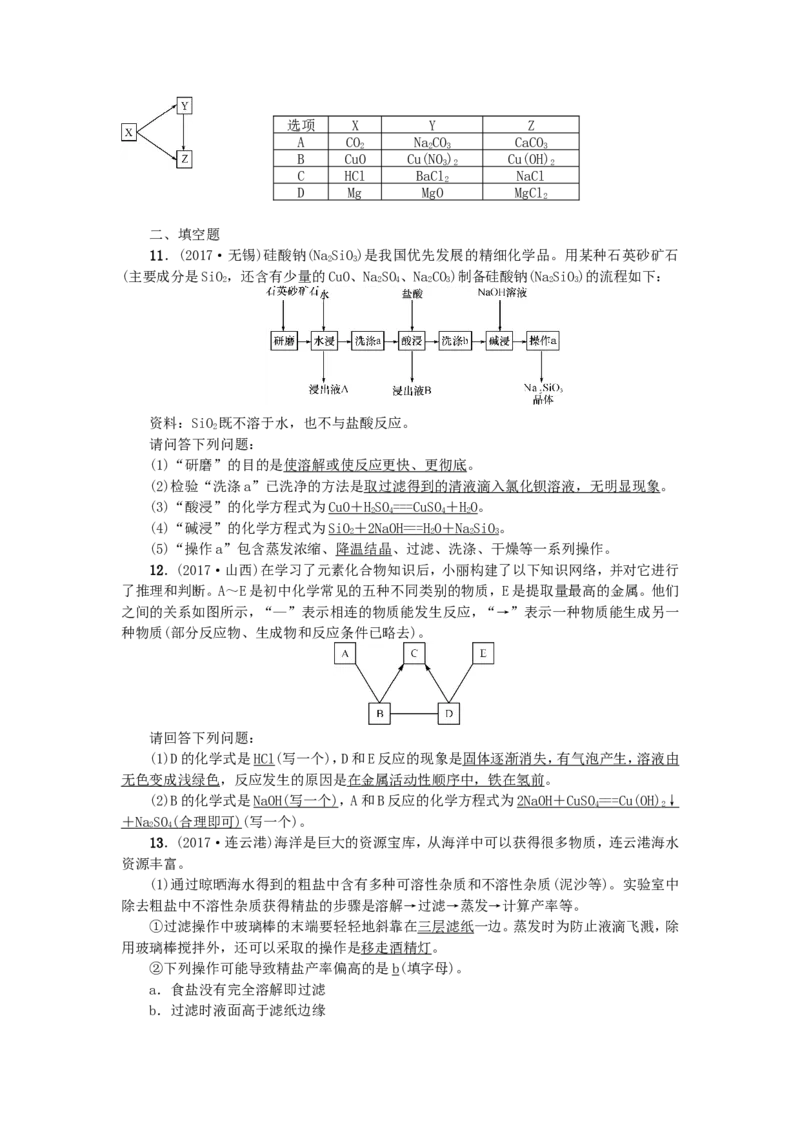
12.(2017·山西)在学习了元素化合物知识后,小丽构建了以下知识网络,并对它进行
了推理和判断。A~E是初中化学常见的五种不同类别的物质,E是提取量最高的金属。他们
之间的关系如图所示,“—”表示相连的物质能发生反应,“→”表示一种物质能生成另一
种物质(部分反应物、生成物和反应条件已略去)。
请回答下列问题:
(1)D的化学式是HCl(写一个),D和E反应的现象是固体逐渐消失,有气泡产生,溶液由
无色变成浅绿色,反应发生的原因是在金属活动性顺序中,铁在氢前。
(2)B的化学式是 NaOH ( 写一个 ),A和B反应的化学方程式为 2NaO H + CuS O = = =Cu(OH )↓
4 2
+ N aSO ( 合理即可 )(写一个)。
2 4
13.(2017·连云港)海洋是巨大的资源宝库,从海洋中可以获得很多物质,连云港海水
资源丰富。
(1)通过晾晒海水得到的粗盐中含有多种可溶性杂质和不溶性杂质(泥沙等)。实验室中
除去粗盐中不溶性杂质获得精盐的步骤是溶解→过滤→蒸发→计算产率等。
①过滤操作中玻璃棒的末端要轻轻地斜靠在三层滤纸一边。蒸发时为防止液滴飞溅,除
用玻璃棒搅拌外,还可以采取的操作是移走酒精灯。
②下列操作可能导致精盐产率偏高的是b(填字母)。
a.食盐没有完全溶解即过滤
b.过滤时液面高于滤纸边缘c.器皿上粘有的精盐没有全部转移到称量纸上
(2)海水中含量最多的氯化物是氯化钠,其次是氯化镁。下图是从海水中获得氯化镁溶
液的流程图。
①在海水中加入石灰乳后,发生反应的化学方程式是 MgCl + Ca(OH ) = = =Mg(OH )↓+
2 2 2
CaCl。
2
②上述过程中试剂A与沉淀B发生的是中和反应,则试剂A是盐酸(填名称)。
14.(2017·北京)下图为“领取奖杯游戏”的物质阶梯。当阶梯上相邻的物质之间能发
生反应,方可向上攀登。例如,攀登阶梯甲能领取奖杯。
(1)认识阶梯甲
①阶梯上的5种物质中,属于氧化物的是CO,俗称纯碱的是NaCO。
2 2 3
②攀登过程中,HSO 与NaCO 发生反应的化学方程式为NaCO + HSO = = =N aSO + H O +
2 4 2 3 2 3 2 4 2 4 2
CO↑。
2
(2)搭建阶梯乙
请你从O、Fe、FeO、HCl、NaOH中选择4种物质,写在图中相应的台阶上,能领取奖杯。
2 2 3
(3)共享物质、重塑阶梯
阶梯乙搭建完成后,若在阶梯甲和阶梯乙中各选择一种物质进行互换,也均能领取奖杯,
则这两种物质是HSO 和 HCl ( 或 F e 和 Mg )(任写一组即可)。
2 4
三、科学探究题
15.(2017·陕西)同学们在实验室用块状大理石和5%的稀盐酸反应制取CO,观察不到
2
气泡产生时,发现固体还有剩余,对此进行探究(杂质不溶于水且不与酸反应)。
【提出问题】不再产生气泡的原因是什么?
【猜想假设】
猜想一:盐酸已经完全反应;
猜想二:剩余固体中无碳酸钙;
猜想三:生成物或杂质附着在大理石表面,阻碍反应继续进行。
【实验探究一】反应后溶液中是否有盐酸。
(1)小亮取上述反应后的清液,测得溶液pH=2,说明溶液显酸性,由此得出猜想一不成
立的结论。
(2)小慧认为此结论不够严谨,还应考虑生成物对溶液酸碱度的影响,补充了如下实验。
①取洁净的烧杯,另配制 氯化钙 ( 或 CaC l)溶液,测得溶液pH=7。
2
②取洁净的试管,加入适量水和紫色石蕊溶液,持续通入CO,发现溶液变为红色。
2
但小亮认为实验②不能说明CO 对溶液酸碱度的影响,他重新改进了实验。
2
③另取洁净的试管,加入适量水,持续通入CO 至饱和,测得溶液pH=5.6。
2
由以上实验可知,该反应的生成物对溶液酸碱度影响不大,猜想一不成立,反应后的溶
液中有盐酸。
【实验探究二】剩余固体中是否有碳酸钙。小亮先振荡反应容器,使剩余固体和液体充分接触,观察到仍无气泡产生。再向容器中
滴加少量5%的稀盐酸,又有气泡产生。一段时间后,不再产生气泡,仍有固体剩余。产生气泡
的化学方程式是CaCO + 2HC l = = =CaC l + C O ↑+ HO。
3 2 2 2
由以上实验可知,猜想二和猜想三不成立。
【得出结论】根据以上实验探究,可得出影响反应能否进行的因素之一是反应物的浓度
大小。
【反思交流】小慧又提出,也可能是反应太慢,无法观察到气泡产生。她设计了如下对比
实验:取出【实验探究二】所得的部分清液,放置一段时间后,测得pH为X,同时测得【实验探
究二】容器中剩余清液的pH为Y,若X<(填“>”“=”或“<”)Y,则她的猜想成立。
四、计算题
16.(2017·江西)学习小组测定某工业废水(含有HSO、HNO,不含固体杂质)中HSO 的
2 4 3 2 4
含量。取100 g废水于烧杯中,加入100 g BaCl 溶液,恰好完全反应,经过滤得到176.7 g
2
溶液。(可溶性杂质不参加反应,过滤后滤液的损失忽略不计)
(1)充分反应后生成沉淀的质量为23.3g;
(2)该工业废水中硫酸的质量分数为多少?(写出计算过程)
(3)为避免工业废水污染环境,排放前应对废水进行中和处理,需加入的物质是氢氧化
钙等。
解:(2)设100 g工业废水中硫酸的质量x。
HSO+BaCl===BaSO↓+2HCl
2 4 2 4
98 233
x 23.3 g
= x=9.8 g
该工业废水中硫酸的质量分数为×100%=9.8%
答:该工业废水中硫酸的质量分数为9.8%。