文档内容
第14讲 物质的检验与鉴别、共存与除杂
命题点1 物质的共存(6年2考)
1.(2017·山西·29题·7分)经过监测和治理,我省的土壤质量已经得到了很好的改善,但个别地区
仍然存在盐碱地。某校化学兴趣小组的同学们为此开展了实践活动,他们采集了本地的土样,并对土样围绕
两个问题进行探究。
【查阅资料】
①枸杞和合欢均可在轻度盐碱地中生存。
②盐碱地显碱性。
③该土样中的可溶性物质只含NaCl、CaCl 和NaCO。
2 2 3
【探究过程】
(1)甲组探究土样的酸碱度
具体操作是 取 p H 试纸于玻璃片上,取少量土样,加入适量水,用玻璃棒蘸取上层清液滴在 p H 试纸上,
与标准比色卡对比,读数,由此得出,该土样的pH>7。
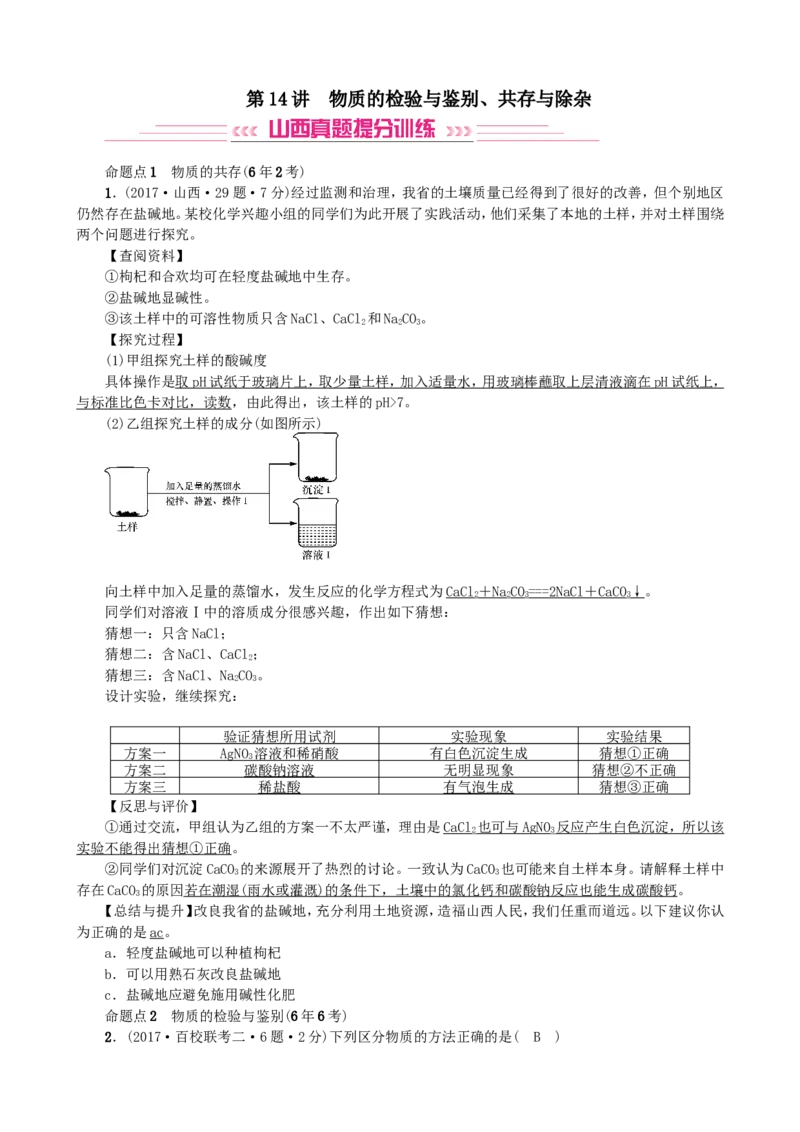
(2)乙组探究土样的成分(如图所示)
向土样中加入足量的蒸馏水,发生反应的化学方程式为CaCl + N aCO = = =2NaC l + CaC O↓。
2 2 3 3
同学们对溶液Ⅰ中的溶质成分很感兴趣,作出如下猜想:
猜想一:只含NaCl;
猜想二:含NaCl、CaCl;
2
猜想三:含NaCl、NaCO。
2 3
设计实验,继续探究:
验证猜想所用试剂 实验现象 实验结果
方案一 AgNO 溶液和稀硝酸 有白色沉淀生成 猜想①正确
3
方案二 碳酸钠溶液 无明显现象 猜想②不正确
方案三 稀盐酸 有气泡生成 猜想③正确
【反思与评价】
①通过交流,甲组认为乙组的方案一不太严谨,理由是CaCl 也可与 AgN O 反应产生白色沉淀,所以该
2 3
实验不能得出猜想①正确。
②同学们对沉淀CaCO 的来源展开了热烈的讨论。一致认为CaCO 也可能来自土样本身。请解释土样中
3 3
存在CaCO 的原因 若在潮湿 ( 雨水或灌溉 ) 的条件下,土壤中的氯化钙和碳酸钠反应也能生成碳酸钙 。
3
【总结与提升】改良我省的盐碱地,充分利用土地资源,造福山西人民,我们任重而道远。以下建议你认
为正确的是ac。
a.轻度盐碱地可以种植枸杞
b.可以用熟石灰改良盐碱地
c.盐碱地应避免施用碱性化肥
命题点2 物质的检验与鉴别(6年6考)
2.(2017·百校联考二·6题·2分)下列区分物质的方法正确的是( B )A.用水区分炭粉和二氧化锰
B.用灼烧法区分合成纤维和羊毛
C.用燃着的木条区分二氧化碳和氮气
D.用酚酞溶液区分氢氧化钠和碳酸钠
3.(2013·山西·27题·7分)化学小组同学为鉴定某工厂排出的无色污水成分,他们查阅工厂的有关
资料后,推测出污水中可能含有HCl、NaSO、NaOH、NaCO 中的一种或几种物质,同学们取污水进行了探究:
2 4 2 3
(已知NaSO 溶液呈中性)
2 4
(1)测污水的pH:取一张pH试纸,放在玻璃片上, 用玻璃棒蘸取污水样品,滴在 p H 试纸上,与标准比色
卡比较,读数为pH=2,由此可知:污水中一定有HCl,可能有NaSO。
2 4
(2)检验NaSO 是否存在:甲同学在一支试管中取少量污水,向试管中滴加少量的 BaCl[Ba(OH) 或
2 4 2 2
Ba(NO)]溶液,振荡,产生了白色沉淀,反应的化学方程式为BaCl + N aSO = = =BaS O ↓+ 2NaCl ( 合理即可 ),
3 2 2 2 4 4
证明污水中有NaSO 存在。乙同学用物理方法也得到了同样的结论,他的实验操作及实验现象是从试管中
2 4
取少量污水蒸干 ( 或玻璃片上滴几滴污水晾干 ) ,有白色固体析出 。
通过探究,同学们确定了污水的成分。
为使排放的污水中不含酸或碱,可向污水中加过量的石灰石。
命题点3 物质的除杂(6年4考)
4.(2014·山西·10题·2分)下列实验室中实验设计不合理的是( C )
选项 实验目的 操作或所用试剂
A 除去NaCl固体中混有的泥沙 溶解、过滤、蒸发
NaOH溶液、
B 除去CO中混有的CO
2 浓HSO
2 4
C 鉴别食盐、蔗糖 品尝
D 鉴别HO、KCl溶液 AgNO 溶液
2 3
5.(2015·山西·10题·2分)下列实验设计能达到实验目的的是( C )
选项 实验目的 实验方案
A 检验某气体是否为二氧化碳 用燃着的木条
B 稀释浓硫酸 将水缓慢加入浓硫酸中,并搅拌
C 区分氧化钙与碳酸钙 取样品,加入适量水
D 除去KSO 溶液中的KOH 加入适量稀盐酸
2 4
6.(2017·百校联考四·8题·2分)下列实验方法不能达到目的的是( D )
A.鉴别硬水和软水——用肥皂水
B.鉴别CuO粉、铁粉——用稀硫酸
C.除去CaO中的CaCO——高温煅烧
3
D.除去FeSO 溶液中的CuSO——加足量锌,过滤
4 4
提分训练1 物质的共存
(易错题)(2017·泰安)下列物质能在pH=13的无色溶液中大量共存的是( D )
A.NaNO、NaCl、KNO、(NH)SO
3 3 4 2 4
B.HSO、HCl、AgNO、NaSO
2 4 3 2 4
C.KMnO、CuCl、Fe(SO)、NaNO
4 2 2 4 3 3
D.KSO、NaCl、KCO、NaOH
2 4 2 3
提分训练2 物质的检验与鉴别
(2017·成都)能用于鉴别氢氧化钠溶液和氢氧化钙溶液的物质是( C )
A.HCl B.KNO
3C.KCO D.FeCl
2 3 3
(2017·达州)下列各组溶液,不外加试剂就能鉴别出来的是( A )
A.NaCO、HCl、BaCl、NaCl
2 3 2
B.NaOH、FeCl、HCl、HNO
3 3
C.NaCO、NaCl、NaSO、Ba(OH)
2 3 2 4 2
D.NaOH、Ba(NO)、NaCl、MgSO
3 2 4
提分训练3 物质的除杂
(2017·广州)下列除杂所选用试剂与操作方法均正确的是( D )
选项 物质(括号内为杂质) 除杂试剂 实验操作
A CaO(CaCO) 水 溶解、过滤
3
B H(CO) 灼热CuO 洗气
2
C NaCl(NaSO) 过量BaCl 溶液 过滤
2 4 2
D NaCl(NaCO) 足量稀盐酸 蒸发结晶
2 3
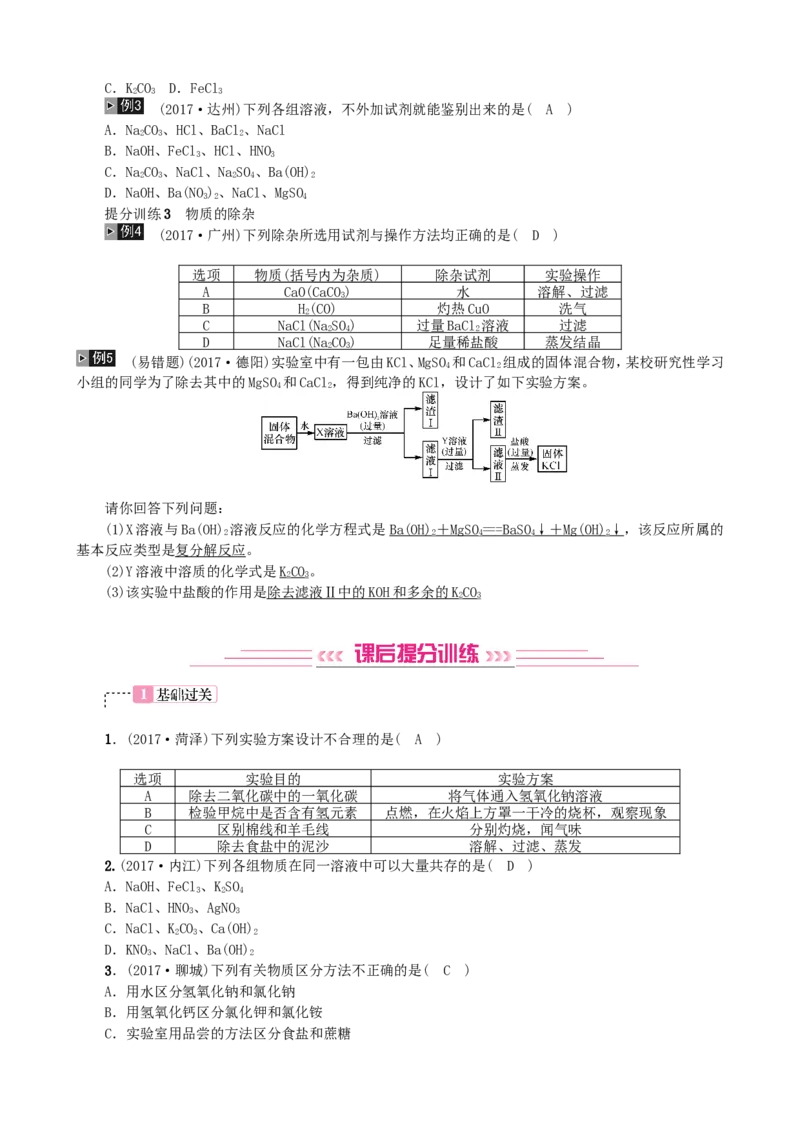
(易错题)(2017·德阳)实验室中有一包由KCl、MgSO 和CaCl 组成的固体混合物,某校研究性学习
4 2
小组的同学为了除去其中的MgSO 和CaCl,得到纯净的KCl,设计了如下实验方案。
4 2
请你回答下列问题:
(1)X溶液与Ba(OH) 溶液反应的化学方程式是Ba(OH) + MgS O = = =BaS O ↓+ Mg(OH )↓,该反应所属的
2 2 4 4 2
基本反应类型是复分解反应。
(2)Y溶液中溶质的化学式是KCO。
2 3
(3)该实验中盐酸的作用是 除去滤液Ⅱ中的 KO H 和多余的 KCO
2 3
1.(2017·菏泽)下列实验方案设计不合理的是( A )
选项 实验目的 实验方案
A 除去二氧化碳中的一氧化碳 将气体通入氢氧化钠溶液
B 检验甲烷中是否含有氢元素 点燃,在火焰上方罩一干冷的烧杯,观察现象
C 区别棉线和羊毛线 分别灼烧,闻气味
D 除去食盐中的泥沙 溶解、过滤、蒸发
2.(2017·内江)下列各组物质在同一溶液中可以大量共存的是( D )
A.NaOH、FeCl、KSO
3 2 4
B.NaCl、HNO、AgNO
3 3
C.NaCl、KCO、Ca(OH)
2 3 2
D.KNO、NaCl、Ba(OH)
3 2
3.(2017·聊城)下列有关物质区分方法不正确的是( C )
A.用水区分氢氧化钠和氯化钠
B.用氢氧化钙区分氯化钾和氯化铵
C.实验室用品尝的方法区分食盐和蔗糖D.用灼烧闻气味的方法区分羊绒线和棉线
4.(2017·德阳)实验室有一包含少量氯化钠杂质的硝酸钾固体,某校化学兴趣小组的同学为了得到纯
净的硝酸钾。设计了如图所示的操作,下列有关分析中正确的是( D )
A.操作Ⅰ~操作Ⅲ分别是溶解、加热蒸发、过滤
B.操作Ⅰ是过滤,将氯化钠固体从硝酸钾中分离除去
C.操作Ⅱ是加热浓缩,趁热过滤,除去杂质氯化钠
D.操作Ⅲ是过滤,将硝酸钾晶体从溶液中分离出来
5.(2017·南充)下列实验操作不能达到实验目的的是( B )
选项 实验目的 实验操作
A 除去氧气中少量的水蒸气 通过盛有浓硫酸的洗气瓶
B 除去NaCl溶液中的NaCO 加适量稀硫酸
2 3
鉴别:①CuSO 溶液;②FeCl 溶液; 不加其他试剂,利用组内物质的颜色和
C 4 3
③NaCl溶液;④NaOH溶液 相互反应进行鉴别
D 除去稀盐酸中混有的少量硫酸 加入适量的BaCl 溶液,再过滤
2
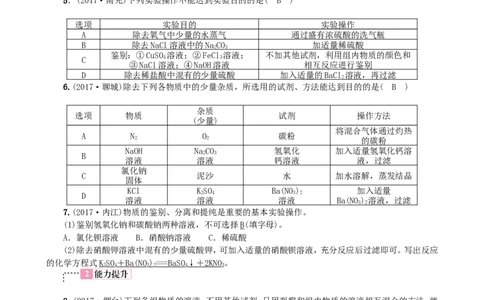
6.(2017·聊城)除去下列各物质中的少量杂质,所选用的试剂、方法能达到目的的是( B )
杂质
选项 物质 试剂 操作方法
(少量)
将混合气体通过灼热
A N O 碳粉
2 2 的碳粉
NaOH NaCO 氢氧化 加入适量氢氧化钙溶
B 2 3
溶液 溶液 钙溶液 液,过滤
氯化钠
C 泥沙 水 加水溶解,蒸发结晶
固体
KCl KSO Ba(NO) 加入适量
D 2 4 3 2
溶液 溶液 溶液 Ba(NO) 溶液,过滤
3 2
7.(2017·内江)物质的鉴别、分离和提纯是重要的基本实验操作。
(1)鉴别氢氧化钠和碳酸钠两种溶液,不可选择B(填字母)。
A.氯化钡溶液 B.硝酸钠溶液 C.稀硫酸
(2)除去硝酸钾溶液中混有的少量硫酸钾,可加入适量的硝酸钡溶液,充分反应后过滤即可。写出反应
的化学方程式KSO + Ba(N O) = = =BaS O ↓+ 2KN O。
2 4 3 2 4 3
8.(2017·烟台)下列各组物质的溶液,不用其他试剂,只用观察和组内物质的溶液相互混合的方法,就
能将它们一一鉴别出来的是( D )
A.NaCl、BaCl、CuSO、KNO
2 4 3
B.Ba(NO)、NaCl、NaSO、HCl
3 2 2 4
C.NaOH、CuCl、NaSO、KCl
2 2 4
D.HCl、NaCO、KCl、CaCl
2 3 2
9.(2017·泰安)现有含杂质的硝酸钠溶液,为确定其组成,某同学设计了如下实验,下列判断正确的是
( D )A.无色溶液B的溶质只有硝酸钙
B.该实验中涉及的基本反应类型不止一种
C.原溶液中的杂质只有氯化钙
D.原溶液中杂质可能由氯化钙、硝酸钙、氯化钠组成
10.(2017·天水)下列各组物质加入水中充分搅拌后,同组反应物恰好完全反应,过滤后,在滤纸上留
下两种不溶物质的是( D )
A.Ca(NO)、BaCl、AgNO
3 2 2 3
B.MgCl、KOH、NaCl
2
C.KCO、CuSO、KCl
2 3 4
D.CuSO、Ba(OH)、Cu(NO)
4 2 3 2
11.(2017·临沂)某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动。请你和他们
一起完成以下实验探究。
【演示实验】将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中。该反应的化学方程式是 2HCl +
Ca(OH) = = =CaC l + 2 HO。
2 2 2
【查阅资料】CaCl 溶液显中性。
2
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质的成分是什么?
【猜想与假设】针对疑问,甲组同学猜想如下:
猜想Ⅰ:只有CaCl;
2
猜想Ⅱ:有CaCl 和HCl;
2
猜想Ⅲ:有CaCl 和Ca(OH);
2 2
猜想Ⅳ:有CaCl、HCl和Ca(OH)。
2 2
乙组同学对以上猜想提出质疑,认为猜想Ⅳ不合理,其理由是 HC l 和 Ca(OH ) 不能共存。
2
【实验探究】为了验证其余猜想,各小组进行了下列三个方案的探究。
实验 滴加紫色 滴加NaCO
通入CO 2 3
方案 石蕊溶液 2 溶液
实验
操作
实验
石蕊溶液变蓝 溶液变浑浊 产生白色沉淀
现象
实验 溶液中含有 溶液中含有 溶液中含有
结论 Ca(OH) Ca(OH) Ca(OH)
2 2 2
【得出结论】通过探究,全班同学一致确定猜想Ⅲ是正确的。
【评价反思】
(1)丙组同学认为滴加NaCO 溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH),请你帮助他们
2 3 2
说明原因CaCl 与 N aCO 反应也会生成白色沉淀,不能证明一定有 Ca(OH ) 存在。
2 2 3 2
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外.还需要考虑反应物是否过量。