文档内容
第3讲 水和溶液
命题点1 水的组成(6年2考)
1.(2013·山西·23题·6分)水是宝贵的自然资源。请回答下列问题:
(1)电解水的化学方程式是2H O ===== 2 H ↑+ O 通过该实验得到的结论是水是由氢、氧
2 2 2
两种元素组成的。
(2)某自来水厂对汾河水进行净化,取水后,首先向其中加入明矾,再经过过滤、消毒灭
菌后使之达到饮水标准。明矾可用于净水,是因为明矾溶于水的生成物可以吸附悬浮于水中
的杂质,加速沉降。要测定饮用水是软水还是硬水,可用肥皂水来检验。
(3)水是一种重要的化学资源,写出实验室用水鉴别的一组物质 碳酸钙和碳酸钠 ( 或生
石灰和熟石灰或硝酸铵、氢氧化钠和氯化钠或硫酸铜和氯化钠等合理即可 )。
2.(2014·山西·6题·2分)有关水的认识正确的是( C )
A.电解水得到H 和O,可知水由氢原子和氧原子组成
2 2
B.生活中用过滤的方法可以降低水的硬度
C.净水的方法有沉降、过滤、吸附、蒸馏
D.KMnO、NaCl、汽油加入一定量的水中都能形成溶液
4
命题点2 水的净化(6年3考)
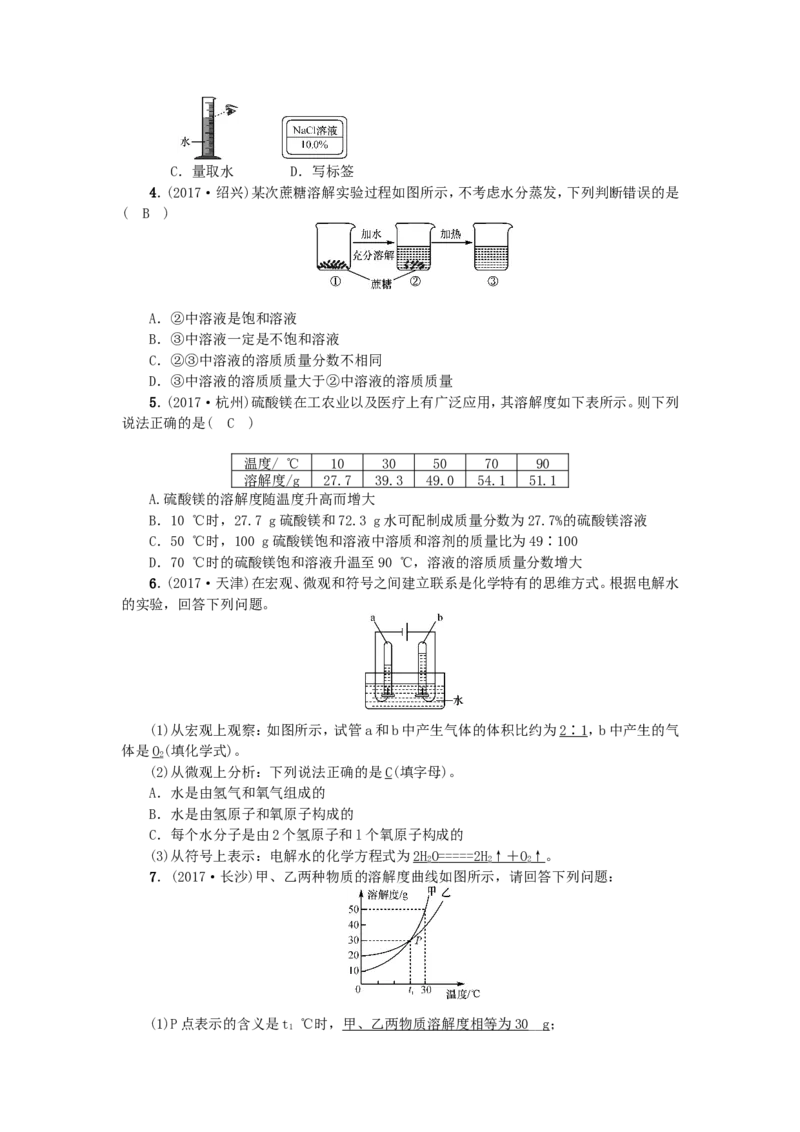
3.(2017·山西·24题·5分)水体污染主要来自工业废水、农业用水和生活污水。水体
被污染,必将影响整个地球的自然环境,对人类产生严重的危害。下图为污水处理流程示意
图,污水经物理、化学或生化方法分级处理后,可达到农灌和废水排放标准或绿化和景观用
水标准。
(1)污水通过“格栅”可去除较大的悬浮物、漂浮物,相当于基本实验操作中的过滤。
(2)污泥处理可得到沼气(主要成分为 CH),写出 CH 燃烧的化学方程式 CH +
4 4 4
2O ==== = C O + 2 HO。
2 2 2
(3)消毒处理属于化学变化。
(4)消毒处理后的某无色透明水样中含有钾盐,用简单的方法证明此水样为混合物取适
量污水于蒸发皿中,蒸干,有白色固体析出 ( 或取适量污水于洁净的透明玻璃片上,晾干,玻璃片上有白色固体析出,答案合理即可 )。
4.(2015·山西·4题·2分)小李学习了水的有关知识后,自制了如图所示的简易净水
器,下列说法正确的是( A )
A.该净水器中的活性炭起吸附作用
B.该净水器可以降低自来水的硬度
C.该净水器能起到杀菌消毒的作用
D.该净水器可将自来水变为蒸馏水
命题点3 溶液的形成及其乳化(6年1考)
5.(2015·山西·3题·2分)下列物质放入水中,不能形成溶液的是( B )
A.蔗糖 B.植物油
C.食盐 D.食用纯碱
6.(2016·百校联考二·6题·2分)生活中处处蕴含着化学知识。下列说法错误的是(
A )
A.厨房天然气泄漏,应立即打开油烟机排气
B.洗涤剂去除油污是由于洗涤剂具有乳化的功能
C.药品中的NaHCO 可与过多胃酸反应
3
D.不可用铁制容器长期贮存食醋
命题点4 溶解度(6年6考)
7.(2015·山西·23题·5分)如图是甲、乙两种固体物质的溶解度曲线。
(1)由图可获得的一条信息是t__℃时,甲和乙的溶解度相等。
1
(2)若乙中混有少量甲,提纯乙的方法是蒸发结晶。
(3)t ℃时,将不饱和的甲溶液转化成该温度下的饱和溶液的一种方法是加入溶质。变
2
化过程中,溶质的质量分数增大(填“增大”“减小”或“不变”)。
(4)将等质量的甲、乙两种物质的溶液由t ℃降温至t ℃时,析出晶体的质量C(填序
2 1
号)。
A.甲>乙 B.甲<乙 C.无法确定
8.(2017·山西·23题·3分)小华在饮用碳酸饮料时。发现有大量气泡冒出。他联系学
过的知识从不同角度加以解释。从物理变化的角度解释为气体溶解度随压强的减小而减小,
打开饮料瓶塞,气压减小,二氧化碳溶解度降低,所以有大量气泡冒出。从化学变化的角度解
释为HCO = = =C O ↑+ HO(化学方程式表示)。
2 3 2 2
命题点5 溶液的配制及浓度的计算(6年5考)
9.(2013·山西·26题·1分)同学们在实验室用5%的HO 溶液制取氧气并进行氧气性
2 2
质实验。
溶液配制:用50 mL 30%的HO 溶液(密度为1.13 g/cm3)配制5%的HO 溶液(密度约为1
2 2 2 2g/cm3)。溶液配制过程中,除用到玻璃棒外还需用到下列仪器中的BDE。
A.托盘天平 B.烧杯 C.漏斗
D.量筒 E.胶头滴管
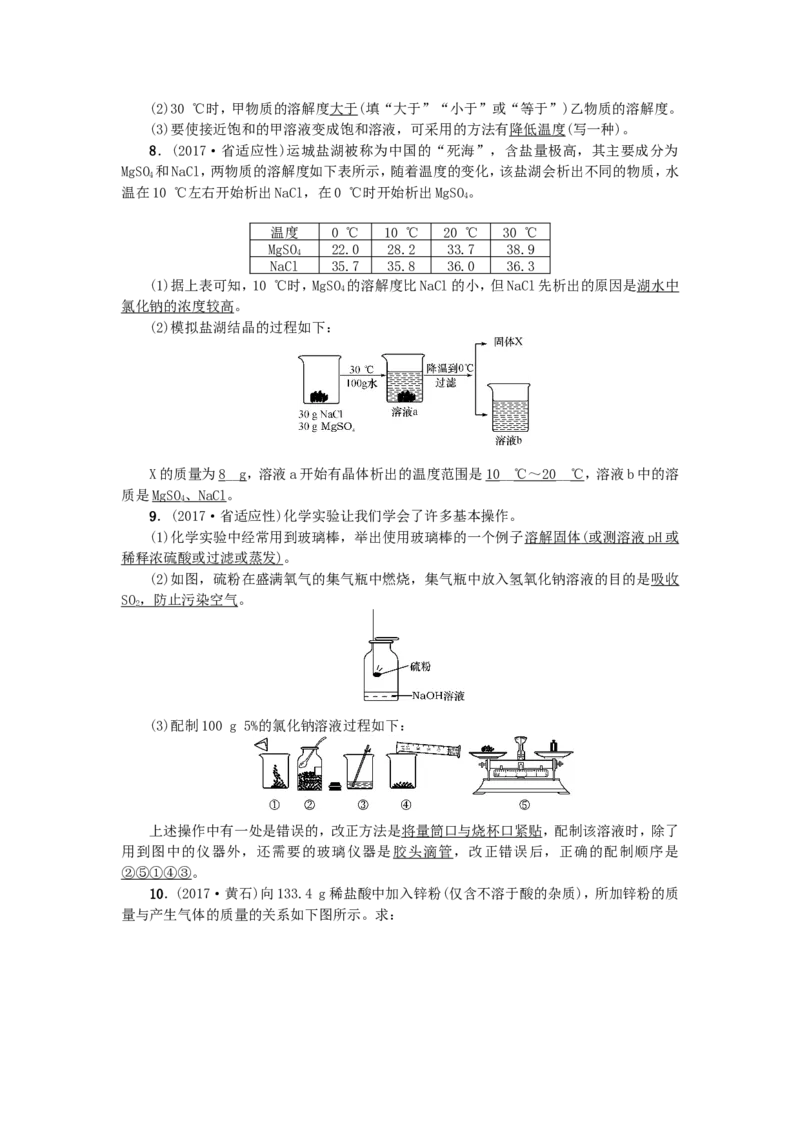
10.(2015·山西·28题·7分)某合作学习小组的同学们欲测定一定量的某种石灰石样
品中碳酸钙的质量,进行了如下实验:
(1)配制溶质质量分数为7.3%的稀盐酸。
①配制100 g溶质质量分数为7.3%的稀盐酸,需图1所示盐酸的质量 20( 1 分 )g。
②量取盐酸与水时,视线要与量筒内液体凹液面的 最低处 ( 1 分 )保持水平,再读出液体
的体积。将两种液体都倒人 烧杯 ( 1 分 )(填仪器名称)中,用玻璃棒搅拌,使溶液混合均匀。
(2)将(1)中配制好的稀盐酸加入盛有石灰石样品的烧杯中,产生气体的质量与加入稀
盐酸的质量关系如图2所示(假设石灰石样品中的杂质不与稀盐酸反应)。计算:该石灰石样
品中碳酸钙的质量。
解:设参加反应的碳酸钙的质量为x。
CaCO+2HCl===CaCl+HO+CO↑
3 2 2 2
100 73
x 75 g×7.3%
=
x=7.5 g
答:该石灰石样品中碳酸钙的质量为7.5 g。
提分训练1 水的净化
(2017·百校联考一)自然界中的水因含有许多杂质而需要净化,下列操作中不
属于水的净化方法的是( C )
A.蒸馏 B.活性炭吸附
C.加入肥皂水 D.过滤
(2017·江西)下列单一操作中,自然界的水净化程度最高的是( B )
A.过滤 B.蒸馏
C.吸附 D.静置沉淀
提分训练2 溶解度
(2017·北京)25 ℃时,向下列4只盛有100 g水的烧杯中,分别加入不同质量
的KCl固体,充分溶解。(1)①中溶液的质量为( D )
A.10 g B.90 g C.100 g D.110 g
(2)上述溶液为饱和溶液的是( D )
A.②③④ B.②④ C.③④ D.④
(3)能将不饱和KCl溶液变为饱和KCl溶液的方法是( C )
A.升高温度 B.加水
C.加KCl固体 D.倒出部分溶液
(4)(易错题)④中溶液的溶质质量分数约为( A )
A.26% B.29% C.35% D.40%
(2014·山西)根据表中的数据,回答下列问题。
温度/℃ 0 20 40 60 80 100
溶解 NaCl 35.7 36.0 36.6 37.3 38.4 39.8
度/g KNO 13.3 31.6 63.9 110 169 246
3
(1)40 ℃时,NaCl的溶解度是36.6__g。
(2)20 ℃时,称取31.6 g KNO 固体加入盛有100 g水的烧杯中,充分溶解形成的溶液
3
是饱和(填“饱和”或“不饱和”)溶液;称取31.6 g KNO 固体时,发现托盘天平指针偏右,
3
接下来的操作是 继续加 KN O 至天平平衡。
3
(3)当KNO 中混有少量NaCl时,提纯KNO 所采用的方法为 降温结晶 ( 或冷却热饱和溶
3 3
液 )。
(4)将等质量KNO 的饱和溶液和NaCl的饱和溶液从60 ℃降温到20 ℃,对所得溶液的
3
叙述正确的是 A 、 C(填序号)。
A.都是饱和溶液 B.溶剂质量:KNO>NaCl C.溶液质量:KNO”“=”或“<”)硝酸钾的溶解度。
②表中某物质的饱和溶液随温度升高析出固体,该物质是Ca(OH)(填化学式)。
2
③20 ℃时,氯化钠饱和溶液中溶质的质量分数为26.5%(结果保留至0.1%)。
④向20 ℃的氢氧化钙饱和溶液中加入少量生石灰,再冷却至20 ℃,此时溶液中溶质
的质量比加入生石灰前溶液中溶质的质量减小(填“增大”“不变”或“减小”)。
⑤混有少量氯化钠的硝酸钾固体,加水配成80 ℃的硝酸钾饱和溶液,再冷却至20 ℃,
析出晶体并得到溶液。下列有关说法中正确的是B(填字母)。
A.析出的晶体中不一定含有硝酸钾
B.所得溶液一定是硝酸钾饱和溶液
C.上述方法可以将两种物质完全分离12.(2017·南京)溶液在生产、生活中起着十分重要的作用。请回答下列问题:
(1)可以作为溶质的是D。
A.只有固体 B.只有液体
C.只有气体 D.气体、液体、固体都可以
(2)配制100 g质量分数为16%的氯化钠溶液,所需氯化钠的质量为16__g,水的体积为
84mL(水的密度近似看作1 g/cm3)。
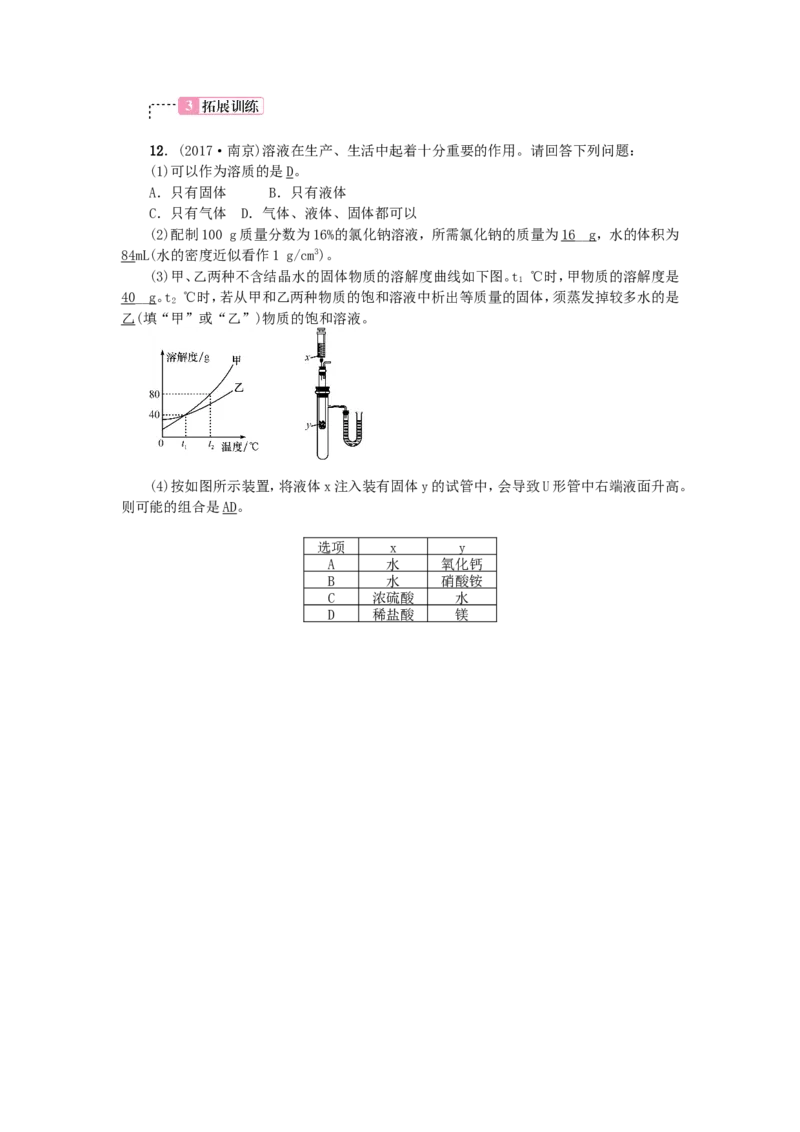
(3)甲、乙两种不含结晶水的固体物质的溶解度曲线如下图。t ℃时,甲物质的溶解度是
1
40__g。t ℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水的是
2
乙(填“甲”或“乙”)物质的饱和溶液。
(4)按如图所示装置,将液体x注入装有固体y的试管中,会导致U形管中右端液面升高。
则可能的组合是AD。
选项 x y
A 水 氧化钙
B 水 硝酸铵
C 浓硫酸 水
D 稀盐酸 镁