文档内容
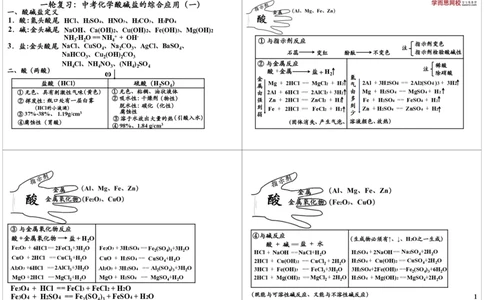
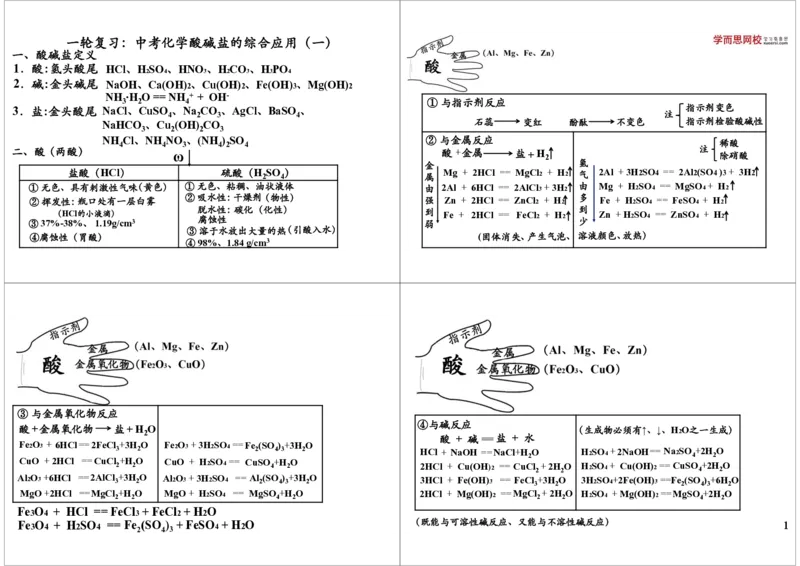
一轮复习:中考化学酸碱盐的综合应用(一)
一、酸碱盐定义
1.酸:氢头酸尾 HCl、H SO 、HNO 、H CO 、H PO
2 4 3 2 3 3 4
2.碱:金头碱尾 NaOH、Ca(OH) 2、Cu(OH) 2、Fe(OH) 3、Mg(OH)
2
NH ·H O == NH + + OH-
3 2 4 ①与指示剂反应
3.盐:金头酸尾 NaCl、CuSO 、Na CO 、AgCl、BaSO 、 指示剂变色
4 2 3 4 注
NaHCO 、Cu (OH) CO 石蕊 变红 酚酞 不变色 指示剂检验酸碱性
3 2 2 3
NH
4
Cl、NH
4
NO
3
、(NH
4
)
2
SO
4
②与金属反应
稀酸
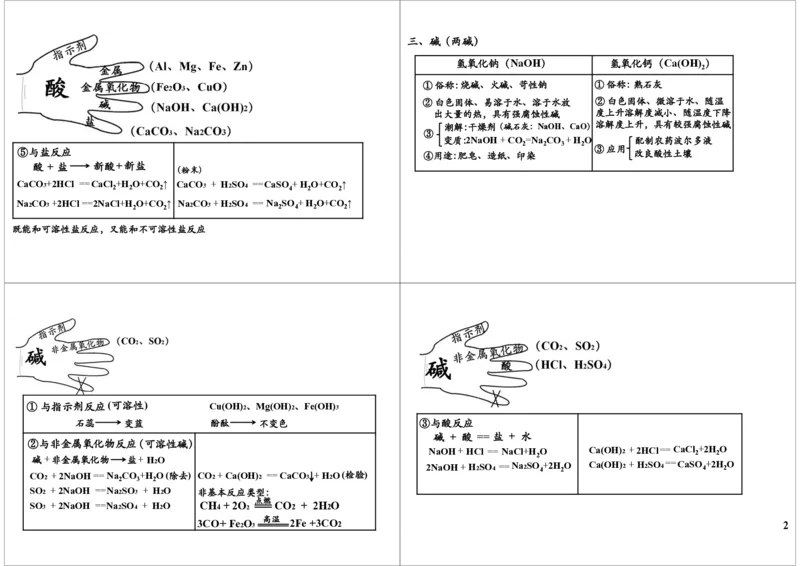
二、酸(两酸) ω 酸 +金属 盐+H 2 注 除硝酸
金 氢
盐酸(HCl) 硫酸(H 2 SO 4 ) 属 Mg + 2HCl == MgCl 2 + H 2 气 2Al + 3H2SO4 == 2Al2(SO4)3+ 3H2
①无色、具有刺激性气味(黄色) ①无色、粘稠、油状液体 由 2Al + 6HCl == 2AlCl 3 + 3H 2 由 Mg + H 2 SO 4 == MgSO 4 + H 2
②挥发性:瓶口处有一层白雾 ②吸水性:干燥剂(物性) 强 Zn + 2HCl == ZnCl 2 + H 2 多 Fe + H 2 SO 4 == FeSO 4 + H 2
③37% ( - H 38 C % l的 、 小液 1.1 滴 9 ) g/cm3 脱 腐 水 蚀 性 性 :碳化(化性) 到 弱 Fe + 2HCl == FeCl 2 + H 2 到 少 Zn + H 2 SO 4 == ZnSO 4 + H 2
③溶于水放出大量的热(引酸入水)
④腐蚀性(胃酸) (固体消失、产生气泡、溶液颜色、放热)
④98%、1.84g/cm3
③与金属氧化物反应
④与碱反应
酸+金属氧化物 盐+H
2
O (生成物必须有↑、↓、H
2
O之一生成)
酸 + 碱==盐 + 水
Fe 2 O 3 + 6HCl==2FeCl 3 +3H 2 O Fe 2 O 3 + 3H 2 SO 4 ==Fe 2 (SO 4 ) 3 +3H 2 O HCl + NaOH ==NaCl+H 2 O H 2 SO 4 +2NaOH== Na 2 SO 4 +2H 2 O
CuO + 2HCl ==CuCl 2 +H 2 O CuO + H 2 SO 4 == CuSO 4 +H 2 O 2HCl + Cu(OH)2 == CuCl 2 + 2H 2 O H 2 SO 4 + Cu(OH) 2 ==CuSO 4 +2H 2 O
Al 2 O 3 +6HCl ==2AlCl 3 +3H 2 O Al 2 O 3 + 3H 2 SO 4 == Al 2 (SO 4 ) 3 +3H 2 O 3HCl + Fe(OH) 3 == FeCl 3 +3H 2 O 3H 2 SO 4 +2Fe(OH) 3 ==Fe 2 (SO 4 ) 3 +6H 2 O
MgO+2HCl ==MgCl 2 +H 2 O MgO+ H 2 SO 4 == MgSO 4 +H 2 O 2HCl + Mg(OH) 2 ==MgCl 2 + 2H 2 O H 2 SO 4 + Mg(OH) 2 ==MgSO 4 +2H 2 O
Fe3O4 + HCl ==FeCl
3
+ FeCl
2
+ H2O
Fe3O4 + H2SO4 == Fe
2
(SO
4
)
3
+ FeSO
4
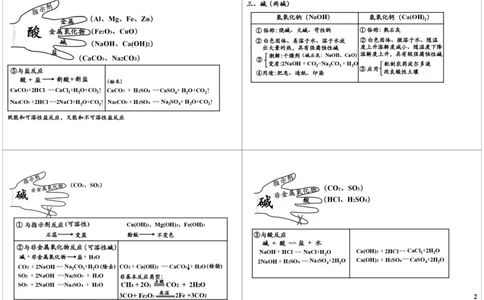
+ H2O (既能与可溶性碱反应、又能与不溶性碱反应) 1三、碱(两碱)
氢氧化钠(NaOH) 氢氧化钙(Ca(OH) )
2
①俗称:烧碱、火碱、苛性钠 ①俗称:熟石灰
②白色固体、易溶于水、溶于水放 ②白色固体、微溶于水、随温
出大量的热,具有强腐蚀性碱 度上升溶解度减小、随温度下降
潮解:干燥剂(碱石灰:NaOH、CaO)溶解度上升,具有较强腐蚀性碱
③
变质:2NaOH + CO =Na CO + H O 配制农药波尔多液
2 2 3 2
⑤与盐反应 ④用途:肥皂、造纸、印染 ③应用 改良酸性土壤
酸 + 盐 新酸+新盐
(粉末)
CaCO 3 +2HCl ==CaCl 2 +H 2 O+CO 2 ↑ CaCO 3 + H 2 SO 4 ==CaSO 4 + H 2 O+CO 2 ↑
Na 2 CO 3 +2HCl ==2NaCl+H 2 O+CO 2 ↑ Na 2 CO 3 + H 2 SO 4 == Na 2 SO 4 + H 2 O+CO 2 ↑
既能和可溶性盐反应,又能和不可溶性盐反应
①与指示剂反应(可溶性) Cu(OH) 2、Mg(OH) 2、Fe(OH)
3
石蕊 变蓝 酚酞 不变色 ③与酸反应
碱 + 酸 == 盐 + 水
②与非金属氧化物反应(可溶性碱)
碱+非金属氧化物 盐+ H
2
O
2
N
N
a
a
O
O
H
H
+
+
H
H
C
2 S
l
O
=
4
=
=
N
=
a
N
C
a
l+
2 S
H
O
2 O
4 +2H 2 O
C
C
a
a
(
(
O
O
H
H
)
)
2
2
+
+
2
H
H
2 S
C
O
l=
4 =
=
=
C
C
a
a
C
S
l
O
2 +
4
2
+
H
2H
2 O
2 O
CO 2 + 2NaOH ==Na 2 CO 3 +H 2 O(除去) CO 2 + Ca(OH) 2 ==CaCO 3 + H 2 O(检验)
SO 2 + 2NaOH ==Na 2 SO 3 + H 2 O 非基本反应类型:
点燃
SO 3 + 2NaOH ==Na 2 SO 4 + H 2 O CH 4 + 2O 2 CO 2 + 2H 2 O
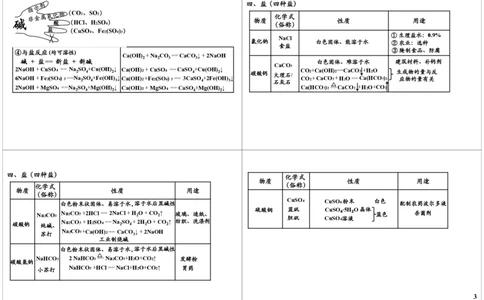
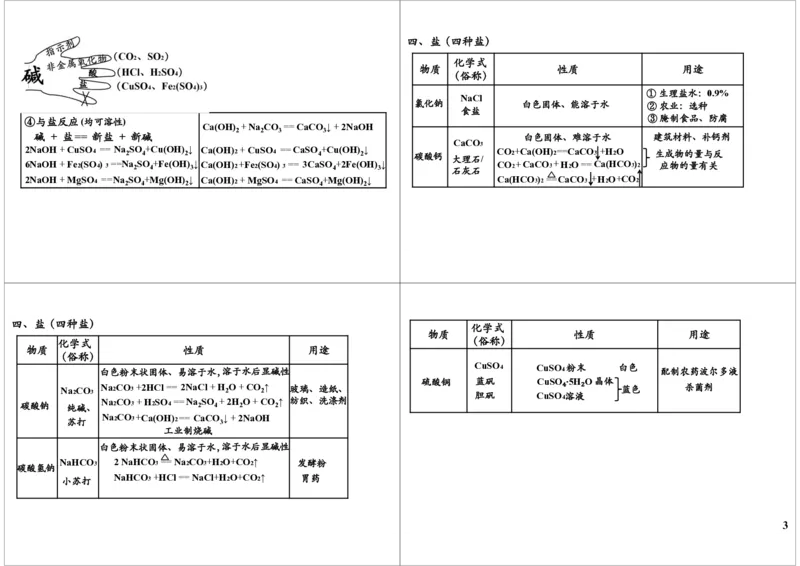
3CO+Fe 2 O 3 高温 2Fe +3CO 2 2四、盐(四种盐)
化学式
物质 性质 用途
(俗称)
①生理盐水:0.9%
NaCl
氯化钠 白色固体、能溶于水 ②农业:选种
食盐
④与盐反应(均可溶性) ③腌制食品、防腐
Ca(OH) + Na CO == CaCO ↓ + 2NaOH
2 2 3 3
碱 + 盐== 新盐 + 新碱 白色固体、难溶于水 建筑材料、补钙剂
CaCO
3
2NaOH + CuSO 4 == Na 2 SO 4 +Cu(OH) 2 ↓ Ca(OH) 2 + CuSO 4 ==CaSO 4 +Cu(OH) 2 ↓ 碳酸钙 大理石/ CO 2 +Ca(OH) 2 ==CaCO 3 +H 2 O 生成物的量与反
6NaOH + Fe 2 (SO 4 ) 3 ==Na 2 SO 4 +Fe(OH) 3 ↓Ca(OH) 2 +Fe 2 (SO 4 ) 3 == 3CaSO 4 +2Fe(OH) 3 ↓ 石灰石 CO 2 +CaCO 3 +H 2 O==Ca(HCO 3 ) 2 应物的量有关
2NaOH + MgSO 4 ==Na 2 SO 4 +Mg(OH) 2 ↓ Ca(OH) 2 + MgSO 4 ==CaSO 4 +Mg(OH) 2 ↓ Ca(HCO 3 ) 2 ==CaCO 3 +H 2 O+CO 2
四、盐(四种盐)
化学式
物质 性质 用途
化学式 (俗称)
物质 性质 用途
(俗称)
白色粉末状固体、易溶于水,溶于水后显碱性
CuSO 4 CuSO 4粉末 白色
配制农药波尔多液
硫酸铜 蓝矾 CuSO₄·5H₂O晶体
Na 2 CO 3 N
N
a
a
2 C
C
O
O
3 +
+
2
H
HC
SO
l ==
==
2N
N
a
a
C
S
l
O
+ H
+
2
2
O
H
+
O
C
+
O
C
2 ↑
O ↑
玻
纺
璃
织
、
、
造
洗
纸
涤
、
剂
胆矾 CuSO 4溶液 蓝色 杀菌剂
碳酸钠 纯碱、 2 3 2 4 2 4 2 2
苏打 Na 2 CO 3+Ca(OH) 2== CaCO 3 ↓ + 2NaOH
工业制烧碱
白色粉末状固体、易溶于水,溶于水后显碱性
NaHCO 3 2 NaHCO 3 == Na 2 CO 3 +H 2 O+CO 2 ↑ 发酵粉
碳酸氢钠
小苏打 NaHCO 3 +HCl== NaCl+H 2 O+CO 2 ↑ 胃药
3①与金属反应 (可溶性)
(1)头是K+、Na+、NH4+, ③与碱反应 (均可溶性)
盐 +金属 新盐 +新金属
Fe + CuSO ==FeSO +Cu 尾是三强酸(SO42-、NO3-、Cl-) 盐 + 碱 == 新盐 + 新碱
Cu + 2AgN
4
O 3 ==2Ag
4
+Cu(NO 3 ) 2
除AgCl、BaSO4均可溶!
CuCl 2 + NaOH ==Cu(OH) 2 ↓+2NaCl CuCl 2 +Ca(OH) 2 ==Cu(OH) 2 ↓+ CaCl 2
(2)溶碱K+、Na+、Ca+、Ba+、NH +
Mg + AgCl == 4 FeCl 3 +3NaOH ==Fe(OH) 3 ↓+3NaCl 2FeCl 3 +3Ca(OH) 2 == 2Fe(OH) 3 ↓+3CaCl 2
②与酸反应 既不溶于水、又不溶于稀酸 MgCl 2 + NaOH==Mg(OH) 2 ↓+2NaCl MgCl 2 + Ca(OH )2 ==Mg(OH) 2 ↓+ CaCl 2
盐 +酸 新盐 +新酸 Cl-:用含Ag+aq ④与盐反应 (均可溶性) (生成物必须有↓生成)
AgNO 3 +HCl ==AgCl↓+HNO 3 (加入AgNO 3溶液,再加入少量稀HNO 3 ) 盐 +盐 新盐 +新盐
BaCl 2 +H 2 SO 4 ==BaSO 4 ↓+2HCl SO42-:用含Ba2+aq AgNO 3 +NaCl ==AgCl↓+ NaNO 3 BaCl 2+ Na 2 SO 4 ==BaSO 4 ↓ + 2NaCl
(加入Ba(NO 3 ) 2溶液,再加入少量稀HNO 3 )
四、离子的检验 2H+ + CO 3 2-== CO 2 ↑+ H 2 O
3.CO 2-:
石蕊 3 Ca2+ + CO 2- == CaCO ↓
3 3
1.H+检验:
pH试纸
Ba2+ + CO 3 2- == BaCO 3 ↓
金属:Mg、Zn、Fe、Al H 2 ↑ 4.Cl-: Ag+
CO 3 2-: CO 2 ↑; HCO 3 - CO 2 ↑; 5.SO 2-: Ba2+
4
石蕊 酚酞
Cu2+ Cu(OH) ↓
2 五、物质的共存(离子的共存)
2.OH-检验 Fe3+ Fe(OH)
3
↓ 1.H+:OH-、CO
3
2-、HCO
3
-
2.OH-:H+、Cu2+、Fe3+、Mg2+、NH +
4
pH试纸 Mg2+ Mg(OH)
2
↓
3.CO 2-:H+、Ca2+ 、Ba2+
3
4.Cl-: Ag+
5.SO 2-: Ba2+
4 4【例1】下列各组物质在某pH=14的无色溶液中,能大量共存的是( ) 【例3】将下列各组物质同时放到适量的水中,只能得到无色透明溶液的是
A.FeCl 、NaCl、KNO B.NaCl、NaOH、NaNO ( )
3 3 3
C.CaCl
2
、NaNO
3
、Na
2
CO
3
D.KNO
3
、H
2
SO
4
、NaCl A. Na
2
CO
3
、NaCl、Na
2
SO
4
B. HCl、CaCl 、Na CO
2 2 3
C. KCl、HCl、CuSO
4
【例2】某溶液能与镁反应产生氢气,则在该溶液中能大量共存的离子组是
D. NaCl、KOH、FeCl
3
( )
A. Al3+、CO 2-、NO -、Ca2+ 【例4】物间的转化,不能一步实现的是( )
3 3
B. Mg2+、NH +、Cl-、OH- A. Mg(OH) → MgCl B. Na CO → NaOH
4 2 2 2 3
C. Ba2+、Fe3+、NO -、Cl- C. CaCO → Ca(OH) D. Fe O → FeCl
3 3 2 2 3 3
D.K+、Na+、CO 2-、SO 2-
3 4
【例5】现有NaOH、NaHCO 、Na CO 三种物质的溶液,加入某种物质分别 【例8】(不定项)向一定量的氢氧化钠溶液中逐滴加入等质量分数的稀盐酸至
3 2 3
与几种发生反应,都有同一种化合物X生成,则化合物X的化学式不可 过量,下列有关量的变化与所加入的稀盐酸质量关系,不正确的是
能为下列物质中的( ) ( )
A.CO B.NaCl C.H O D.Na SO
2 2 2 4
【例6】用Mg、MgO、Mg(OH) 、H SO 溶液、CuSO 溶液五种物质两两进行
2 2 4 4
反应,能得到MgSO 的方法有( )
4
A. 3种 B. 4种 C. 5种 D. 无法确定
【例7】下列实验中,所得溶液的pH>7的是( )
A.向Na CO 溶液中滴加CaCl 溶液至恰好完全反应
2 3 2
B.向盐酸中滴加NaOH溶液至恰好完全反应
C.将一定量的CO 通入氢氧化钠溶液中
2
D.向盐酸中加入一定量的水
5