文档内容
中考总复习分类专题训练化学(三)
(内容:周围的空气和水)
班级 姓名 学号 成绩
说明:1.测试时间45分钟,满分100分。
2. 可能用到的相对原子质量: K:39 Cl: 35.5 O : 16
一、单项选择题(以下第1-10小题,每小题3分,共30分。每小题只有一个正确答案)
1.要在一充满空气的瓶子中,将其中的氧气除去,又不增加其他气体的成分。下列物质在瓶中
燃烧可达到目的的是 ( )
A.木炭 B.硫磺 C.铁丝 D.红磷
2. 2014年广东省运会若用大型遥控飞艇作广告。为了安全,艇内充入的气体最好是 ( )
A.氢气 B.氧气 C.氦气 D.二氧化碳
3.氧气是空气的主要成分之一,下列有关氧气的说法错误的是( )
A.用加热高锰酸钾的方法可以制取氧气 B.用带火星的木条可以检验氧气
C.鱼类能在水中生存证明氧气易溶于水 D.铁丝能在氧气中燃烧,火星四溅,产生黑色固体
4.利用下列原理制取氧气,具有反应快操作简便能耗少无污染的是 ( )
MnO
2 △
A.2KClO △ 2 KCl + 3O ↑ B.2KMnO KMnO + MnO + O ↑
3 2 4 2 4 2 2
MnO △
C.2H O 2HO + O↑ D.2HgO 2Hg + O↑
2 2 2 2 2 2
5.下列关于水的说法正确的是 ( )
A.水的污染会引起土壤污染 B.地球上淡水资源非常丰富
C.过滤能够除去水中所有杂质 D.水由氢气和氧气组成
6.下列关于氧气的说法正确的是 ( )
A.氧气能支持燃烧,可作燃料 B.氧气能跟所有物质发生氧化反应
C.水中生物能靠微溶于水中的氧气而生存 D.带火星木条一定能在含氧气的集气瓶中复燃
7.据报道,太湖水由于水体富营养化,导致蓝藻快速繁殖生长,死亡腐烂,水位下降后,太湖底
泥上泛,使水体产生异味。为改善水质,除去水中的异味,下面建议不合理的是 ( )
A.人工捞藻,投加活性炭 B.加入大量生石灰和明矾
C.增加水量,促进水体流动 D.严格控制各种污染源,确保达标后排放
8.为判断某化合物是否含碳、氢、氧三种元素,取一定质量该化合物在氧气中充分燃烧,接下来
还需进行的实验有 ( )
①用无水硫酸铜检验是否有水生成; ②用澄清石灰水检验是否有二氧化碳生成;
③用带火星的木条检验氧气; ④测定水和二氧化碳的质量
A.①②③ B.①②④ C.②③④ D.①②③④
9. 科学家发现特殊条件下,水能表现出许多有趣的结构和性质。一定条件下给水施加一个弱电
场,常温常压下水结成冰,俗称“热冰”,下图为模拟图。下列说法正确的是( )
A.水结成“热冰”的过程中原子个数发生变化
B.上述变化过程中分子问间隔没有发生变化
C.在弱电场下,水分子运动从有序转变为无序
D.利用该性质,人们在常温常压下可建成溜冰场
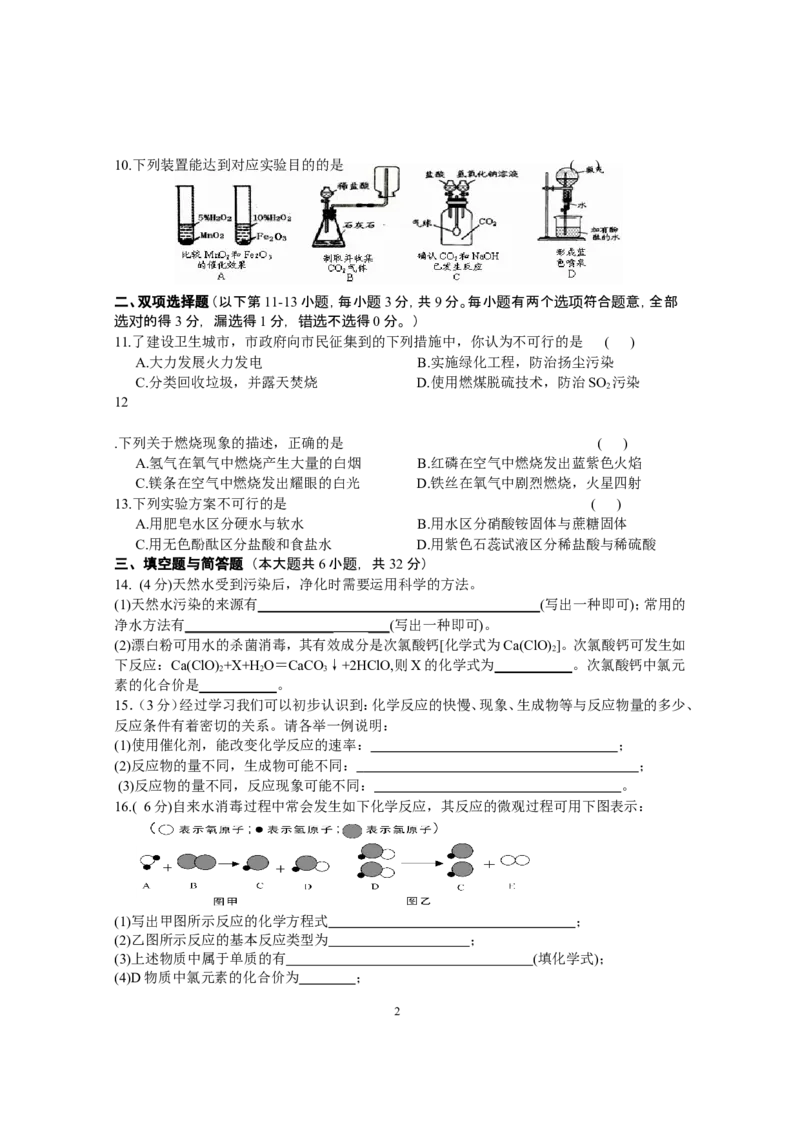
110.下列装置能达到对应实验目的的是 ( )
二、双项选择题(以下第11-13小题,每小题3分,共9分。每小题有两个选项符合题意,全部
选对的得3分,漏选得1分,错选不选得0分。)
11.了建设卫生城市,市政府向市民征集到的下列措施中,你认为不可行的是 ( )
A.大力发展火力发电 B.实施绿化工程,防治扬尘污染
C.分类回收垃圾,并露天焚烧 D.使用燃煤脱硫技术,防治SO 污染
2
12
.下列关于燃烧现象的描述,正确的是 ( )
A.氢气在氧气中燃烧产生大量的白烟 B.红磷在空气中燃烧发出蓝紫色火焰
C.镁条在空气中燃烧发出耀眼的白光 D.铁丝在氧气中剧烈燃烧,火星四射
13.下列实验方案不可行的是 ( )
A.用肥皂水区分硬水与软水 B.用水区分硝酸铵固体与蔗糖固体
C.用无色酚酞区分盐酸和食盐水 D.用紫色石蕊试液区分稀盐酸与稀硫酸
三、填空题与简答题(本大题共6小题,共32分)
14. (4分)天然水受到污染后,净化时需要运用科学的方法。
(1)天然水污染的来源有________________________________________(写出一种即可);常用的
净水方法有 _____________________ ___ (写出一种即可)。
(2)漂白粉可用水的杀菌消毒,其有效成分是次氯酸钙[化学式为Ca(ClO) ]。次氯酸钙可发生如
2
下反应:Ca(ClO) +X+H O=CaCO ↓+2HClO,则X的化学式为___________。次氯酸钙中氯元
2 2 3
素的化合价是___________。
15.(3分)经过学习我们可以初步认识到:化学反应的快慢、现象、生成物等与反应物量的多少、
反应条件有着密切的关系。请各举一例说明:
(1)使用催化剂,能改变化学反应的速率: ;
(2)反应物的量不同,生成物可能不同: ;
(3)反应物的量不同,反应现象可能不同: 。
16.( 6分)自来水消毒过程中常会发生如下化学反应,其反应的微观过程可用下图表示:
(1)写出甲图所示反应的化学方程式 ;
(2)乙图所示反应的基本反应类型为 ;
(3)上述物质中属于单质的有 (填化学式);
(4)D物质中氯元素的化合价为 ;
2(5)以甲图为例分析,你能总结出的一条结论是 。
17. ( 7分)化学反应的程度与反应物的浓度之间有一定的规律可循。某实验小组各取等质量的
木炭和等质量的硫分别在容积相同的机器瓶中燃烧。记录如下:
实验 实验步骤 实验现象 化学方程式
①木炭在空气中燃烧 ①木炭红热
产生的气体都能使
A ______________
澄清石灰水变浑浊
②木炭在氧气中燃烧 ②_______________
③硫在空气中燃烧 ③微弱的淡蓝色火焰
产生的气体都有刺
B ______________
激性气味
④硫在氧气中燃烧 ④_______________
通过A、B两组对比实验的现象,可以得出的规律是: 。
18(. 6分)过去教材中实验室制氧气,常用氯酸钾与二氧化锰混合加热制取,装置如图所示,从
预热到收集满一瓶(250mL)氧气大约需8~10分钟,从反应后剩余的固体
中回收二氧化锰比较困难,曾有同学去闻自己收集到的氧气,想找找吸氧的
感觉,结果却闻到刺激性气味(少量氯酸钾发生副反应生成有毒的氯气)。
现行教材已改用过氧化氢溶液和二氧化锰混合制取氧气,
写出反应的化学方程式: 。
你认为这样做的优点都有哪些?
(1) ;(2) ;
(3) ;(4) 。
19. (6分)对知识的归纳与整理是学习化学的一种重要方法。现有三个化学反应如下:
点燃 点燃 点燃
①S+O==== SO ②2CO+O =====2CO ③3Fe+2O ===== Fe O
2 2 2 2 2 3 4
(1)通过比较我们发现:它们有许多相似之处,其一 ;其二
我能另写一个符合这两点的化学方程式 ;它们之间也存在
相异之处,其中一个反应与众不同,这个反应和它的不同之处是 。
△
(2)课外学习Cu (OH) CO ===2=CuO +H O + CO 后,我们又发现它也和上述三个反应有
2 2 3 2 2
相似之处,其相似之处是 。
四、实验探究题(本大题共3小题,共22分)
20. (8分)实验室常用下列装置研究气体的制取和性质,根据所学知识回答下列问题。
A B C D E
(1)写出F实验室制取氧气的一个化学方程式 _________ ___ 。利用该反
应制取氧气,发生装置应选____________(填序号,下同)。
(2)一氧化氮气体难溶于水,在空气中容易发生下列反应2NO+O ==2NO ,则收集一氧化氮气体
2 2
时不能用的装置是(填序号)____________。
(3)按图F作细铁丝在氧气中燃烧的实验,我观察到的现象有 ____________ (只答一条),
其相关的化学方程式是 。
(4)实验室里将制得的二氧化碳气体通入澄清石灰水中,始终未出现浑浊现象,可能的原因是
321. (6分)研究性学习小组选择“HO 生成O 的快慢与什么因素有关”的课题进行探究,以
2 2 2
下是他们探究的主要过程:
【假 设】HO 生成O 的快慢与催化剂种类有关
2 2 2
【实验方案】常温下,在两瓶同质量、同浓度的HO 溶液中,分别加入相同质量的MnO 和水
2 2 2
泥块,测量各生成一瓶(相同体积)O 所需的时间。
2
【进行实验】右图是他们进行实验的装置图,气体发生装置中A仪器名称是 ,
此实验中B处宜采用的气体收集方法是 。
【实验记录】
实验编号 1 2
反应物 5%H 2 O 2 5%H 2 O 2 A
B
催化剂 1g水泥块 1gMnO
2
时间 165秒 46秒
【 结 论】该探究过程得出的结论是 。
【 反 思】HO 在常温下分解缓慢,加入MnO 或水泥块后反应明显加快,若要证明MnO
2 2 2 2
和水泥块是该反应催化剂,还需增加实验来验证它们在化学反应前后的 是
否改变。
HO 生成O 的快慢与哪些因素有关?请你帮助他们继续探究。(只要求提出一种影响HO
2 2 2 2 2
生成O 的快慢的因素以及相关假设和实验方案)
2
【假 设】 。
【实验方案】 。
22.( 8分)(1)保持水的化学性质的最小粒子是 。
(2)右图是活性炭净水器示意图,其中活性炭的作用是:不仅可以 的
物质,还可以 的杂质。(3)有一杯主要含有MgCl 和CaCl 的硬水。某
2 2
兴趣小组设计出软化水的部分实验方案,请你一起来完成。可供选用的物质有:
Ca(OH) 溶液、NaOH溶液、饱和NaCO 溶液、肥皂水
2 2 3
实验步骤 现象 结论或化学方程式
①取少量水样于试管中,向其中滴加 MgCl +Ca(OH) =Mg(OH) ↓
有白色沉淀产生 2 2 2
Ca(0H) 溶液,直到不再产生沉淀 +CaCl
2 2
②继续向上述试管中滴加 ,
有白色沉淀产生 化学方程式:
直到不再产生沉淀
③过滤 滤液澄清 (此空空白)
④ 证明硬水已软化
五、计算题(本大题包括1小题,共7分)
23.为测定实验室中氯酸钾样品的纯度,取一定质量的该样品与1g二氧化锰混合,总质量为6g,
依次加热该混合物t,t,t t 时间后分别冷却,称量剩余固体质量,记录的有关数据如下表(样品中
1 2 3,4
杂质不参加化学反应)
加热时间 t t t t
(1) 时间后,样品中氯酸钾已完全反应. 1 2 3 4
剩余固体质量(g) 4.24 4.16 4.08 4.08
(2)完全反应后产生氧气的总质量为 。
(3)样品中氯酸钾的纯度是多少。
4