文档内容
碳和碳的氧化物附答案
课题1 金刚石、石墨和C60
课题2 二氧化碳制取的研究
课题3 二氧化碳和一氧化碳
一、选择题
1.继“分子足球”C 之后,科学家又发现另一种“分子足球”N 。一定条件下N 中积累的
60 60 60
巨大能量会在一瞬间释放出来,是未来的火箭燃料,N 属于
60
A.金属单质 B.非金属单质 C.化合物 D.混合物
2.有关H、CO、C三种物质的下列说法正确的是
2
A.都是目前最理想的清洁燃料 B.与金属氧化物发生的反应都属于置换反应
C.在氧气中燃烧,都产生淡蓝色火焰 D.与金属氧化物反应后,一定有化合物生成
3.贝壳(含CaCO )煅烧后得CaO,CaO加到海水(含有MgCl )池中得Mg(OH) 沉淀,
3 2 2
Mg(OH) 与盐酸反应得MgCl 溶液。上述生产过程中没有涉及到的反应类型是
2 2
A.化合反应 B.置换反应 C.复分解反应 D.分解反应
4.某些食品包装袋内常有一小包物质,用来吸收氧气和水分,以防止食品腐败,常称“双吸
剂”。下列物质属于“双吸剂”的是
A.炭粉 B.铁粉 C.氯化钙 D.生石灰
5.超临界CO 流体是一种具有和水相似、能阻燃、溶解能力强的溶剂,被誉为“绿色环保溶
2
剂”。下列说法正确的是
①超临界CO 流体性质特殊,因此,与干冰的化学组成不同
2
②CO 是自然界中存在的物质,它参与自然界的碳元素循环
2
③超临界CO 流体是一种特殊的物质,容易燃烧
2
④超临界CO 流体可代替许多有害、有毒、易燃的溶剂
2
A.①② B.②④ C.①③ D.①②③④
6.下列各组物质中,都由分子构成的是
A.水、二氧化碳 B.氧气、金刚石 C.铜、食盐 D.氢气、氢氧化钠
7.在空气中敞口放置的一瓶无水酒精,没有燃烧的原因是
A.没有与氧气接触 B.无水酒精是液体
C.没有达到着火点 D.酒精没有可燃性
8.以下表示的是碳及其化合物的相互转化关系:
其中涉及的基本反应类型依次为
A.置换、化合、分解、复分解 B.置换、化合、复分解、分解
C.化合、置换、分解、复分解 D.化合、置换、复分解、分解
9.区分0、H、C0 三种气体的最简便的方法是
2 2 2
A.将气体通入澄清石灰水 B.将气体通过红热的铜网
C.将气体通过灼热的氧化铜 D.用燃着的木条伸入集气瓶中
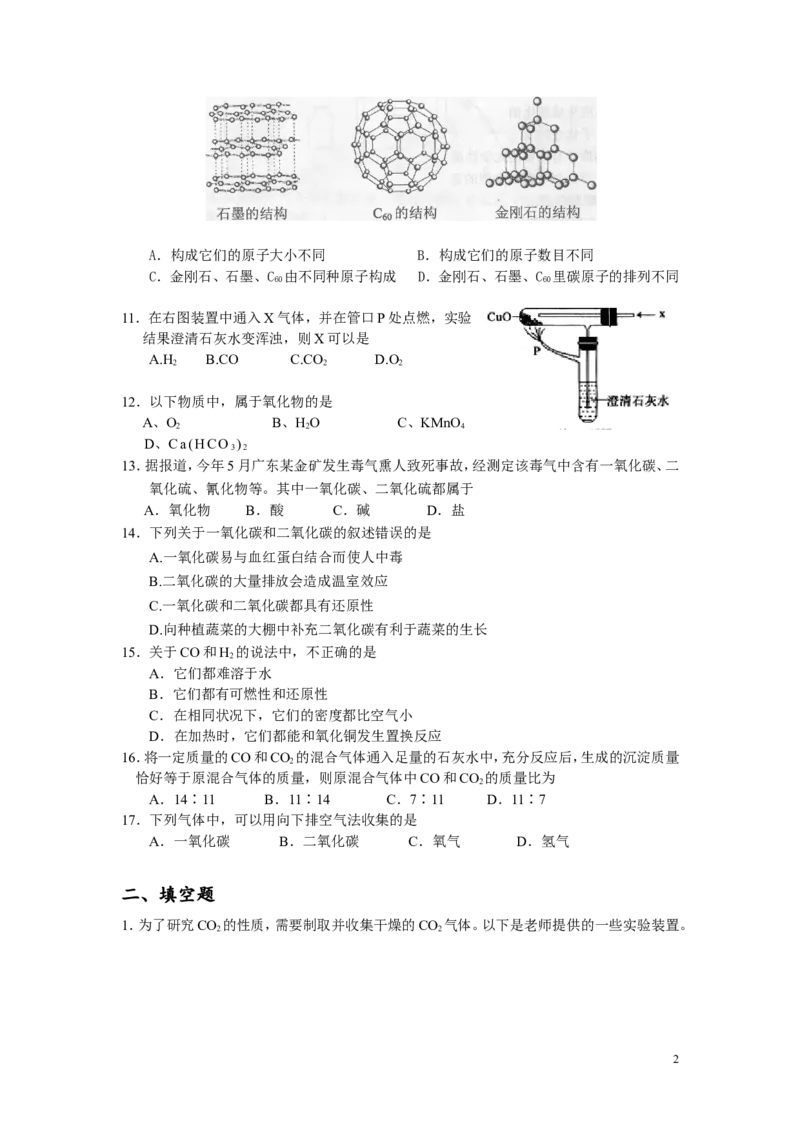
10.下图是金刚石、石墨、C 的结构示意图,.它们的化学性质相似,物理性质却有很大差异。
60
其原因是
1A.构成它们的原子大小不同 B.构成它们的原子数目不同
C.金刚石、石墨、C 由不同种原子构成 D.金刚石、石墨、C 里碳原子的排列不同
60 60
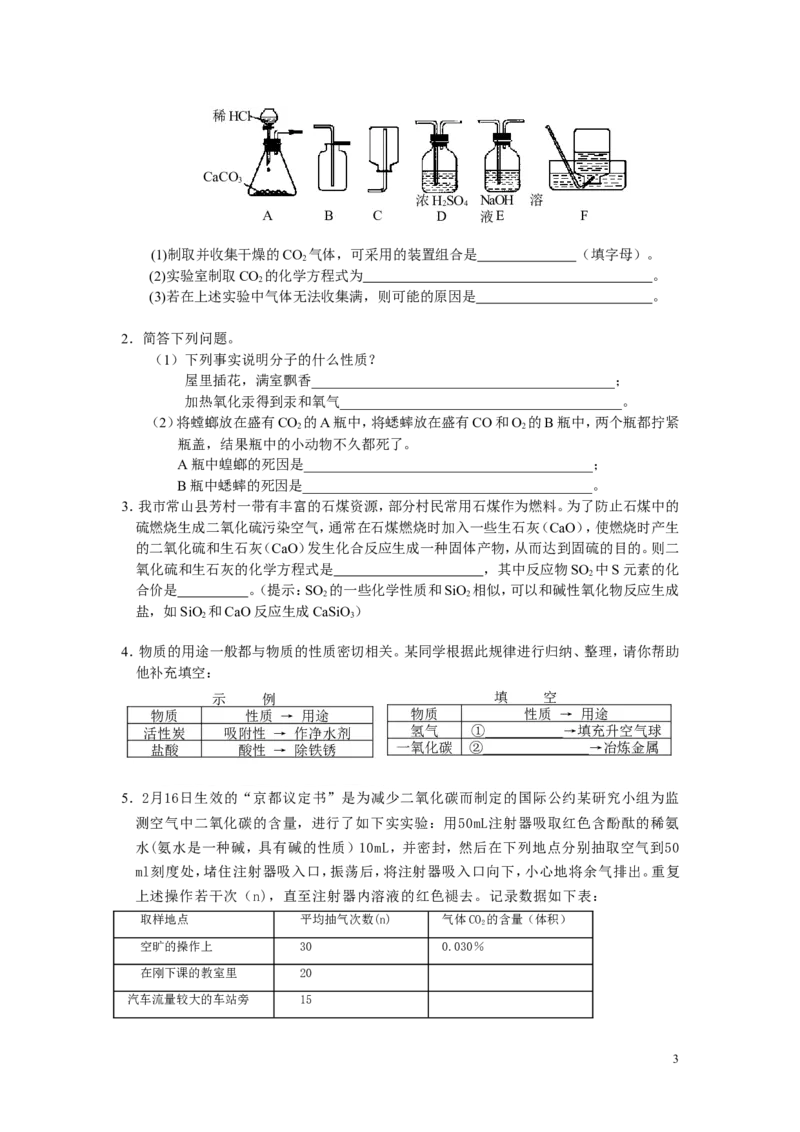
11.在右图装置中通入X气体,并在管口P处点燃,实验
结果澄清石灰水变浑浊,则X可以是
A.H B.CO C.CO D.O
2 2 2
12.以下物质中,属于氧化物的是
A、O B、HO C、KMnO
2 2 4
D、Ca(HCO )
3 2
13.据报道,今年5月广东某金矿发生毒气熏人致死事故,经测定该毒气中含有一氧化碳、二
氧化硫、氰化物等。其中一氧化碳、二氧化硫都属于
A.氧化物 B.酸 C.碱 D.盐
14.下列关于一氧化碳和二氧化碳的叙述错误的是
A.一氧化碳易与血红蛋白结合而使人中毒
B.二氧化碳的大量排放会造成温室效应
C.一氧化碳和二氧化碳都具有还原性
D.向种植蔬菜的大棚中补充二氧化碳有利于蔬菜的生长
15.关于CO和H 的说法中,不正确的是
2
A.它们都难溶于水
B.它们都有可燃性和还原性
C.在相同状况下,它们的密度都比空气小
D.在加热时,它们都能和氧化铜发生置换反应
16.将一定质量的CO和CO 的混合气体通入足量的石灰水中,充分反应后,生成的沉淀质量
2
恰好等于原混合气体的质量,则原混合气体中CO和CO 的质量比为
2
A.14∶11 B.11∶14 C.7∶11 D.11∶7
17.下列气体中,可以用向下排空气法收集的是
A.一氧化碳 B.二氧化碳 C.氧气 D.氢气
二、填空题
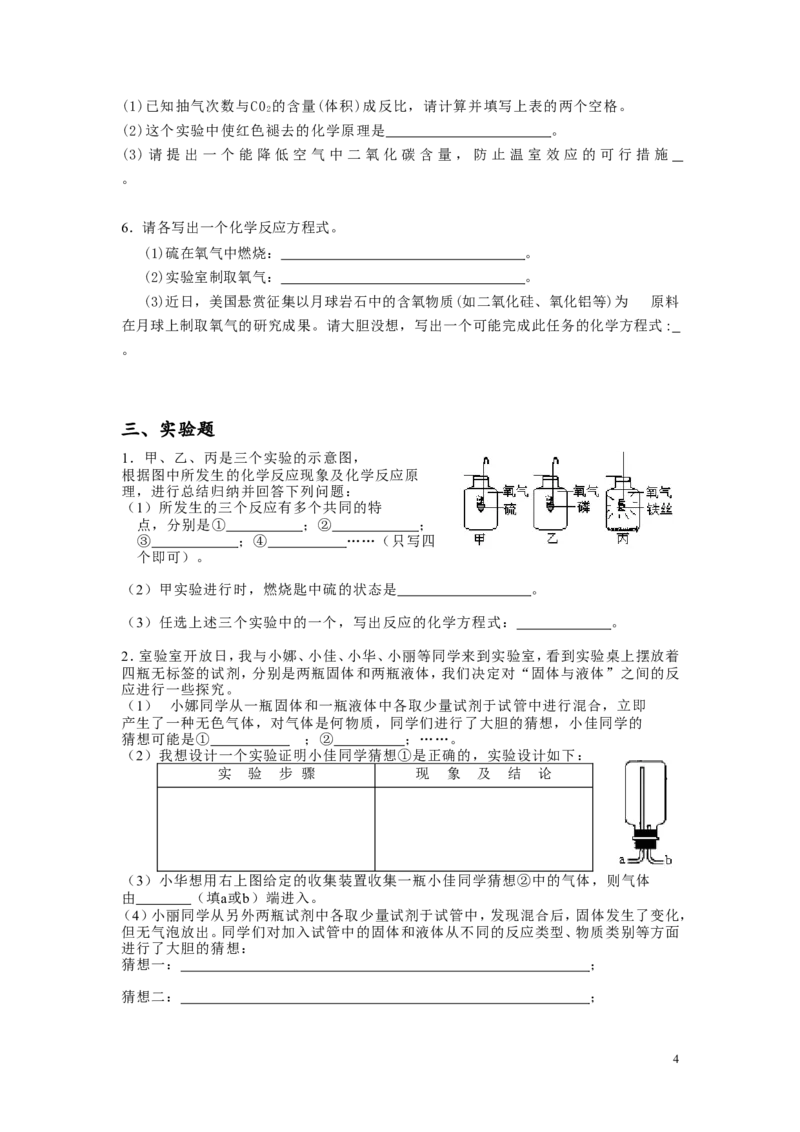
1.为了研究CO 的性质,需要制取并收集干燥的CO 气体。以下是老师提供的一些实验装置。
2 2
2稀HCl
CaCO
3
浓H SO NaOH 溶
2 4
A B C D 液E F
(1)制取并收集干燥的CO 气体,可采用的装置组合是 (填字母)。
2
2实验室制取CO 的化学方程式为 。
2
3若在上述实验中气体无法收集满,则可能的原因是 。
2.简答下列问题。
(1)下列事实说明分子的什么性质?
屋里插花,满室飘香___________________________________________;
加热氧化汞得到汞和氧气________________________________________。
(2)将螳螂放在盛有CO 的A瓶中,将蟋蟀放在盛有CO和O 的B瓶中,两个瓶都拧紧
2 2
瓶盖,结果瓶中的小动物不久都死了。
A瓶中蝗螂的死因是_________________________________________;
B瓶中蟋蟀的死因是_________________________________________。
3.我市常山县芳村一带有丰富的石煤资源,部分村民常用石煤作为燃料。为了防止石煤中的
硫燃烧生成二氧化硫污染空气,通常在石煤燃烧时加入一些生石灰(CaO),使燃烧时产生
的二氧化硫和生石灰(CaO)发生化合反应生成一种固体产物,从而达到固硫的目的。则二
氧化硫和生石灰的化学方程式是 ,其中反应物SO 中S元素的化
2
合价是 。(提示:SO 的一些化学性质和SiO 相似,可以和碱性氧化物反应生成
2 2
盐,如SiO 和CaO反应生成CaSiO )
2 3
4.物质的用途一般都与物质的性质密切相关。某同学根据此规律进行归纳、整理,请你帮助
他补充填空:
示 例 填 空
物质 性质 → 用途 物质 性质 → 用途
活性炭 吸附性 → 作净水剂 氢气 ① →填充升空气球
盐酸 酸性 → 除铁锈 一氧化碳 ② →冶炼金属
5.2月16日生效的“京都议定书”是为减少二氧化碳而制定的国际公约某研究小组为监
测空气中二氧化碳的含量,进行了如下实实验:用50mL注射器吸取红色含酚酞的稀氨
水(氨水是一种碱,具有碱的性质)10mL,并密封,然后在下列地点分别抽取空气到50
ml刻度处,堵住注射器吸入口,振荡后,将注射器吸入口向下,小心地将余气排出。重复
上述操作若干次(n),直至注射器内溶液的红色褪去。记录数据如下表:
取样地点 平均抽气次数(n) 气体CO 的含量(体积)
2
空旷的操作上 30 0.030%
在刚下课的教室里 20
汽车流量较大的车站旁 15
3(1)已知抽气次数与C0 的含量(体积)成反比,请计算并填写上表的两个空格。
2
(2)这个实验中使红色褪去的化学原理是 。
(3)请提出一个能降低空气中二氧化碳含量,防止 温室效应的可行措施
。
6.请各写出一个化学反应方程式。
(1)硫在氧气中燃烧: 。
(2)实验室制取氧气: 。
(3)近日,美国悬赏征集以月球岩石中的含氧物质(如二氧化硅、氧化铝等)为 原料
在月球上制取氧气的研究成果。请大胆没想,写出一个可能完成此任务的化学方程式:
。
三、实验题
1.甲、乙、丙是三个实验的示意图,
根据图中所发生的化学反应现象及化学反应原
理,进行总结归纳并回答下列问题:
(1)所发生的三个反应有多个共同的特
点,分别是① ;② ;
③ ;④ ……(只写四
个即可)。
(2)甲实验进行时,燃烧匙中硫的状态是 。
(3)任选上述三个实验中的一个,写出反应的化学方程式: 。
2.室验室开放日,我与小娜、小佳、小华、小丽等同学来到实验室,看到实验桌上摆放着
四瓶无标签的试剂,分别是两瓶固体和两瓶液体,我们决定对“固体与液体”之间的反
应进行一些探究。
(1) 小娜同学从一瓶固体和一瓶液体中各取少量试剂于试管中进行混合,立即
产生了一种无色气体,对气体是何物质,同学们进行了大胆的猜想,小佳同学的
猜想可能是① ;② ;……。
(2)我想设计一个实验证明小佳同学猜想①是正确的,实验设计如下:
实 验 步 骤 现 象 及 结 论
(3)小华想用右上图给定的收集装置收集一瓶小佳同学猜想②中的气体,则气体
由 (填a或b)端进入。
(4)小丽同学从另外两瓶试剂中各取少量试剂于试管中,发现混合后,固体发生了变化,
但无气泡放出。同学们对加入试管中的固体和液体从不同的反应类型、物质类别等方面
进行了大胆的猜想:
猜想一: ;
猜想二: ;
4猜想三: ;
……。
3.H、CO、CO、CH 四种物质中,某种物质在某一点(或某几点)上具有与其他三种物质不同
2 2 4
之处(其他三种物质在这一点上则有相同或相似之处),请按要求及示例填写下表。
物 质 该物质与其它三种物质不同之处
例:H H 组成上不含碳元素,其它三种物质均含有碳元素
2 2
4.碳酸钙在高温下煅烧一段时间后,得到白色固体。两研究性学习小组的同学为了确定白色
固体的成分,对其可能的组成进行探究。
[提出问题]白色固体的成分是什么?
I组:[作出猜想]白色固体的成分可能是CaC0 和Ca0的混合物。
3
[实验验证】(请你写出实验的步骤和现象):
_________________________________________________________________
【实验结论]白色固体的成分是CaC0 和CaO的混合物。
3
II组:[作出猜想】白色固体可能全部是氧化钙。
[设计方案】取试样于试管中,加入水,再通入二氧化碳,变浑浊。
II组的方案正确吗?__________,理由是__________________________________
I组为了进一步研究碳酸钙分解的质量分数,设计了如下的实验方案:称取一定
量白色固体,用足量盐酸溶解,产生的气体经除杂、__________后,被已称量好的足
量的“吸收剂”吸收……“吸收剂”宜选用__________,该方案中还需补充的步骤
是 _____________。
5.请填写下列有关实验操作中的空格:
(1)点燃可燃性气体时,都要先 ,再点燃。
(2)用向上排空气法收集二氧化碳时,导气管要伸到 。
(3)做铁丝在氧气中燃烧的实验时,集气瓶中应预先 。
6.为了研究从长期使用的热水瓶中倒出的片状固体(水垢)的成分,学生进行以下探究:
操 作 现 象 结 论
实 水垢变白、变疏松
水垢
验 澄 澄清石灰水变浑浊 水垢分解产物中
清
石 有 (写
灰
① 水 化学式)
实 固体部分溶解,测得 该滤液呈 性
棒玻
的测
PH约为12
水 璃
验 定
滤
液
实验①试 5
管中的剩
PH
余固体
滤液②
根据上述探究,估计此水垢的成分中含有 (写物质名称)。
写出实验①中发生反应的化学方程式: ;
。
7.为弄清楚某废弃的防空洞内气体成分中是否含有水蒸气、一氧化碳和二氧化碳,某校化学
兴趣实验小组用下列盛有药品的仪器(图中夹持仪器等均省略),检验防空洞内气体成分。
气 体 样 品
→
A B C D
(1)请你提出一种采集气体样品的方法 ;
(2)通过你对实验现象的观察和思考分析,填写下表空格:
装置序号 A B C
实验现象 白色粉末变蓝 黑色粉末逐渐变红
结论与分析 说明含有CO
2
(3)选用C装置的目的是干燥气体,瓶内应盛 ;
(4)你对这套装置有何评价 ;
(5)干涸的深井中有可能含有较多的二氧化碳,最简单的方法用“灯火”实验来确定能否进
入,其原因是 。
8.某化学兴趣小组通过查阅资料得知:固体草酸(HC O·2H O)受热可分解其化学
2 2 4 2
HC O·2H O
方程式为 2 2 4 2 ,
该课题小组的同学在实验室分别进行了如下实验
请回答下列问题:
⑴ 甲同学利用右图装置制取并收集CO:
①B装置的作用 ______________。
② CO 集满后,将集气瓶由水槽中加盖取出,然后先_________________,再
_________________________。
⑵ 乙同学为了验证草酸的分解产物,设计了四个方案,分别将混合气体(包括水蒸气)依
次通过足量的下列试剂:
A.石灰水、灼热的氧化铜、无水硫酸铜、氢氧化钠溶液
B.无水硫酸铜、氢氧化钠溶液、灼热的氧化铜、石灰水
C.石灰水、无水硫酸铜、灼热的氧化铜、石灰水
6D.无水硫酸铜、石灰水、灼热的氧化铜、石灰水
你认为其中正确的方案是_________________。
⑶ 丙同学按下图装置利用草酸分解产生的CO测定某种铁的氧化物的组成。
① 当C装置中铁的氧化物全部被还原后,称量剩余的质量为a g,同时测的D装置的
质 量 增 加 b g , 则 该 铁 的 氧 化 物 中 铁 元 素 和 氧 元 素 的 质 量 比 为
_____________________。
② 丁同学认为去掉A装置,对测定结果无影响,他的观点(填“正确”或“不正确”)
你的判断理由是________________________________。而戊同学认为在D装置后还
应再增加某装置,该装置的__________________;若无此装置,对测定结果是否有影
响?______________________(填“是”或“否”)。
9.甲同学在某食品包装袋内,发现有一个装有白色颗粒状固体A的小纸袋,上面写着“生石
灰干燥剂,请勿食用”。甲同学随手将小纸袋拿出来放在空气中,经过一段时间后,发现
纸袋内的白色颗粒粘在一起成为块状固体B。请你与甲同学一起对块状固体B进行探究。
(1)猜想一:块状固体B中除氧化钙外还可能有: 、 。
写出白色颗粒状固体A在空气中转化为块状固体B的化学反应方程式:
; 。
(2)猜想二:块状固体B溶于水可能有 现象(填“放热”或“吸热”)。请设计实
验方案验证你的这一猜想(至少写出两种方案):
① ;② ;③ 。
(3)取适量块状固体B加入盛有一定量水的试管中,振荡、静置、过滤,得到少量白色固体C。
就白色固体C的成分,甲同学与乙同学进行讨论,一起猜想。
甲同学认为,白色固体C可能是:氢氧化钙;
乙同学认为,白色固体C可能是:碳酸钙;
你认为,白色固体C还可能是: 。
请设计实验证明你的猜想(填写下表):
方 案 现 象 和 结 论
10.环境问题是人类可持续发展必须解决的一个重要问题,温室效应被列为 21世纪人类面
临的最大威胁之一,已引起人们的广泛关注。旨在限制发达国家温室气体排放量、抑制全
球范围内气候持续变暖的《京都议定书》,已于2005年2月16日正式生效。
(Ⅰ)二氧化碳是大气中的主要温室气体,我国二氧化碳的排放量位居世界第二,为减少二
氧化碳这种温室气体的排放,我们可以采取的措施有(只填2种):
; 。
7(Ⅱ)为减缓二氧化碳使全球变暖的趋势,有科学家提出大胆设想:将排放到空气中的二
氧化碳压缩使其液化,然后将其压入到冰冷的深海中。但也有科学家担心海水中富含二氧化
碳后酸度会增加,可能会杀死一些海洋生物,甚至会溶解掉部分海床,同时气候变化也可能
改变海洋环流,把海底的二氧化碳又带回海面,另外把二氧化碳压入海底所消耗的能源可能
会再增加二氧化碳的排放。
⑴ 二氧化碳气体转变为液体时将会 能量(填“释放”或“消耗”);
⑵ 二氧化碳使海水酸度增加的原理用化学方程式表示为: ;
⑶二氧化碳在深海中的溶解度比在通常状况下的水中的溶解度 ,原因是
。
11.我国科学家陈乾旺等最新研究成果表明,在440℃和800大气压条件下,二氧化碳和金属
钠反应产生金刚石和碳酸钠,合成的金刚石最大达1.2mm,完全可以满足工业用途。
⑴二氧化碳与金属钠反应生成金刚石和碳酸钠的化学方程式为:
。
⑵请从人类生存的角度分析,金刚石与水相比谁更宝贵? ,
理由是: 。
四、物质推断题
1.已知X是有毒且不溶于水的气体,Y是不支持燃烧的气体,Z是不溶于水的固体,X、Y、Z
之间有如下转化关系。请回答下列问题。
(1)写出X的化学式___________________________________________;
(2)写出Z和稀盐酸反应生成Y的化学方程式:___________________________
(3)“物质的组成与结构决定物质的性质”是重要的化学思想。气体 X、Y都含有
________元素和________元素,但它们的物理性质、化学性质都不同。请举出X、Y
性质不同的一个例子________________________________。
2.现有A~F六种常见物质,其中B是食品包装中的常用的干燥剂,A、B、C三种白色固体都
含有同种金属元素,E是固体单质,D、E、F都含有同种非金属元素,它们的转化关系如下
图。请回答:
A E
C D
B F
(1)写出下列物质的化学式:
C_____________ B_____________ E_______________。
8(2)写出下列变化的化学方程式:
A C:___________________________________________;
F D:_______ __________________________________。
五、计算题
1.石灰石是我市最丰富的矿藏之一,用途极为广泛。除了可以用于生产生石灰和水泥外,工
业上还常常用沉淀法生产碳酸钙。用这种方法得到的碳酸钙是一种极细的粉末,在工业
又称为轻质碳酸钙,是一种重要的工业原料,具有很高的经济价值。我市某工厂利用下列
工艺流程生产轻质碳酸钙:
请根据以上信息回答下列问题:
⑴ 工厂每天用16吨含碳酸钙65%的石灰石作为原料,如果碳酸钙在高温下全部分解,可
得到多少吨生石灰?[假设石灰石中的杂质在高温下不发生化学反应,计算结果保留一
位小数]
⑵ 氢氧化钠是上述生产轻质碳酸钙工艺流程中的副产品,工厂为了提高经济效益,通常
回收氢氧化钠固体出售。现市场上氢氧化钠固体的价格为每吨3400元,如果该工厂每
天生产10吨轻质碳酸钙,试计算工厂每天可从出售氢氧化钠固体中得到多少收入?
⑶ 根据初中已学的知识,如果还是用石灰石作为原料,请你写出另一种制取轻质碳酸钙
的方案。对照题给的生产轻质碳酸钙工艺流程,议一议你设计的方案是否适宜工业上生
产,有什么优缺点。
2.某厂用石灰石高温煅烧制得生石灰,若每天消耗含杂质5%的石灰石原料300吨。请根据
计算回答下列问题:
⑴ 理论上每天可生产氧化钙多少吨(假设杂质受热不分解)?
⑵ 若每吨石灰石以100元的价格买入,制得的生石灰(含原杂质)以每吨250元卖出,扣
除每吨石灰石原料生产的加工费30元,则该厂每天可获利润多少元?
3.某钙片的标签如右图所示,可知此钙片成分中只有碳酸钙含有钙元素。
(1) 请通过计算说明此标签中的含钙量是否错误。
执行标准:GB1413-99
主要成分:碳酸钙
(2)为测定其真实的含钙量,小东每次取10片钙片放 含钙量:每片含钙0.75g
入已称量的含足量盐酸的烧杯中,发生的化学反应是;每瓶50片,重 40 g
(中外合资xx公司出品)
CaCO +2HCl=CaCl+H O+CO ↑,充分反应后再
3 2 2
称取烧杯和剩余物的总质量。小东做了三次实验,数据如下:
物质的质量 第一次 第二次 第三次 平均值
反应前:烧杯+盐酸 22 g 22 g 22 g 22 g
10片钙片 8 g 8 g 8 g 8 g
反应后:烧杯十剩余物 26.7 g 26.5 g 26.9 g 26.7g
① 请列式计算每片此钙片含碳酸钙的质量。
②请列式计算每片此钙片的含钙量,并建议厂家如何改标签。
9答 案 与 提 示
一、选择题
1.B 2.D 3.B 4.B 5.B 6.A 7.C 8.B
9.D 10.D 11.B 12.B 13.A 14.C 15.D 16.A
17.D
二、填空题
1.(1)A、D、C (2)略 (3)药品量不足或气密性不好等。
2.(1)分子在不停的运动;分子在化学变化中可以再分
(2)缺氧窒息;CO中毒
3.26.SO+CaO CaSO +4
2 3
4.密度比空气小很多(密度小);还原性
5.(1)0.045% 0.060%
(2)二氧化碳与碱反应后溶液的碱性减弱,至接近中性时。使酚酞褪色
(3)本题是一个开放性问题,只要有利于空气中二氧化碳的减少,有一定的可行性的措施均可
给分。可能的答案:
①减少二氧化碳排放类:使用H 等新能源;控制汽车增多等。
2
②增加二氧化碳消耗类:植树造林;设法将空气中的二氧化碳固定等。
点燃
6.(1) S+O SO
2 2
MnO △
(2) 2HO 2 2HO+O↑ 或 2KMnO KMnO +MnO +O↑
2 2 2 2 4 2 4 2 2
(3) 本题是开放性问题,目的在于考查学生的创新能力,评分时只要有氧气生成,化学式正确,符合
质量守恒定律,不管该反应能否实现,均参照给分。可能的答案有:
SiO == Si + O2↑ 2 A1 O =4 Al+3O ↑
2 2 3 2
三、实验题
1.(1)①都是化合反应;②都与氧气反应;③生成物都是氧化物;④反应都放出大量的
热;⑤反应条件都是点燃;⑥都是气体与固体反应……
(2)液态 (3)S+O SO (或4P+5O 2P O ;或3Fe+2O Fe O )
2 2 2 2 5 2 3 4
2.(1)①CO ;②H [或O …… ]
2 2 2
(2)如①是CO [或H ;或O ……]
2 2 2
实 验 步 骤 现 象 及 结 论
将气体通入澄清石灰水中 石灰水变浑浊,则证明是二氧化碳。
[将试管口堵一会儿,点燃此气体;或将带 [或能燃烧,产生淡蓝色火焰;或听到
火星的木条插入试管中…]… 爆鸣声,则证明是氢气;或木条复燃,
证明是氧气……]
(3)②中如果是氢气 填 a (如是氧气或二氧化碳填 b )
(4) 猜想一:金属与盐溶液发生置换反应;
猜想二:金属氧化物与酸溶液反应;
猜想三:碱与酸溶液发生复分解反应;
10猜想四:氧化物(如CaO)与水发生化合反应
猜想五:可溶于水的固体物质
猜想六:……
3. ①CO CO 在通常状况下的密度比空气大,其它三种物质密度均小于空气
2 2
②H H 是单质,其它三种物质均为化合物
2 2
③CO CO有毒,其它三种物质均无毒
④CO CO 在空气中不能燃烧,其它三种物质在空气中均能燃烧
2 2
⑤CO CO 能溶于水且与水反应,其它三种物质均不溶于水,也不与水反应
2 2
……
4.【实验验证】取试样于试管中,加入稀盐酸,有气泡产生
不正确 因为生成的氢氧化钙微溶于水,不通入C0 也会有浑浊现象产生
2
干燥 NaOH浓溶液 称量、计算
5.(1)检验纯度(2)集气瓶底部(3)放少量的沙(或放少量的水)
6.CO;碱;碳酸钙;CaCO CaO+CO ↑;CO+Ca(OH) →CaCO ↓+H O
2 3 2 2 2 3 2
7.(1)用大注射器吸取(其他方法正确也给分)
(2)A:含有水蒸汽 B:澄清石灰水变浑浊 D:含有CO
(3)浓硫酸
(4)不完善,缺少尾气处理装置
(5)二氧化碳既不燃烧,也不支持燃烧
8.⑴ ①除去CO ②将导管从水槽中移出,熄灭酒精灯
2
⑵ D
⑶ ①11a/(8b) , ②不正确;空气中的CO 会进入装置,使测定结果不准确;
2
盛有氢氧化钠溶液的洗气瓶(或装有碱石灰的干燥管); 是
9.⑴ Ca(OH) ;CaCO CaO+H O=Ca(OH) ;Ca(OH) +CO =CaCO ↓+H O
2 3 2 2 2 2 3 2
⑵ 放热;
①取适量块状固体B放入烧杯中,加入少量水,用手触摸烧杯外壁。
②取适量块状固体B放入烧杯中,加入少量水,立即用温度计测定溶液温度的变化。
③在试管中加入适量块状固体B,加入少量水,立即塞上带导管的单孔橡皮塞,同时
将导管的另一端放入盛水的水槽中,观察导管口是否有气泡放出。
④在试管中加入适量块状固体B,加入少量水,立即在试管口套上一只瘪气球,观察
气球体积的变化。
(3)Ca(OH) 和CaCO 的混合物;
2 3
方 案 现象和结论
步骤①:将所得固体C加入到试管中,
加入少量水,振荡,再向其中滴入两滴酚
①若溶液变红,则白色固体C中含有Ca(OH)
酞试液; 2
若溶液不变红,则白色固体C中不含有Ca(OH)
步骤②:再向试管中滴入稀盐酸。 2
②若有气泡产生,则白色固体C中含有CaCO
3
若无气泡产生,则白色固体C中不含有CaCO
3
10.(Ⅰ).开发新能源;减少矿石燃料的使用或提高燃料的利用率。
(Ⅱ)⑴释放; ⑵CO+H O=HCO; ⑶大;
2 2 2 3
深海中,压强大,温度低。
1111.(1)3CO+4Na 2NaCO+C;
2 2 3
(2)水更宝贵;
以人为本,水是维持生命所必需的物质;没有水就没有生命;没有水,一切生物将无法
生存。
四、物质推断题
1.(1)CO
(2)CaCO +2HC1==CaCl +HO+CO↑
3 2 2 2
(3)碳(C);氧(O) CO有毒,CO 无毒(或其他正确答案)
2
2.(1)CaCO CaO C(2)Ca(OH) +CO = CaCO↓+ H O
3 2 2 3 2
五、计算题
1.解:⑴设可得到X吨生石灰
CaCO CaO+CO↑
3 2
100 56
16×65% X
100:56=(16×65%):X X=5.8吨
答:略。
⑵设生产10吨轻质碳酸钙可得到Y吨氢氧化钠
Ca(OH) +NaCO=2NaOH+CaCO ↓
2 2 3 3
80 100
Y 10
80:100=Y:10 Y=8(吨)
出售8吨氢氧化钠固体可得收=8×3400=27200(元)
答:略。
由于生产成本太高,不适宜工业上生产。
2.(1)解:设理论上每天生成氧化钙的质量为x
CaCO 高温 CaO + CO ↑
3 2
100 56
300 t×(1-5%) x
= x=159.6t
答:理论上每天可生产氧化钙159.6t。
(2)解:该厂每天的利润为:(159.6 t +300 t×5%)×250元/ t-300 t×(100+30) 元/ t
=4650元
答:该厂每天可获利润4650元
3.解:(1)本品若为纯碳酸钙,其含钙量为
1213