文档内容
第五单元 测试试卷
(化学方程式)
可能用到的相对原子质量: C:12 H:1 O:16 K:39 Mn:55
题号 一 二 三 四 总分
得分
一.选择题:(每小题2分,共40分)
题
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20
号
答
案
[来网源ZX:X学K]科 [来科源#网:学]#
1. 质量守恒定律揭示了化学反应中:
A. 反应条件 B. 哪些物质是反应物
C. 哪些物质是生成物 D. 反应物和生成物的质量关系
2. 化学反应前后,一定发生改变:
A. 分子种类 B. 原子的相对质量 C. 原子个数 D. 原子种类
3. 天文学家观察到“百武”彗星因受到越来越强的阳光照射而产生喷气现象。喷出气体包括:CO、
CHOH(甲醇)、HCHO(甲醛)、HCN(氢氰酸)等有毒物质和水蒸气。根据这一信息可以推测:
3
A.“百武”彗星至少含有C、H、N、O元素 B.“百武”彗星中存在单质和化合物
C.“百武”彗星是一个液态混合物 D.“百武”彗星可能存在生命
4. 等质量的下列物质完全燃烧,消耗氧气的质量最多的是:
A.H B.C C.S D.Mg
2
5. 17世纪人们认为水能变土,1768年科学家拉瓦锡对此进行研究。他将一定量的蒸馏水加入特
殊的蒸馏器,反复加热蒸馏101天,发现蒸馏器内产生少量沉淀,称得整个蒸馏装置的总质量没
变、水的质量也没变、沉淀的质量等于蒸馏器减少的质量。对于这项研究的说法错误的是:
A. 精确称量是科学研究的重要方法 B. 水在长时间加热后能转变为土
C. 物质变化过程中总质量守恒 D. 沉淀物来自于蒸馏器本身
6. 有X、Y两元素,使12g X 与XY 反应生成24gC,化学方程式为:X+XY=3C。则X、Y两元素的相对
2 3 2 3
原子质量之比:
A. 1:1 B. 1:2 C. 3:1 D. 3:4
7. 在3B+2A=C的反应中,10gA与足量的B反应能生成22gC,则A、B、C三种物质的相对分子质量
之比为:
A.3∶2∶1 B.12∶10∶22 C.4∶5∶22 D.5∶4∶22
8. 加热6.32 g KMnO,当剩余物的质量为5.68 g时,停止加热,则剩余物中含有的物质是:
4
A. KMnO B. KMnO、KMnO、MnO
4 4 2 4 2
C. KMnO、MnO D.KMnO、KMnO
2 4 2 4 2 49. 下列化学方程式书写完全正确的是:
点燃 MnO 2
A. 4Fe+3O ==== 2FeO B. 2KClO====2KCl+3O↑
2 2 3 3 2
△ 点燃
C. 4P+5O 2PO D. 2CH+5O====4CO+2HO
2 2 5 2 2 2 2 2
10. 在反应3Cu+8HNO=3Cu(NO)+2X↑+4HO中的X的化学式是:
3 3 2 2
A. N B. NO C. NO D. NO
2 2 2 5
11. 下列叙述中正确的是:
A. 镁带在空气中燃烧后,生成物的质量跟原镁带的质量相等
B. 按任意体积混合后的氢气和氧气的总质量,跟反应后生成水的质量相等
C. 二氧化硫气体通入氢氧化钠溶液时,溶液增加的质量就是被吸收的二氧化硫的质量
D. 煤球燃烧后质量减轻,这不符合质量守恒定律
12. 镁在空气中燃烧,生成氧化镁,其固体质量变化可用图表示,则(80-48)克表示的质量为:
固
体
质
量
80 克
48 克
0
A. 生成物MgO的质量 时 间 B. 参加反应O 的质量
2
C. 参加反应的镁的质量 D. 生成物MgO与参加反应的O 的质量和
2
13. 若23克某正一价元素的单质和8克氧气恰好完全反应,所生成氧化物的相对分子质量是:
[来源:学科网]
A . 31 B. 46 C. 54 D. 62
14. 下列四个反应中生成物都是C,如果C的化学式为A B,则该反应的化学方程式为:
2 3
A. AB + B = 2C B. AB + 2B = 2C
2 2 2 2
C. 2AB + B =2C D. 4AB + B =2C
2 2 2
15. 氯酸钾与二氧化锰按7:3的质量比均匀混合,加热至不再产生氧气为止,残余固体中,氯化钾
的质量分数:
A. 等于70% B. 大于70% C. 小于70% D. 等于100%
16. 某可燃物4.6g 在足量氧气充分燃烧,生成8.8g 二氧化碳和5.4g 水,则该可燃物的组成为:
A. 一定含碳、氢、氧三种元素元素 B. 一定含碳、氢元素,可能含氧元素
C. 一定含碳、氢元素,不含氧元素 D. 所含元素大于三种
△
17. 用IO 可以测定空气受CO污染的程度,发生反应的化学方程式如下:IO+ 5CO==== I+ 5CO,
2 5 2 5 2 2
根据生成CO 的多少,可以判定CO的含量,关于这个反应,下列说法正确的是:
2
A. 参加反应的IO 的质量等于生成I 的质量
2 5 2
B. 参加反应的各物质中的氧原子总数等于生成的CO 中氧原子的总数
2
C. 参加反应的IO 和CO的质量比等于生成I 和CO 的质量比
2 5 2 2
D. 反应物所含元素种类与生成物所含元素种类不同18. 硫和磷的单质各A g分别在氧气中充分燃烧,得到二氧化硫M g,得到五氧化二磷N g,M 和N
的关系正确的是:
A. M=N B. M<N C. M>N D. M=N=64
19. 化学方程式 2A+B====C+2D中,A、B、C的相对分子质量依次分别为103、71、160,则D相对分子
质量为:
A. 58.5 B. 117 C. 114 D. 14
20. A和B的混合物212 g恰好完全反应生成C和D,已知2A+5B====4C+2D,测得C与D的质量比
为44∶9,则生成的C的质量为:
A.176 g B.141.3 g C.44 g D.36 g
二.填空题:(每空1分,化学方程式2分,共26分)
21. 在反应 S + O SO 中,若生成m个SO 分子,则参加反应的氧原子个数为 .
2 2 2
22. 现以2HO 2H↑ +O↑ 为例,请用分子和原子的观点解释质量守恒定律。(1)反应前后
2 2 2
没变;(2)反应前后 不变;(3)而 不变,故反应前参加反应的水的质量
等于反应后生成的H 质量和O 质量总和。
2 2
23. 11月13日,中石油吉林石化公司双苯厂发生爆炸,造成松花江水环境污染,事故产生的主要污
染物为苯(CH)和硝基苯等有机物,对人体十分有害。其中苯是一种常见的有机溶剂,具有挥发性,
6 6
硝基苯是制一种剧烈炸药的原料,它们都具有可燃性,请写出苯充分燃烧生成二氧化碳和水的化学
方程式 。
24. 我国使用的燃料主要是煤炭和石油,产生的SO 遇到雨水成为酸雨。目前有一种较有效的方法,
2
即用直升飞机喷洒碳酸钙粉末,脱硫效果可达85%,碳酸钙与SO 及空气中的氧反应生成硫酸钙和
2
二氧化碳,写出化学方程式________________________________________。
25. 石油资源紧张是制约中国发展轿车工业,尤其是制约轿车进入家庭的重要因素。为此,我国在
某些省市已开始推广“车用乙醇汽油”,即在汽油中加少量乙醇(CHOH),写出乙醇完全燃烧的化
2 5
学方程式_____________________________________________。
26. 安全火柴梗头及火柴盒侧面的物质如右
图所示,当两者摩擦时,生热点燃红磷而使火柴梗着火。
写出有关化学方程式:
、 。
27. 体育课上,剧烈运动后血液中产生了较多乳酸(CHO),使人肌肉酸痛,经过一段时间放松,
3 6 3
由于乳酸与吸入的氧气反应,生成二氧化碳和水,酸痛感消失。该反应的化学方程式为
____________________________________________。
28. 将A、B两种物质各8 g,混合后加热使它们充分反应,反应结束后发现B全部用完,生成新物
质C 3 g,D 9 g,则反应中A和B的质量比是 。
29. 我国古代炼丹术用的铅丹与硝酸反应的化学方程式是:铅丹 ,则
铅丹的化学式为 。
30. 有化学反应 A+B=C+2D。已知 49gA 恰好与 29gB 完全反应,生成了 60gC,则同时生成
D__________g。现已知物质的相对分子质量:A为98,B为58,C为120,则D的相对分子质量__________。
31. 五 配平下列化学方程式 (每1分,共6分)
⑴ NH + CI === N + NH Cl
3 2 2 4
⑵ FeS + O === Fe O + SO
2 2 2 3 2
⑶ C H + O === CO + HO
3 8 2 2 2
⑷ NO + Fe === Fe O + N
2 3 3 4 2
⑸ FeS+ O === Fe O+ SO
2 2 2 3 2
⑹ Al(OH) + HSO === Al (SO )+ HO
3 2 4 2 4 3 2
三.信息与探究:(32题10分;33题8分;34题4分;共18分)
32. 阅读下面小文章,回答问题。
氢气在通常状况下,是一种无色无味、难溶于水、在相同条件下密度最小的气体。它在空气中能
安静的燃烧,产生淡蓝色的火焰。氢气常在实验室被使用,如它能和氧化铜反应,将氧化铜还原成
铜,并生成水。氢气被人们所喜爱,因为它有着很多优点。如资源丰富(以水为原料制取)、燃烧产物
是水(无污染)、燃烧放出热量多等等。
⑴ 试想,如果在实验室制取氢气,应用什么方法收集?
⑵ 写出所有文中出现的反应的化学方程式。
⑶ 根据文中信息,写出利用氢气物理性质和化学性质的用途各一条。
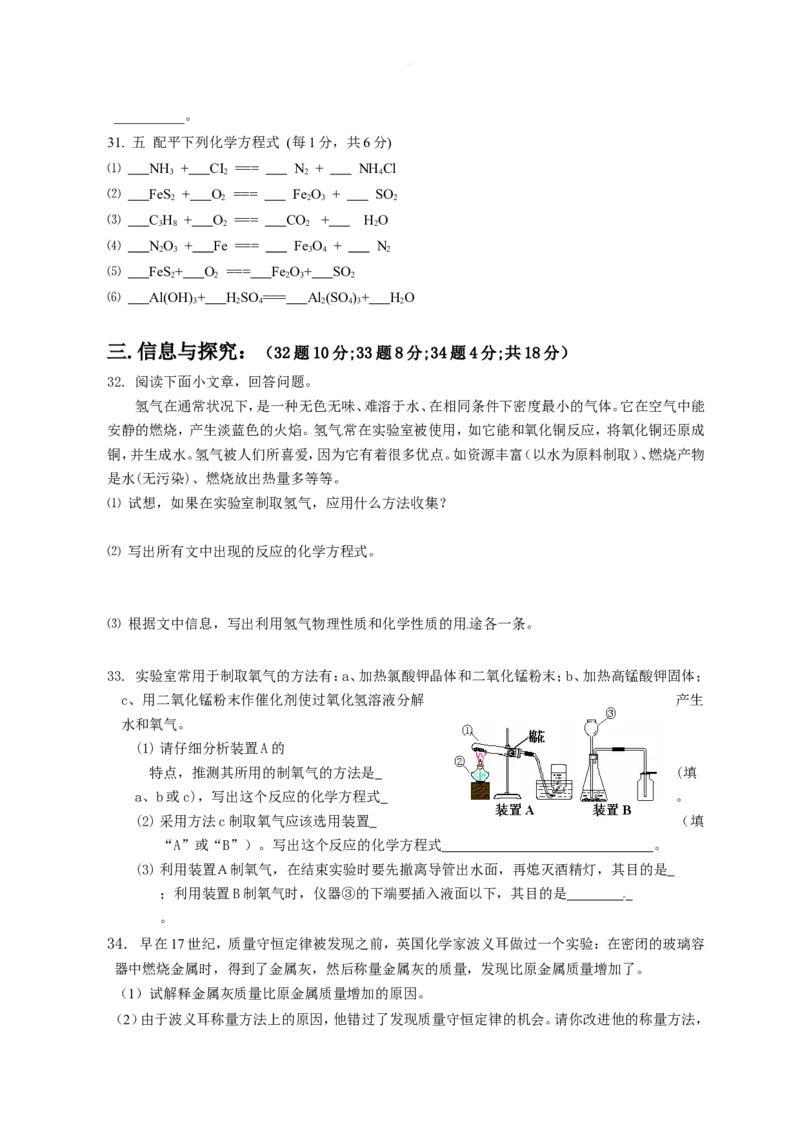
33. 实验室常用于制取氧气的方法有:a、加热氯酸钾晶体和二氧化锰粉末;b、加热高锰酸钾固体;
c、用二氧化锰粉末作催化剂使过氧化氢溶液分解 产生
水和氧气。
(1)请仔细分析装置A的
特点,推测其所用的制氧气的方法是 (填
a、b或c),写出这个反应的化学方程式 。
(2)采用方法c制取氧气应该选用装置 (填
“A”或“B”)。写出这个反应的化学方程式 。
(3)利用装置A制氧气,在结束实验时要先撤离导管出水面,再熄灭酒精灯,其目的是
;利用装置B制氧气时,仪器③的下端要插入液面以下,其目的是
。
34. 早在17世纪,质量守恒定律被发现之前,英国化学家波义耳做过一个实验:在密闭的玻璃容
器中燃烧金属时,得到了金属灰,然后称量金属灰的质量,发现比原金属质量增加了。
(1)试解释金属灰质量比原金属质量增加的原因。
(2)由于波义耳称量方法上的原因,他错过了发现质量守恒定律的机会。请你改进他的称量方法,以验证质量守恒定律。
四.计算题:(每小题8分,共16分)
35. 将0.5g二氧化锰与一定量氯酸钾共热到质量不减少为止,称得残渣质量为15.4g。求:(1)生
成氧气多少克? (2)原先氯酸钾的质量是多少克?
36. 有20克H 和O 的混合气体,点燃充分反应后,产生18克水,则原混合气体的成分组成情况是
2 2
怎样的,通过计算说明.
参考答案:
一.选择题:
题 14
15
1 2 3 4 5 6 7 8 9 10 11 12 13 16 17 18 19 20
号 [来 网 源 ZX : X 学 K] 科
答
D A A A B C D C D B C B D D C A B B A A
案
二.填空题:
21. 2m 22. 氢原子总数 氧原子总数 同种原子的质量
23. 2CH+15O 12CO + 6HO 24. 2CaCO+2SO+O==2CaSO+2CO
6 6 2 2 2 3 2 2 4 2
25. CHOH + 3O 2CO + 3HO
2 5 2 2 2
MnO
2
26. 2KClO======2KCl+3O↑ 4P+5O 2PO
3 2 2 2 5
27. CHO+3O2==3CO+3HO 28. 1∶229. PbO 30. 18 18 31.⑴ 8;3;1;6
3 6 3 2 2 3 4
⑵4;11;2;8 ⑶1;5;3;4 ⑷ 4;9;3;4 ⑸ 2;3;1;6 ⑹4;11;2;8
三.信息与探究:
32. ⑴ 排水法或向下排空气法(均写得2分)通电
⑵2H + O 2HO 2HO ==== 2H↑ + O↑ H + CuO === Cu + HO
2 2 2 2 2 2 2 2
⑶ 本题属开放题,回答合理即给分,但必须是物性和化性各一 。
33. (1) b 2KMnO ===== KMnO + MnO + O↑
4 2 4 2 2
(2) B 2H
2
O
2
=M==n=O=2 2H
2
O + O
2
↑
(3) 防止水槽中水倒吸,引起试管破;防止生成的气体从长颈漏斗中逸出
34. (1)金属燃烧是金属与氧气发生化合反应,生成金属氧化物。根据质量守恒定律可知,参加反
应的金属与氧气的质量之和等于生成的金属氧化物质量。生成的金属灰是金属氧化物,所以金属
灰的质量比原金属的质量增加了。
(2)分别称量反应前后密闭容器的质量。
四.计算题:35.(1)9.6g(2)24.5g 36. 2克H 和18克O 或 4克H 和16克O
2 2 2 2