文档内容
冲刺专题三——推断题
一、顺推法
解题思路:根据条件按照题意顺序逐一推测,去伪存真,作出结论。
例1 某混合物中,可能含有碳酸钠、氯化钙、硫酸铜、硫酸钠、氯化钡中的几种物质,根
据下表所列的事实,推断原混合物中肯定有 ,肯定没有
可能有
化学实验步骤 实验现象
1、取固体混合物溶解于水 得到无色透明溶液和白色沉淀
2、加入过量硝酸 沉淀全部溶解且产生无色无气味气体
3、加少量硫酸钠溶液 又产生白色沉淀
二、逆推法
解题思路:抓住突破口→层层上推→得出结论
(这类解法常适用于以物质相互转化为主要内容的推断)
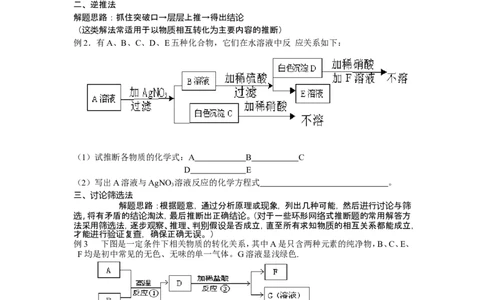
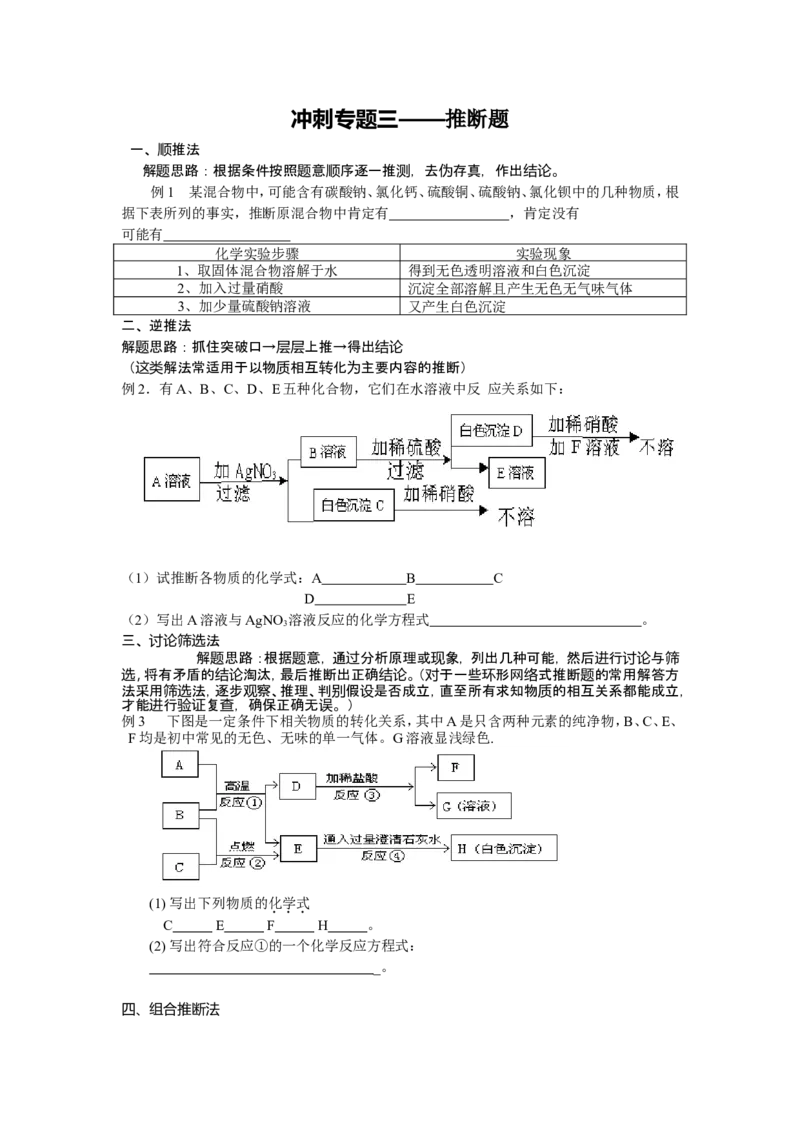
例2.有A、B、C、D、E五种化合物,它们在水溶液中反 应关系如下:
(1)试推断各物质的化学式:A B C
D E
(2)写出A溶液与AgNO 溶液反应的化学方程式 。
3
三、讨论筛选法
解题思路:根据题意,通过分析原理或现象,列出几种可能,然后进行讨论与筛
选,将有矛盾的结论淘汰,最后推断出正确结论。(对于一些环形网络式推断题的常用解答方
法采用筛选法,逐步观察、推理、判别假设是否成立,直至所有求知物质的相互关系都能成立,
才能进行验证复查,确保正确无误。)
例3 下图是一定条件下相关物质的转化关系,其中A是只含两种元素的纯净物,B、C、E、
F均是初中常见的无色、无味的单一气体。G溶液显浅绿色.
(1) 写出下列物质的化学式
C E F H 。
(2) 写出符合反应①的一个化学反应方程式:
_。
四、组合推断法解题思路:据题设条件,按步分析,逻辑推理,层层推进,“对号入座”得出结论
解题时注意:(1)思维过程展示注意逻辑性;(2)发散性结论(几种可能组合)按序排列分析,
防止遗漏或重复,(3)表述要清楚
例4.若从HSO 、NaCO、NaSO 、NaCl、NaNO、Cu(NO)、H NO 七种溶液中取出其中的两
2 4 2 3 2 4 3 3 2 3
种,进行混合及有关实验,所观察到的现象记录如下表。试根据各步实验及其现象先进行分
步推断,再推断所取的两种溶液的可能组合。
步骤 实验操作 实验现象 推断(或结论)
混合溶液无色、澄清 混合液中肯定不含:
(1) 将取出的两种溶液混合
无明显现象 混合溶液肯定不是下列组合:
用pH试纸测定混合溶
(2) 测定结果:pH=2
液的pH
向混合溶液中滴入足量Ba
(3) 有白色沉淀出现
(NO)溶液
3 2
向上述过滤所得的滤液中
(4) 无明显现象
滴加AgNO 溶液
3
①_________________________
混合溶液的可能组合(写出溶 ②__________________________
质的化学式,有几组写几组) ③__________________________
④__________________________
五、定性与定量结合法
解题思路:抓住题供性质、现象等条件正确进行定性推理,还需抓住题供数量条件进行计算
等定量分析,使定性与定量高度统一,才能作出正确判断,
例5 某KCO 样品中含有NaCO、KNO 和Ba(NO ) 三种杂质的一种或两种,现将13.8克
2 3 2 3 3 3 2
样品加入足量水,样品全部溶解,再加入过量的CaCl 溶液,得到9克沉淀,对样品所含杂质
2
的正确判断肯定含有 ,可能还有 ,肯定没有
分类跟踪练习
一、叙述式推断题
1.有一包粉末,可能由NaCl、NaCO、FeCl 、NaSO 中的一种或几种组成,依次进行如下实
2 3 3 2 4
验:
(1)白色粉末溶于水,得无色透明溶液,加入足量BaCl 溶液生成白色沉淀;
2
(2)过滤后,向所得沉淀中加入盐酸,沉淀不溶解;
(3)向滤液中加入AgNO 溶液,产生白色沉淀,再加入足量稀硝酸,沉淀不溶解。以上实验,
3
不能确定混合物中是否含有 ,若要检验不能确定的物质是否存在,则上述实验的
操作(1)中应加入的试剂是 。
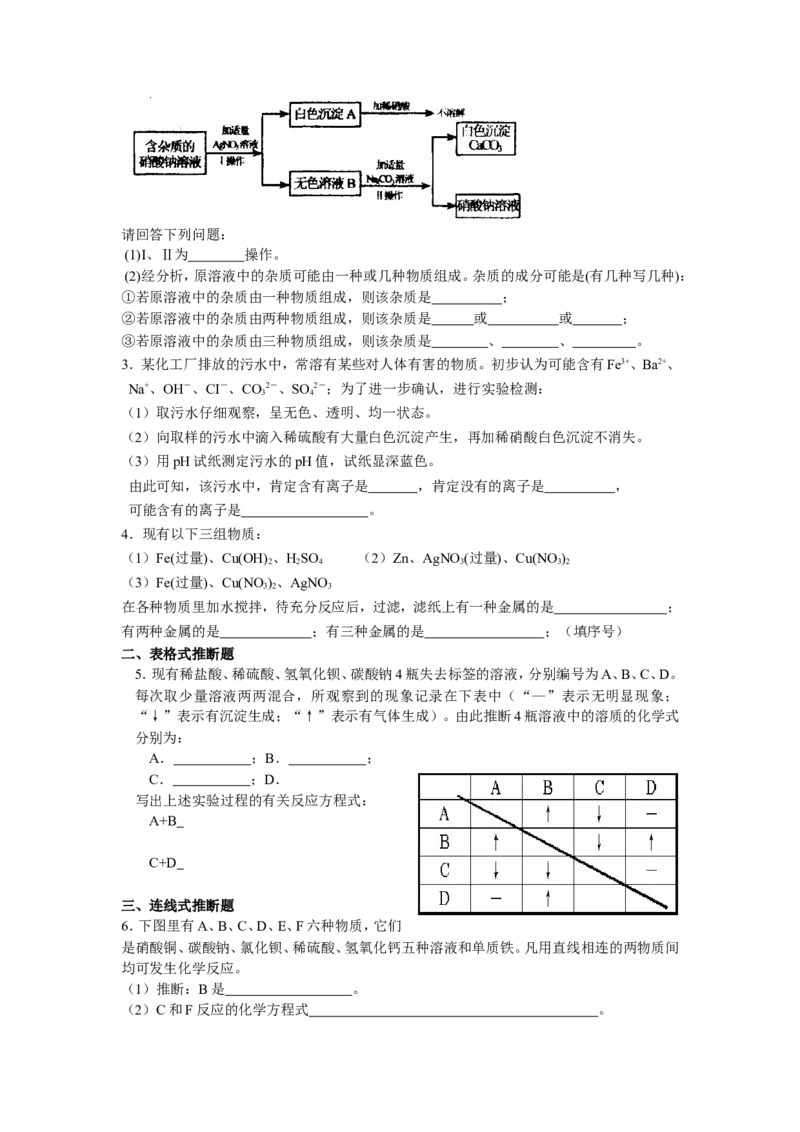
2.为了确定某含杂质的硝酸钠溶液中所含杂质的成分,某同学设计了如下实验:请回答下列问题:
(1)I、Ⅱ为 操作。
(2)经分析,原溶液中的杂质可能由一种或几种物质组成。杂质的成分可能是(有几种写几种):
①若原溶液中的杂质由一种物质组成,则该杂质是 ;
②若原溶液中的杂质由两种物质组成,则该杂质是 或 或 ;
③若原溶液中的杂质由三种物质组成,则该杂质是 、 、 。
3.某化工厂排放的污水中,常溶有某些对人体有害的物质。初步认为可能含有Fe3+、Ba2+、
Na+、OH-、CI-、CO2-、SO 2-;为了进一步确认,进行实验检测:
3 4
(1)取污水仔细观察,呈无色、透明、均一状态。
(2)向取样的污水中滴入稀硫酸有大量白色沉淀产生,再加稀硝酸白色沉淀不消失。
(3)用pH试纸测定污水的pH值,试纸显深蓝色。
由此可知,该污水中,肯定含有离子是 ,肯定没有的离子是 ,
可能含有的离子是 。
4.现有以下三组物质:
(1)Fe(过量)、Cu(OH) 、HSO (2)Zn、AgNO(过量)、Cu(NO )
2 2 4 3 3 2
(3)Fe(过量)、Cu(NO )、AgNO
3 2 3
在各种物质里加水搅拌,待充分反应后,过滤,滤纸上有一种金属的是 ;
有两种金属的是 ;有三种金属的是 ;(填序号)
二、表格式推断题
5.现有稀盐酸、稀硫酸、氢氧化钡、碳酸钠4瓶失去标签的溶液,分别编号为A、B、C、D。
每次取少量溶液两两混合,所观察到的现象记录在下表中(“—”表示无明显现象;
“↓”表示有沉淀生成;“↑”表示有气体生成)。由此推断4瓶溶液中的溶质的化学式
分别为:
A. ;B. ;
C. ;D.
写出上述实验过程的有关反应方程式:
A+B
C+D
三、连线式推断题
6.下图里有A、B、C、D、E、F六种物质,它们
是硝酸铜、碳酸钠、氯化钡、稀硫酸、氢氧化钙五种溶液和单质铁。凡用直线相连的两物质间
均可发生化学反应。
(1)推断:B是 。
(2)C和F反应的化学方程式 。四、框图式推断题
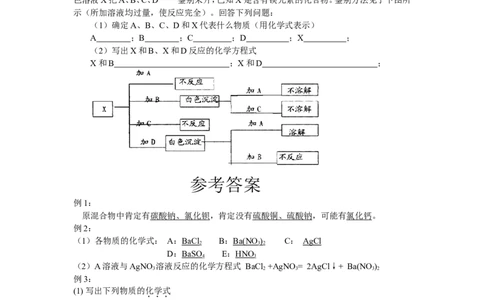
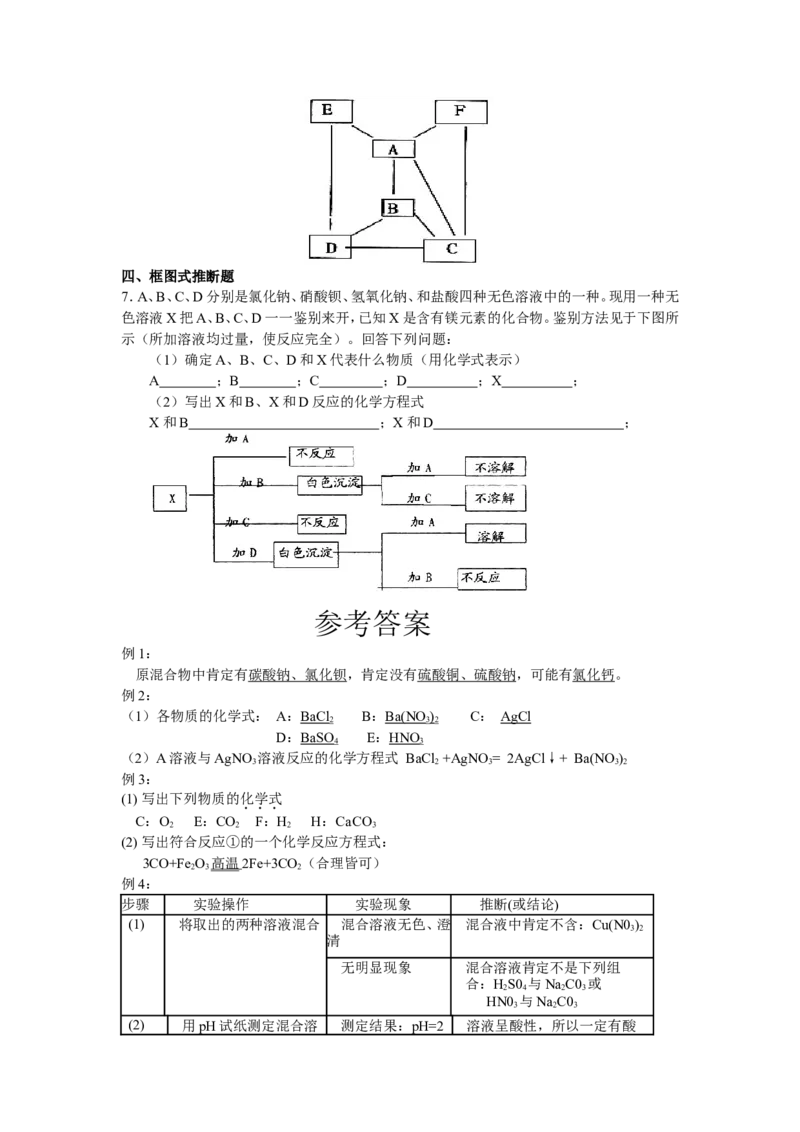
7.A、B、C、D分别是氯化钠、硝酸钡、氢氧化钠、和盐酸四种无色溶液中的一种。现用一种无
色溶液X把A、B、C、D一一鉴别来开,已知X是含有镁元素的化合物。鉴别方法见于下图所
示(所加溶液均过量,使反应完全)。回答下列问题:
(1)确定A、B、C、D和X代表什么物质(用化学式表示)
A ;B ;C ;D ;X ;
(2)写出X和B、X和D反应的化学方程式
X和B ;X和D ;
参考答案
例1:
原混合物中肯定有碳酸钠、氯化钡,肯定没有硫酸铜、硫酸钠,可能有氯化钙。
例2:
(1)各物质的化学式: A:BaCl B:Ba(NO ) C: AgCl
2 3 2
D:BaSO E:HNO
4 3
(2)A溶液与AgNO 溶液反应的化学方程式 BaCl +AgNO = 2AgCl↓+ Ba(NO )
3 2 3 3 2
例3:
(1) 写出下列物质的化学式
C:O E:CO F:H H:CaCO
2 2 2 3
(2) 写出符合反应①的一个化学反应方程式:
3CO+Fe O 高温 2Fe+3CO (合理皆可)
2 3 2
例4:
步骤 实验操作 实验现象 推断(或结论)
(1) 将取出的两种溶液混合 混合溶液无色、澄 混合液中肯定不含:Cu(N0 )
3 2
清
无明显现象 混合溶液肯定不是下列组
合:HS0 与NaC0 或
2 4 2 3
HN0 与NaC0
3 2 3
(2) 用pH试纸测定混合溶 测定结果:pH=2 溶液呈酸性,所以一定有酸液的pH 性物质存在,如HS0 或
2 4
HN0
3
(3) 向混合溶液中滴入足 有白色溶液出现 HS0 或NaS0 (或HS0
2 4 2 4 2 4
量Ba(N03)2溶液 和NaS0 同时共存)
2 4
(4) 向上述溶液过滤所的 无明显现象 不含NaCl
滤液中滴加AgN03溶
液
混合溶液的可能组合(写出溶 ①HN0 H S0
3 2 4
质的化学式,有几组写几组) ②HN0 Na S0
3 2 4
③HS0 Na S0
2 4 2 4
④HSO NaN0
2 4 3
例5:
肯定含有KNO,可能还有NaCO,肯定没有Ba(NO )
3 2 3 3 2
分类跟踪练习
1.不能确定混合物中是否含有:NaCl,操作(1)中应加入的试剂是Ba(NO )
3 2
2.(1)过滤
(2)①CaCl ;
2
②CaCl 、NaCl或CaCl 、Ca(NO ) 或Ca(NO )、NaCl;
2 2 3 2 3 2
③CaCl 、Ca(NO )、NaCl
2 3 2
3.污水中肯定含有离子是 B a 2+ 、 OH - ,肯定没有的离子是 F e 3+ 、 CO 2 - 、 SO 2-,
3 4
可能含有的离子是 N a + 、 CI - 。
4.(2) (1) (3)
5.4瓶溶液中的溶质的化学式分别为:
A:H S 0 B:NaCO C:Ba(OH) D:HCl
2 4 2 3 2
有关反应方程式:
A+B:HS0 + NaCO= NaS0+ H O+CO↑
2 4 2 3 2 4 2 2
C+D:Ba(OH) + 2HCl = BaCl + 2HO
2 2 2
6.(1)B是Ca(OH)
2
(2)C和F反应的化学方程式:NaCO+ BaCl =BaCO ↓+2 NaCl
2 3 2 3
7.(1)A、B、C、D的化学式:
A :HCl;B:;C:NaCl;D:NaOH;X:MgSO
4
(2)有关化学方程式
X和B:MgSO + Ba(NO )= BaSO↓+Mg(NO )
4 3 2 4 3 2
X和D:MgSO + 2NaOH= Mg (OH) ↓+Na SO
4 2 2 4