文档内容
课 时 计 划
科目: 化学 时间: 年 月 日 第 个教案 主备老师: 史慧娟
主备教案 集体备课
课题1燃烧和灭火
课 题
1、知识与技能
⑴认识燃烧的条件与灭火的方法
⑵了解常用灭火器的灭火原理和使用方法。
[来源:学*科*网]
2、过程与方法
通过活动与探究,学生对获得的事实进行分析得出结论的科
学习目标 学方法
3、情感态度与价值观
⑴通过对燃烧条件的探究,了解内因和外因的辨证关系
⑵在解决问题的过程中,激发学生的进取心,让学生获得成
就感
围绕课题让学生通过实验探究、讨论交流得出燃烧的条件和灭
重点
火的原理。使学生感受到化学知识来源于生活,并应用于生活。
教
材 难点 燃烧条件的探究;认识灭火的原理并应用于解决实际生活问题
分
析
教具 1、媒体资源:自制课件
[录像]播放有关燃烧的镜头
[引入]燃烧着的火给人类带来光明和温暖,但是也会给人类带来灾难。燃
烧是生活中一种常见的现象,今天我们就来研究有关燃烧的条件和灭火的
原理。
[录像]播放有关燃烧的镜头
[引入]燃烧着的火给人类带来光明和温暖,但是也会给人类带来灾难。燃
烧是生活中一种常见的现象,今天我们就来研究有关燃烧的条件和灭火的
原理。
[讲述]燃烧是一种常见的现象,那么这种现象的发生需要条件吗?
教
学 [指出]氧气确实是燃烧所需要的条件,但是只有氧气,燃烧能发生吗?大
过 气中也含有氧气,可不见得到处在燃烧,可见氧气并不是燃烧的唯一条件,
程 那么燃烧还需要什么条件呢?
一、认识燃烧的条件
1、认识燃烧需要可燃物
[讨论]根据你的经验和想法谈一谈燃烧除了需要氧气外还需要什么条件?
是不是所有的物体都能燃烧?
[展示]一些物体的图片,判断哪些能燃烧,哪些不能?
[设问]有了可燃物和氧气,燃烧是不是就能发生?例如空气中有氧气,放
在空气中的火柴能燃烧吗?怎样才能使火柴点燃?摩擦起什么作用?以
上事实说明了什么?[讲解]我们把可燃物开始燃烧所需的最低温度叫做着火点。
[演示]探究实验
[讨论]:
1、实验中铁片上的白磷燃烧而红磷不燃烧的事实,说明燃烧需要什么条
件?
2、铁片上的白磷燃烧而热水中的白磷不燃烧的事实,说明燃烧需要什么条
件?
3、本来在热水中不燃烧的白磷,在通入氧气后燃烧的事实,说明燃烧需要
什么条件?
4、综合上述讨论,可得出燃烧需要那些条件?
[归纳小结]
1、燃烧的定义
2、燃烧的条件
[思考]
1、如果不往煤炉里添煤,炉火还能继续燃烧吗?为什么?
2、炉门关得严严的,一点气也不通
炉火还能继续燃烧吗?为什么?
4、如果把炉里正在燃烧的煤夹出来,煤能继续燃烧吗?
[过渡]燃烧的火会给人类带来光明和温暖,但是有时也会带来灾难。那么
如果发生了火灾,我们应该怎么灭火呢?可以根据所学的燃烧的原理进行思
考
二、灭火的原理和方法
[设问]根据燃烧的条件,我们应该如何来灭火呢?
[演示]实验7-1
[小结]灭火的原理
[讨论]根据灭火的实例,分析灭火的原理。
[活动与探究]灭火器的原理。
[媒体展示]几种常见的灭火器
布 [布置作业] P131习题1、2、3、5 金榜学案
置
作
业
板
书
①是可燃物;
设
计 一、物质燃烧的条件: ②与氧气(或空气接触); 同时具备,缺一不可
③温度达到着火点。
①可燃物与助燃物;
二、认识燃烧: ②现象:发光、放热;③实质:剧烈的氧化反应。
三、易燃物和易爆物
①清除或隔离可燃物;
四、灭火方法和原理: ②降低温度到物质着火点以下;
③隔绝空气(或氧气)
破坏其一,燃烧熄灭
教
学
后
记课 时 计 划
科目: 化学 时间: 年 月 日 第 个教案 主备老师: 史慧娟
主备教案 集体备课
课题2 燃料和热量教案
课 题
学习目标 1、知识与技能
(1)知道化石燃料是人类重要的自然资源,对人类生活
起着重要作用;同时,了解化石燃料的不可再生性,认识合理
开采和节约使用化石燃料的重要性。
(2)知道石油炼制出的几种主要产品及其用途。
(3)了解化学反应中的能量变化,认识燃料充分燃烧的
重要性。
2、过程与方法
(1)运用思考、讨论的方法来获取信息。
(2)运用实验的方法来得出结论。
3、情感态度与价值观
通过对化石燃料的形成、使用年限,对人类所起的重要
作用的了解,使学生认识到合理开发的重要性,培养节约利
用资源的意识。
1.了解化石燃料的形成过程和不可再生性。
重点 2.认识化石燃料对人类所起的重要作用。
3.了解化学反应中的能量变化。
教
1.培养学生独立思考、加工信息的能力。
材
分 难点 2.拓展性课题“煤和石油的综合利用”。
析
教具 (1)投影仪,冷而干燥的烧杯,试管,小烧杯,玻璃片;
[以新旧知识的联系,创设情境]
[学习情景]展示柴草、煤、塑料片、布料等实物。
教 [设问]看到这些实物,你想说些什么?
[来源:学科网]
学
[学生回答]如:1.它们都是与人类关系十分密切的可燃物。
过
程 2.它们在外界条件,如氧气、温度等条件适宜的情况下,都可以燃
烧。
3.想告诉大家,平时生活中注意安全。4.想知道煤、塑料等物质是怎样形成的。
……
[新课引入]在日常生活中,许多物质都能发生燃烧反应,从最早使用
的柴草。到煤、石油和天然气,发展至今天,出现了许许多多的新型燃料。
这节课我们就来学习燃料和能量。
[板书]课题2 燃料和热量
[设问]燃料的燃烧在人类社会的发展过程中起着相当重要的作用,
你能举出一些例子吗?
[学生回答、交流]
[讲解]生活中的各个角落都在使用燃料,正是因为燃料的燃烧,推
动了历史的进步。火,是原始人类征服自然的武器。起初,当他们面对熊
熊大火时,祖先们不知所措,惊恐万状。但原始人天生的好奇心和探索
欲,战胜了恐惧和胆怯,慢慢地他们学会了用火来烧烤食物。熟食增强了
入的体质,为身体发育提供了更多的营养,熟食使咀嚼机能减退,于是牙
齿变小,颌部短据,面貌变得愈来愈像现代人。
[过渡]现在我们的生活中,经常使用的燃料以煤、石油和天然气最为
常见。因为它们都是由古代生物的遗骸经一系列复杂变化而形成的,所以
我们称之为化石燃料。下面,我们就以天然气为例,来对化石燃料进行学
习。
[“煤和石油”放在拓展性课题中]
[板书]一、化石燃料——天然气
[讲解]天然气主要是由碳和氢组成的气态碳氢化合物,其中最主要
的是甲烷。下面,同学们注意按照课本P 页[实验7—3]进行活动探究,做
134
一做甲烷的燃烧实验。探究内容如下:
[投影]
1.观察甲烷颜色、状态。
[来源:学科网]
2.在实验结束后,烧杯上出现了什么现象?
3.迅速把烧杯倒转过来,向烧杯内注入澄清石灰水后,振荡,又出现
了什么现象?
4.在实验开始时,点燃前为什么要先检验甲烷的纯度?
5.在实验中烧杯的条件“冷而干燥”是实验成败的关键吗?为什么?
6.这个实验说明甲烷含有哪些元素?
7.你能写出这个实验中涉及到的化学方程式吗?
[学生活动,教师巡视]
[总结、思考、讨论]
[结论]1.甲烷是无色气体。
[思考]1.甲烷在水中的溶解性怎么样呢?
2.甲烷的密度和空气比较起来怎么样呢?
[答案]1.甲烷极难溶于水。
2.甲烷的密度比空气的小。
[设问]那么,同学们想一想,这样的特点,给我们在收集甲烷气体
时,提供了怎样的信息呢?
[回答]收集时,可以用排水法,也可以用向下排空气法。
[评价]回答得非常好,我们在学习中要注意新、旧知识的联系。
[板书]1.甲烷的物理性质:无色、无味的气体,密度比空气小,极难溶于水。
[结论]2.甲烷燃烧时火焰明亮并呈蓝色,可以看到,烧杯内壁上有
水滴生成。
[设问]有水滴生成,说明了什么问题呢?
[回答]说明甲烷的成分里一定含有氢元素。
[结论]3.向烧杯内注入澄清石灰水后,发现烧杯内澄清的石灰水变
浑浊。
[设问]这一现象又说明了什么问题呢?
[回答]这说明甲烷燃烧时有二氧化碳生成,也就是说明了甲烷的成
分里一定含有碳元素。
[教师讲解]甲烷是由碳和氢组成的化合物,化学式是CH。它燃烧时
4
生成二氧化碳和水,同时放出大量的热。
[板书]2.甲烷的燃烧
点燃
CH+2O CO+2HO
4 2 2 2
[结论]4.点燃甲烷和氧气或甲烷和空气的混合物都很可能会发生爆
炸,所以要先验纯。
[延伸]煤矿的矿炕里经常有甲烷逸出,由此,同学们想到了什么呢?
[回答]1.煤矿里必须采取通风设施。
2.煤矿里一定要严禁明火。
[结论]5.“冷而干燥”是这个实验成败的关键。“冷”有利于水汽
的凝集,“干燥”可以判断是否有水滴生成。
6.这个实验说明甲烷中含有碳元素和氢元素。
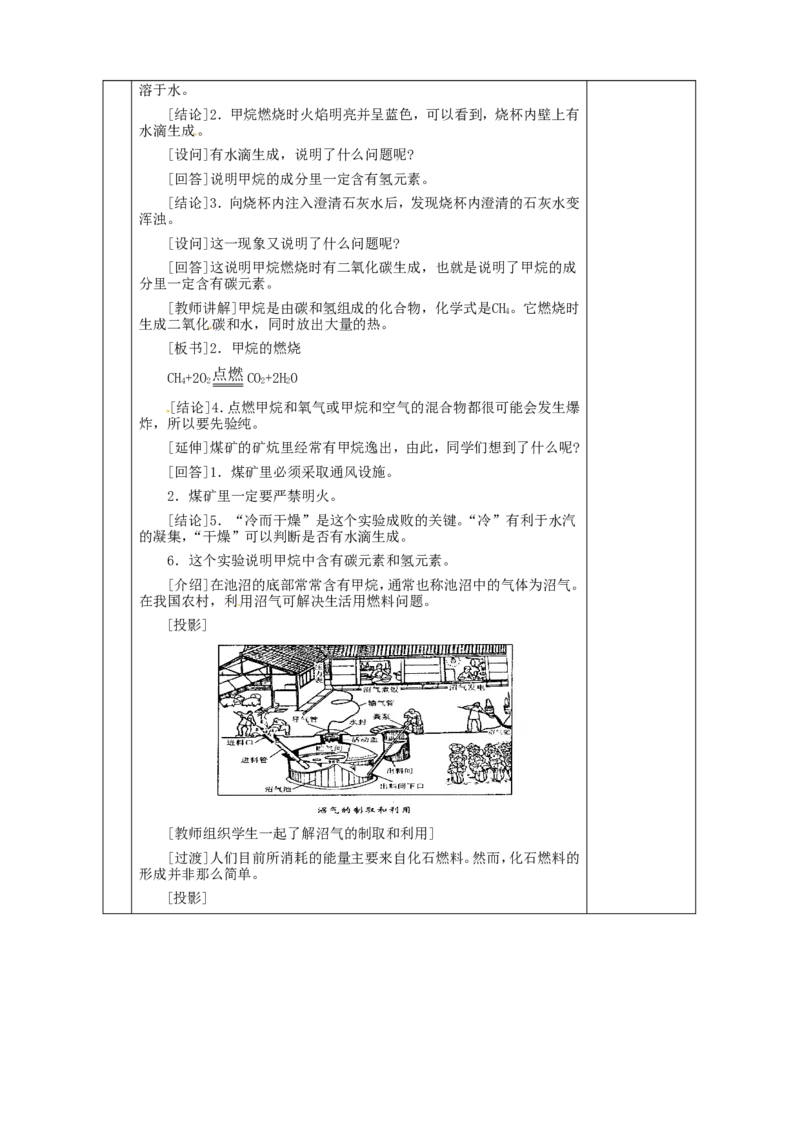
[介绍]在池沼的底部常常含有甲烷,通常也称池沼中的气体为沼气。
在我国农村,利用沼气可解决生活用燃料问题。
[投影]
[教师组织学生一起了解沼气的制取和利用]
[过渡]人们目前所消耗的能量主要来自化石燃料。然而,化石燃料的
形成并非那么简单。
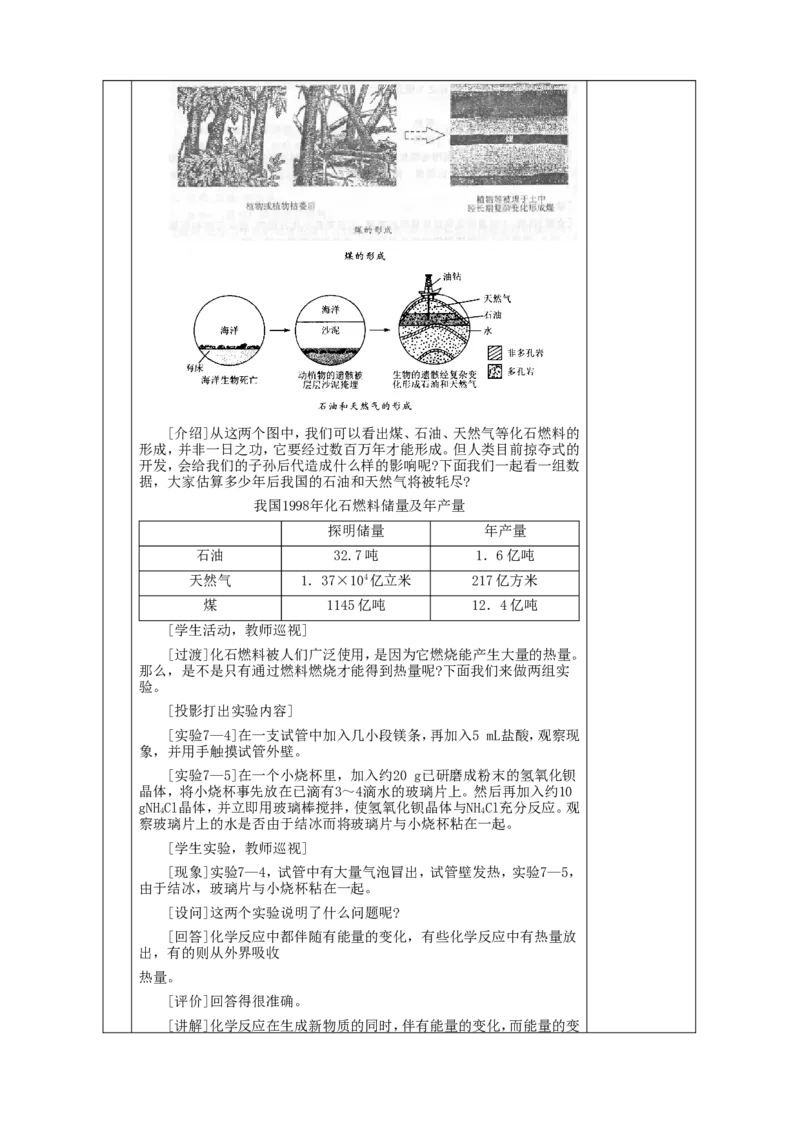
[投影][介绍]从这两个图中,我们可以看出煤、石油、天然气等化石燃料的
形成,并非一日之功,它要经过数百万年才能形成。但人类目前掠夺式的
开发,会给我们的子孙后代造成什么样的影响呢?下面我们一起看一组数
据,大家估算多少年后我国的石油和天然气将被牦尽?
我国1998年化石燃料储量及年产量
探明储量 年产量
石油 32.7吨 1.6亿吨
天然气 1.37×104亿立米 217亿方米
煤 1145亿吨 12.4亿吨
[学生活动,教师巡视]
[过渡]化石燃料被人们广泛使用,是因为它燃烧能产生大量的热量。
那么,是不是只有通过燃料燃烧才能得到热量呢?下面我们来做两组实
验。
[投影打出实验内容]
[实验7—4]在一支试管中加入几小段镁条,再加入5 mL盐酸,观察现
象,并用手触摸试管外壁。
[实验7—5]在一个小烧杯里,加入约20 g已研磨成粉末的氢氧化钡
晶体,将小烧杯事先放在已滴有3~4滴水的玻璃片上。然后再加入约10
gNHCl晶体,并立即用玻璃棒搅拌,使氢氧化钡晶体与NHCl充分反应。观
4 4
察玻璃片上的水是否由于结冰而将玻璃片与小烧杯粘在一起。
[学生实验,教师巡视]
[现象]实验7—4,试管中有大量气泡冒出,试管壁发热,实验7—5,
由于结冰,玻璃片与小烧杯粘在一起。
[设问]这两个实验说明了什么问题呢?
[回答]化学反应中都伴随有能量的变化,有些化学反应中有热量放
出,有的则从外界吸收
热量。
[评价]回答得很准确。
[讲解]化学反应在生成新物质的同时,伴有能量的变化,而能量的变化通常表现为热量的
变化。类似于可燃物燃烧,镁和盐酸这样的反应,我们称之为放热反应。
像碳与二氧化碳:氢氧化钡晶体和NHCl的反应,称之为吸热反应。
4
[板书]
吸热
二、化学反应中的能量变化
放热
[介绍]在当今社会,人们利用化学反应,有时主要是为了制取所需要
的物质,有时却主要是为了利用化学反应所释放出的能量。同学们能举出
一些利用化学反应的热量和能量的实例吗?
[学生讨论,举例]
[介绍]目前,人类通过化学反应获得的能量,大多来自于化石燃料,
而化石燃料资源是有限的。那么,同学们认为怎样利用能源才可以使它
的使用期限得以延长呢?
[学生讨论,回答]
[讲解]总体来讲,如果我们能提高煤等燃料的燃料利用率,就相当于
延长煤的使用期限。要使燃料燃烧通常考虑两点:一是要有足够的空气;
二是要使燃料与空气有足够大的接触面。
[设问]在实际生活中我们是怎样来克服这些困难的呢?我们来看投
影。
[投影]
因为在许多情况下,不能直接燃烧固态煤,如汽车或拖拉机等;或者
虽然能够直接燃烧,但效率很低,如蒸汽机车热利用率只有8%,一般民
用煤炉只有20%左右。所以在石油、天然气不足的情况下,不得不考虑把
煤加工成为气态的、液态的或固态的高级清洁燃料的问题,以提高煤的热
量的利用和减轻环境污染。煤在加工过程中,本身的潜在能量会受到一些
损失。但由于加工成的气态或液态燃料的热利用率高,因此在一些情况
下,煤经过气化或液化而取得的热效益高于直接燃煤。
现在还有相当大的一部分锅炉直接燃烧煤。对低硫煤可以采用粉煤
锅炉,但需加烟道脱硫装置。对高硫煤,要用沸腾床燃烧系统,掺石灰实
行炉内脱硫和降低氧化氮的生成。以上方法都是为了减轻污染、保护环
境。
[小结]通过这节课的学习,我们了解了一些化石燃料,我们还知道化
石燃料已经面临被耗尽的危险,应合理开采,并节约使用。
同时,我们还应认识到,物质发生化学反应的同时,伴随着能量的变
化,通常表现为热量变化,即有放热现象或吸热现象发生。
布 [布置作业]课后习题1、2、3、4、5
置
金榜学案
作
业
板 课题2 燃料和热量
书
一、化石燃料——天然气
设
计 1.甲烷的物理性质:无色、无味的气体,密度比空气小,极难溶于水。
2.甲烷的燃烧:
点燃
CH+2O CO+2HO
4 2 2 2吸热
二、化学反应中的能量变化
放热
教
学
后
记
课 时 计 划
科目: 化学 时间: 年 月 日 第 个教案 主备老师: 史慧娟
主备教案 集体备课
第三课题 使用燃料对环境的影响教案
课 题
1、知识与技能
(1)了解化石燃料对环境的影响。
(2)认识使用和开发清洁燃料及各种能源的重要性。
2、过程与方法
(1)运用模拟实验,认识酸雨的危害。
(2)运用讨论的方法,获取更多的新知识。
学习目标
3、情感态度与价值观
(1)增强保护环境的意识。
(2)激发更强的求知欲。
(3)逐步培养学生用辩证的眼光看“燃料的燃烧。
(4)培养对化学、对科学的热爱。
1.了解化石燃料对环境的影响。
教 重点
2.认识使用和开发清洁燃料及各种能源的重要性
材
分 1.逐步培养学生对现有资料进行分析的能力。
析 难点
2.提高学生综合应用的能力。教具 1、媒体资源:自制课件
[以图片的对比,创设情境]
[教师]在开始学习新内容前,我们先来观看两组幻灯片。(或投影)
[投影]
第一组:课本P 图7—24。
128
第二组:课本P 图7—30、图7—31、图7—32。
134
[设问]这样的两组画面给同学们传递了什么样的信息呢?
[学生回答]第一组画面显示的是化石燃料在人类生活中的用途;第
二组画面显示了燃料在燃烧提供能量的同时,却给环境造成了不良的影
响,腐蚀岩石,污染空气。
[过渡]非常好。我们这节课就一起来学习“使用燃料对环境的影
响”。
[板书]课题3 使用燃料对环境的影响
[新课引入]燃料的使用,给人们的生活带来了很多方便,但却对环
教 境造成了不良的影响。我们主要从燃料燃烧对空气的影响的角度来学
学 习。
过
[板书]一、燃料燃烧对空气的影响
程
[设问]你知道哪些有关这方面的知识呢?
[学生讨论]
[回答]可能有的答案:
1.石油、煤等化石燃料以及它们的加工产品在燃烧过程中会产生一
些含氮、含硫的化合物,排放到大气中,对空气造成污染。
2.1930年12月1日至5日,在比利时的马斯河谷工业区,由于燃料的
燃烧排放出了大量的有害气体,在逆温的条件下大量积累,使60多人中
毒死亡,几千人患呼吸道疾病,许多家禽死亡。
3.汽车中的燃料——柴油或汽油,燃烧时产生的一些物质会直接排
放到空气中,尾气中含有一些一氧化碳,未燃烧的碳氢化合物,氮的氧化
物,含铅氧化物和烟尘等,对空气造成了严重的污染。比如在20世纪50年
代初期,美国洛杉矶市发生了严重的光化学污染事件,65岁以上的老人
死亡400人。由于该市三面环山,高速公路纵横交错,汽车漏油、汽油不完
全燃烧和汽车排放尾气,城市上空聚积近千吨的石油废气、氮氧化物和
一氧化碳。这些物质在阳光的照射下,形成了淡蓝邑的光化学烟雾。
4.光化学烟雾对污染环境危害性很大,但这种现象是在一定条件下
形成的,不是经常出现的。目前酸雨的危害日趋严重,酸度不断增加,范
围日益扩大。据报道,过去酸雨只限于大城市和工业集中区,近年来已发
展到中小城市甚至农村。
[评价]大家联系生活实际回答问题是一个很大的进步,非常好。
[过渡]说到酸雨,我们从刚才的图片上已经看到酸雨对森林、雕像
都造成了严重的危害。下面,我们一起通过酸雨危害的模拟实验来认识一下酸雨对环境的破坏(教材P 页)。
140
[活动与探究]
(因制SO存在污染问题,所以教师课前配好模拟酸雨水,课上供给
2
学生做实验。)
[现象]1.植物叶片(或果皮)都变色。
2.有气泡冒出,镁条或锌粒逐渐变小。
3.有气泡冒出。
[教师补充]煤燃烧时会排放出二氧化硫、二氧化氮等污染物,这些
气体溶于雨水,会形成
酸雨。
[设问]那么,同学们根据上述的实验,能否具体谈淡酸雨对环境和
人类等造成了哪些危害呢?
[回答]1.酸雨引起河流、湖泊的水体酸化,严重影响水生动植物的
生长。
2.它能破坏土壤、植被、森林。
3.酸雨对金属、油漆、皮革、纺织品及建筑材注有腐蚀性。
4. 酸雨渗入地下,可能引起地下水酸化。
5. 对人体的健康有直接的危害,硫酸雾和硫酸盐雾的毒性比二氧
化硫大得多,可以侵入肺的深部组织,引起肺水肿等疾病而使人致死。
……
[过渡]我们生活的家园——地球,她在流泪,她在滴血,她的儿女们
不能坐以待毙。那我们应该采取怎样的措施来保护她呢?
[学生讨论]
[来源:学§科§网Z§X§X§K]
[回答]1.减少人为排放的污染物。
2.减少煤中的含硫量,对煤炭中的硫资源进行合理的开发和利用。
[来源:
学科网ZXXK]
3.改进设备,使燃料充分燃烧;增加催化净化装置,使有害气体转化
成无害气体。
[来源:学_科_网]
4.使用无铅汽油,禁止含铝物质排放。
5.开发新能源。
……
[教师和学生一起总结刚才的内容并板书]
[板书]
[过渡]煤和石油虽然是重要的化工原料,由于它们燃烧时对空气造
成污染,所以人类把眼光放在了使用和开发清洁的燃料上。
[板书]二、使用和开发新的燃料及能源
[投影]
车用乙醇汽油
乙醇是以高梁、玉米、小麦、薯类、糖蜜等为原料,经发酵、蒸馏而制
成的。将乙醇液中含有的水进一步除去,再添加适量的变性剂(为防止饮用)可形成变性燃料乙醇。车用乙醇汽油是将变性燃料乙醇和汽油以一
定的比例混合而形成的一种汽车燃料。使用这种燃料不但可以节省石油
资源和有效地减少汽车尾气的污染,还可以促进农业生产。 乙醇汽油
在一些国家已成功使用多年,目前在我国也开始受到重视。2001年4月2
日,国家质量技术监督局发布了《变性燃料乙醇》和《车用乙醇汽油》两项
国家标准;并于2001年4月15日开始实施。我国将根据具体情况,在一些
城市逐步推广使用乙醇汽油。
[讲解]乙醇俗称酒精,它是无色透明,具有特殊气味的液体。乙醇还
容易挥发,能与水以任意比互溶,而且还是一种优良的有机溶剂。
乙醇的成分里含有碳、氢、氧三种元素,它的化学式是CHOH。
2 5
[设问]根据乙醇的化学式,你认为作为汽车变性燃料的乙醇与氧气
发生反应的生成物是什么呢?
[回答]二氧化碳和水。
[追问]为什么呢?
[回答]根据质量守恒定律,从微观的角度来讲,反应前后原子的种
类和数目不变。
[评价]非常好!大家学习时要注意新旧知识的联系。
[板书]1.乙醇(酒精)
CHOH+3O 2CO+3HO
2 5 2 2 2
[引申]在街上吃火锅时,有的火锅下面燃烧的是一种外观类似于冰
的一种物质,它真的是冰吗?
[回答]不是,这种类似于冰的物质其实是一种固体酒精。
[教师补充]从这个实例中我们可以看出乙醇同样有着三态变化。由
于乙醇燃烧时能放出大量的热,所以它被用作酒精灯、火锅、内燃机等的
燃料。
[设问]除了乙醇之外,你还知道哪些新型的燃料或者能源。
[回答]1.氢气被认为是最清洁的燃料,它点燃后生成了水,并且放
出大量的热。但由于氢气的制取成本高和贮存困难,所以还没有被广泛
使用。
2.地热。地球的地心是高达几千摄氏度的熔岩,地热能的总量,相当
于煤炭总量的1.7亿倍。
3.潮汐能。它是一种不消耗的燃料,是没有污染,不受洪水或枯水
影响,用之不竭的再生
能源。在海洋能源中,潮汐能的开发利用最为现实,最为方便。
……
[板书]2.氢气
2H+O 2HO
2 2 2
[过渡]科学家在开发新能源上,已经取得了累累硕果。让我们一起
来看看这个可喜的成果。(或投影或制成课件)
[投影]
[来源:Zxxk.Com]
一、用地热水发电
产生地热能源需要两个条件:发热的岩石和滚烫的水。在冰岛,这两
者都具备,而且丰富得很。由此派生出地热利用的两种模式,一种是直接
将地下热水抽出,另一种是向地下有热岩的地方注入冷水,利用热岩加
热冷水,再把热水从另一处抽出。前一种方式较省事,但地下热水中含有
多种腐蚀物,对供热管道的腐蚀极大,如不采取有效措施事先加以预防,
这种地热利用是不会长久的。后一种方式虽然腐蚀问题不严重,但是,很难控制地下那个巨大的“加热炉”(即热岩)的活动。总之,不论采用哪
种方式利用地热,都必须拥有先进的科学技术和工业基础。
冰岛利用地热主要靠注入冷水取得地热能。利用地下沸水的内斯韦
利热能发电厂,居然提供了雷克雅未克所需热能的1/3。该厂位于地热
高温区,地下2000米深处的温度已达400℃。从18个钻孔中冒出水与蒸汽
的混合物。这些混合物经过热交换器,冷水就被加热到约90℃。不过,由
于水中存在的大量的氧气对管道系统具有相当强的腐蚀作用,所以必须
去除水中的氧气。为此,人们不仅使用普通的排气法,还在水中添加少量
硫化氢。硫化氢与氧气发生反应后,就可以除去剩余的氧气,这就是为什
么雷克雅未克的热水中常常会有一股淡淡的臭鸡蛋味的缘故。
冰岛人采用的这一措施还真有效,如果来自地层深处的沸水直接进
入管道系统,管壁很快就会穿孔。因为地下水中含有丰富的矿物质以及
酸性腐蚀物质,即使采用最好的钢管,用不了几个月也会被腐蚀。而硅
酸、氯化钠及铁、钙等元素在冷却时却会凝固成黏合物,很快将水龙头堵
塞。若在水中添加少量硫化氢,上述弊端即都能克服。
在日本,新源产业技术综合机构则于1991年末成功地进行了地下热
水发电实验。他们将热水在低温下与沸腾的煤体进行热量交换,利用交
换过程中产生的蒸汽发电。
由于日本拥有大量的温泉,因此在温泉旁打井,然后安装设备,利用
地下热水发电是很方便的,目前,这项实验正在进行中。
二、太阳灶
收集太阳能代替煤、电,用来煮水烧饭,是大阳灶的特长。
例如,我国四川省攀枝花市注重能源利用和环境保护,这里的城乡
居民普遍使用太阳灶,住宅民房顶上的太阳能器具群已成为该市的一大
景观。
澳大利亚悉尼大学的一个太阳能研究小组研制了一种新型的太阳
能灶,效率很高。该装置的关键设备是一个独特的太阳能集热器,其形状
为弓状的不锈钢镜子,镜子长5英尺(约合152厘米)、宽2英尺(约合61厘
米)。将这种太阳灶置于屋外的地面上,镜子始终正对着太阳光,在其正
中央布置一套发散式吸热管,通过管子循环的水由于被加热而变成蒸
汽;再用管子将蒸汽引到屋内的灶上,用这种办法可使灶温达到180℃。
在这么高的温度下可进行各种烹调,既能炸制、烤制食品,也能蒸煮食
品,一个灶可供应25个人就餐。
此外,由于白天在压力容器中产生的热量散发的速度很慢,所以甚
至到深夜,炉灶也能保持高温,故在夜间仍可使用。三、干净的核能
1986年,世界核电装机容量还只有2.5亿千瓦,7年后的1993年就发
展到4亿千瓦,占世界发电总量的17%,预计再过7年,到本世纪末,核电
装机容量还将增加到5亿千瓦,发电量将占世界发电量的1/3~1/2。尤
其是少煤缺油的法国与日本,1993年已建成投入运行的核反应堆已有56
座与48座,分列世界第一位与第二位。发电总功率也达到了0.6亿千瓦与
0.4亿千瓦。就是那些拥有丰富的煤炭、石油资源的国家,也在大力发展
核电,其中羌国运行的核反应堆在80年代未就已超过了100座。而英国、
俄国、德国的运行堆数在1993年也分别达到了35座、29座和20座。由此可
见,进入21世纪后,能源结构中核电的比重将进一步增大,其作用和地位
也将日显重要。到那时,核能将像现在的煤、油、气等天然常规能源那样,
日渐为众多的人们所接受,进入寻常的百姓人家。
[小结]通过这节课的学习,我们知道,在人类利用燃料的同时,也给
人类所赖以生存的环境——地球,带来了极大的危害。作为地球人类的
一员,我们应该团结起来保护我们的家园,努力学习,投身于现代化建设
中。
布 [布置作业] P131习题1、2、3、5 金榜学案
置
作
业
板 课题3 使用燃料对环境的影响
书
一、燃料燃烧对空气的影响
设
计
二、使用和开发新的燃料及能源
1.乙醇(酒精)
CHOH+3O 2CO+3HO
2 5 2 2 2 [来源:学|科|网]
2.氢气
2H+O 2HO
2 2 2教
学
后
记