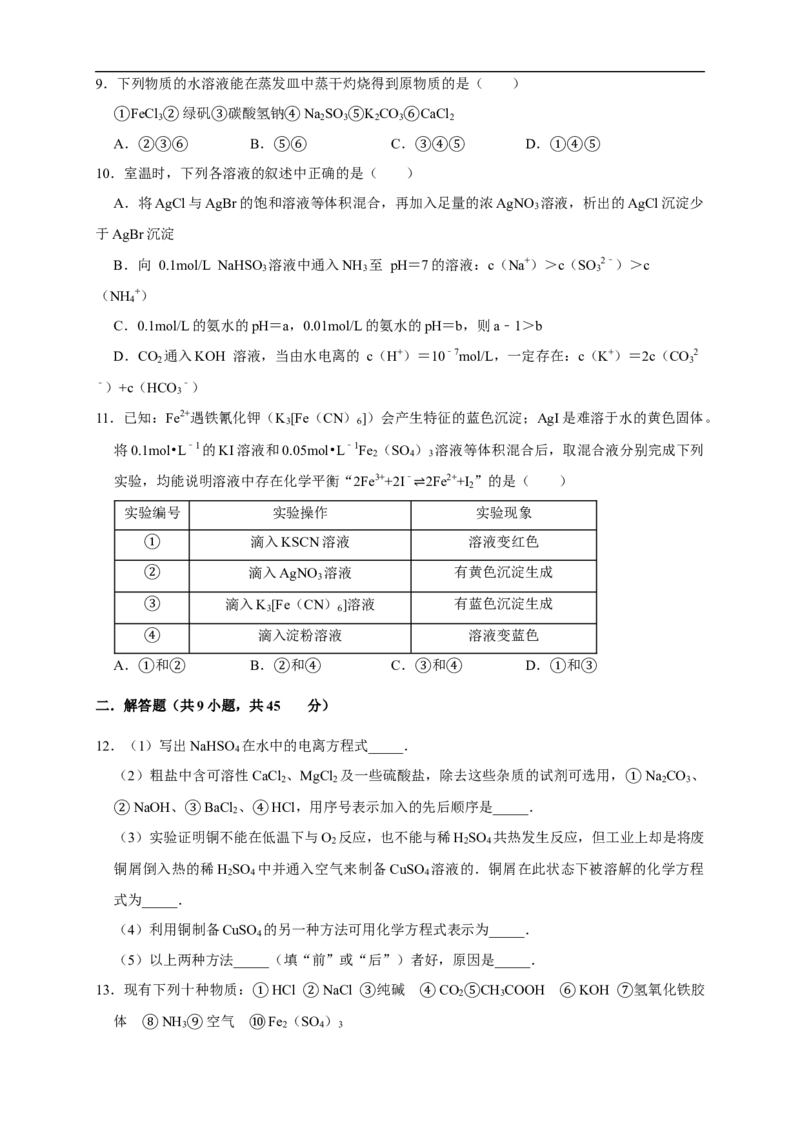文档内容
第三章 总结与检测 练习(原卷版)
一.选择题(共11小题,每题5分,共55分)
1.能说明醋酸是弱电解质的事实是( )
A.醋酸溶液的导电性比盐酸弱
B.醋酸溶液与碳酸钙反应,缓慢放出二氧化碳
C.醋酸溶液用水稀释后,氢离子浓度下降
D.0.1mol•的CH COOH溶液中,氢离子浓度约为0.001mol
3
2.某温度下,重水( D O)的离子积常数为 1.6×10﹣15,若用定义 pH 一样规定 pD=﹣lgc
2
(D+),则在该温度下,下列叙述正确的是( )
A.纯净的重水中,c(D+)•c(OD﹣)>1.0×10﹣14
B.l L溶解有0.01 mol DCl的重水溶液,其pD=2
C.1 L溶解有0.01 mol NaOD的重水溶液,其pD=12
D.纯净的重水中,pD=7
3.下列图象与对应的说法正确的是( )
A. 向NaOH溶液中加水稀释
B. 等质量的Al、Zn与足量的稀硫酸反应
C. 向稀硫酸中加入Ba(OH) 溶液
2
D. 恒温下,适量蒸发饱和NaCl溶液的水分
4.下列图示与对应的叙述相符的是( )A.图1表示常温下,稀释HA、HB两种酸的稀溶液时,溶液PH随加水量的变化,则等物质的
量浓度的NaA和NaB混合溶液中:C(Na+)>C(A﹣)>C(B﹣)>C(OH﹣)>C(H+)
B.图2中在b点对应温度下,将pH=2的H SO 溶液与pH=12的NaOH溶液等体积混合后,
2 4
溶液显中性
C.用0.010 0 mol/L硝酸银标准溶液,滴定浓度均为0.100 0 mol/L Cl﹣、Br﹣及I﹣的混合溶液,
由图3曲线,可确定首先沉淀的是Cl﹣
D.图4表示在N (g)+3H (g) 2NH (g)达到平衡后,减少NH 浓度时速率的变化
2 2 3 3
5.用标准盐酸滴定未知浓度的NaOH⇌溶液,下列各操作中会引起实验误差的是( )
A.滴定前酸式滴定管需用标准盐酸润洗
B.用蒸馏水洗净锥形瓶后,立即装入一定体积的NaOH溶液后进行滴定
C.往盛有20.00 mL NaOH溶液的锥形瓶中,滴入几滴酚酞指示剂后进行滴定
D.用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗,然后装入一定体积的NaOH溶液
6.T℃时,满足下列条件的溶液一定呈酸性的是( )
A.pH=6的溶液
B.含有H+的溶液
C.c(H+)>c(OH﹣)
D.能与金属A1反应放出H 的溶液
2
7.下列化学方程式中,属于水解反应的是( )
A.H
2
O+H
2
O H
3
O++OH﹣ B.HS﹣+OH﹣ H
2
O+S2﹣
C.HS﹣+H
2
O⇌ H
3
O++S2﹣ D.HS﹣+H
2
O⇌H
2
S+OH﹣
8.一定条件下,⇌Na CO 溶液中存在平衡:CO 2﹣+H O HCO⇌ ﹣+OH﹣.下列有关说法正确的是(
2 3 3 2 3
) ⇌
A.通入 CO ,溶液 pH 增大
2
B.升高温度,上述反应平衡常数不变
C.加水稀释, 变大
D.加入 NaOH 固体,平衡向正反应方向移动9.下列物质的水溶液能在蒸发皿中蒸干灼烧得到原物质的是( )
FeCl 绿矾 碳酸氢钠 Na SO K CO CaCl
3 2 3 2 3 2
①A. ② ③ B. ④ ⑤ C.⑥ D.
10.室温②时③,⑥下列各溶液的叙⑤述⑥中正确的是( )③④⑤ ①④⑤
A.将AgCl与AgBr的饱和溶液等体积混合,再加入足量的浓AgNO 溶液,析出的AgCl沉淀少
3
于AgBr沉淀
B.向 0.1mol/L NaHSO 溶液中通入NH 至 pH=7的溶液:c(Na+)>c(SO 2﹣)>c
3 3 3
(NH +)
4
C.0.1mol/L的氨水的pH=a,0.01mol/L的氨水的pH=b,则a﹣1>b
D.CO 通入KOH 溶液,当由水电离的 c(H+)=10﹣7mol/L,一定存在:c(K+)=2c(CO 2
2 3
﹣)+c(HCO ﹣)
3
11.已知:Fe2+遇铁氰化钾(K [Fe(CN) ])会产生特征的蓝色沉淀;AgI是难溶于水的黄色固体。
3 6
将0.1mol•L﹣1的KI溶液和0.05mol•L﹣1Fe (SO ) 溶液等体积混合后,取混合液分别完成下列
2 4 3
实验,均能说明溶液中存在化学平衡“2Fe3++2I﹣ 2Fe2++I ”的是( )
2
实验编号 实验操作 ⇌ 实验现象
滴入KSCN溶液 溶液变红色
① 滴入AgNO 溶液 有黄色沉淀生成
3
② 滴入K [Fe(CN) ]溶液 有蓝色沉淀生成
3 6
③ 滴入淀粉溶液 溶液变蓝色
A. ④和 B. 和 C. 和 D. 和
① ② ② ④ ③ ④ ① ③
二.解答题(共9小题,共45 分)
12.(1)写出NaHSO 在水中的电离方程式_____.
4
(2)粗盐中含可溶性CaCl 、MgCl 及一些硫酸盐,除去这些杂质的试剂可选用, Na CO 、
2 2 2 3
NaOH、 BaCl 、 HCl,用序号表示加入的先后顺序是_____. ①
2
②(3)实验证③明铜不能在④低温下与O
2
反应,也不能与稀H
2
SO
4
共热发生反应,但工业上却是将废
铜屑倒入热的稀H SO 中并通入空气来制备CuSO 溶液的.铜屑在此状态下被溶解的化学方程
2 4 4
式为_____.
(4)利用铜制备CuSO 的另一种方法可用化学方程式表示为_____.
4
(5)以上两种方法_____(填“前”或“后”)者好,原因是_____.
13.现有下列十种物质: HCl NaCl 纯碱 CO CH COOH KOH 氢氧化铁胶
2 3
体 NH 空气 ①Fe (S②O ) ③ ④ ⑤ ⑥ ⑦
3 2 4 3
⑧ ⑨ ⑩(1)上述十种物质中,属于强电解质的有_____,属于弱电解质的有_____属于非电解质的有
_____;
(2)有两种物质在水溶液中可发生反应,离子方程式为 H++OH﹣=H O,该反应的化学方程式
2
为_____;
(3)标准状况下,_____L 中含有0.2mol氧原子;
(4)现有100mL 溶液中④含Fe3+5.6g,则溶液中SO
4
2﹣的物质的量浓度是_____。
14.(1)在25°C时⑩,纯水中C(H+)•C(OH﹣)=_____;
(2)在NH Cl溶液中C(H+)_____10﹣7mol/L(大于、小于或等于),pH_____7(大于、小于
4
或等于);
(3)在Na CO 溶液中C(H+)_____10﹣7mol/L (大于、小于或等于),pH_____7(大于、小
2 3
于或等于)
(4)在NaCl溶液中C(H+)_____10﹣7mol/L (大于、小于或等于),pH_____7(大于、小于
或等于).
15.室温下,把下列各题的结果填在横线上
(1)c(OH﹣)=1×10﹣3mol/L的溶液的pH=_______
(2)0.01mol/L HNO 溶液中,水电离出的H+的物质的量的浓度c(H+)=_______
3
(3)某溶液由水电离出H+的物质的量的浓度c(H+)=1×10﹣5mol/L,则该溶液可以是_____
(填“硫酸”或“氯化铵”或“氢氧化钠”或“氯化钠”)溶液
(4)将0.39g过氧化钠溶于足量水中并配成100mL溶液,则溶液的pH=_____
(5)0.12mol/LHCl溶液与0.1mol/L的NaOH溶液等体积混合,混合液的pH=_____
16.某一元弱酸(用HA表示)在水中的电离方程式是HA H++A﹣,回答下列问题:
(1)向纯水中加入适量HA,水的电离平衡将向_____(⇌填“正”、“逆”)反应方向移动,理
由是_____。
(2)若向(1)所得溶液中加入适量NaCl溶液,以上平衡将向_____(填“正”、“逆”)反
应方向移动,溶液中c(A﹣)将_____(填“增大”、“减小”或“不变”),溶液中c(OH
﹣)将_____(填“增大”、“减小”或“不变”)。
17.设计一个简单的一次性完成实验的装置图,验证醋酸溶液、二氧化碳水溶液、苯酚溶液的酸性
强弱顺序是CH COOH>H CO >C H OH.
3 2 3 6 5
(1)利用如图所示的仪器可以组装实验装置,则仪器的连接顺序是_____接D,E接_____,
_____接_____.
(2)有关反应的化学方程式为_____.
(3)有的同学认为此装置不能验证H CO 和C H OH的酸性强弱,你认为是否有道理?怎样改
2 3 6 5进实验才能验证H CO 和C H OH的酸性强弱?_____.
2 3 6 5
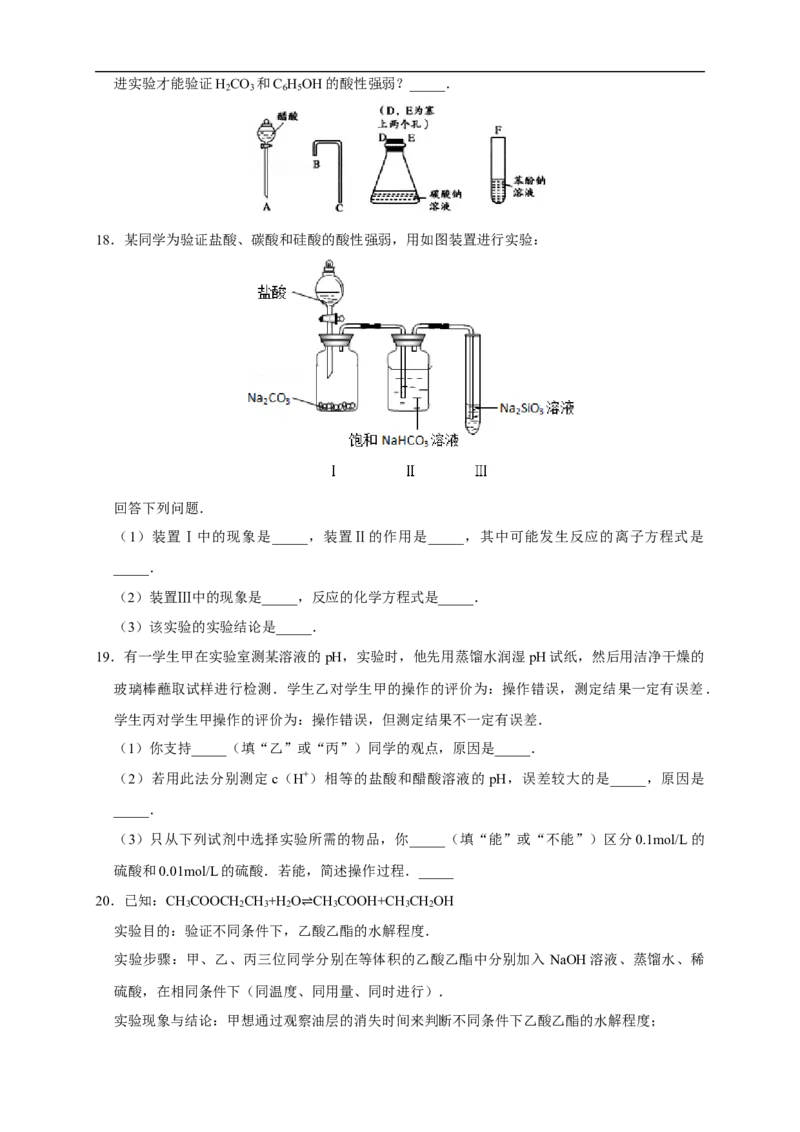
18.某同学为验证盐酸、碳酸和硅酸的酸性强弱,用如图装置进行实验:
回答下列问题.
(1)装置Ⅰ中的现象是_____,装置Ⅱ的作用是_____,其中可能发生反应的离子方程式是
_____.
(2)装置Ⅲ中的现象是_____,反应的化学方程式是_____.
(3)该实验的实验结论是_____.
19.有一学生甲在实验室测某溶液的pH,实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的
玻璃棒蘸取试样进行检测.学生乙对学生甲的操作的评价为:操作错误,测定结果一定有误差.
学生丙对学生甲操作的评价为:操作错误,但测定结果不一定有误差.
(1)你支持_____(填“乙”或“丙”)同学的观点,原因是_____.
(2)若用此法分别测定c(H+)相等的盐酸和醋酸溶液的pH,误差较大的是_____,原因是
_____.
(3)只从下列试剂中选择实验所需的物品,你_____(填“能”或“不能”)区分0.1mol/L的
硫酸和0.01mol/L的硫酸.若能,简述操作过程._____
20.已知:CH COOCH CH +H O CH COOH+CH CH OH
3 2 3 2 3 3 2
实验目的:验证不同条件下,乙⇌酸乙酯的水解程度.
实验步骤:甲、乙、丙三位同学分别在等体积的乙酸乙酯中分别加入 NaOH溶液、蒸馏水、稀
硫酸,在相同条件下(同温度、同用量、同时进行).
实验现象与结论:甲想通过观察油层的消失时间来判断不同条件下乙酸乙酯的水解程度;乙想通过测定乙酸的浓度或含量来判断不同条件下乙酸乙酯的水解程度;
丙想通过…
根据上述回答下列问题:
(1)甲同学为何可以通过观察油层的消失时间来达到实验目的:_____
(2)乙同学认为可以通过pH试纸测定溶液的pH来判断其不同条件下的水解程度,测定pH的
操作是_____该方法是否可行?_____(填“行”或不可行”)理由是:_____.
(3)你认为丙同学可以通过_____来判断不同条件下乙酸乙酯的水解程度.
(4)要在水解后的溶液中通过蒸馏,得到无水乙醇,除了加入生石灰外,还需要加入_____,
在蒸馏实验中除了酒精灯、蒸馏烧瓶、温度计、接引器外还需要的玻璃仪器有:_____.