文档内容
课题 3 二氧化碳和一氧化碳
答案:
(1)大 (2)能 (3)干冰 (4)CO +HO===HCO (5)Ca(OH) +CO===CaCO↓+HO
2 2 2 3 2 2 3 2
(6)温室效应 (7)灭火 (8)难 (9)2CO+O=====2CO (10)还原 (11)CO+CuO=====Cu
2 2
+CO
2
1.二氧化碳的性质
(1)实验探究
① 倾倒二氧化碳实验
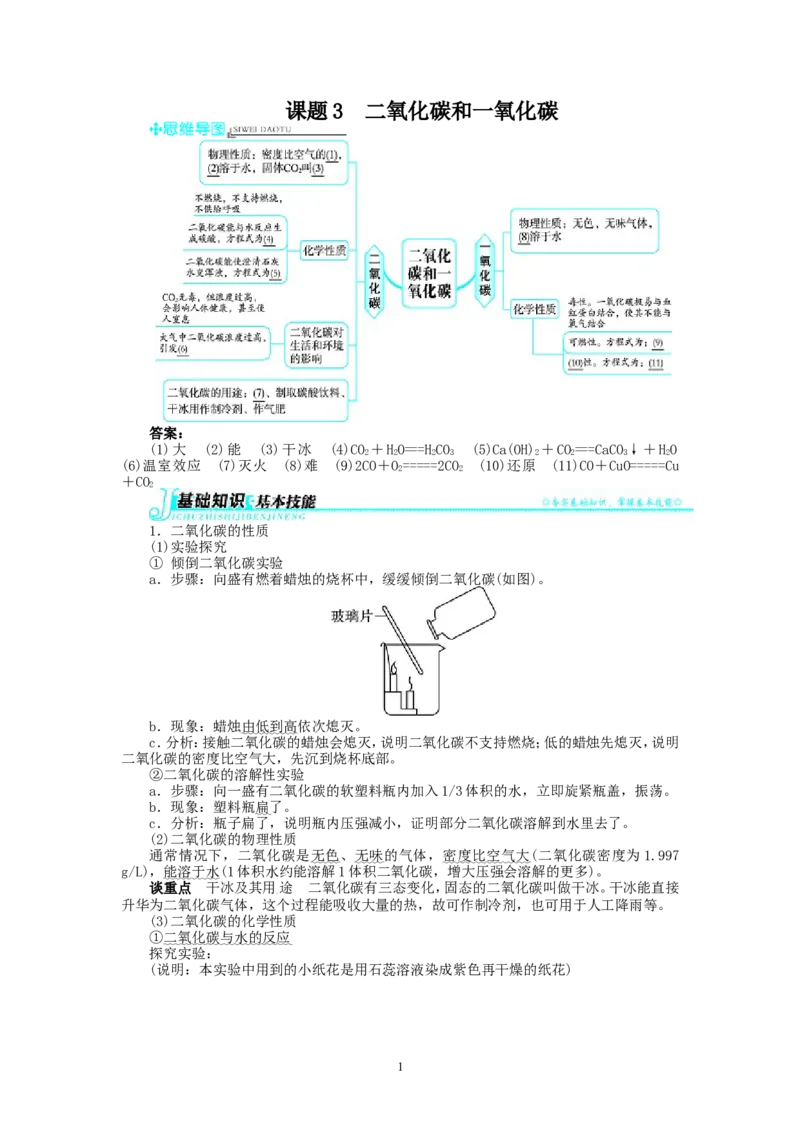
a.步骤:向盛有燃着蜡烛的烧杯中,缓缓倾倒二氧化碳(如图)。
b.现象:蜡烛由低到高依次熄灭。
c.分析:接触二氧化碳的蜡烛会熄灭,说明二氧化碳不支持燃烧;低的蜡烛先熄灭,说明
二氧化碳的密度比空气大,先沉到烧杯底部。
②二氧化碳的溶解性实验
a.步骤:向一盛有二氧化碳的软塑料瓶内加入1/3体积的水,立即旋紧瓶盖,振荡。
b.现象:塑料瓶扁了。
c.分析:瓶子扁了,说明瓶内压强减小,证明部分二氧化碳溶解到水里去了。
(2)二氧化碳的物理性质
通常情况下,二氧化碳是无色、无味的气体,密度比空气大(二氧化碳密度为1.997
g/L),能溶于水(1体积水约能溶解1体积二氧化碳,增大压强会溶解的更多)。
谈重点 干冰及其用途 二氧化碳有三态变化,固态的二氧化碳叫做干冰。干冰能直接
升华为二氧化碳气体,这个过程能吸收大量的热,故可作制冷剂,也可用于人工降雨等。
(3)二氧化碳的化学性质
①二氧化碳与水的反应
探究实验:
(说明:本实验中用到的小纸花是用石蕊溶液染成紫色再干燥的纸花)
1操
作
喷稀
喷水 喷水后放入CO
醋酸 2
直接放入CO 中 中,取出再烘干
2
小花
现 小花 小花不
小花不变色
象 变红 变色 变红;烘干后变
紫
二氧化碳和水作
分 稀醋酸能使小花 水不能使石蕊变 干燥的CO 不能 用生成了碳酸,
2
析 变红 红 使石蕊变红 碳酸不稳定,受
热易分解
a.二氧化碳和水反应生成碳酸:
结 CO+HO===HCO
2 2 2 3
论 b.碳酸不稳定,易分解:
HCO===HO+CO↑
2 3 2 2
②二氧化碳与澄清石灰水反应
将二氧化碳通入澄清的石灰水中,石灰水变浑浊了。这是二氧化碳与石灰水发生了化学
反应,生成了不溶于水的白色碳酸钙的缘故。化学实验中常用这个现象来检验二氧化碳。有
关反应的化学方程式为:
Ca(OH)+CO===CaCO ↓+HO
2 2 3 2
辨误区 检验二氧化碳的方法 检验二氧化碳,常用澄清石灰水。一般不用燃着的木条
来检验二氧化碳,因为氮气也不支持燃烧。
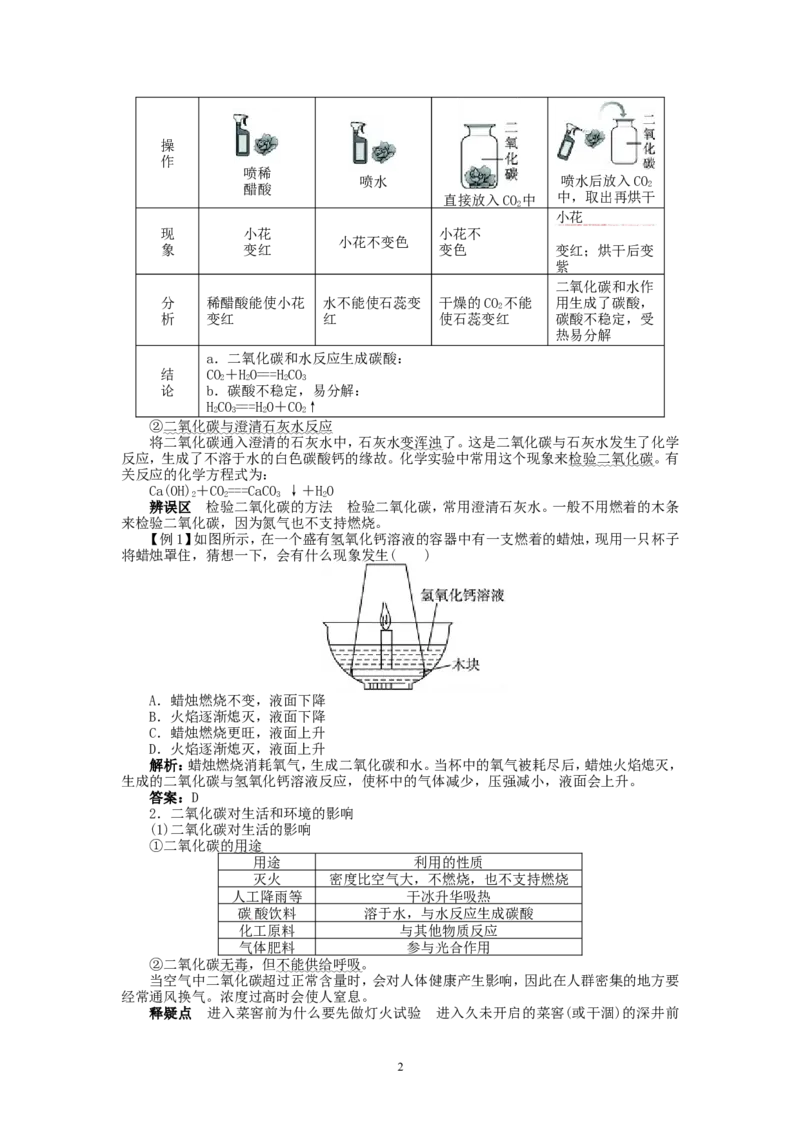
【例1】如图所示,在一个盛有氢氧化钙溶液的容器中有一支燃着的蜡烛,现用一只杯子
将蜡烛罩住,猜想一下,会有什么现象发生( )
A.蜡烛燃烧不变,液面下降
B.火焰逐渐熄灭,液面下降
C.蜡烛燃烧更旺,液面上升
D.火焰逐渐熄灭,液面上升
解析:蜡烛燃烧消耗氧气,生成二氧化碳和水。当杯中的氧气被耗尽后,蜡烛火焰熄灭,
生成的二氧化碳与氢氧化钙溶液反应,使杯中的气体减少,压强减小,液面会上升。
答案:D
2.二氧化碳对生活和环境的影响
(1)二氧化碳对生活的影响
①二氧化碳的用途
用途 利用的性质
灭火 密度比空气大,不燃烧,也不支持燃烧
人工降雨等 干冰升华吸热
碳酸饮料 溶于水,与水反应生成碳酸
化工原料 与其他物质反应
气体肥料 参与光合作用
②二氧化碳无毒,但不能供给呼吸。
当空气中二氧化碳超过正常含量时,会对人体健康产生影响,因此在人群密集的地方要
经常通风换气。浓度过高时会使人窒息。
释疑点 进入菜窖前为什么要先做灯火试验 进入久未开启的菜窖(或干涸)的深井前
2应先做一个灯火试验。方法是将一支燃着的蜡烛,放入菜窖内,若蜡烛燃烧不旺或熄灭,说明
二氧化碳的浓度较高,人不宜进入。
(2)二氧化碳对环境的影响
①大气中二氧化碳的产生和消耗途径
产生途径 消耗途径
动植物呼吸;工厂废气;含碳燃料燃烧;微生物分解 植物光合作用
以上两个方面若保持相对平衡,空气中二氧化碳的含量是相对稳定的。若产生
的二氧化碳大于消耗,会使空气中二氧化碳含量升高而导致温室效应
②温室效应
大气中的二氧化碳气体能像温室的玻璃或塑料薄膜那样,使地面吸收的太阳光的热量
不易散失,从而使全球变暖,这种现象叫温室效应。
a.产生温室效应的原因
人类消耗的能源急剧增加,向空气中排放了大量二氧化碳,同时森林遭到破坏,使二氧
化碳的吸收量减小,导致大气中二氧化碳含量不断上升。
b.温室效应的危害
气温上升导致冰川融化、海平面上升、沿海城市被淹没;地球表面的水分蒸发,使土地沙
漠化。
c.防治温室效应的措施
减少使用煤、石油、天然气等化石燃料;开发新能源,利用太阳能、风能、地热能等;大力
植树造林,禁止乱砍滥伐。
释疑点 能产生温室效应的气体 能产生温室效应的气体除二氧化碳外,还有臭氧
(O)、甲烷(CH)、氟氯代烷(商品名为氟利昂)等。
3 4
温室效应好可怕啊,我讨厌CO
2!
任何事物都有利弊,CO 对人类的利大于弊,关键是我们应合理利用哦!
2
【例2】联合国气候变化框架公约《京都议定书》要求发达国家限制CO 等温室气体的排
2
放量,以控制日趋严重的温室效应。请回答下列问题:
(1)绿色植物通过____________作用吸收CO,放出____________。
2
(2)为了缓解大气中的CO 含量的增加,以下建议可行的是______________(填字母)。
2
A.开发太阳能、水能、风能、地热能等新型能源
B.禁止使用煤、石油、天然气等化石燃料
C.提倡植树造林,禁止乱砍滥伐
解析:(1)绿色植物通过光合作用,将水、二氧化碳转变成有机物,同时释放氧气。(2)能
减少二氧化碳的生成及增大二氧化碳的消耗的建议都是可行的。
答案:(1)光合 氧气(或O) (2)AC
2
3.一氧化碳
(1)物理性质
通常情况下,一氧化碳(CO)是一种无色、无味的气体,密度比空气的略小,难溶于水(1
体积水里可溶解0.02体积CO)。
(2)化学性质
①可燃性:2CO+O=====2CO,产生蓝色火焰,放出大量的热。
2 2
②毒性:CO有剧毒,CO极易与血液中的血红蛋白结合,从而使血红蛋白不能很好地与氧
结合,造成生物体内缺氧,严重时会危及生命。
谈重点 使用CO时应注意什么 若CO不纯,点燃时可能发生爆炸,因此点燃前一定要
检验纯度;CO有毒,冬天用煤取暖时一定要装烟囱,并注意通风。
③还原性:CO + CuO=====Cu+CO
2
还原剂 氧化剂
一氧化碳和木炭一样能够夺取含氧化合物里的氧,表现还原性。
(3)一氧化碳的性质与用途的关系
性质 用途
可燃性 作燃料,管道煤气的主要成分就是一氧化碳
冶炼金属,如工业常用CO来炼铁
还原性
3CO+FeO=====2Fe+3CO
2 3 2
CO有利也有弊。不纯的CO易爆炸,CO有剧毒,是大气污染物,它无色无味,又是“隐
形”杀手;CO可作燃料,也是冶金工业中的重要还原剂。
(4)一氧化碳还原氧化铜的实验探究
实验
3装置
③实验结束后,先
实验 ②先通入CO,再加
①检验CO的纯度 停止加热,继续通
步骤 热
CO,直到冷却
防止玻璃管中进入
原因 防止CO中混有氧 排尽玻璃管中的空
空气,生成的铜重
分析 气,加热时爆炸 气,防止加热爆炸
新被氧化
实验 ①黑色粉末变为红色;
现象 ②澄清的石灰水变浑浊
CO具有还原性,将氧化铜还原为铜,同时生成CO,即CO+
结论 2
CuO=====Cu+CO
2
谈重点 CO还原CuO实验的操作要点 ①实验开始,要先通一氧化碳再加热;实验结束,
要先停止加热,再停止通一氧化碳。即一氧化碳要“早来晚走”。“早来”的目的是排尽试
管中的空气,避免加热时发生爆炸;“晚走”的目的是保护生成的铜不被氧化。相反,酒精灯
要“迟到早退”。②因为一氧化碳有毒,所以做一氧化碳还原氧化铜实验时,一定要有尾气
处理装置,防止一氧化碳扩散到空气中。
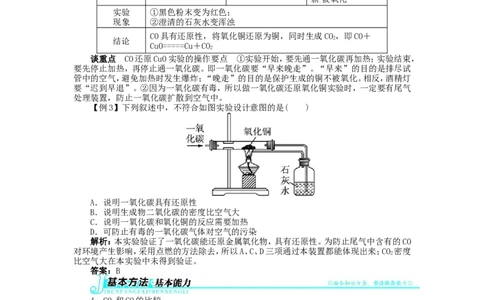
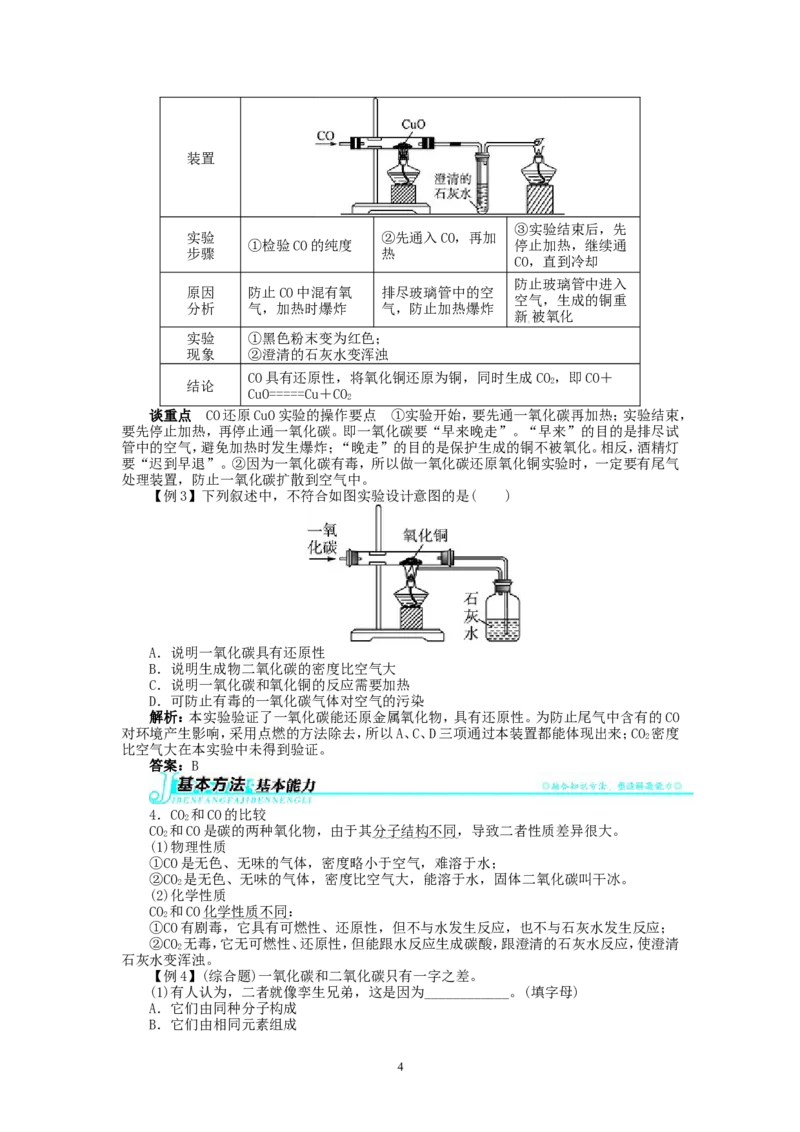
【例3】下列叙述中,不符合如图实验设计意图的是( )
A.说明一氧化碳具有还原性
B.说明生成物二氧化碳的密度比空气大
C.说明一氧化碳和氧化铜的反应需要加热
D.可防止有毒的一氧化碳气体对空气的污染
解析:本实验验证了一氧化碳能还原金属氧化物,具有还原性。为防止尾气中含有的CO
对环境产生影响,采用点燃的方法除去,所以A、C、D三项通过本装置都能体现出来;CO 密度
2
比空气大在本实验中未得到验证。
答案:B
4.CO 和CO的比较
2
CO 和CO是碳的两种氧化物,由于其分子结构不同,导致二者性质差异很大。
2
(1)物理性质
①CO是无色、无味的气体,密度略小于空气,难溶于水;
②CO 是无色、无味的气体,密度比空气大,能溶于水,固体二氧化碳叫干冰。
2
(2)化学性质
CO 和CO化学性质不同:
2
①CO有剧毒,它具有可燃性、还原性,但不与水发生反应,也不与石灰水发生反应;
②CO 无毒,它无可燃性、还原性,但能跟水反应生成碳酸,跟澄清的石灰水反应,使澄清
2
石灰水变浑浊。
【例4】(综合题)一氧化碳和二氧化碳只有一字之差。
(1)有人认为,二者就像孪生兄弟,这是因为____________。(填字母)
A.它们由同种分子构成
B.它们由相同元素组成
4C.它们都有毒
D.它们都能溶于水
(2)有人 认为,二 者化学性质 相差甚远 ,请给 出一条支持 他的理由:
____________________________。
(3) 其 实 , 二 者 是 可 以 相 互 转 化 的 , 请 用 化 学 方 程 式 表 示 此 过 程 :
____________________________。
解析:问题(1)要从组成上找出二氧化碳和一氧化碳的共性;而问题(2)是找二者性质上
的差异;问题(3)二者的转化,要体现相互性。
答案:(1)B (2)二氧化碳不能燃烧,一氧化碳可以燃烧(二氧化碳能与水反应,一氧化
碳不能;或二氧化碳能与石灰水反应,一氧化碳不能;或一氧化碳能与氧化铜反应,二氧化碳
不能) (3)2CO+O=====2CO(或3CO+FeO=====3CO+2Fe或C+CO=====2CO)
2 2 2 3 2 2
5.CO 与CO性质的应用
2
(1)鉴别CO 与CO
2
鉴别两种物质时,要考虑利用二者性质的差异;其次,要考虑不同的性质所产生的现象
是否相同。鉴别的直接依据是现象的不同。鉴别CO与CO 可用下列方法:
2
①用燃烧的木条伸入瓶口——能被点燃的是CO,能使燃烧的木条立即熄灭的是CO;
2
②通入澄清的石灰水——能使澄清的石灰水变浑浊的是CO,不能变浑浊的是CO;
2
③通入紫色石蕊溶液——能使紫色石蕊溶液变红色的是CO,不能变色的是CO;
2
④通过灼热的CuO——能使黑色的氧化铜粉末变为红色的是CO,不能变色的是CO。
2
(2)除去CO 中的少量CO
2
CO 中混有少量CO时,宜将混合气体通过灼热的CuO,从而将CO转化为CO,不能采用点
2 2
燃的方法,因为少量的CO在大量的CO 中不能被点燃。
2
(3)除去CO中的少量CO
2
CO中混有少量CO 时,宜将混合气体通入澄清石灰水(或NaOH溶液),以除去少量的CO,
2 2
不宜通入水中,因为CO 在水中的溶解度不大。
2
【例5—1】(探究题)CO和CO 尽管分子中只差一个氧原子,但性质差别很大。下面是四位
2
同学设计的鉴别CO和CO 的方法,你认为不正确的是( )
2
①通入澄清的石灰水中 ②通入水中 ③通过灼热的氧化铜 ④闻气体的气味
A.①② B.②③
C.②④ D.①③
解析:CO 能使澄清石灰水变浑浊,而CO不能;CO能使灼热的氧化铜变为红色的铜,而
2
CO 不能,故①、③都可作为鉴别CO和CO 的方法。有些同学错误地认为,CO 能与水反应而CO
2 2 2
不能,故也可据此鉴别CO和CO,产生这种错误认识的原因是没有想到CO 能与水反应,但没
2 2
有明显现象,仅用水无法鉴别,若在水中滴加紫色石蕊溶液,就可以鉴别。④中CO和CO 都无
2
色、无味,通过气味不能鉴别,且CO 有毒,不能直接闻,故也不正确。
答案:C
【例5—2】(综合题)下列说法正确的是( )
A.二氧化碳有毒,会使人中毒死亡
B.CO 的增加是造成温室效应的主要原因,因此空气中CO 含量越低越好
2 2
C.可以用点燃的方法除去CO 中混有的少量CO
2
D.可用澄清石灰水区别CO 和CO两种气体
2
解析:CO 无毒,但不供给呼吸,A错误;CO 的增加是造成温室效应的主要原因,但同时
2 2
CO 也是光合作用的原料,B错误;通常情况下,CO 不支持燃烧,也不燃烧,当CO 中混有少量
2 2 2
CO时,CO无法被点燃,故C错误;CO 能使澄清石灰水变浑浊,CO不能,故可用澄清石灰水区
2
别CO 和CO。
2
答案:D
5