文档内容
第二章 总结与检测 练习(原卷版)
一.选择题(共21小题,每题4分,共84分)
1.在2A(g)+B(g)═3C(g)+4D(g)反应中,下面表示的反应速率最快的是( )
A.v(A)=0.5mo1/(L•s) B.v(B)=1.8mo1/(L•min)
C.v(C)=0.9mo1/(L•s) D.v(D)=1.0mo1/(L•s)
2.在2L密闭容器中充入一定量的SO 和O ,化学方程式是2SO +O 2SO .经测定反应开始后3s
2 2 2 2 3
末O 的物质的量减小了1.5mol,则前3s内SO 的平均反应速率为(⇌ )
2 2
A.0.25mol•L﹣1•s﹣1 B.0.5mol•L﹣1•s﹣1
C.0.75mol•L﹣1•s﹣1 D.0.83mol•L﹣1•s﹣1
3.反应4A(s)+3B(g)═2C(g)+D(g)经2min后,B的浓度减少了0.6mol•L﹣1.下列说法
正确的是( )
A.用A表示的化学反应速率是0.4mol•L﹣1•min﹣1
B.分别用B、C、D表示化学反应速率,其比是3:2:1
C.在2min末的反应速率用B表示是0.3mol•L﹣1•min﹣1
D.若改变条件2min内v(D)=0.2mol•L﹣1•min﹣1,则反应速率减慢
4.已知反应 :C(s)+CO (g) 2CO(g)(吸热反应),反应 :2SO (g)+O (g)
2 2 2
2SO (g)① (放热反应)。下列⇌说法不正确的是( ) ②
3
⇌A.其他条件不变,压缩容器体积,反应 和反应 的逆反应速率均增大
B.其他条件不变,降低温度,反应 的①正反应速率②减小,反应 的逆反应速率增大
C.其他条件不变,增加CO
2
的用量①,一段时间后,反应 的逆②反应速率增大
D.其他条件不变,使用催化剂,反应 的逆反应速率增①大
5.下列说法中正确的是( ) ②
A.增大反应物浓度,使活化分子百分数增大,化学反应速率增大
B.升高温度,反应物分子中活化分子的百分数增大,从而增大化学反应速率
C.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率
D.有气体参加的反应,压强增大时,活化分子百分数一定增加,从而使反应速率增大
6.下列有关有效碰撞的说法不正确的是( )
A.能发生有效碰撞的分子一定是活化分子
B.有效碰撞是发生化学反应的充要条件
C.只要条件合适,普通分子之间的碰撞也可能是有效碰撞
D.活化分子间的碰撞不一定是有效碰撞
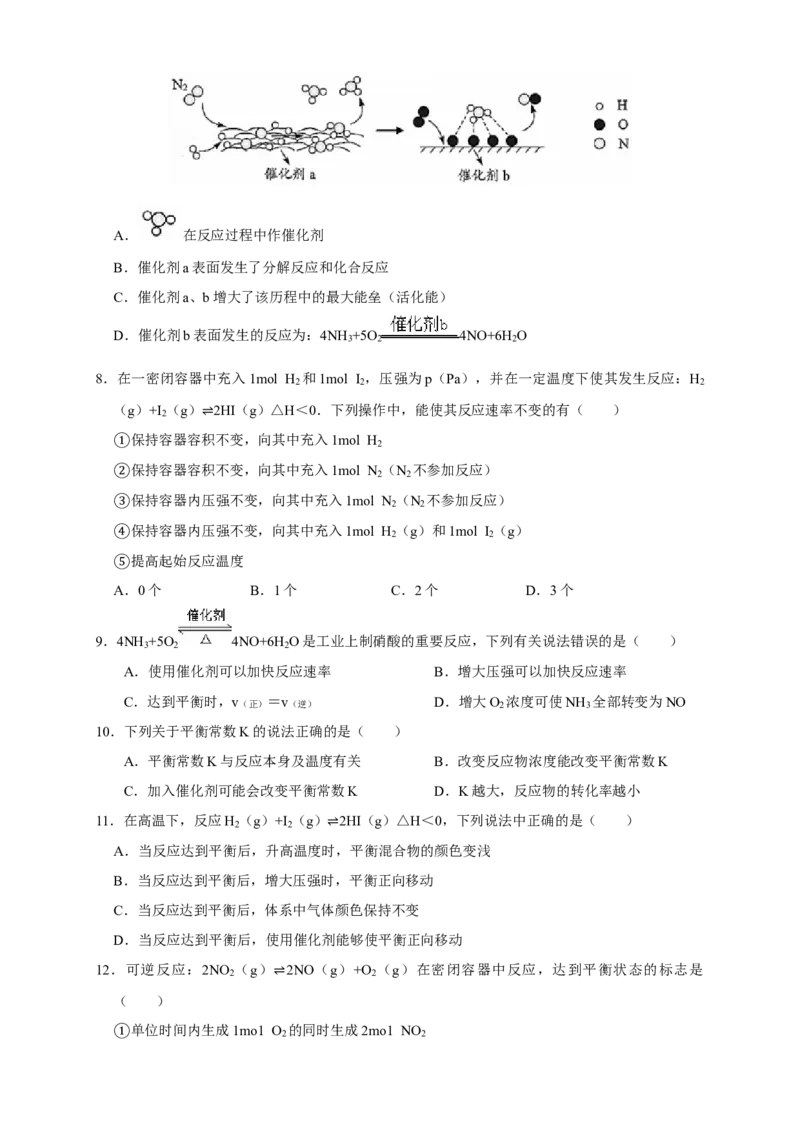
7.N 分子在催化剂的作用下发生的一系列转化如图所示。下列叙述正确的是( )
2A. 在反应过程中作催化剂
B.催化剂a表面发生了分解反应和化合反应
C.催化剂a、b增大了该历程中的最大能垒(活化能)
D.催化剂b表面发生的反应为:4NH +5O 4NO+6H O
3 2 2
8.在一密闭容器中充入1mol H 和1mol I ,压强为p(Pa),并在一定温度下使其发生反应:H
2 2 2
(g)+I (g) 2HI(g)△H<0.下列操作中,能使其反应速率不变的有( )
2
保持容器容积⇌不变,向其中充入1mol H
2
①保持容器容积不变,向其中充入1mol N
2
(N
2
不参加反应)
②保持容器内压强不变,向其中充入1mol N
2
(N
2
不参加反应)
③保持容器内压强不变,向其中充入1mol H
2
(g)和1mol I
2
(g)
④提高起始反应温度
⑤A.0个 B.1个 C.2个 D.3个
9.4NH +5O 4NO+6H O是工业上制硝酸的重要反应,下列有关说法错误的是( )
3 2 2
A.使用催化剂可以加快反应速率 B.增大压强可以加快反应速率
C.达到平衡时,v(正) =v(逆) D.增大O
2
浓度可使NH
3
全部转变为NO
10.下列关于平衡常数K的说法正确的是( )
A.平衡常数K与反应本身及温度有关 B.改变反应物浓度能改变平衡常数K
C.加入催化剂可能会改变平衡常数K D.K越大,反应物的转化率越小
11.在高温下,反应H (g)+I (g) 2HI(g)△H<0,下列说法中正确的是( )
2 2
A.当反应达到平衡后,升高温度时⇌,平衡混合物的颜色变浅
B.当反应达到平衡后,增大压强时,平衡正向移动
C.当反应达到平衡后,体系中气体颜色保持不变
D.当反应达到平衡后,使用催化剂能够使平衡正向移动
12.可逆反应:2NO (g) 2NO(g)+O (g)在密闭容器中反应,达到平衡状态的标志是
2 2
( ) ⇌
单位时间内生成1mo1 O 的同时生成2mo1 NO
2 2
①单位时间内生成1mo1 O 的同时,消耗2mo1 NO
2 2
②v(NO
2
)
正
=v(NO)
逆
③混合气体的颜色不再改变的状态
④
O 的物质的量不再改变的状态
2
⑤
A. B. C. D.
①③④⑤ ②③④ ②③⑤ ①②④⑤
13.4NH +5O 4NO+6H O是工业上制硝酸的重要反应,下列有关说法错误的是( )
3 2 2
A.使用催化剂可以加快反应速率 B.增大压强可以加快反应速率
C.反应达到平衡时,v(正)=v(逆) D.增大O 的量可使NH 100%转变为NO
2 3
14.将E(s)和F(g)加入密闭容器中,在一定条件下发生反应:E(s)+4F(g) G(g),已
知该反应的平衡常数如表。下列说法正确的是( ) ⇌
温度℃ 25 80 230
平衡常数/(L3•mol﹣3) 5×104 2 1.9×10﹣5
A.正反应是吸热反应
B.25℃时,反应G(g) E(s)+4F(g)的平衡常数是0.5mo13•L﹣3
C.80℃时,测得某时刻F⇌、G的浓度均为0.5mol•L﹣1,此时v正 >v逆
D.恒温恒容下,向容器中再充入少量G(g),达新平衡时,G的体积分数增大
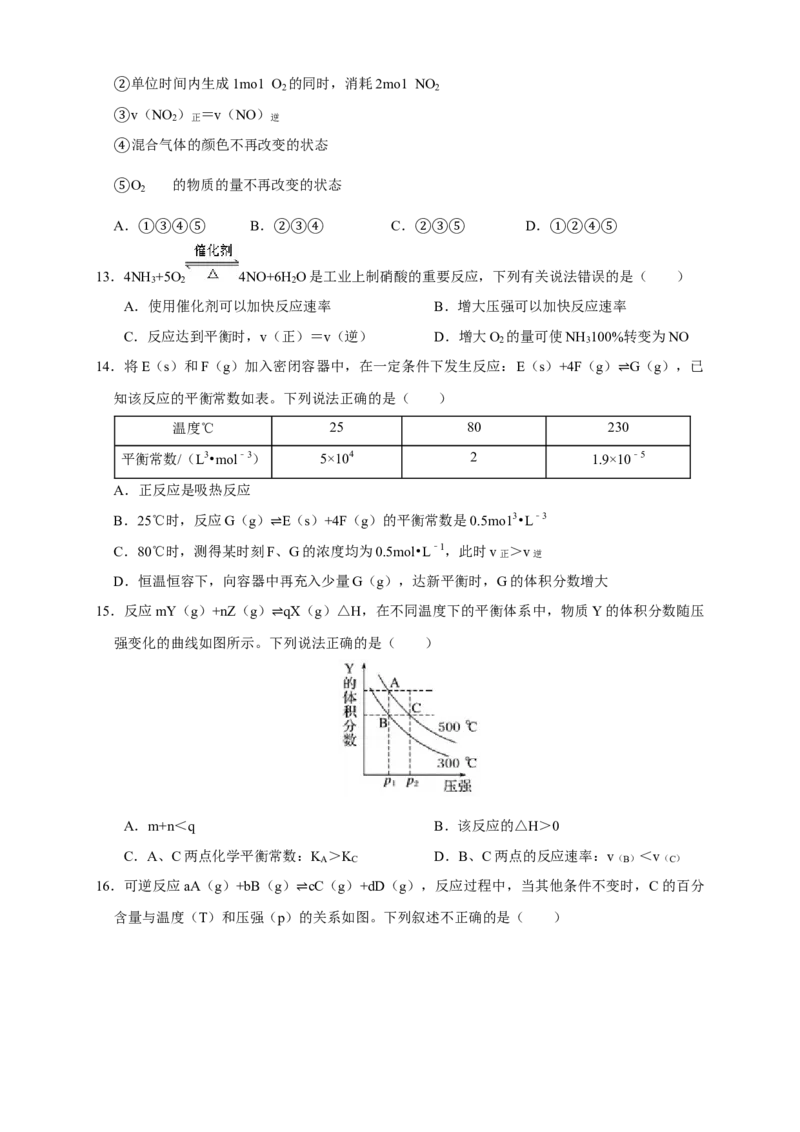
15.反应mY(g)+nZ(g) qX(g)△H,在不同温度下的平衡体系中,物质Y的体积分数随压
强变化的曲线如图所示。下⇌列说法正确的是( )
A.m+n<q B.该反应的△H>0
C.A、C两点化学平衡常数:K
A
>K
C
D.B、C两点的反应速率:v(B) <v(C)
16.可逆反应aA(g)+bB(g) cC(g)+dD(g),反应过程中,当其他条件不变时,C的百分
含量与温度(T)和压强(p)⇌的关系如图。下列叙述不正确的是( )A.达平衡后,若升温,平衡左移
B.达平衡后,加入催化剂,则C的百分含量不变
C.化学方程式中a+b>c+d
D.达平衡后,减小A的量有利于平衡向左移动
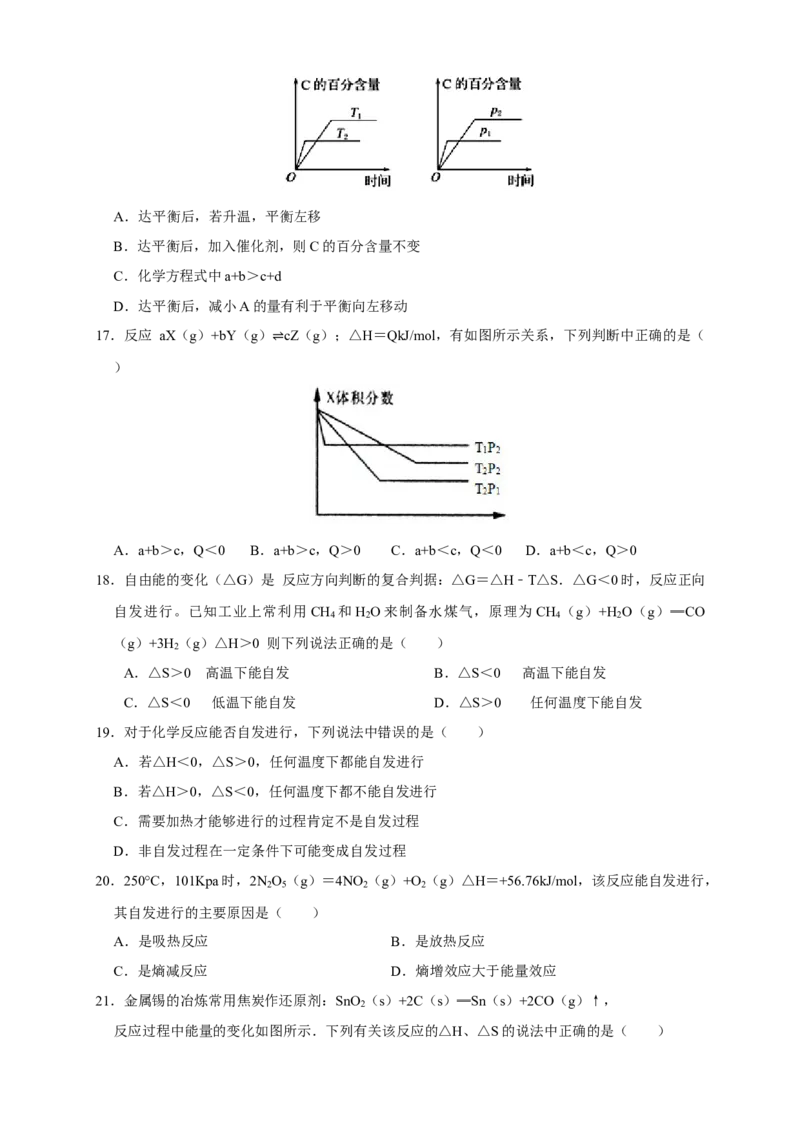
17.反应 aX(g)+bY(g) cZ(g);△H=QkJ/mol,有如图所示关系,下列判断中正确的是(
) ⇌
A.a+b>c,Q<0 B.a+b>c,Q>0 C.a+b<c,Q<0 D.a+b<c,Q>0
18.自由能的变化(△G)是 反应方向判断的复合判据:△G=△H﹣T△S.△G<0时,反应正向
自发进行。已知工业上常利用 CH 和H O来制备水煤气,原理为CH (g)+H O(g)═CO
4 2 4 2
(g)+3H (g)△H>0 则下列说法正确的是( )
2
A.△S>0 高温下能自发 B.△S<0 高温下能自发
C.△S<0 低温下能自发 D.△S>0 任何温度下能自发
19.对于化学反应能否自发进行,下列说法中错误的是( )
A.若△H<0,△S>0,任何温度下都能自发进行
B.若△H>0,△S<0,任何温度下都不能自发进行
C.需要加热才能够进行的过程肯定不是自发过程
D.非自发过程在一定条件下可能变成自发过程
20.250°C,101Kpa时,2N O (g)=4NO (g)+O (g)△H=+56.76kJ/mol,该反应能自发进行,
2 5 2 2
其自发进行的主要原因是( )
A.是吸热反应 B.是放热反应
C.是熵减反应 D.熵增效应大于能量效应
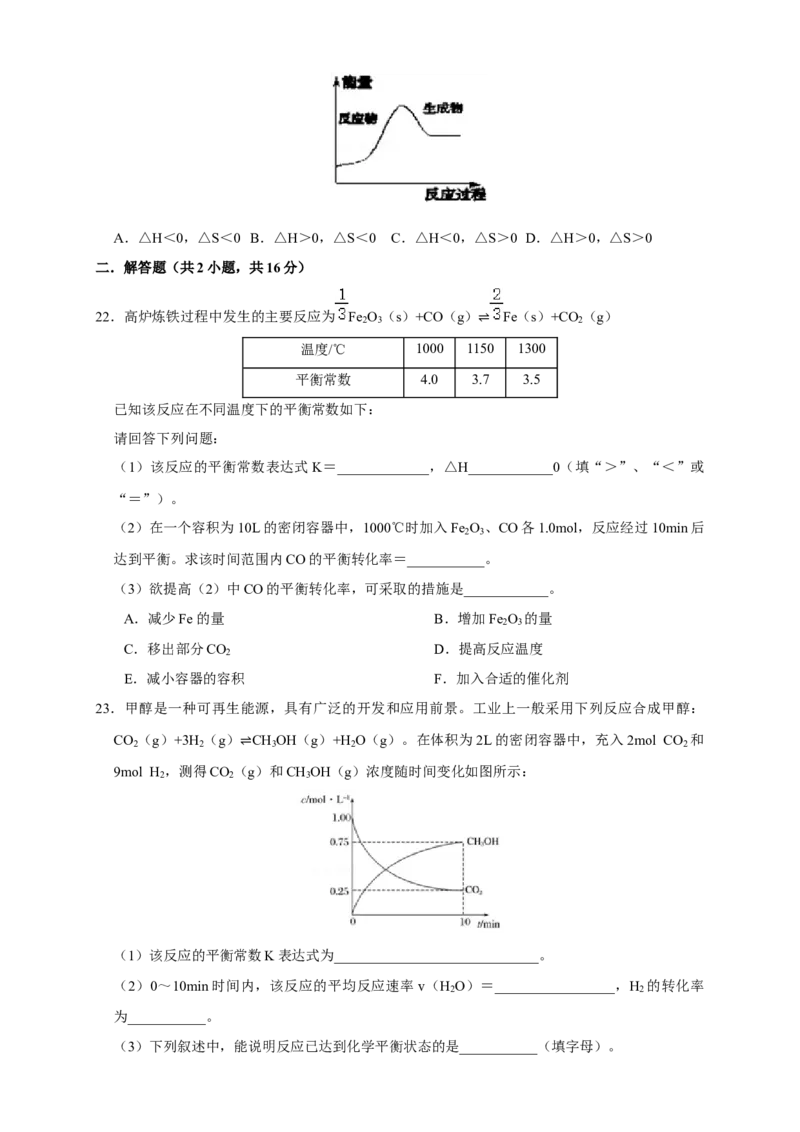
21.金属锡的冶炼常用焦炭作还原剂:SnO (s)+2C(s)═Sn(s)+2CO(g)↑,
2
反应过程中能量的变化如图所示.下列有关该反应的△H、△S的说法中正确的是( )A.△H<0,△S<0 B.△H>0,△S<0 C.△H<0,△S>0 D.△H>0,△S>0
二.解答题(共2小题,共16分)
22.高炉炼铁过程中发生的主要反应为 Fe O (s)+CO(g) Fe(s)+CO (g)
2 3 2
温度/℃ 1000 11⇌50 1300
平衡常数 4.0 3.7 3.5
已知该反应在不同温度下的平衡常数如下:
请回答下列问题:
(1)该反应的平衡常数表达式K=_____________,△H____________0(填“>”、“<”或
“=”)。
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe O 、CO各1.0mol,反应经过10min后
2 3
达到平衡。求该时间范围内CO的平衡转化率=___________。
(3)欲提高(2)中CO的平衡转化率,可采取的措施是____________。
A.减少Fe的量 B.增加Fe O 的量
2 3
C.移出部分CO D.提高反应温度
2
E.减小容器的容积 F.加入合适的催化剂
23.甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列反应合成甲醇:
CO (g)+3H (g) CH OH(g)+H O(g)。在体积为2L的密闭容器中,充入2mol CO 和
2 2 3 2 2
9mol H ,测得CO (⇌g)和CH OH(g)浓度随时间变化如图所示:
2 2 3
(1)该反应的平衡常数K表达式为_____________________________。
(2)0~10min时间内,该反应的平均反应速率v(H O)=_________________,H 的转化率
2 2
为___________。
(3)下列叙述中,能说明反应已达到化学平衡状态的是___________(填字母)。A.容器内CO 、H 、CH OH、H O(g)的浓度之比为1:3:1:1
2 2 3 2
B.v正 (CO
2
):v逆 (H
2
)=1:3
C.平衡常数K保持不变
D.混合气体的平均相对分子质量保持不变