文档内容
课题 2 二氧化碳制取的研究
答案:
(1)CaCO+2HCl===CaCl+HO+CO↑ (2)将生成的气体通入澄清石灰水,若石灰水变
3 2 2 2
浑浊,证明气体是二氧化碳 (3)口 (4)熄灭 (5)反应物的状态 (6)反应条件 (7)密度
(8)是否溶于水,是否与水反应
1.实验室制取二氧化碳的反应原理
(1)药品
大理石(或石灰石)和稀盐酸
大理石或石灰石的主要成分是碳酸钙,化学式是CaCO。
3
(2)反应原理
CaCO+2HCl===CaCl+HCO
3 2 2 3
碳酸钙 氯化钙 碳酸
碳酸不稳定,容易分解生成二氧化碳和水。
HCO===HO+CO↑
2 3 2 2
总的化学方程式是:
CaCO+2HCl===CaCl+HO+CO↑
3 2 2 2
释疑点 实验室制取CO 时不用稀硫酸、浓盐酸的原因 ①实验室制取二氧化碳不用稀
2
硫酸,因为稀硫酸与石灰石反应生成的硫酸钙微溶于水,覆盖在石灰石表面,阻碍石灰石与
硫酸接触,使反应中断。②不用浓盐酸。浓盐酸易挥发出氯化氢气体,导致二氧化碳不纯。
【例1】在实验室里制取二氧化碳气体,可选择的药品是( )
A.碳酸钠粉末与浓盐酸
B.块状石灰石与稀硫酸
C.石灰石
D.块状大理石和稀盐酸
解析:
A × 碳酸钠粉末与浓盐酸反应过快,且浓盐酸易挥发,碳酸钠价格贵
B × 不能用稀硫酸,因为反应生成的硫酸钙会阻止反应继续进行
C × 高温分解石灰石是二氧化碳的工业制法
D √ 反应速率适中,易于操作和收集,是合适的药品
答案:D
2.制取气体的一般思路
(1)制取装置的选择
实验室制取气体的装置包括发生装置和收集装置。发生装置主要由反应物的状态、反应
条件决定,收集装置主要考虑生成气体的物理性质(溶解性、密度大小)。
(2)发生装置的选择
装置 反应类型 反应条件 举例
固体+固 KMnO
加热 4
体(加热)型 制O
2
1固体+液 HO 制O,
不加热 2 2 2
体(常温)型 制CO
2
(3)收集装置的选择
装置 收集方法 气体性质 举例
排水法 不易溶于水,不与水反应 O、H
2 2
向上排
密度比空气大,不与空气反应 O、CO
空气法 2 2
向下排
密度比空气小,不与空气反应 H
空气法 2
点技巧 判断气体的密度比空气的大还是小的方法 空气的平均相对分子质量为29。
如果某气体的相对分子质量大于29,则这种气体的密度比空气大;如果小于29,则密度比空
气小。
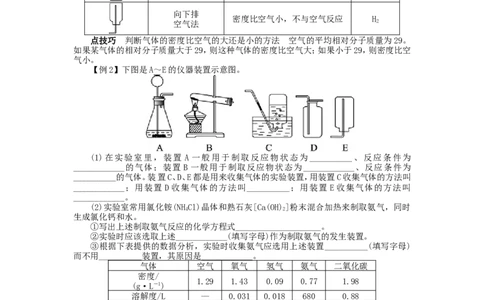
【例2】下图是A~E的仪器装置示意图。
(1)在实验室里,装置 A 一般用于制取反应物状态为__________、反应条件为
____________的气体;装置 B 一般用于制取反应物状态为____________、反应条件为
__________的气体。装置C、D、E都是用来收集气体的实验装置,用装置C收集气体的方法叫
____________;用装置 D 收集气体的方法叫__________;用装置 E 收集气体的方法叫
____________。
(2)实验室常用氯化铵(NHCl)晶体和熟石灰[Ca(OH)]粉末混合加热来制取氨气,同时
4 2
生成氯化钙和水。
①写出上述制取氨气反应的化学方程式____________________。
②实验时应该选取上述____________(填写字母)作为制取氨气的发生装置。
③根据下表提供的数据分析,实验时收集氨气应选用上述装置__________(填写字母)
而不用__________装置,其原因是____________。
气体 空气 氧气 氢气 氨气 二氧化碳
密度/
1.29 1.43 0.09 0.77 1.98
(g·L-1)
溶解度/L — 0.031 0.018 680 0.88
解析:实验室制取氨气,是用氯化铵晶体和熟石灰粉末混合后加热制取,故选装置B制
气。从题给的数据分析,氨气极易溶于水,1 L水可以溶解680 L氨气,故不能用排水集气法;
氨气的密度小于空气的密度,故可用向下排空气集气法来收集。
答案:(1)固态和液态 常温 固态和固态 加热 排水集气法 向上排空气集气法
向下排空气集气法 (2)①2NHCl+Ca(OH)=====2NH↑+2HO+CaCl ②B ③E C和D
4 2 3 2 2
氨气的密度比空气的密度小,而且氨气极易溶于水
3.实验室制取二氧化碳
(1)发生装置:实验室制取二氧化碳是固体和液体反应,不需加热,因此可任意选择下列
发生装置:
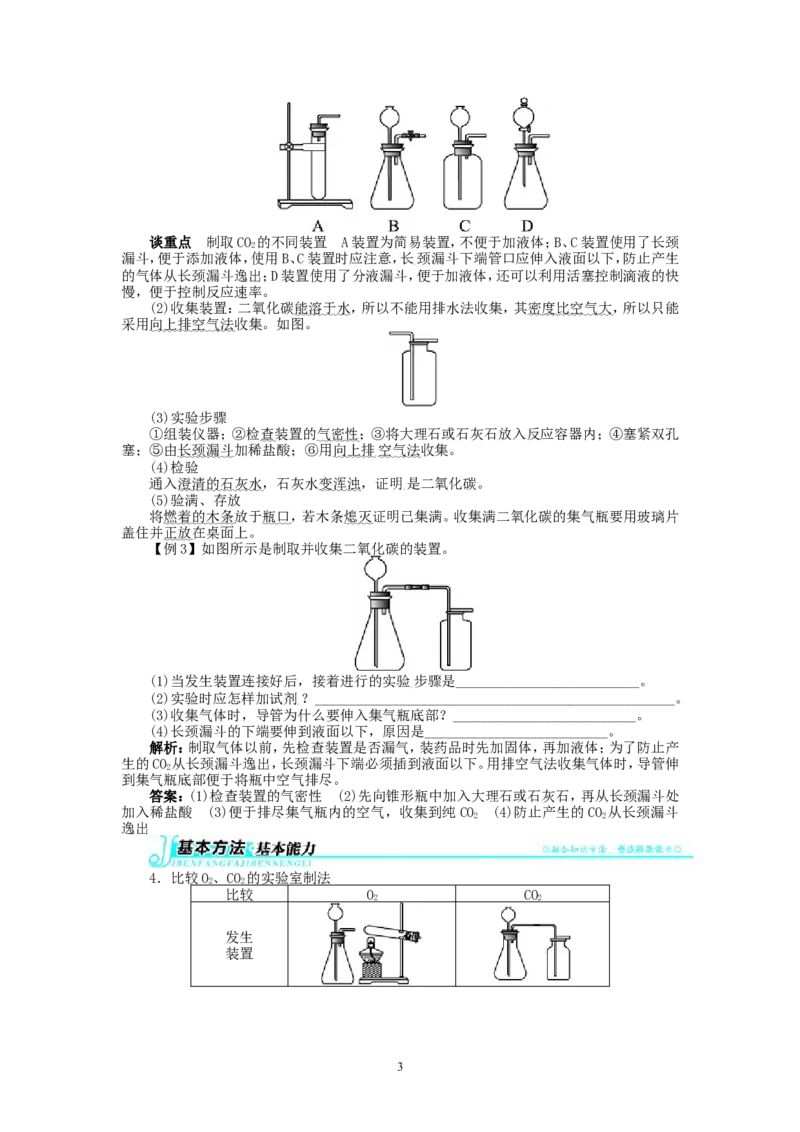
2谈重点 制取CO 的不同装置 A装置为简易装置,不便于加液体;B、C装置使用了长颈
2
漏斗,便于添加液体,使用B、C装置时应注意,长颈漏斗下端管口应伸入液面以下,防止产生
的气体从长颈漏斗逸出;D装置使用了分液漏斗,便于加液体,还可以利用活塞控制滴液的快
慢,便于控制反应速率。
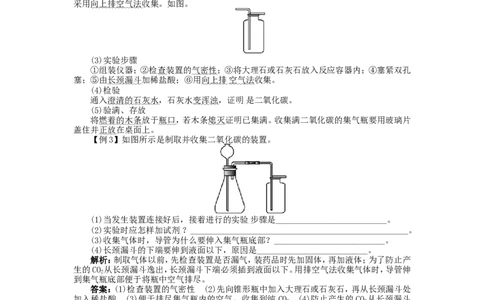
(2)收集装置:二氧化碳能溶于水,所以不能用排水法收集,其密度比空气大,所以只能
采用向上排空气法收集。如图。
(3)实验步骤
①组装仪器;②检查装置的气密性;③将大理石或石灰石放入反应容器内;④塞紧双孔
塞;⑤由长颈漏斗加稀盐酸;⑥用向上排空气法收集。
(4)检验
通入澄清的石灰水,石灰水变浑浊,证明是二氧化碳。
(5)验满、存放
将燃着的木条放于瓶口,若木条熄灭证明已集满。收集满二氧化碳的集气瓶要用玻璃片
盖住并正放在桌面上。
【例3】如图所示是制取并收集二氧化碳的装置。
(1)当发生装置连接好后,接着进行的实验步骤是__________________________。
(2)实验时应怎样加试剂?___________________________________________________。
(3)收集气体时,导管为什么要伸入集气瓶底部?__________________________。
(4)长颈漏斗的下端要伸到液面以下,原因是__________________________。
解析:制取气体以前,先检查装置是否漏气,装药品时先加固体,再加液体;为了防止产
生的CO 从长颈漏斗逸出,长颈漏斗下端必须插到液面以下。用排空气法收集气体时,导管伸
2
到集气瓶底部便于将瓶中空气排尽。
答案:(1)检查装置的气密性 (2)先向锥形瓶中加入大理石或石灰石,再从长颈漏斗处
加入稀盐酸 (3)便于排尽集气瓶内的空气,收集到纯CO (4)防止产生的CO 从长颈漏斗
2 2
逸出
4.比较O、CO 的实验室制法
2 2
比较 O CO
2 2
发生
装置
3收集
装置
实验 药品① 药品②
原理 方程式③ 方程式④
检验
带火星的木条放入瓶内 通入澄清石灰水
方法
验满
带火星的木条放在瓶口 燃着的木条放在瓶口
方法
注:①:过氧化氢与二氧化锰;
高锰酸钾;氯酸钾与二氧化锰
②石灰石(或大理石)与稀盐酸
③2KClO=====2KCl+3O↑;
3 2
2KMnO=====KMnO+MnO+O↑;
4 2 4 2 2
2HO=====2HO+O↑
2 2 2 2
④CaCO+2HCl===CaCl+HO+CO↑
3 2 2 2
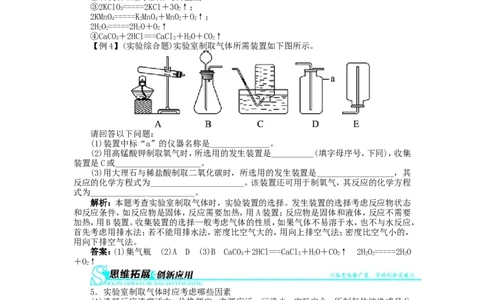
【例4】(实验综合题)实验室制取气体所需装置如下图所示。
请回答以下问题:
(1)装置中标“a”的仪器名称是______________。
(2)用高锰酸钾制取氧气时,所选用的发生装置是__________(填字母序号,下同),收集
装置是C或____________________。
(3)用大理石与稀盐酸制取二氧化碳时,所选用的发生装置是__________________,其
反应的化学方程式为______________________。该装置还可用于制氧气,其反应的化学方程
式为________________________。
解析:本题考查实验室制取气体时,实验装置的选择。发生装置的选择考虑反应物状态
和反应条件,如反应物是固体,反应需要加热,用A装置;反应物是固体和液体,反应不需要
加热,用B装置。收集装置的选择一般考虑气体的性质,如果气体不易溶于水,也不与水反应,
首先考虑用排水法;若不能用排水法,密度比空气大的,用向上排空气法;密度比空气小的,
用向下排空气法。
答案:(1)集气瓶 (2)A D (3)B CaCO+2HCl===CaCl+HO+CO↑ 2HO=====2HO
3 2 2 2 2 2 2
+O↑
2
5.实验室制取气体时应考虑哪些因素
(1)选择反应速度适中、价格便宜、来源广泛、污染少、实验安全,所制气体纯净或易分
离的药品。例如,实验室制取二氧化碳时,不用浓盐酸制取,因易挥发;不用碳酸钠制取,因其
价格贵且反应太快;不用稀硫酸制取,因其与石灰石反应生成微溶物硫酸钙,使反应难以继
续进行。
(2)选择原理科学、节能、操作简便的反应。例如,高温分解石灰石也能产生二氧化碳,但
需消耗燃料,不节能,且操作麻烦,不适合实验室制取。
【例5】(探究题)下列反应都能生成二氧化碳:
①人和动物的呼吸作用
②木炭在空气中燃烧
③蜡烛燃烧
④碳和氧化铜反应
⑤石灰石(块状)与硫酸
⑥碳酸钙粉末与稀盐酸
⑦石灰石(块状)与浓盐酸
4⑧石灰石(块状)与稀盐酸
其中可用于实验室制CO 的是( )
2
A.⑥⑧ B.⑧
C.⑥⑦⑧ D.①②③④⑤⑥⑦⑧
解析:⑥反应太快,不易收集;⑦用浓盐酸制取,得到的二氧化碳不纯,混有从发生装置
中挥发出来的氯化氢气体,故不选A、C、D;⑧反应符合实验室制取气体选用药品的原则,故
选B。
答案:B
5