文档内容
课题1 常见的酸和碱
教学目标:初步了解什么是酸、碱、盐;能完成简单的探究实验。过程与方法:在学习了什么是
酸后,完成对碱的模拟自主探究,运用实验的方法获取信息,运用比较、归纳、概括等方法对
获取的信息进行加工。情感态度与价值观:增强对化学现象的探究欲,发展善于合作,勤于思
考的科学精神。
重点:从离子观点了解什么是酸、碱、盐。
难点:运用酸碱指示剂检验酸溶液和碱溶液。
教学过程:
本课题在知识结构上可分为三部分。
首先,从酸碱指示剂的实验,简单地反映酸和碱能与指示剂反应并显示不同的颜色,从
而说明酸和碱作为不同类物质具有不同的性质,使学生对酸和碱有一些初步的认识。在此基
础上,具体介绍了几种常见酸和碱的性质、用途等,并通过学生总结的方式,简单归纳几种酸
和碱各自相似的化学性质。关于酸和碱的腐蚀性是结合具体物质来介绍的;最后,在学生对
酸和碱的性质有了一些认识以后,通过酸和碱溶液的导电实验,来说明酸和碱为什么会具有
一些共同的性质。
本课题在介绍酸和碱的化学性质时,采用了探究式的写法,目的是使学生能积极参与学
习,能根据学过的知识来主动探究未知,从而对这部分内容有更深的认识。
课题 1 常见的酸和碱 教学建议
1.在介绍常见的酸和碱之前,可以启发学生列举出见过或知道的酸和碱。然后再用指示
剂进行实验,实验用的酸和碱也可根据实际情况选择。
2.关于用植物的花等做指示剂的探究活动,可事先让学生准备一些花或果实;应叮嘱学
生不要随意采摘公共场所等地的花。
3.关于酸和碱的化学性质,有些反应学生已经学过,如酸与金属的反应、氢氧化钙与二
氧化碳的反应、酸碱与指示剂的反应等。教学中可利用教材提供的活动与探究,引导学生回
忆、类推,井指导学生进行简单的归纳和小结。
4.对于酸和碱,教材最初介绍酸类物质和碱类物质对没有给出定义,在介绍酸碱溶液导
电实验后,也没有直接给酸和碱下严格的定义,只是解释酸和碱为什么具有相似的化学性质,
帮助学生认识酸和碱。所以,教学中不要过分强调死记定义,可根据学生的具体情况,从解离
的角度介绍酸和碱的定义,但不宜加深和拓宽。
5.关于酸和碱的通性,课程标准没有作出具体的要求,教材只是以讨论的形式让学生从
学过的几种物质来进行简单归纳,教师可在教学中进行指导,并在课题小结对做适当总结。
[提问]:试管中的紫色石蕊试液,在不借助任何化学药品的情况下,能否使之变成红色学生
演示:向试管中吹气。紫色石蕊试液变成红色。
[追问]:为什么会变色?学生回答:二氧化碳与水反应生成碳酸。
[提问]:除了碳酸,还有其他物质能使紫色石蕊试液变色吗?
探究实验:分别在下表溶液中滴加紫色石蕊试液或酚酞。
加入紫色石蕊试液后溶液的颜 加入无色酚酞试液后溶液的颜色变化
色变化
食醋
石灰水
盐酸
氢氧化钠溶液石蕊和酚酞溶液叫酸碱指示剂,它们能跟酸或碱反应而显示不同颜色,
用花卉或果实加酒精浸泡自制指示剂
自制指示剂 在不同溶液中颜色的变化
食醋 石灰水 盐酸 氢氧化钠溶液
一:常见的酸
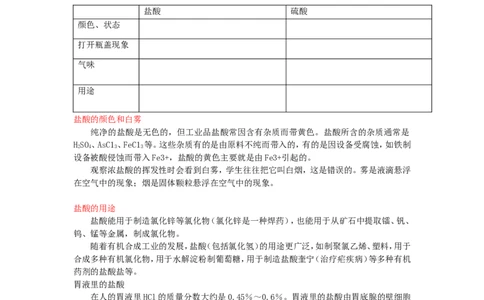
1:观察盐酸、硫酸的物理性质及主要用途
盐酸 硫酸
颜色、状态
打开瓶盖现象
气味
用途
盐酸的颜色和白雾
纯净的盐酸是无色的,但工业品盐酸常因含有杂质而带黄色。盐酸所含的杂质通常是
HSO、AsC1、FeC1 等。这些杂质有的是由原料不纯而带入的,有的是因设备受腐蚀,如铁制
2 4 3 3
设备被酸侵蚀而带入Fe3+,盐酸的黄色主要就是由Fe3+引起的。
观察浓盐酸的挥发性时会看到白雾,学生往往把它叫白烟,这是错误的。雾是液滴悬浮
在空气中的现象;烟是固体颗粒悬浮在空气中的现象。
盐酸的用途
盐酸能用于制造氯化锌等氯化物(氯化锌是一种焊药),也能用于从矿石中提取镭、钒、
钨、锰等金属,制成氯化物。
随着有机合成工业的发展,盐酸(包括氯化氢)的用途更广泛,如制聚氯乙烯、塑料,用于
合成多种有机氯化物,用于水解淀粉制葡萄糖,用于制造盐酸奎宁(治疗疟疾病)等多种有机
药剂的盐酸盐等。
胃液里的盐酸
在人的胃液里HCl的质量分数大约是0.45%~0.6%。胃液里的盐酸由胃底腺的壁细胞
所分泌,它具有以下的功用:
(1)促进胃蛋白酶的作用,使蛋白质容易水解被人体吸收;
(2)使二糖类物质如蔗糖、麦芽糖水解;
(3)杀菌。
硫酸的用途:
硫酸大量用于清洗钢铁的表面。在钢铁进行冷轧、冷拔和冲压等加工之前,必须清除钢铁表
面的氧化铁,否则,在冷轧、冷拔和冲压时氧化铁就可能被压入钢铁中,使钢铁的表面很粗糙,
甚至造成废品。氧化铁的存在也会使轧辊或冲模等工具很快被磨损。在金属表面镀镍或镀铬
时,也要用硫酸清洗金属表面,否则镀层很容易脱落下来。硫酸还是生产化肥的原料。把氨通
入75%硫酸中,可以生成硫酸铵。这个反应放出大量的热,这些热量用来将水分蒸发,便可得到硫酸铵晶体。硫酸铵和尿素都是重要的氮肥。硫酸也是生产过磷酸钙肥料的原料。在石油
精炼中,要用浓硫酸除去汽油和润滑油中的杂质──硫化物和不饱和碳氢化合物,每精炼1t
石油要用24kg浓硫酸。在有机化工中,硫酸是生产农药敌百虫、以及合成洗涤剂烷基苯磺酸
钠的原料。很多基本有机化工原料如甲酸、草酸、柠檬酸、苯酚、乙酸乙酯也要用硫酸做原料
在无机化工生产中,硫酸用于生产氢氟酸、铬酸、磷酸、硫酸铜、硫酸铝、硫酸锌、硫酸镍以及
钛白粉、立德粉等颜料。总而言之,在肥料、冶金、石油精炼、农药、炸药、纺织、染料、塑料、油
漆、电池、制革、颜料、药品和洗涤剂等工业中,处处都离不开硫酸。
浓硫酸的吸水性
浓硫酸具有吸水性,是由于它能跟水结合生成不同组成的水合物,同时放出热。硫酸的
水合物有HSO·HO、HSO·2HO、HSO·4HO等,当降低硫酸溶液的温度时,这些水合物便
2 4 2 2 4 2 2 4 2
以晶体形式析出。
稀释浓硫酸时会放出大量的热,正是由于硫酸跟水结合形成水合物时放出的热量多于
它的分子扩散时所吸收的热量之故。
浓硫酸的脱水性
浓硫酸能使蔗糖、淀粉、纤维素等物质失水碳化,并不是因为浓硫酸吸取了有机物内部
所含有的水分(结晶水),而是把组成有机物成分里的氢、氧元素的原子按2:1的比率(水的
组成比)从有机物里夺取出来,形成硫酸的水合物,同时剩下有机物组成中的碳。对浓硫酸来
说,它起了脱水作用,对有机物来说,则发生了碳化现象。
浓硫酸的氧化性
在浓硫酸中,硫酸大都是以分子状态存在的。分子中两个氢原子的半径很小,极化能力
很强,很容易钻入硫酸根内部,它们对氧有较强的极化作用,削弱了硫和氧之间的作用,从而
大大减弱硫酸根的稳定性。所以硫易被还原,浓硫酸有氧化性。这种氧化性是未电离的硫酸
分子的特征。稀硫酸中的硫元素不表现氧化性,这是由于硫酸溶于水后完全电离,硫元素完
全是以SO2-形式存在的,SO2-的空间构型近似为正四面体,而且硫原子居于正四面体的中心,
4 4
2个单位的负电荷属于整个SO2-。这样对称的结构不易受外界作用而极化,所以性质稳定。
4
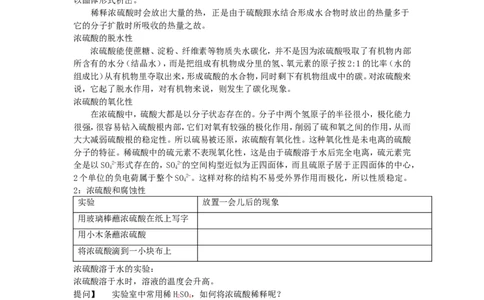
2:浓硫酸和腐蚀性
实验 放置一会儿后的现象
用玻璃棒蘸浓硫酸在纸上写字
用小木条蘸浓硫酸
将浓硫酸滴到一小块布上
浓硫酸溶于水的实验:
浓硫酸溶于水时,溶液的温度会升高。
提问】 实验室中常用稀HSO,如何将浓硫酸稀释呢?
2 4
【演示】 实验“稀释浓硫酸”(可请同学用手接触烧杯外壁)。
[讲解] 浓HSO 溶于水放出大量热。
2 4
【提问】 为什么切不可将水倒入浓HSO 中?(请同学参考课有关内容回答)
2 4
【板书】 浓HSO 的稀释:酸入水、沿内壁、慢慢搅动。
2 4
【提问】浓硫酸为什么可做干燥剂?如果不慎在皮肤或衣服上沾上浓硫酸应如何处理?
3:酸的化学性质:
加入物质 稀盐酸中发生的现象和反应式 稀硫酸中发生的现象和反应式
滴入紫色石蕊试液
滴入无色酚酞试液镁 现象 现象
反应式 反应式
铝 现象 现象
反应式 反应式
锌 现象 现象
反应式 反应式
铁 现象 现象
反应式 反应式
铁锈 现象 现象
反应式 反应式
氧化铜 现象 现象
反应式 反应式
盐酸和硫酸的检验
检验盐酸和电离时产生Cl-的化合物的试剂是AgNO 溶液和硝酸溶液。其反应原理可用下列
3
化学方程式表示
HCl+AgNO=AgCl↓+HNO NaCl+AgNO=AgCl↓+NaNO
3 3 3 3
两个反应中生成的AgCl是既不溶于水又不溶于硝酸的白色沉淀
若给某一溶液中加入AgNO 溶液后,得到白色沉淀,再给其中加入硝酸溶液,此白色沉淀又不
3
溶解,则该溶液中一定会有Cl-离子,该溶液不是盐酸就是电离时能产生Cl-的化合物溶液检
验硫酸或电离时产生SO2-的化合物的试剂是BaCl[或Ba(NO) 或Ba(OH)]溶液和硝酸。
4 2 3 2 2
其反应原理可用下列化学方程式表示:
HSO+BaCl=BaSO↓+2HNO NaSO+BaCl=BaSO↓+2NaCl
2 4 2 4 3 2 4 2 4
两个反应中生成的BaSO 是既不溶于水又不溶于硝酸的白色沉淀。
4
其实用这样的方法只能检验出SO2-离子,但还不能确定溶液一定就是硫酸溶液,要进一步确
4
定是否是硫酸溶液,还要检验H+是否存在。检验H+可用石蕊试液。另取试样溶液,加入石蕊试
液后溶液变红,即可证明是硫酸溶液
[小结过渡]:碳酸、稀盐酸、稀硫酸都能使紫色石蕊试液变红色,它们还有其他的共性吗?探
究实验:稀盐酸、稀硫酸与锌粒及氧化铜粉末的反应。[小结过渡]:稀盐酸、稀硫酸都能与锌
粒及氧化铜粉末反应,由此可见,它们在性质上是有了些共性的。为什么它们会具有一些相
似的性质呢?探究实验:氯化钠导电性实验。[提问]:氯化钠溶液为什么会导电?回忆物理
中学习的导电的原理,推测氯化钠溶液导电的原因。
酸的通性:酸有相似化学性质的原因:
a:酸溶液能跟酸碱指示剂起反应。
酸能使 色石蕊试液变 色, 色酚酞试液 色
b:酸能跟多种活泼金属起反应,通常生成盐和氢气。金属+硫酸 盐+氢气(置换反应)
Zn+HSO-- Fe+HCl—
2 4
金属活动性顺序(要背熟)排在氢前面的
c:酸能跟某些金属氧化物(碱性氧化物)起反应,生成盐和水。
金属氧化物+硫酸 盐+水(复分解反应)
FeO+HSO-- CuO + HCl---
2 3 2 4
碱性氧化物:
d:酸能跟某些盐起反应,生成另一种酸和另一种盐。
NaCO+HSO-- HCl + MgCO -
2 3 2 4 3
碱+硫酸 盐+水(复分解反应)e:酸能跟碱起中和反应反应,生成盐和水。
H SO + NaOH - HSO + Cu(OH)-
2 4 2 4 2
日常生活里的酸
人们在购买葡萄、柑桔等水果时,常习惯地问问“酸不酸?”的确,许多未成熟的水果是很
酸的,这是因为它含有许多有机酸,如苹果酸、琥珀酸、柠檬酸、酒石酸等。随着水果的成熟,
有些酸会逐渐分解,酸味也就随之减轻。有的同学说:“新摘下来的柿子并不酸,倒是涩得舌
头发麻。”其实,这也是酸在作怪,这种酸叫鞣酸。可见,酸不一定都有酸味。我们判定一种物
质是不是属于酸类,主要是看它的组成和性质。酸也不一定都是液态。例如上面说的鞣酸是
淡黄色粉末,硅酸则像白色浆糊,硼酸是白色小片,硬脂酸类似石蜡,纯净的醋酸能形成冰块
一样的晶体,故称“冰醋酸”。苦味酸有苦味,甘氨酸、水杨酸有甜味,羊肉的膻气则是挥发
性很强的癸酸引起的……。生活中遇到的酸很多。比如食醋,因含有乙酸(俗称醋酸)而具有
酸味。醋是常用的调味品。做鱼时,放点儿黄酒和醋,能解鱼腥,味道也更鲜美。烧菜时放点醋,
可以使维生素C不受或少受破坏。吃凉拌菜时放点醋,既可调味,又能杀菌;同时还可降低致
癌物亚硝酸盐的含量。用浸过醋的布将肉包起来,可使鲜肉不易变质。夏天多吃点醋,有预防
肠道传染病的作用。把醋煮沸喷洒在房间中,可以预防感冒。据记载,有一个生产醋的工厂,
几十年来只有一两个工人患感冒,原因是车间里的醋酸蒸气保护了工人们的身体健康。日常
生活中另一种重要的酸是乳酸。面团发酵时能产生乳酸,加点儿碱(NaCO)或起子(NaHCO),
2 3 3
能中和掉乳酸,并产生二氧化碳气体。二氧化碳从面团里钻出来,留下许多小窟窿,使面团蓬
松胀大。这就是蒸馒头、烤面包的道理。许多人喜欢吃酸奶、酸菜、泡菜,也都要靠乳酸帮忙。
久不活动,偶尔参加一次体力劳动或剧烈运动,常感到腰酸腿疼,这就是因为肌肉中的葡萄
糖在新陈代谢中分解成了乳酸,剧烈的活动使肌肉里蓄积了较多的乳酸,故有酸痛之感。酸
跟人们的日常生活息息相关。制汽水时加点儿柠檬酸,能起到利尿作用。鸡汤的味道既鲜美,
又富有营养,因为里面含有丰富的氨基酸。草酸能帮助你洗掉衣服上的蓝墨水或铁锈。蚊子、
蚂蚁叮咬了人的皮肤,因分泌了少量甲酸而使人发痒。口腔里的细菌能产生酸性物质,腐蚀
牙齿,造成龋洞。而胃液里极稀的盐酸又有帮助消化和杀灭细菌的作用,但当胃酸过多时,它
又使人“烧心”和“返酸水”。总之,日常生活中能接触到各种各样的酸。它们的性质不同,
形态各异,有的造福人类,有的也危及人体健康。只有充分认识它们的特性,才能扬长避短,
化害为利。
为什么通常用铁桶盛装和运输浓硫酸
浓硫酸的化学性质和稀硫酸不一样,它具有强氧化性、吸水性和脱水性。吸水性是指浓硫酸
极易吸收水分,所以可用来作为某些气体的干燥剂。脱水性是指浓硫酸将某些含碳、氢、氧元
素的化合物按个数比2:1将氢氧元素脱去(可认为脱H2O)。强氧化性是指金属和浓硫酸反应
时不能置换出氢气,而是生成二氧化硫和水等。铁和浓硫酸在常温下接触时,在表面反应形
成一层致密的氧化物保护膜,防止浓硫酸继续和铁反应,故常用铁桶来运装浓酸酸。实际上,
铁和浓硫酸在加热的条件下反应速度较快。反应方程式为:
2Fe+6HSO(浓) Fe(SO)+2SO↑+6HO
2 4 2 4 3 2 2
盐酸
盐酸是氯化氢气体溶于水生成的酸。在工业上,曾经用氯化钠和浓硫酸作用来生产盐酸。
这种方法不但产量低,而且用浓硫酸制取浓盐酸也是不太经济的。因此,从19世纪开始,便
建立了电解氯化钠水溶液的工厂。在电解时,阳极上产生氯气,阴极上产生氢气。把氯气和氢
气混合起来,便产生氯化氢气体。把氯化氢气体溶解在水中,就可制造盐酸。电解时还产生有
用的氢氧化钠,所以这是一种大规模生产盐酸的方法。盐酸也是一种强酸,是无色透明的液
体,工业产品中因为含有氯化铁和氯气而带黄色。盐酸中所含的氯化氢容易挥发,当氯化氢气体挥发后遇到空气中的水蒸气时,就会结合成盐酸小液滴而形成酸雾。因此,打开盛盐酸
的玻璃瓶的瓶盖时,会冒白烟,而且有强烈的刺激性气味。盐酸的用处不比硫酸少,例如用锡
进行焊接时,也要在焊接处涂点焊药,焊锡才能牢固地把金属焊住。把锌片溶解在稀盐酸里,
便生成了氯化锌和稀盐酸溶液,它便是最简单的焊药。把焊药涂在要焊接的地方,焊药便与
金属表面的锈层(金属氧化物)相互作用,生成溶解于水的氯化物,这样就把锈层除去,金属
表面被清理干净,保证焊锡和金属表面牢固地结合在一起。盐酸能使木材变成葡萄糖。木材
由纤维素、半纤维素和木质素构成。纤维素是由千万个葡萄糖基用“氧桥”连接而成的物质。
如果能找到一把“剪刀”,把“氧桥”剪断,葡萄糖基便会和水结合,生成葡萄糖。这个反应
叫做水解反应,盐酸便是剪断“氧桥”的“剪刀”。于是工业上可以用木屑和盐酸制造葡萄
糖,进一步还可以通过葡萄糖发酵,分解为酒精和二氧化碳,这种方法可以大大节约粮食。在
人体内的胃液里也含有一定量的盐酸,叫做胃酸,它能促进食物消化,并能杀死某些病菌。如
果人喝水太多,就会把胃酸冲淡,减弱了杀菌能力,这时病菌侵入人体,就有可能患病。如果
胃酸过多,就容易得胃痛病。
硫酸
最早制得的酸和被古代利用的酸大概要算醋了。古人利用空气将发酵的水果汁(实际
上就是一种果子酒)氧化来制造醋,即酒被氧化便得到了醋。不过这种醋不是纯的醋酸,而是
一种不纯的很稀的醋酸溶液。现在,醋酸并不是最重要的酸,最有用的是硫酸、盐酸和硝酸。
实验室一般用石蕊试纸检验酸的存在,酸能将试纸由蓝色变为红色。古时候制造硫酸的方法
是,将硫酸铁放在蒸馏器中蒸馏,得到一种油状物的产品,就是硫酸。随着对硫酸需要量的增
加,开始用铅室法生产硫酸。所用的原料是硫铁矿,让硫铁矿在铅室中燃烧,与空气反应生成
二氧化硫,再用一氧化氮做催化剂(能改变化学反应速率而本身的量和化学性质并不改变的
物质),使二氧化硫转化为三氧化硫,三氧化硫溶于水生成硫酸。由于铅不与硫酸发生反应,
因此铅不会被腐蚀,所以当时考虑用铅室做反应器。但是生产中所用的铅室很大,需要用很
多金属铅建造,成本很高,而且产品硫酸的溶质的质量分数只有82%,不是浓硫酸溶质的质量
分数98%,因此铅室法不久就彼淘汰了。现在生产硫酸的方法是接触法,原料仍然是硫铁矿。
将硫铁矿在空气中氧化生成二氧化硫,再用五氧化二钒、氧化铁和氧化亚铜做催化剂,将二
氧化硫氧化为三氧化硫,三氧化硫与水反应生成硫酸。所得的硫酸为98%,称为浓硫酸。浓硫
酸是一种强酸,是无色透明的液体,具有很强的腐蚀性。如果不小心将浓硫酸溅到衣服上,它
会立即使衣服的纤维素碳化,在衣服上出现小洞。浓硫酸有很强的脱水性,把它加到白糖中,
糖中的氢原子和氧原子按2∶1的比例(水分子的组成比)脱掉,剩下的是黑色的炭。硫酸大
量用于清洗钢铁的表面。在钢铁进行冷轧、冷拔和冲压等加工之前,必须清除钢铁表面的氧
化铁,否则,在冷轧、冷拔和冲压时氧化铁就可能被压入钢铁中,使钢铁的表面很粗糙,甚至
造成废品。氧化铁的存在也会使轧辊或冲模等工具很快被磨损。在金属表面镀镍或镀铬时,
也要用硫酸清洗金属表面,否则镀层很容易脱落下来。硫酸还是生产化肥的原料。把氨通入
75%硫酸中,可以生成硫酸铵。这个反应放出大量的热,这些热量用来将水分蒸发,便可得到
硫酸铵晶体。硫酸铵和尿素都是重要的氮肥。硫酸也是生产过磷酸钙肥料的原料。在石油精
炼中,要用浓硫酸除去汽油和润滑油中的杂质──硫化物和不饱和碳氢化合物,每精炼 1t
石油要用24kg浓硫酸。在有机化工中,硫酸是生产农药敌百虫、以及合成洗涤剂烷基苯磺酸
钠的原料。很多基本有机化工原料如甲酸、草酸、柠檬酸、苯酚、乙酸乙酯也要用硫酸做原料。
在无机化工生产中,硫酸用于生产氢氟酸、铬酸、磷酸、硫酸铜、硫酸铝、硫酸锌、硫酸镍以及
钛白粉、立德粉等颜料。总而言之,在肥料、冶金、石油精炼、农药、炸药、纺织、染料、塑料、油
漆、电池、制革、颜料、药品和洗涤剂等工业中,处处都离不开硫酸。
干燥剂
能除去物质(固体、液体、气体)中水分的物质称为干燥剂。实验室中干燥气体常用的干燥剂有无水氯化钙、氧化钙、五氧化二磷、碱石灰、浓硫酸、分子筛等,适合干燥有机化合物的干燥
剂除上所述,还有无水硫酸钙、无水硫酸铜,无水硫酸镁、无水硫酸钠等。对干燥剂的要求有:
(1)和被干燥物质不发生任何化学反应,例如酸性物质不能用碱性干燥剂,碱性物质不能用
酸性干燥剂。
(2)干燥速度快,干燥力强。
(3)不溶于被干燥的液体中,例如固体氢氧化钠能溶解于低级醇中。
(4)对有机溶质或溶剂无催化作用,例如强碱性干燥剂氧化钙、氢氧化钠能催化某些醛类或
酮类发生缩合、自动氧化等反应。
(5)价格经济,以少量干燥剂即可干燥大量物质。
二:常见的碱:
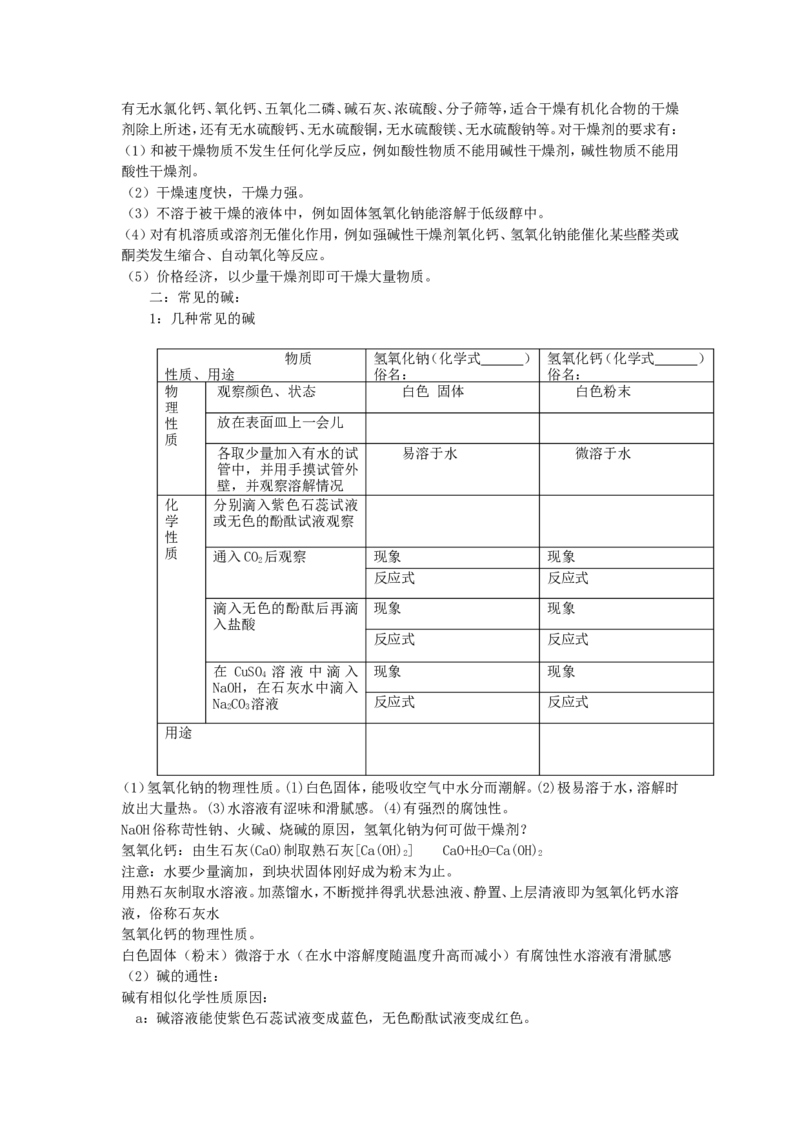
1:几种常见的碱
物质 氢氧化钠(化学式 ) 氢氧化钙(化学式 )
性质、用途 俗名: 俗名:
物 观察颜色、状态 白色 固体 白色粉末
理
性 放在表面皿上一会儿
质
各取少量加入有水的试 易溶于水 微溶于水
管中,并用手摸试管外
壁,并观察溶解情况
化 分别滴入紫色石蕊试液
学 或无色的酚酞试液观察
性
质 通入CO 后观察 现象 现象
2
反应式 反应式
滴入无色的酚酞后再滴 现象 现象
入盐酸
反应式 反应式
在 CuSO 溶液中 滴入 现象 现象
4
NaOH,在石灰水中滴入
NaCO 溶液 反应式 反应式
2 3
用途
(1)氢氧化钠的物理性质。(l)白色固体,能吸收空气中水分而潮解。(2)极易溶于水,溶解时
放出大量热。(3)水溶液有涩味和滑腻感。(4)有强烈的腐蚀性。
NaOH俗称苛性钠、火碱、烧碱的原因,氢氧化钠为何可做干燥剂?
氢氧化钙:由生石灰(CaO)制取熟石灰[Ca(OH)] CaO+HO=Ca(OH)
2 2 2
注意:水要少量滴加,到块状固体刚好成为粉末为止。
用熟石灰制取水溶液。加蒸馏水,不断搅拌得乳状悬浊液、静置、上层清液即为氢氧化钙水溶
液,俗称石灰水
氢氧化钙的物理性质。
白色固体(粉末)微溶于水(在水中溶解度随温度升高而减小)有腐蚀性水溶液有滑腻感
(2)碱的通性:
碱有相似化学性质原因:
a:碱溶液能使紫色石蕊试液变成蓝色,无色酚酞试液变成红色。b:碱和非金属氧化物(酸性氧化物)反应,生成 Ca(OH)+CO
2 2
- 2NaOH+CO- 2NaOH+SO -
2 2
酸性氧化物: c:
碱和酸发生中和反应,生成 2NaOH+HSO-
2 4
Ca(OH)+2HNO-
2 3
d:碱与某些盐反应,生成 注意:两种反应物必须是溶液,生成物必
须要有一种是难溶的。如:NaOH+CuSO-
4
NaOH+FeCl- Ca(OH)+NaCO-
3 2 2 3
氢氧化钠的用途
(1)制造肥皂。肥皂的主要成分是高级脂肪酸的钠盐,通常用油脂和氢氧化钠为原料经过皂
化反应而制成。
(2)精炼石油。石油产品经硫酸洗涤后还含有一些酸性物质,必须用氢氧化钠溶液洗涤,再经
水洗,才能得到精制产品。
(3)造纸。造纸的原料是木材或草类植物,这些植物里除含纤维素外,还含有相当多的非纤维
素(木质素、树胶等)。加入稀的氢氧化钠溶液可将非纤维素成分溶解而分离,从而制得以纤
维素为主要成分的纸浆。
(4)纺织。人造纤维如人造棉、人造毛、人造丝等,大都是粘胶纤维,它们是用纤维素(如纸
浆)、氢氧化钠、二硫化碳(CS)为原料制成粘胶液,经喷丝、凝结而制得 。
2
(5)印染。棉织品用烧碱溶液处理后,能除去覆盖在棉织品上的蜡质、油脂、淀粉等物质,同
时能增加织物的丝光色泽,使染色更均匀。
用石灰改良土壤
在土壤里,由于有机物在分解过程中会生成有机酸,矿物的风化也可能产生酸性物质。
另外,使用无机肥料如硫酸铵、氯化铵等,也会使土壤呈酸性。施用适量石灰能中和土壤里的
酸性物质,使土壤适合作物生长,并促进微生物的繁殖。土壤中Ca2+增加后,能促使土壤胶体
凝结,有利于形成团粒,同时又可供给植物生长所需的钙素。
氢氧化钠的保存方法
氢氧化钠在保存过程中一定要注意密封。因为氢氧化钠容易潮解,更重要的是氢氧化钠
容易跟空气中的二氧化碳反应生成碳酸钠和水,这样氢氧化钠就变质了。所以保存固体氢氧
化钠或氢氧化钠溶液都要密封。还要注意存放氢氧化钠溶液的玻璃瓶不能用玻璃塞,因为普
通玻璃的组成中含有较多的二氧化硅,氢氧化钠能和二氧化硅反应:
2NaOH + SiO=NaSiO + HO
2 2 3 2
当水分蒸发后,NaSiO(硅酸钠)能使玻璃瓶与瓶塞牢固地粘连在一起,所以实验室中盛
2 3
放氢氧化钠溶液的试剂瓶都用胶塞或软木塞。
书写碱的化学式应该注意什么
碱是由金属元素和氢氧根所组成。这是书写碱的化学式的依据。其命名是“氢氧化某”
或“氢氧化亚某”。这决定碱的化学式的书写顺序。
具体方法要注意两点:(1)顺序问题:先读的后写;后读的先写。如氢氧化铜,先写金属铜
元素后写氢氧根,氢氧根写成OH,而不能写成HO且符号均为大写。
(2)括号问题:如果碱的组成中有一个氢氧根,则不必用括号,用了不仅多余,而且是错
误。在碱的组成中有两个以上的氢氧根,则必须用括号,如果不用便是错误。如氢氧化钙的化
学式写成Ca(OH)。
2
漂白粉
CaCl 与Ca(ClO) 混合物,有效成分为次氯酸钙Ca(ClO) 有效氯约35%,高级品可达
2 2 270%。是白色粉末,微溶于水,有氯的气味。暴露在空气里会潮解失效。遇水或酒精会分解。
在漂白时因稀酸或二氧化碳的作用,使漂白粉生成次氯酸而氧化掉有色有机物。工业上用熟
石灰吸收氯气制取。用为漂白、消毒和杀菌剂。
主要成分是次氯酸钙Ca(ClO) 和碱式氯化钙CaCl·Ca(OH)·HO。漂白粉的有效成分
2 2 2 2
是Ca(ClO),它水解后产生次氯酸,因此有漂白作用:
2
Ca(ClO)+2HO→Ca(OH)+2HClO 2HClO→2HCl+O
2 2 2 2
HClO+HCl→HO+Cl
2 2
漂白粉可被二氧化碳分解;在潮湿空气中,会逐渐分解,不易保存。漂白粉的有效氯含量
为35%左右。氯气作用于消石灰即得漂白粉。它除作漂白剂外,还可作水的杀菌剂和野外作
业中用于制备氯气。商品名称为漂粉精,高级漂白粉的有效氯含量可达70%,由氯气通入氢
氧化钙溶液制得,主要成分是Ca(ClO),它比普通漂白粉易溶于水,其漂白能力接近纯氯。
2
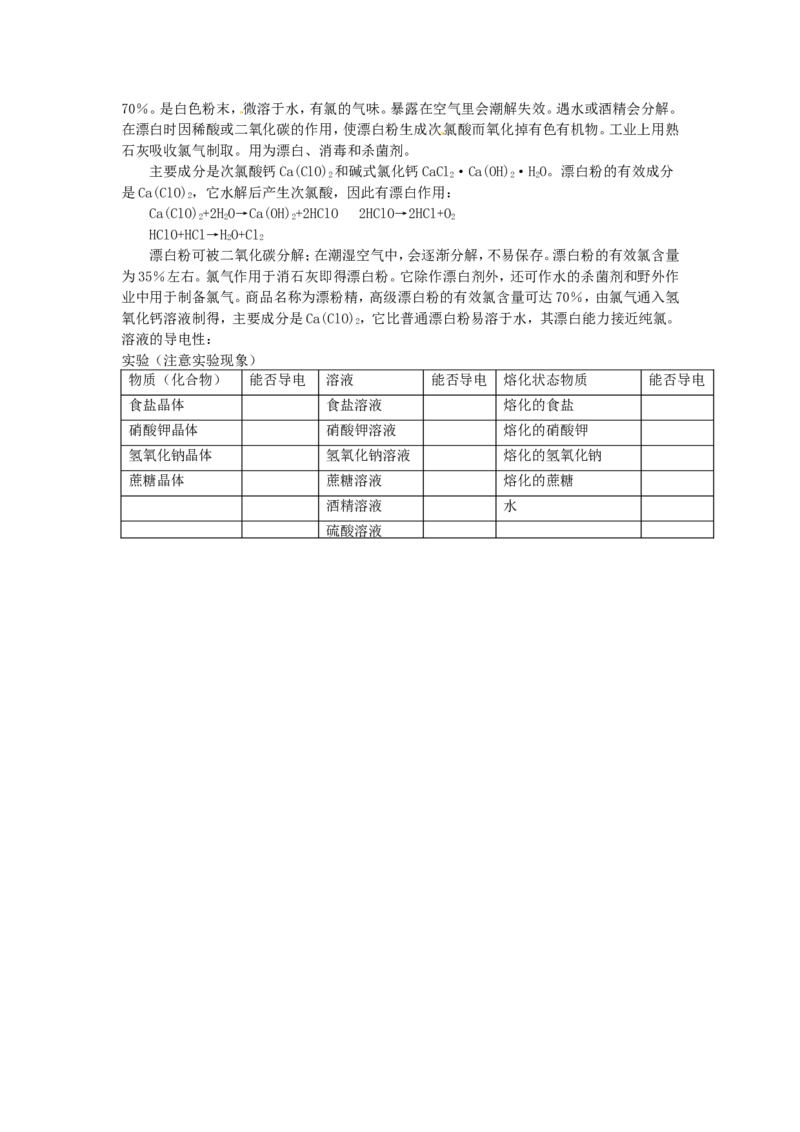
溶液的导电性:
实验(注意实验现象)
物质(化合物) 能否导电 溶液 能否导电 熔化状态物质 能否导电
食盐晶体 食盐溶液 熔化的食盐
硝酸钾晶体 硝酸钾溶液 熔化的硝酸钾
氢氧化钠晶体 氢氧化钠溶液 熔化的氢氧化钠
蔗糖晶体 蔗糖溶液 熔化的蔗糖
酒精溶液 水
硫酸溶液