文档内容
课后达标训练/训练·提升作业
【基础达标】
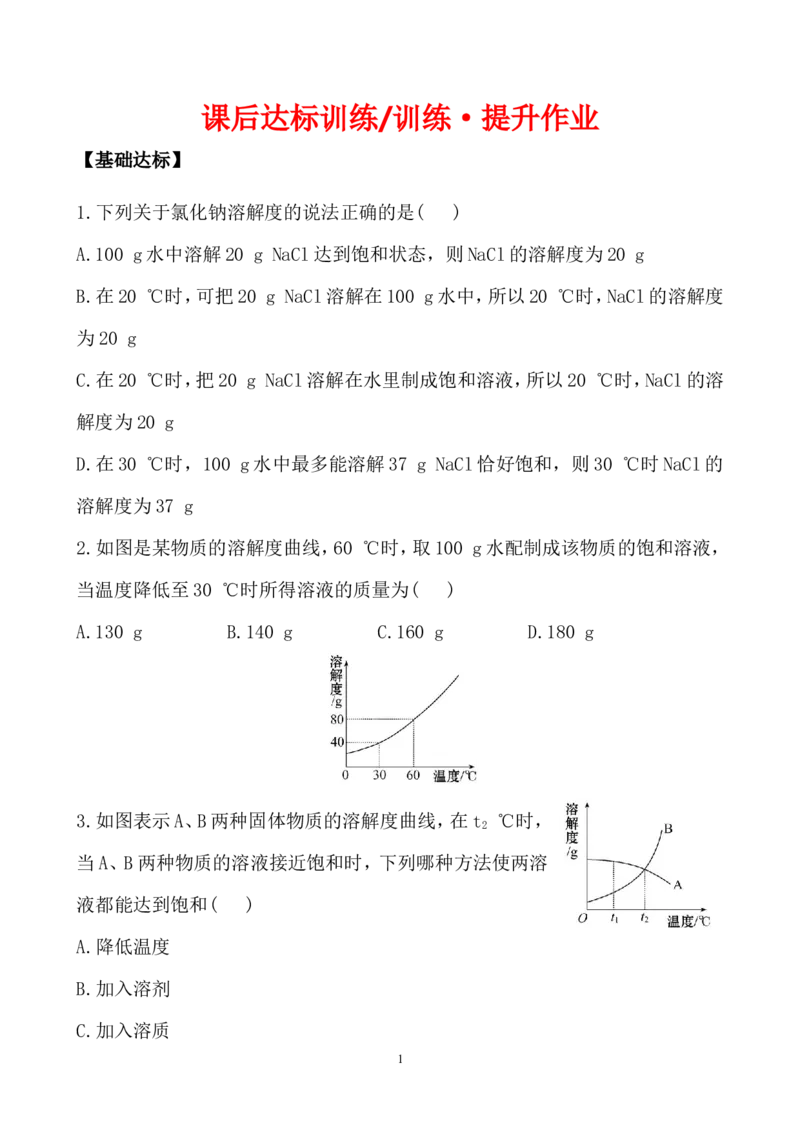
1.下列关于氯化钠溶解度的说法正确的是( )
A.100 g水中溶解20 g NaCl达到饱和状态,则NaCl的溶解度为20 g
B.在20 ℃时,可把20 g NaCl溶解在100 g水中,所以20 ℃时,NaCl的溶解度
为20 g
C.在20 ℃时,把20 g NaCl溶解在水里制成饱和溶液,所以20 ℃时,NaCl的溶
解度为20 g
D.在30 ℃时,100 g水中最多能溶解37 g NaCl恰好饱和,则30 ℃时NaCl的
溶解度为37 g
2.如图是某物质的溶解度曲线,60 ℃时,取100 g水配制成该物质的饱和溶液,
当温度降低至30 ℃时所得溶液的质量为( )
A.130 g B.140 g C.160 g D.180 g
3.如图表示A、B两种固体物质的溶解度曲线,在t ℃时,
2
当A、B两种物质的溶液接近饱和时,下列哪种方法使两溶
液都能达到饱和( )
A.降低温度
B.加入溶剂
C.加入溶质
1D.倒出部分溶液
4.20 ℃时,50 g水中溶解10.48 g物质M恰好达到饱和,则物质M属于( )
A.易溶物质 B.可溶物质
C.微溶物质 D.难溶物质
5.生活中的下列现象不能说明气体溶解度随温度的升高而减小的是( )
A.用水壶烧水时,水沸腾前有气泡逸出
B.喝下汽水感到有气体冲到鼻腔
C.揭开啤酒瓶盖,有大量泡沫溢出
D.夏季,池塘里的鱼常浮出水面
6.氢氧化钙的溶解度随温度升高而减小。要想把一瓶接近饱和的石灰水变成饱
和,具体措施有:①加入氢氧化钙;②升高温度;③降低温度;④加入水;⑤蒸发
水。其中措施正确的是( )
A.①②④ B.①③④ C.①③⑤ D.①②⑤
7.固体物质W在水、乙醇两种溶剂中的溶解度随温度
变化的曲线如图所示。下列说法错误的是( )
A.物质W能溶解在水和乙醇中
B.t ℃时,物质W在水中的溶解度为m g
1
C.t ℃时,物质W在水中与在乙醇中的溶解度相同
2
D.将t ℃时物质W的饱和水溶液升温至t ℃时有晶体析出
1 2
8.甲、乙两物质的溶解度曲线如图所示:
(1)当温度为_________℃时,甲乙两物质的溶解度相等。
(2)欲将t ℃时甲物质的不饱和溶液变为饱和溶液,可
2
2采用的方法是___________________(写出一种即可)。
(3)t ℃时将乙物质的饱和溶液m g,升温到t ℃,所得溶液的质量
1 2
___________(填“>”“<”或“=”)m g。
【知能提升】
1.在30 ℃时,50 g水中最多溶解A物质5 g,在60 ℃时20 g水中最多能溶解
B物质10 g,则( )
A.A的溶解度比B大 B.B的溶解度比A大
C.二者的溶解度相等 D.无法比较
2.如图所示是甲、乙、丙三种固体物质的溶解度曲线。在t
℃时,将甲、乙、丙分别配制成接近饱和的溶液,升高温度
(溶剂不变),可使之变成饱和溶液的是( )
A.只有甲的溶液
B.只有丙的溶液
C.甲、乙的溶液
D.甲、乙、丙的溶液
3.甲、乙两种物质的溶解度曲线如图所示,下列叙述错
误的是( )
A.t ℃时,甲的溶解度小于乙的溶解度
1
B.t ℃时,加入甲物质,可使不饱和的甲溶液变成饱和
1
C.t ℃时,甲或乙两种物质饱和溶液中溶质与溶剂的比是W∶100
2
D.将甲、乙饱和溶液的温度从t ℃降到t ℃时,乙先析出晶体
3 2
34.如图是三种固体物质的溶解度曲线。请你根据曲
线回答下列问题:
(1)氯化钠和硫酸锂在0 ℃时的溶解度是
____________g;
(2)在20 ℃时,P点表示硝酸钾的溶液______
______(填“饱和”或“不饱和”),若要将硝酸钾从溶液中结晶析出,可采用
___________。
(3)将硝酸钾和硫酸锂的饱和溶液,从20 ℃降温到10 ℃,有晶体析出的是
___________。
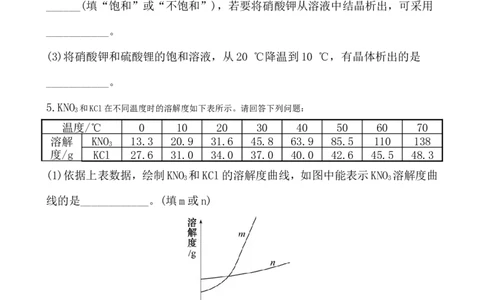
5.KNO
3和KCl在不同温度时的溶解度如下表所示。请回答下列问题:
温度/℃ 0 10 20 30 40 50 60 70
溶解 KNO 13.3 20.9 31.6 45.8 63.9 85.5 110 138
3
度/g KCl 27.6 31.0 34.0 37.0 40.0 42.6 45.5 48.3
(1)依据上表数据,绘制KNO 和KCl的溶解度曲线,如图中能表示KNO 溶解度曲
3 3
线的是____________。(填m或n)
(2)由表中数据分析可知, KNO 和KCl在某一温度时具有相同的溶解度x,则x
3
的取值范围是____________。
(3)10 ℃时,131 g 饱和KCl溶液,蒸发10 g水后,再降温到10 ℃,可析出KCl
晶体的质量为________________。
4(4)如图所示,20 ℃时,将盛有饱和KNO 溶液的小试管放入盛水的烧杯中,向水
3
中加入某物质后,试管中有晶体析出。加入的物质可能是下列中的__________
_______(填字母序号)。
A.氢氧化钠固体 B.食盐
C.冰块 D.硝酸铵固体
【探究创新】
如图是A、B两种物质的溶解度曲线,根据图示回答下列问题:
(1)t ℃时,向两只盛有100 g 水的烧杯中,分别加入A、B两种物质至不能溶解
1
为止,所得溶液中溶质质量较大的是溶液______________(填“A”或“B”)。
(2)t ℃时,欲配制等质量的A、B两种物质的饱和溶液,所需水的质量关系是
2
A______________B(填写“>”“<”或“=”,下同)。
(3)将t ℃的A、B两种物质的饱和溶液各200 g,降温至t ℃,析出晶体的质量
2 1
关系是A______________B。
(4)将t ℃的A、B两种物质的饱和溶液各200 g,升温至t ℃,欲使它们仍为饱
2 3
和溶液,若不改变溶剂质量,所需加入固体溶质的质量关系是A___________B。
5答案解析
【基础达标】
1.【解析】选D。根据固体物质溶解度的四个条件:一定温度、100 g溶剂、饱和状
态、溶质质量(单位是g)可知:A少了温度;B没指明是否饱和;C中没指明100 g
溶剂。故选D。
2.【解析】选B。根据该物质的溶解度曲线,60 ℃时该物质的饱和溶液温度降低
至30 ℃时,溶液仍为饱和溶液,并且30 ℃时该物质的溶解度是40 g,所以在
60 ℃ 100 g水配制成该物质的饱和溶液降低至30 ℃时溶液的质量为100 g
+40 g=140 g。
3.【解析】选C。降低温度时,B物质的溶解度会减小,因此B溶液会达到饱和,而
A物质的溶解度会增大,因此A溶液仍不饱和;加入溶剂时,两溶液会溶解更多溶
质,两溶液仍不饱和;加入溶质至溶质不能溶解时,均能变为饱和溶液;由于溶液
具有均一性,倒出部分溶液后,仍不会饱和。
4.【解析】选A。由于在20 ℃时,50 g水中溶解10.48 g物质M恰好达到饱和,可
知在20 ℃该物质的溶解度为10.48 g×2=20.96 g>10 g,故物质M属于易溶物
质。
5.【解析】选C。由题中信息可知,此题考查的是温度对气体溶解度的影响。水在
6加热的过程中由于温度不断升高,溶解在水中的气体会由于温度升高溶解度降
低而逸出,故A选项不符合题意;喝下汽水后,由于胃内温度高,气体的溶解度会
减小,部分气体会逸出,故会感到有气体冲到鼻腔,故B选项不符合题意;揭开啤
酒瓶盖,有大量泡沫逸出,是由于压强变小气体的溶解度变小而导致的,故C选
项符合题意;夏季天气闷热,大气压强变小,气体的溶解度变小,水中氧气变少,
鱼会浮出水面,故D选项不符合题意。
6.【解析】选D。向接近饱和的溶液中增加溶质或蒸发溶剂都可以使溶液变成饱
和溶液,故把一瓶接近饱和的石灰水变成饱和,可以采取:①加入氢氧化钙、⑤蒸
发水的方法;由于氢氧化钙的溶解度随温度升高而减小,升高温度后氢氧化钙的
溶解度变小,故把一瓶接近饱和的石灰水变成饱和,还可以采取②升高温度的方
法。故①②⑤符合题意。
7.【解析】选D。W能溶解在水和乙醇中是正确的;由溶解度曲线图可判断t ℃时
1
W在水中的溶解度是m g,B正确;t ℃时两曲线相交于一点,可知W在水中和在
2
乙醇中溶解度相等,C正确;由t ℃升温至t ℃,W在水中的溶解度增加,饱和
1 2
溶液会变成不饱和溶液,不会析出固体,所以D说法是不正确的。
8.【解析】(1)由图中可以看出t ℃时,甲、乙两物质的溶解度相等;(2)欲将t
1 2
℃时甲物质的不饱和溶液变为饱和溶液,可采用的方法:降低温度、增加甲物质、
蒸发水(任选一个即可);(3)t ℃时将乙物质的饱和溶液m g,升温到t ℃所得
1 2
溶液的质量小于m g。因为乙物质的溶解度随温度的升高而减小,乙物质饱和溶
液由t ℃升高到t ℃时,有溶质析出,所以溶液质量减少。
1 2
答案:(1)t (2)降低温度、增加甲物质、蒸发水(任选一个即可)
1
(3)<
【知能提升】
1.【解析】选D。根据溶解度的概念可知,30 ℃时,A物质的溶解度是10 g,60 ℃
时,B物质的溶解度是50 g,由于它们的温度不相同,物质也不相同,它们的溶解
度随温度的变化规律也未知,故无法比较它们的溶解度的大小。
2.【解析】选B。由于甲和乙的溶解度都随温度的升高而增大,而丙的溶解度随温
度的升高而减小,因此升高温度时,不饱和溶液能变为饱和溶液的应该是丙。
【拓展归纳】溶液存在的状态是有条件的,当外界条件改变时,溶液的状态将会发
生改变,一般规律为:不饱和溶液 加溶质、蒸发溶剂、降温 饱和溶液,对于不同
升温、加溶剂
溶质而言,改变溶质、溶剂的量都可以实现上述转化,但改变温度要具体分析:如
KNO 等大多数随着温度升高溶解度增大的固体物质适合上述规律;特殊的物质
3
如熟石灰的溶解度随温度的升高而减小,将熟石灰的不饱和溶液转化为饱和溶
液,在改变温度时应升高温度,反之若将熟石灰的饱和溶液转化为不饱和溶液则
应降低温度。
3.【解析】选D。本题考查溶解度曲线及其应用。t ℃时,乙的溶解度大于甲的溶
1
解度,A正确;加入相应的物质,能使该物质的不饱和溶液变为饱和溶液,B正确;
t ℃时,甲、乙的溶解度都是W g,即在该温度下,100 g水最多溶解甲或乙的质
2
量都是W g,所以在该温度下,甲、乙饱和溶液中溶质与溶剂的质量比都是
W∶100,C正确;甲、乙的溶解度都随着温度的升高而增大,所以对甲、乙t ℃时
3
的饱和溶液降温会同时析出晶体,D错。
4.【解析】本题以溶解度曲线为主题,主要考查学生从溶解度曲线查找物质的溶
解度、分析点的意义、物质结晶的方法等知识点。从图中可以查出,0 ℃时氯化钠
7和硫酸锂的溶解度相等,为36 g;20 ℃时,P点在硝酸钾溶解度曲线的下方,所
以是不饱和溶液。因为硝酸钾的溶解度随着温度的升高而增大,所以采用降温的
方法可以使其结晶;硫酸锂的溶解度随着温度的升高而减小,所以降低温度时不
会析出晶体。
答案:(1)36 (2)不饱和 降温 (3)硝酸钾溶液
5.【解析】(1)由表中数据可以看出,KNO 和KCl中,KNO 的溶解度受温度的影响
3 3
较大,所以,能表示KNO 溶解度曲线的是m;(2)在20 ℃~30 ℃之间,KNO 和
3 3
KCl的溶解度可能相等;(3)10 ℃时,KCl的溶解度为31.0 g,说明100 g水中溶
解31.0 g KCl达到饱和,则10 g水中溶解3.1 g KCl达到饱和,所以蒸发10 g
水,会析出3.1 g KCl;(4)试管中有晶体析出,说明溶液的温度降低,即加入水
中的物质溶于水是吸热的,冰块和硝酸铵固体溶于水时吸热;氢氧化钠溶于水是
放热的;食盐溶于水时温度没有明显的变化,故选C和D。
答案:(1)m (2)34.0 g (4)>
8