文档内容
第三节 无机非金属材料
[明确学习目标] 1.知道常见的硅酸盐材料玻璃、水泥、陶瓷及生产它们的
主要原料。2.了解高纯硅的制备原理。知道硅和二氧化硅的用途。3.知道一些新
型的无机非金属材料硅和二氧化硅、新型陶瓷和碳纳米材料等。
学生自主学习
硅酸盐材料
1.无机非金属材料多含有 □ 硅 、 □ 氧 等元素,具有 □ 耐高温 、 □ 抗腐蚀 、 □ 硬
度高等特点,以及特殊的 □ 光学 、 □ 电学 等性能。
2.硅酸盐材料主要包括 □ 陶瓷 、 □ 玻璃 、 □ 水泥 等。
3.在硅酸盐中,Si和O构成了 □ 硅氧四面体 ,决定了硅酸盐材料大多具有
硬度高、熔点高、难溶于水、化学性质稳定、耐腐蚀等特点。
4.下列硅酸盐材料的主要原料分别是:
陶瓷: □ 黏土 ;玻璃: □ 纯碱、石灰石、石英砂 ;水泥: □ 黏土和石灰石 。
新型无机非金属材料
1.硅元素在周期表中的位置为: □ 第三周期、第 Ⅳ A 族 ,其单质的导电性介
于导体与绝缘体之间,是应用最为广泛的 □ 半导体 材料。
高纯硅的制备原理为:□SiO +2C=====Si+2CO↑;
2
□Si+3HCl=====SiHCl +H ;□SiHCl +H =====Si+3HCl。
3 2 3 2
高纯硅可用于生产计算机芯片和硅太阳能电池。二氧化硅可用来生产光导纤
维。
2.常见的新型陶瓷有: □ 高温结构陶瓷、压电陶瓷、透明陶瓷、超导陶瓷 。
碳化硅——俗称 □ 金刚砂 ——具有类似 □ 金刚石 结构——硬度很大——可作砂
纸、砂轮的磨料。
3.碳纳米材料主要包括 □ 富勒烯、碳纳米管、石墨烯 等。
1.单质硅在常温下化学性质稳定,所以硅在自然界中以游离态存在,这种
说法是否正确?为什么?提示:不正确。硅属于亲氧元素,虽然在常温下稳定,但在漫长的地质年代
中,硅元素和氧结合在一起,都以化合态存在,主要以二氧化硅及硅酸盐的形式
存在。
2.实验室中盛放碱液的试剂瓶为什么用橡胶塞而不用玻璃塞?
提示:玻璃中含有SiO ,SiO 与碱反应生成具有黏合作用的硅酸盐,使瓶口
2 2
和瓶塞黏结在一起而难以开启。
课堂互动探究
一、二氧化硅
1.硅元素的存在
2.二氧化硅
(1)存在
SiO 存在形态有结晶形和无定形两大类,统称硅石。石英、水晶、玛瑙、沙
2
子、光导纤维的主要成分均是SiO 。
2
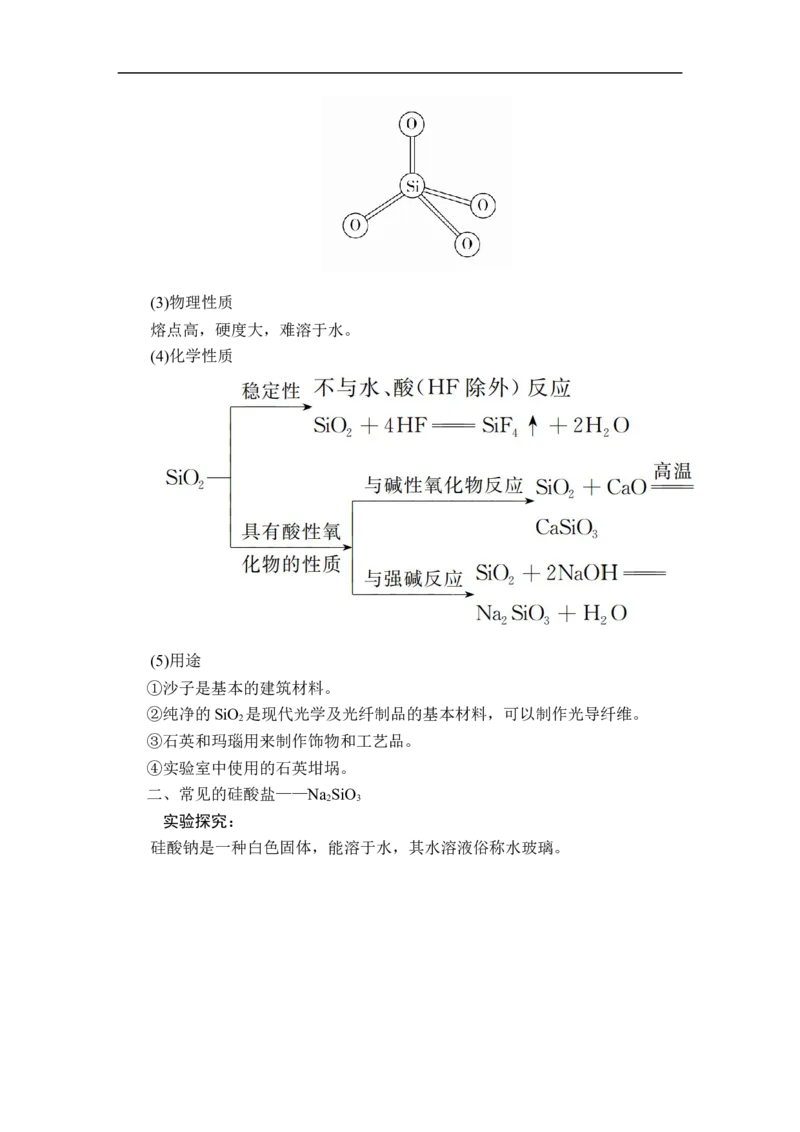
(2)结构
SiO 晶体是由Si和O按原子数之比为1∶2的比例组成的正四面体结构的晶
2
体。每个硅原子周围结合4个O原子,每个O原子周围结合2个Si原子。(3)物理性质
熔点高,硬度大,难溶于水。
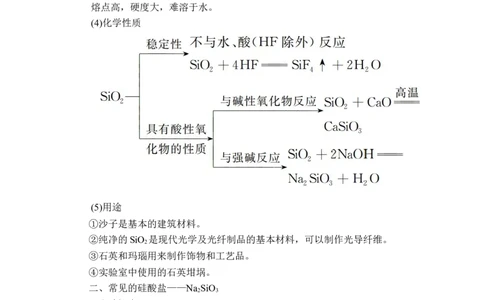
(4)化学性质
(5)用途
①沙子是基本的建筑材料。
②纯净的SiO 是现代光学及光纤制品的基本材料,可以制作光导纤维。
2
③石英和玛瑙用来制作饰物和工艺品。
④实验室中使用的石英坩埚。
二、常见的硅酸盐——Na SiO
2 3
实验探究:
硅酸钠是一种白色固体,能溶于水,其水溶液俗称水玻璃。三、硅酸盐氧化物形式的书写
硅酸盐由于组成比较复杂,通常用氧化物的形式表示其组成,改写时的规律
为:
(1)顺序:活泼金属氧化物→较活泼金属氧化物→二氧化硅→水;氧化物之间
以“·”隔开。
(2)原则:各元素原子总个数比符合原来的组成,若出现分数应化为整数。
例 如 : 钠 长 石 NaAlSi O 不 能 写 成 Na O·Al O ·3SiO , 应 写 成
3 8 2 2 3 2
Na O·Al O ·6SiO 。
2 2 3 2
(3)各元素的化合价不能改变。
矿泉水一般是由岩石风化后,被地下水溶解其中的可溶部分生成的,
此处所指的风化作用是指矿物与水和CO 同时作用的过程。例如长石(KAlSi O )
2 3 8
风化生成高岭土[Al Si O (OH) ],此反应的离子方程式为:
2 2 5 4
2KAlSi O +2H CO +5H O===2K++2HCO+4H SiO +Al Si O (OH)
3 8 2 3 2 2 3 2 2 5 4
(1)将上述复杂硅酸盐改写成氧化物形式。
①KAlSi O _____________________________________________________。
3 8
②Al Si O (OH) _________________________________________________。
2 2 5 4
(2)上述反应能够发生的原因是__________________________。
[批注点拨][解析] (1)将硅酸盐化学式写成氧化物时,需将氧以外的元素写成同价态的
氧化物,并按活动性顺序排列,用“·”将它们连接起来,各种元素原子个数比
符合原来的组成。
(2)此反应属于酸与盐发生的复分解反应,能发生的原因是酸性:
H CO >H SiO 。
2 3 2 3
[答案] (1)①K O·Al O ·6SiO ② Al O ·2SiO ·2H O (2)H CO 的酸性比
2 2 3 2 2 3 2 2 2 3
H SiO 强
2 3
[练1] 用氧化物的形式表示硅酸盐的组成,其中正确的是( )
A.钙沸石[Ca(Al Si O )·3H O],表示为Al O ·CaO·3SiO ·3H O
2 3 10 2 2 3 2 2
B.镁橄榄石(Mg SiO ),表示为MgO·SiO
2 4 2
C.钾云母(K Al Si H O ),表示为K O·2H O·3Al O ·6SiO
2 6 6 4 24 2 2 2 3 2
D.硅酸铜钡(BaCuSi O ),表示为BaO·CuO·2SiO
2 6 2
答案 D
解析 A项,Ca(Al Si O )·3H O应改为 CaO·Al O ·3SiO ·3H O(排序错);B
2 3 10 2 2 3 2 2项,Mg SiO 应改为2MgO·SiO (不能在系数中出现分数);C项,
2 4 2
K Al Si H O 应改为K O·3Al O ·6SiO ·2H O(排序错)。
2 6 6 4 24 2 2 3 2 2
[练 2] 将过量的 CO 分别通入:① CaCl 溶液;②浓 Na SiO 溶液;
2 2 2 3
③Ca(OH) 溶液;④饱和Na CO 溶液。最终溶液中有白色沉淀析出的是( )
2 2 3
A.①②③④ B.②④
C.①②③ D.②③
答案 B
解析 CO 溶于水:CO +H OH CO ,H CO 的酸性比盐酸弱,而比硅酸
2 2 2 2 3 2 3
强。根据酸与盐反应的规律,CO 通入CaCl 溶液无明显现象;过量的CO 通入
2 2 2
浓 Na SiO 溶液中有白色沉淀 H SiO 生成;CO 通入 Ca(OH) 溶液至过量,
2 3 2 3 2 2
Ca(OH) +CO ===CaCO ↓+H O,CaCO +H O+CO ===Ca(HCO ) ,最终生成
2 2 3 2 3 2 2 3 2
Ca(HCO ) 而无沉淀;过量 CO 通入饱和 Na CO 溶液中:Na CO +H O+
3 2 2 2 3 2 3 2
CO ===2NaHCO ↓,生成的NaHCO 溶解度比Na CO 溶解度小而结晶析出,故
2 3 3 2 3
选B。
规律方法
强酸制弱酸原理
强酸可与弱酸盐反应生成相应的弱酸和强酸盐,而弱酸一般不与强酸盐反应。
如:
(1)2CH COONa+H SO ===2CH COOH+Na SO
3 2 4 3 2 4;
(2)2CH COOH+Na CO ===2CH COONa+H O+CO ↑;
3 2 3 3 2 2
(3)Na SiO +CO +H O===Na CO +H SiO ↓;
2 3 2 2 2 3 2 3(4)CaCl +CO +H O不反应。
2 2 2
本课归纳总结
1.硅酸钠水溶液俗称水玻璃,常用于制备黏合剂、防腐剂和耐火材料。
2.传统的无机非金属材料主要有水泥、玻璃和陶瓷。
3.硅以化合态存在于自然界中,常用作半导体材料和合金材料。
4.石英、水晶、沙子、玛瑙、光导纤维的主要成分均是SiO 。
2
5.必记的几个反应
(1)SiO +2C=====Si+2CO↑
2
(2)Si+3HCl=====SiHCl +H
3 2
(3)SiHCl +H =====Si+3HCl
3 2
(4)SiO +4HF===SiF ↑+2H O
2 4 2
(5)SiO +2NaOH===Na SiO +H O
2 2 3 2
学习效果检测
1.SiO 属于酸性氧化物的理由主要是( )
2
A.硅是非金属元素
B.SiO 对应的水化物是可溶性弱酸
2
C.SiO 能与强碱反应生成盐和水
2
D.SiO 不能与酸反应
2
答案 C
2.在①浓硝酸、②水、③盐酸、④氢氟酸、⑤氢氧化钾溶液中,常温时能
与二氧化硅起化学反应的有( )
A.①② B.②④ C.④⑤ D.③④
答案 C
3.和空气接触可发生非氧化还原反应的物质是( )
①Na ②Na SiO 溶液 ③Na O ④烧碱溶液
2 3 2 2
⑤石灰水 ⑥Fe(OH)
2
A.①③④ B.②④⑤
C.②③⑥ D.①④⑤
答案 B解析 Na在空气中与O 反应生成Na O;Na O 在空气中与CO 和H O均能
2 2 2 2 2 2
反应生成O ;Fe(OH) 在空气中与O 和水反应生成Fe(OH) ,以上过程均有元素
2 2 2 3
化合价的变化,是氧化还原反应。
4.下列说法正确的是( )
A.CO +H O+Na SiO ===H SiO ↓+Na CO ,说明酸性:H CO >H SiO
2 2 2 3 2 3 2 3 2 3 2 3
B.SiO +Na CO =====Na SiO +CO ↑,说明酸性:H SiO >H CO
2 2 3 2 3 2 2 3 2 3
C.在复分解反应中必须是酸性强的生成酸性弱的
D.已知酸性:H CO >HClO>HCO,则 CO +H O+2NaClO===Na CO +
2 3 2 2 2 3
2HClO
答案 A
解析 由于H CO 能与盐反应生成H SiO ,则说明H CO 酸性大于H SiO ,
2 3 2 3 2 3 2 3
A正确;在B项中,由于在高温条件下反应,CO 为气体溢出,不能说明酸性强
2
弱;在C项中,H S+CuSO ===CuS↓+H SO ,此反应为弱酸生成强酸;在 D
2 4 2 4
项中由HClO>HCO,产物应为NaHCO 。
3
5.NaOH、KOH等碱性溶液可以贮存在下列哪种试剂瓶中( )
A.具有玻璃塞的细口瓶 B.具有玻璃塞的广口瓶
C.带滴管的滴瓶 D.具有橡胶塞的细口瓶
答案 D
解析 NaOH、KOH等碱性溶液能与玻璃中的SiO 反应生成具有黏性的物质,
2
将瓶塞和瓶口黏结在一起以及液体存放在细口瓶中,固体存放在广口瓶中。
6.某研究性学习小组进行了“实验室制Si”的研究,他们以课本为基础,
查阅资料得到以下可供参考的信息:
①工业上在高温时用C还原SiO 可制得Si;
2
②Mg在点燃的条件下按质量比8∶5与SiO 反应生成一种白色固体化合物和
2
另一种硅化物;
③金属硅化物与稀硫酸反应生成硫酸盐与SiH ;
4④Si和SiO 均不能与稀H SO 反应;
2 2 4
⑤SiH 在空气中自燃。
4
他们的研究报告中记载着“……选用合适的物质在适合的条件下充分反应;
再用足量稀硫酸溶解固体产物;然后过滤、洗涤、干燥,最后称量……用稀硫酸
溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期的 63%左右。”请
回答下列问题:
(1)该小组“实验室制Si”的化学反应方程式是________________。
(2)写出②的反应方程式:______________________________________。
(3)该过程中产率比预期低的原因是________________________________。
(4)你估计“用稀硫酸溶解固体产物时,发现有爆鸣声和火花”的原因是什么?
请用必要的文字和化学方程式予以说明:_________________。
答案 (1)2C+SiO =====Si+2CO↑
2
(2)SiO +4Mg=====2MgO+Mg Si
2 2
(3)部分硅与镁反应生成了硅化镁
(4)SiH 能自燃,而有爆鸣声和火花就是由 SiH 的自燃引起的,SiH +
4 4 4
2O ===SiO +2H O
2 2 2
解析 (1)碳可以在高温下还原 SiO 制得 Si。反应的化学方程式为 2C+
2
SiO =====Si+2CO↑。
2
(2)(3)Mg与SiO 反应类似于Mg与CO 的反应,先生成MgO和Si,Si再和
2 2
Mg反应生成Mg Si,故可生成MgO和Mg Si。
2 2