文档内容
北京师大附中 2019-2020 学年上学期高一年级期末考试化学试卷
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 A1-27 S-32 Cl-35.5 Fe-56
一、选择题(30道小题,每小题2分,共60分,每小题只有1个选项符合题意)
1.合金是一类用途广泛的金属材料。下列物质不属于合金的是
A. 不锈钢 B. 青铜 C. 生铁 D. 水银
2.下列物质中,属于电解质的是
A. Cu B. NaCl溶液 C. NaOH固体 D. 乙醇
3.下列微粒中,既具有氧化性又具有还原性的是( )
A. Fe2+ B. O C. Cl- D. Na
2
4.下列物质的电子式书写正确的是( )
A. Cl:Cl B. C. D.
5.下列四种基本反应类型与氧化还原反应的关系图中,正确的是( )
A. B.
C. D.
6.在元素周期表中金属与非金属的分界处,可以找到( )
A. 合金 B. 农药 C. 催化剂 D. 半导体材料
7.下列元素中,原子半径最大的是
A. Na B. Mg C. Al D. Si
8.重水(2HO)是重要的核工业原料,下列说法不正确的是
2
A. 氘(2H)原子核内有1个质子 B. 1H与2H是不同的核素
C. 1H18O与2H16O的相对分子质量相同 D. 1HO与2HO互为同位素
2 2 2 2
9.下列各组离子中,能在溶液里大量共存的是( )
A. H+、Na+、SO 2-、Cl- B. Ca2+、Na+、CO2-、NO -
4 3 3
C. K+、Fe3+、OH-、SO 2- D. Na+、H+、HCO -、Cl-
4 3
10.下列溶液中的c(SO 2-)与50mL1mol·L-1Al (SO ) 溶液中的c(SO 2-)相等的是
4 2 4 3 4
A. 150mL1mol·L-1NaSO 溶液
2 4
B. 75mL2mol·L-1(NH )SO 溶液
4 2 4C. 150mL3mol·L-1KSO 溶液
2 4
D. 20mL1.5mol·L-1Fe (SO ) 溶液
2 4 3
11.在标准状况下,下列物质体积最大的是( )
A. 3gH B. 6.02×1023个H C. 44.8LH D. 0.5molH
2 2 2 2
12.下列说法中,符合VIIA族元素结构与性质特征的是( )
A. 原子易形成-2价阴离子
B. 单质均为双原子分子,具有氧化性
C. 原子半径随原子序数递增逐渐减小
D. 氢化物的稳定性随原子电子层数递增依次增强
13.在3NO+HO=2HNO +NO中,氧化剂与还原剂的分子个数比为
2 2 3
.
A 2∶1 B. 1∶2 C. 3∶1 D. 1∶3
14.下列有关试剂保存的说法中,不正确的是( )
A. 新制氯水保存在棕色试剂瓶中
B. 金属Na保存在煤油中
C. 漂白粉保存在敞口容器中
D. 过氧化钠应密封保存
15.下列关于NaCO 和NaHCO 性质的说法中,不正确的是( )
2 3 3
A. 热稳定性:NaCO>NaHCO
2 3 3
B. 相同温度下,溶解度:NaCO>NaHCO
2 3 3
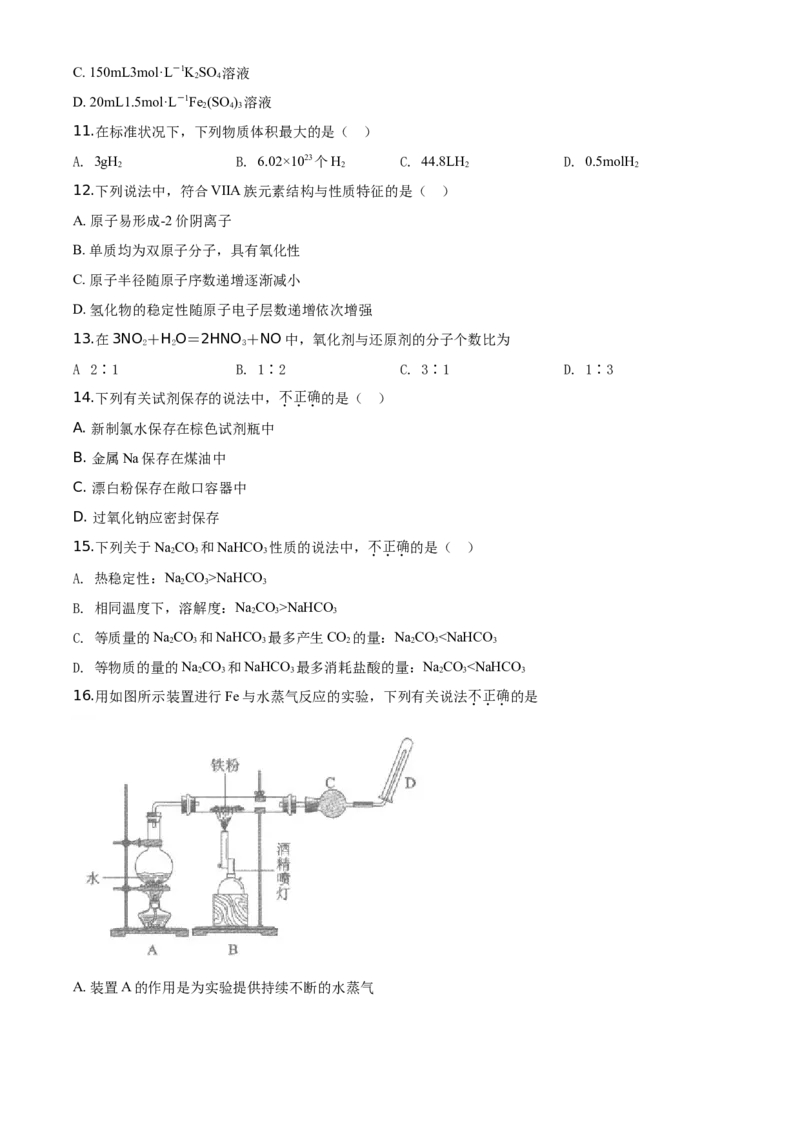
C. 等质量的NaCO 和NaHCO 最多产生CO 的量:NaCOCu2+)( )
A. 溶液中一定含有Cu2+
B. 加入KSCN溶液一定不变红色
C. 溶液中一定含有Fe2+
.
D 剩余固体中一定含铜
26.某化学小组用如图所示装置验证卤素单质氧化性的相对强弱。下列说法不正确的是( )A. A处棉花球变成黄色,说明Cl 的氧化性比Br 强
2 2
B. B处棉花球变成蓝色,说明Br 的氧化性比I 强
2 2
C. A处发生反应的离子方程式为:Cl+2Br-=2Cl-+Br
2 2
D. C装置中与NaOH溶液反应的离子方程式为:Cl+2OH-=ClO-+Cl-+H O
2 2
27.下列反应所得溶液中一定只含一种溶质的是( )
A. 向AlCl 溶液中加入一定量的NaOH
3
B. 向NaOH溶液中通入足量CO 气体(不考虑CO 溶于水)
2 2
C. 向含1molNaHCO 溶液中,加入1molNa O 粉末
3 2 2
D. 向含1molNa CO 溶液中,加入含1molHCl的盐酸
2 3
28.下列“实验结论”与“实验操作及现象”相符的一组是( )
选项 实验操作及现象 实验结论
A 向某溶液中加入AgNO 溶液,有白色沉淀生成 该溶液中一定含有Cl-
3
B 向某溶液中加入稀盐酸,有无色气体产生 该溶液中一定含有CO2-
3
C 向某溶液中加入BaCl 溶液,有白色沉淀生成 该溶液中一定含有SO 2-
2 4
D 向某溶液中加入NaOH溶液,立即产生红褐色沉淀 该溶液中一定含有Fe3+
A. A B. B C. C D. D
29.根据表1信息,判断以下叙述正确的是( )
表1 部分短周期元素的原子半径及主要化合价
元素代号 L M Q R T
原子半径/nm 0.160 0.143 0.112 0.104 0.066
主要化合价 +2 +3 +2 +6、-2 -2A. 氢化物的沸点为HT<HR B. 单质与稀盐酸反应的速率为L<Q
2 2
C. M与T形成的化合物具有两性 D. L2+与R2-的核外电子数相等
30.高铁酸钠(Na FeO)是一种高效的饮用水处理剂,工业上可由下列方法制得:Fe O+3Na O
2 4 2 3 2 2
2NaFeO+Na O,下列关于该反应的说法中正确的是( )
2 4 2
A. 反应中NaO 既是氧化剂又是还原剂
2 2
B. Fe O 可以通过铁丝在氧气中燃烧制得
2 3
C. 生成1molNa FeO,有3mol电子转移
2 4
D. 在NaFeO 中Fe为+4价,具有强氧化性,能杀菌消毒
2 4
二、非选择题(共8道小题,共40分)
31.补齐物质及其用途的连线___。
32.金属钛因具有良好的抗腐蚀能力、熔点高、硬度大、可塑性强、密度小等优点,被誉为“21世纪金属”。
工业冶炼钛的第一步反应为:TiO+2C+2Cl TiCl +2CO。在此反应中,氧化剂是__,氧化产物是__,生
2 2 4
成1molTiCl 转移电子的物质的量是__mol。
4
33.用化学用语表达。
(1)小苏打受热易分解,化学方程式为__。
(2)金属钠着火不能用水扑灭,用离子方程式解释其原因__。
(3)工业上用氯气和熟石灰制备漂白粉,化学方程式 为__。
34.无机化合物按照组成和性质可进行如下分类。其中②、③、⑥均由Na、K、H、O、S中的3种元素组成。
强酸 强碱 可溶性盐 ……
①HCl ③___ ⑤NaCO ⑦CO
2 3 2
②__ ④Ba(OH) ⑥__ ⑧SO
2 3
(1)图中“……”可以代表的物质类别是___。
(2)③的水溶液为碱性,写出电离方程式___。(写一种即可)(3)②与④在水溶液中发生反应的离子方程式是__。
(4)⑤与⑦在水溶液中发生反应的化学方程式是__。
(5)②与⑥能发生复分解反应,则⑥的化学式是__。(写一种即可)
35.为了检验市场上常见两种金属饮料瓶的主要成分,某小组取甲、乙两种饮料瓶,分别剪成小片制成样品
甲和乙,并按下述步骤进行实验:
I.分别取少量样品于试管中,加入盐酸,充分反应后过滤。
II.分别取少量滤液于试管中,向其中滴加氢氧化钠溶液。
步骤II的实验现象如下:
样品甲 先生成白色沉淀,后沉淀消失
样品乙 生成白色沉淀,并迅速变为灰绿色,最终变为红褐色
(1)样品甲中金属的主要成分是__,白色沉淀消失反应的离子方程式是__。
(2)样品乙进行步骤I后所得滤液中一定含有的金属离子是__,白色沉淀变为红褐色沉淀反应的化学方程
式是__。
36.某实验需要500mL0.10mol/L的NaCO 溶液,现通过如下步骤配制:
2 3
①把称量好的固体NaCO 放入小烧杯中,加适量蒸馏水搅拌溶解;
2 3
②用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀;
③盖好瓶塞,反复上下颠倒,摇匀;
④把溶解固体后所得溶液冷却至室温,转入仪器A中;
⑤继续加蒸馏水至液面距刻度线1~2cm处,改用胶头滴管滴加蒸馏水至溶液的凹液面与刻度线相切;
(1)操作步骤的正确顺序为__(填序号)。
(2)称量的NaCO 固体质量应为__g。
2 3
(3)仪器A的名称是__。
(4)取出100mL配制好的溶液,加蒸馏水稀释至c(Na CO)=0.02mol/L。则稀释后溶液的体积为__。
2 3
(5)下列关于容量瓶的使用方法中,正确的是__(填字母序号)。
A.使用前要检验是否漏水
B.在容量瓶中直接溶解固体或稀释液体
C.在烧杯中溶解固体后,迅速将溶液转移到容量瓶中
D.向容量瓶中转移溶液用玻璃棒引流
E.加水时水量超过了刻度线,迅速用胶头滴管将过量的水吸出
(6)下列操作会使所配溶液的物质的量浓度偏低的是__(填字母序号)。
A.将烧杯中 的溶液转移到容量瓶时不慎洒到容量瓶外B.定容读数时,俯视容量瓶上的刻度线
C.加水定容时,水量超过了刻度线
D.洗涤步骤中,洗涤液没有转入容量瓶
37.元素X、Y、Z、M、R均为短周期主族元素,且原子序数依次增大。已知:Y为地壳中含量最多的元
素,M原子的最外层电子数与次外层电数之比为3:4;R-、Z+、X+离子半径逐渐减小;化合物XR常温下
为气体,请回答下列问题:
(1)M在元素周期表中的位置__;Z+离子的结构示意图为__。
(2)写出X、Y、R按原子个数之比1:1:1形成的化合物的电子式__。
(3)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式__。
(4)实验室制备R的单质,该反应的离子方程式为__。
(5)R非金属性强于M,下列选项中能证明这一事实的是__(填字母序号)。
A.常温下的R单质熔沸点比M单质的高
B.R的氢化物比M的氢化物更稳定
C.一定条件下R和M的单质都能与NaOH溶液反应
D.最高价氧化物对应水化物的酸性强弱:R>M
(6)由X、Y、Z、M四种元素组成的一种弱酸酸式盐A。向A溶液中通入氯气,得到无色溶液,写出该
反应的离子方程式__。
38.某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量硫酸铁、硫酸亚铁固体,均配制成100mL0.1mol/L的溶液。在配制FeSO 溶液时需加入
4
少量铁屑,其目的是__。
(2)甲组同学取2mLFeSO 溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl 可将
4 2
Fe2+氧化。FeSO 溶液与氯水反应的离子方程式为___。
4
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeSO 溶液中先加入0.5mL煤油,再于液面下依
4
次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是__。
(4)丙组同学研究pH对FeSO 稳定性的影响,得到如图所示结果,增强Fe2+稳定性的措施为__。(写出一
4
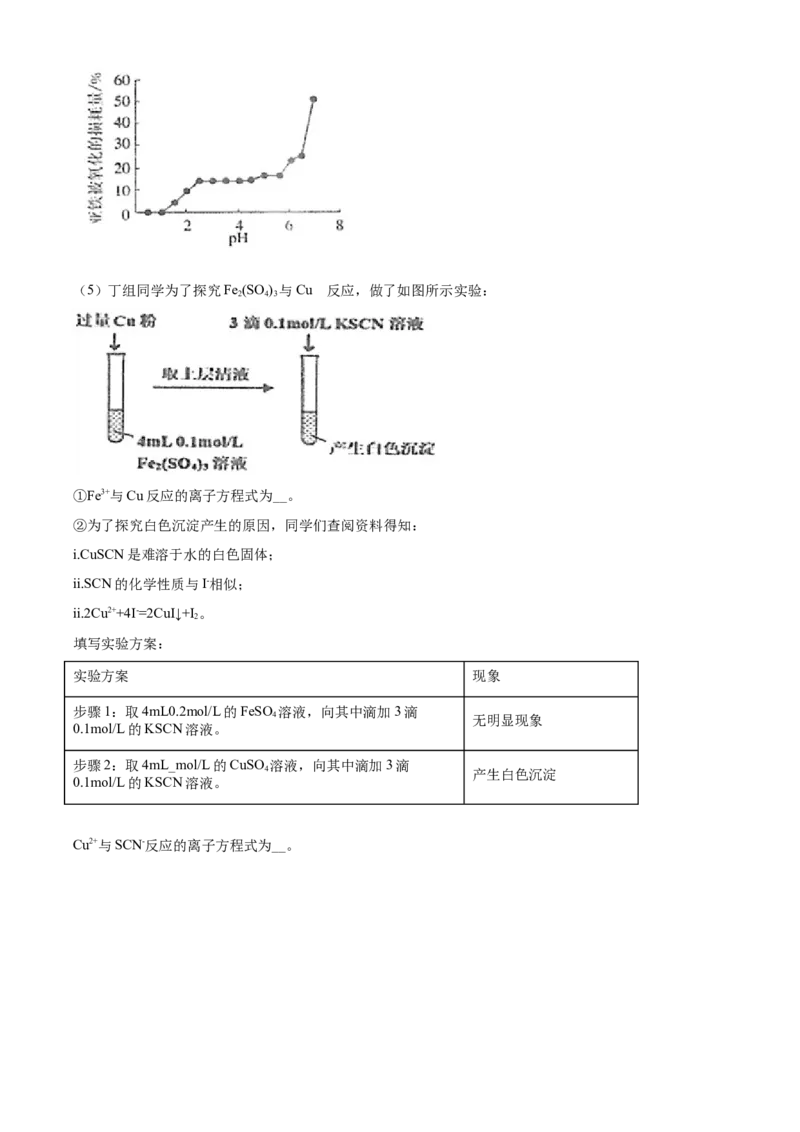
条即可)(5)丁组同学为了探究Fe (SO ) 与Cu 的反应,做了如图所示实验:
2 4 3
①Fe3+与Cu反应的离子方程式为__。
②为了探究白色沉淀产生的原因,同学们查阅资料得知:
i.CuSCN是难溶于水的白色固体;
ii.SCN的化学性质与I-相似;
ii.2Cu2++4I-=2CuI↓+I 。
2
填写实验方案:
实验方案 现象
步骤1:取4mL0.2mol/L的FeSO 溶液,向其中滴加3滴
4 无明显现象
0.1mol/L的KSCN溶液。
步骤2:取4mL_mol/L的CuSO 溶液,向其中滴加3滴
4 产生白色沉淀
0.1mol/L的KSCN溶液。
Cu2+与SCN-反应的离子方程式为__。