文档内容
北京市西城区 2019—2020 学年高一下学期期末试卷
化学试题
1.下列能量的转化过程中,由化学能转化为电能的是
A B C D
太阳能集热 燃气燃烧 风力发电 手机电池工作
A. A B. B C. C D. D
2.维生素C(C HO)广泛存在于新鲜水果和蔬菜中,在人体内有重要的功能。维生素C属于
6 8 6
A. 有机物 B. 单质 C. 氧化物 D. 盐
3.下列金属中,通常用热分解法冶炼的是
A. 钠 B. 铁 C. 铝 D. 银
4.下列关于甲烷的说法不正确的是
A. 甲烷分子具有正四面体结构 B. 甲烷是无色无味的气体
C. 甲烷是最简单的烷烃 D. 甲烷能使酸性高锰酸钾溶液褪色
5.常温下,下列溶液可用铁质容器盛装的是
A. 浓硝酸 B. 稀硫酸 C. 稀硝酸 D. 稀盐酸
6.下列物质或方法中不能用来鉴别乙醇和乙酸的是
A. 观察颜色 B. 碳酸钠溶液 C. 扇闻气味 D. 紫色石蕊溶液
7.下列说法不正确的是
A. 乙烯的官能团是碳碳双键
B. 75%的乙醇溶液可以杀菌消毒
C. 乙酸的酸性比碳酸弱
D. 酯化反应是可逆反应
8.下列关于化学反应与能量的说法不正确的是
A. 乙醇的燃烧是放热反应B. Mg与盐酸的反应是吸热反应
C. 反应物化学键 的断裂要吸收能量
D. 化学反应伴随有能量的变化
9.实验室中,下列行为不符合安全要求 的是
A. 点燃甲烷前,先验纯
B. 用手将灼热的蒸发皿拿离火焰,直接放在实验台上
C. 实验结束后,将废液倒入指定容器中
D. 稀释浓硫酸时,将浓硫酸沿烧杯壁缓缓倒入水中并不断搅拌
10.关于如图所示的原电池,下列说法正确的是
A. 该装置能将电能转化为化学能
B. 锌片上发生还原反应
C. 电子由锌片通过导线流向铜片
D. 铜片上发生的反应为Cu2++2e-=Cu
11.下列反应属于加成反应的是
A. CH +Cl CHCl+HCl
4 2 3
B. CH=CH +H CHCH
2 2 2 3 3
C. 2CHCHOH+2Na→2CH CHONa+H↑
3 2 3 2 2
D. C H+3O 2CO+2HO
2 4 2 2 2
12.下列关于浓硫酸的说法不正确的是
.
A 能干燥氯气
B. 具有强腐蚀性
C. 可与金属反应制取氢气
D. 加热时能与木炭发生反应
13.下列关于海水资源综合利用的说法不正确的是
A. 蒸馏法是海水淡化的方法之一
B. 海水晒盐是化学变化
C. 从海水中可制取钠、镁、溴等化工产品D. 从海水获得物质和能量具有广阔的前景
14.其他条件不变时,下列措施中能减慢化学反应速率的是
A. 用煤粉代替煤块燃烧
B. 食物存放在冰箱里
C. 滴入少量FeCl 溶液催化HO 分解
3 2 2
D. 用1mol·L−1HSO 代替0.1mol·L−1HSO 与锌粒反应
2 4 2 4
15.在一定条件下,对于密闭容器中进行的反应:X(g) + Y(g) 2Z(g),下列说法能充分说明该反应已达到
化学平衡状态的是 ( )
A. X、Y、Z的浓度相等 B. 正、逆反应速率均等于零
C. X、Y、Z在容器中共存 D. X、Y、Z的浓度均不再改变
16.下列解释事实的方程式不正确的是
A. NH 遇HCl产生白烟:NH +HCl=NHCl
3 3 4
B. NO遇空气变为红棕色:2NO+O=2NO
2 2
C. NH 发生催化氧化反应生成NO:4NH +5O 4NO+6HO
3 3 2 2
D. Cu与稀HNO 混合产生无色气体:Cu+2 +4H+=Cu2++2NO ↑+2HO
3 2 2
17.根据乙烯的性质推测丙烯(CH=CH-CH)的性质,下列说法不正确的是
2 3
A. 丙烯能在空气中燃烧
B. 丙烯能使酸性高锰酸钾溶液褪色
C. 丙烯与Br 的加成产物是CHBr-CH-CHBr
2 2 2 2
D. 聚丙烯可以用 来表示
18.下列实验结论与实验现象相符合的一组是
选项 实验 现象 结论
产生的气体能使湿润的
A 向某盐溶液中加入浓NaOH溶液,加热 原溶液中含有
红色石蕊试纸变蓝
B 把SO 通入紫色的酸性高锰酸钾溶液中 溶液紫色褪去 SO 具有漂白性
2 2
C 向蔗糖中滴加浓硫酸 蔗糖变黑 浓硫酸具有吸水性
NaNO 是催化剂,可增
向盛有Cu片的试管中加入稀HSO ,无 Cu片逐渐溶解,产生气 3
D 2 4 大Cu与稀HSO 反应
明显现象,再加入NaNO 固体 2 4
3 泡,溶液变蓝 的化学反应速率A. A B. B C. C D. D
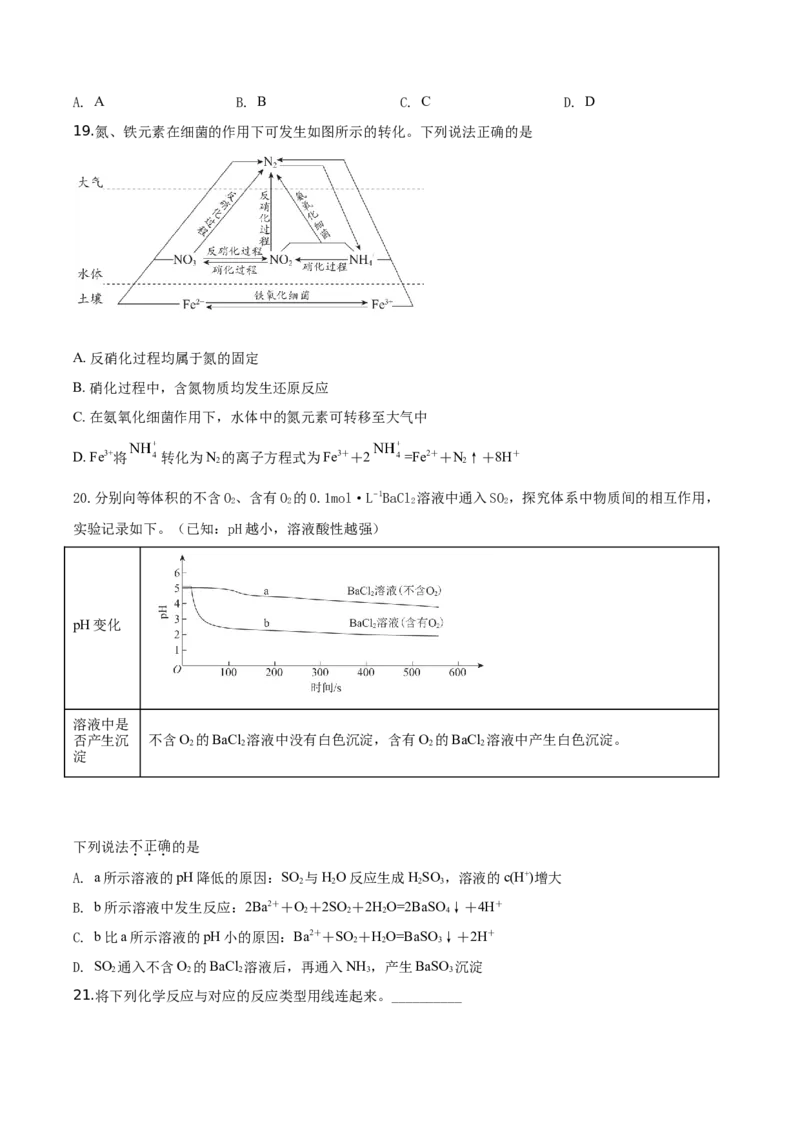
19.氮、铁元素在细菌的作用下可发生如图所示的转化。下列说法正确的是
A. 反硝化过程均属于氮的固定
B. 硝化过程中,含氮物质均发生还原反应
C. 在氨氧化细菌作用下,水体中的氮元素可转移至大气中
D. Fe3+将 转化为N 的离子方程式为Fe3++2 =Fe2++N↑+8H+
2 2
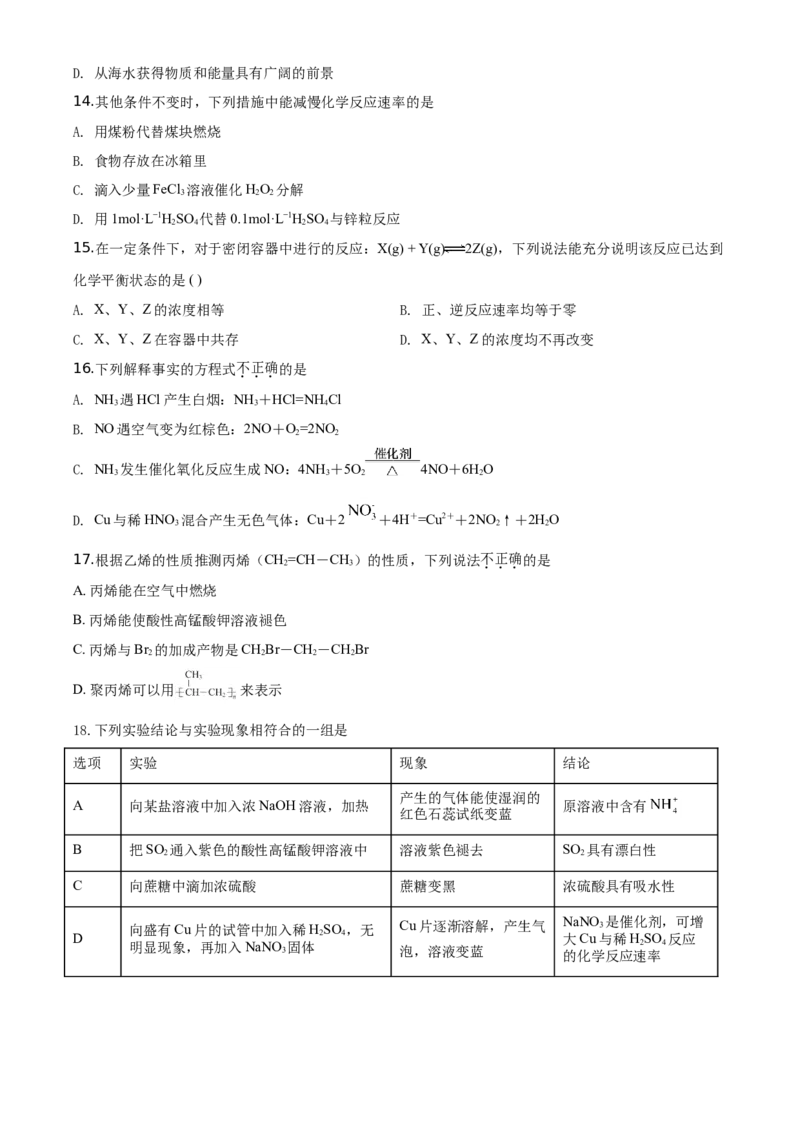
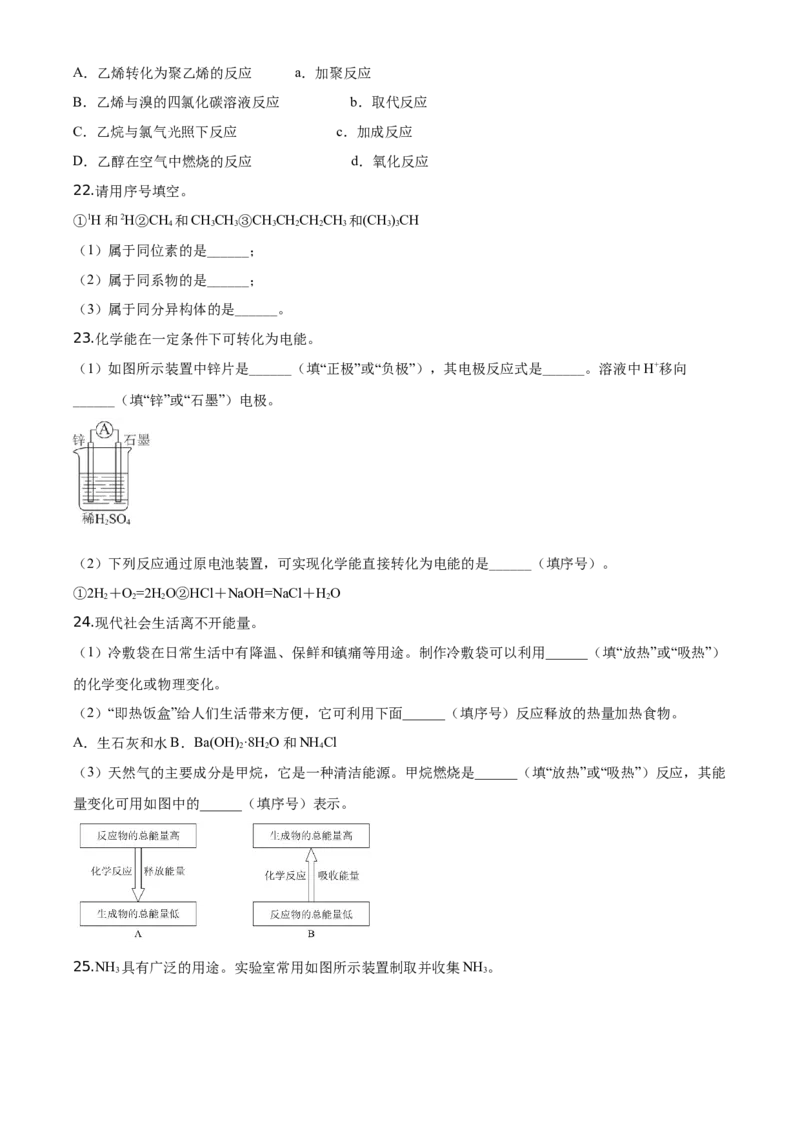
20.分别向等体积的不含O、含有O 的0.1mol·L−1BaCl 溶液中通入SO,探究体系中物质间的相互作用,
2 2 2 2
实验记录如下。(已知:pH越小,溶液酸性越强)
pH变化
溶液中是
否产生沉 不含O 的BaCl 溶液中没有白色沉淀,含有O 的BaCl 溶液中产生白色沉淀。
2 2 2 2
淀
下列说法不正确的是
A. a所示溶液的pH降低的原因:SO 与HO反应生成HSO ,溶液的c(H+)增大
2 2 2 3
B. b所示溶液中发生反应:2Ba2++O+2SO +2HO=2BaSO↓+4H+
2 2 2 4
C. b比a所示溶液的pH小的原因:Ba2++SO +HO=BaSO↓+2H+
2 2 3
D. SO 通入不含O 的BaCl 溶液后,再通入NH ,产生BaSO 沉淀
2 2 2 3 3
21.将下列化学反应与对应的反应类型用线连起来。__________A.乙烯转化为聚乙烯的反应 a.加聚反应
B.乙烯与溴的四氯化碳溶液反应 b.取代反应
C.乙烷与氯气光照下反应 c.加成反应
D.乙醇在空气中燃烧的反应 d.氧化反应
22.请用序号填空。
①1H和2H②CH 和CHCH③CHCHCHCH 和(CH)CH
4 3 3 3 2 2 3 3 3
(1)属于同位素的是______;
(2)属于同系物的是______;
(3)属于同分异构体的是______。
23.化学能在一定条件下可转化为电能。
(1)如图所示装置中锌片是______(填“正极”或“负极”),其电极反应式是______。溶液中H+移向
______(填“锌”或“石墨”)电极。
(2)下列反应通过原电池装置,可实现化学能直接转化为电能的是______(填序号)。
①2H+O=2H O②HCl+NaOH=NaCl+HO
2 2 2 2
24.现代社会生活离不开能量。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用______(填“放热”或“吸热”)
的化学变化或物理变化。
(2)“即热饭盒”给人们生活带来方便,它可利用下面______(填序号)反应释放的热量加热食物。
A.生石灰和水B.Ba(OH) ·8H O和NH Cl
2 2 4
(3)天然气的主要成分是甲烷,它是一种清洁能源。甲烷燃烧是______(填“放热”或“吸热”)反应,其能
量变化可用如图中的______(填序号)表示。
25.NH 具有广泛的用途。实验室常用如图所示装置制取并收集NH 。
3 3(1)实验室用NH Cl和Ca(OH) 制取NH 的化学方程式为______。
4 2 3
(2)干燥NH 应选用的干燥剂是______。
3
(3)图1中方框内收集NH 的装置可选用图2中的______(填序号)。
3
(4)尾气处理装置中使用倒置漏斗 的作用是______。
26.化学反应的速率和限度对人类生产生活有重要的意义。
(1)已知NaSO+HSO=NaSO+S↓+SO+HO。甲同学通过测定该反应发生时溶液变浑浊的时间,研究外
2 2 3 2 4 2 4 2 2
界条件对化学反应速率的影响,设计实验如下(所取溶液体积均为2 mL):
实验编号 温度/℃ c(Na SO)/mol·L-1 c(H SO )/mol·L-1
2 2 3 2 4
Ⅰ 25 0.1 0.1
Ⅱ 25 0.2 0.1
Ⅲ 50 0.2 0.1
①上述实验中溶液最先变浑浊的是______(填实验编号,下同)。
②为探究浓度对化学反应速率的影响,应选择______和______。
(2)某温度下,在1 L密闭容器中,发生反应:2X(g)+Y(g) 2Z(g),X的物质的量随时间的变化如下
表:
时间/s 0 1 2 3 4 5
X的物质的量/mol 0.02 0.01 0.008 0.007 0.007 0.007
①用X的浓度变化表示0~2 s的平均化学反应速率为______mol/(L·s)。
②在3 s以后X的浓度不再改变,反应达到了______状态。
③能说明该反应已达到化学平衡状态的是______(填序号)。
A.v (X)=v (X)
正 逆
B.单位时间内有2 mol X生成同时有1 mol Y生成
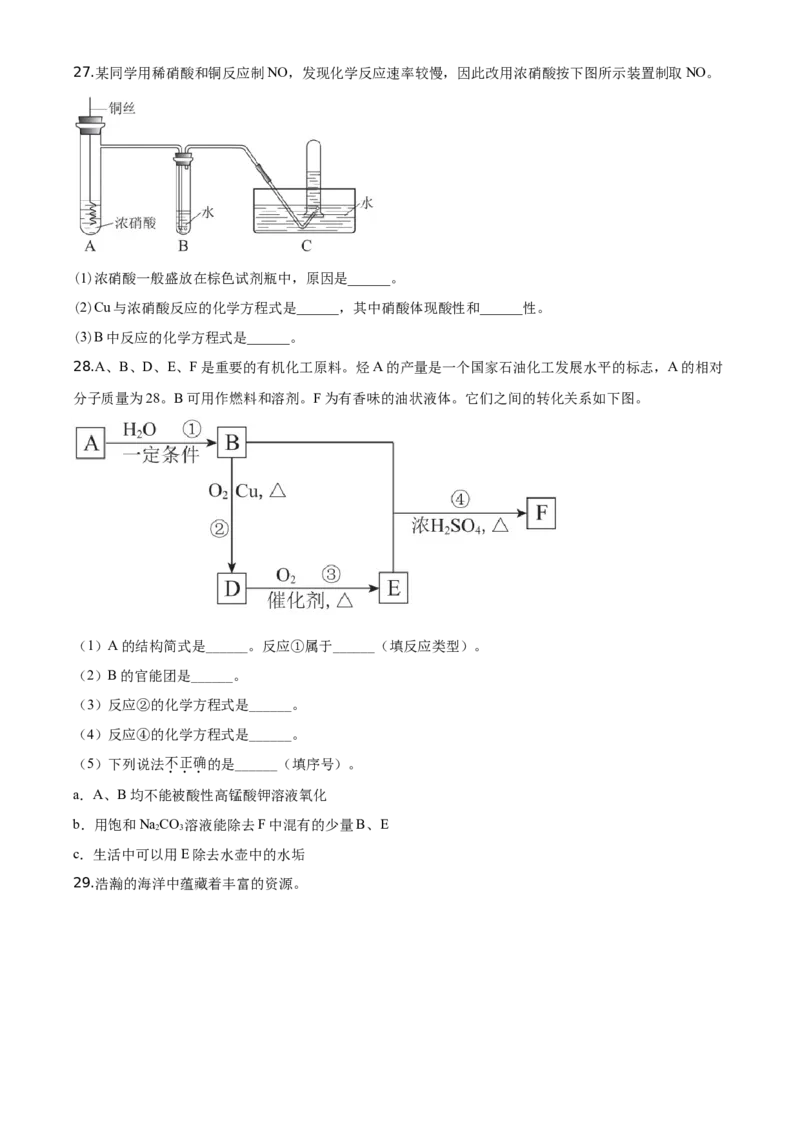
C.X、Y、Z的分子数之比为2∶1∶227.某同学用稀硝酸和铜反应制NO,发现化学反应速率较慢,因此改用浓硝酸按下图所示装置制取NO。
(1)浓硝酸一般盛放在棕色试剂瓶中,原因是______。
(2)Cu与浓硝酸反应的化学方程式是______,其中硝酸体现酸性和______性。
(3)B中反应的化学方程式是______。
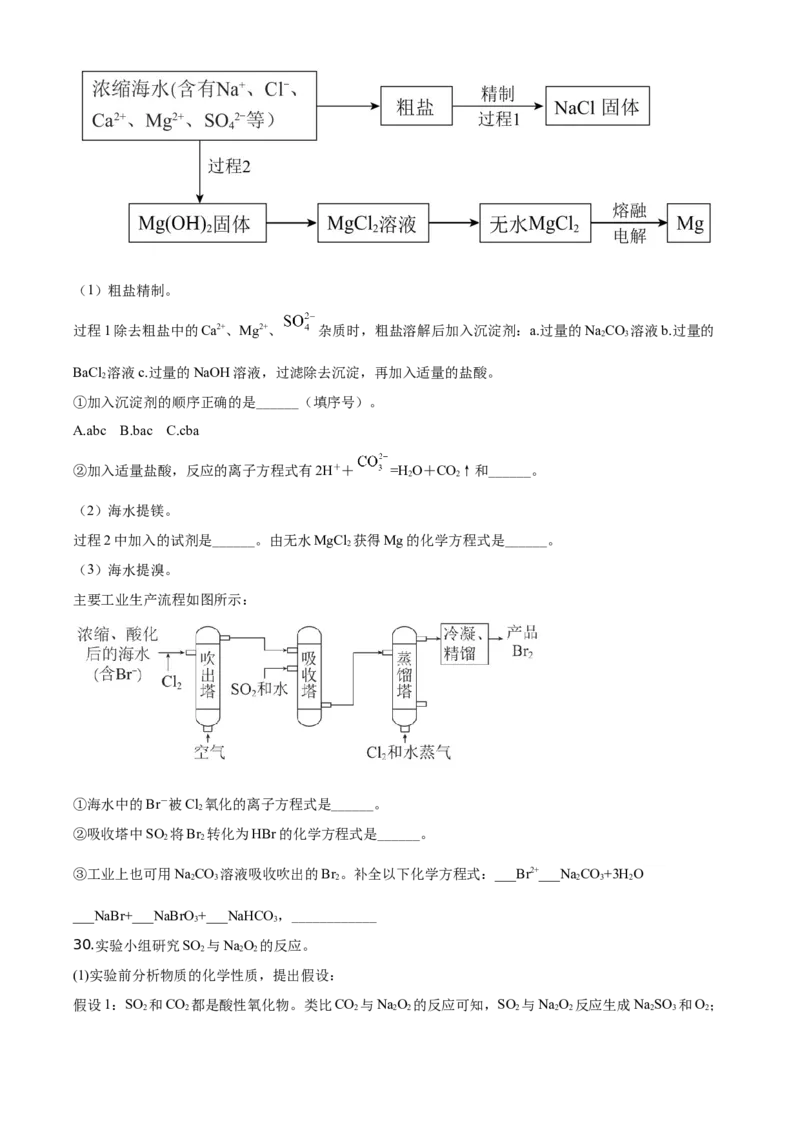
28.A、B、D、E、F是重要的有机化工原料。烃A的产量是一个国家石油化工发展水平的标志,A的相对
分子质量为28。B可用作燃料和溶剂。F为有香味的油状液体。它们之间的转化关系如下图。
(1)A的结构简式是______。反应①属于______(填反应类型)。
(2)B的官能团是______。
(3)反应②的化学方程式是______。
(4)反应④的化学方程式是______。
(5)下列说法不正确的是______(填序号)。
a.A、B均不能被酸性高锰酸钾溶液氧化
b.用饱和NaCO 溶液能除去F中混有的少量B、E
2 3
c.生活中可以用E除去水壶中的水垢
29.浩瀚的海洋中蕴藏着丰富的资源。(1)粗盐精制。
过程1除去粗盐中的Ca2+、Mg2+、 杂质时,粗盐溶解后加入沉淀剂:a.过量的NaCO 溶液b.过量的
2 3
BaCl 溶液c.过量的NaOH溶液,过滤除去沉淀,再加入适量的盐酸。
2
①加入沉淀剂的顺序正确的是______(填序号)。
A.abc B.bac C.cba
②加入适量盐酸,反应的离子方程式有2H++ =H O+CO↑和______。
2 2
(2)海水提镁。
过程2中加入的试剂是______。由无水MgCl 获得Mg的化学方程式是______。
2
(3)海水提溴。
主要工业生产流程如图所示:
①海水中的Br-被Cl 氧化的离子方程式是______。
2
②吸收塔中SO 将Br 转化为HBr的化学方程式是______。
2 2
③工业上也可用NaCO 溶液吸收吹出的Br 。补全以下化学方程式:___Br2+___NaCO+3H O
2 3 2 2 3 2
___NaBr+___NaBrO +___NaHCO,____________
3 3
30.实验小组研究SO 与NaO 的反应。
2 2 2
(1)实验前分析物质的化学性质,提出假设:
假设1:SO 和CO 都是酸性氧化物。类比CO 与NaO 的反应可知,SO 与NaO 反应生成NaSO 和O;
2 2 2 2 2 2 2 2 2 3 2假设2:SO 具有______性,SO 与NaO 反应生成NaSO 。
2 2 2 2 2 4
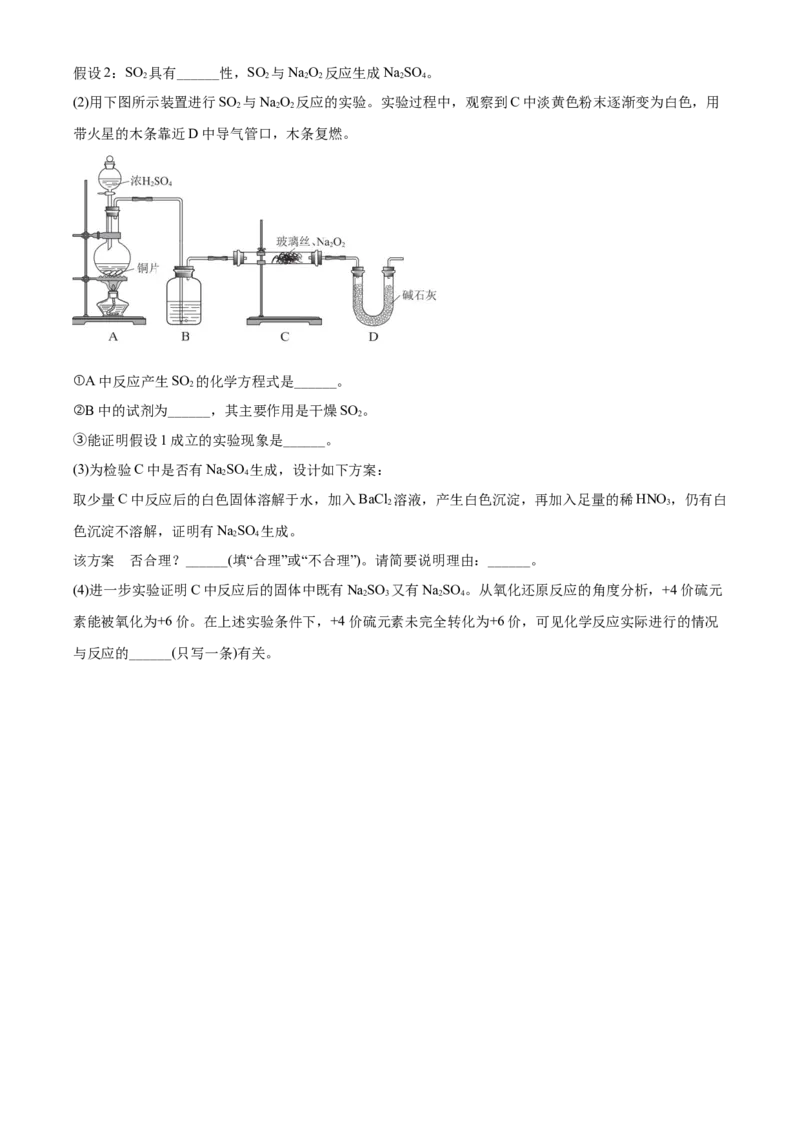
(2)用下图所示装置进行SO 与NaO 反应的实验。实验过程中,观察到C中淡黄色粉末逐渐变为白色,用
2 2 2
带火星的木条靠近D中导气管口,木条复燃。
①A中反应产生SO 的化学方程式是______。
2
②B中的试剂为______,其主要作用是干燥SO 。
2
③能证明假设1成立的实验现象是______。
(3)为检验C中是否有NaSO 生成,设计如下方案:
2 4
取少量C中反应后的白色固体溶解于水,加入BaCl 溶液,产生白色沉淀,再加入足量的稀HNO,仍有白
2 3
色沉淀不溶解,证明有NaSO 生成。
2 4
该方案 是否合理?______(填“合理”或“不合理”)。请简要说明理由:______。
(4)进一步实验证明C中反应后的固体中既有NaSO 又有NaSO 。从氧化还原反应的角度分析,+4价硫元
2 3 2 4
素能被氧化为+6价。在上述实验条件下,+4价硫元素未完全转化为+6价,可见化学反应实际进行的情况
与反应的______(只写一条)有关。