文档内容
单元综合测试
可能用到的相对原子质量:H:1 O:16 C:12 N:14 Na:23 Cl:35.5 K:39 P:31
Ca:40
一、选择题
1.下列物质中属于复合肥料的是( )
A.KCO B.CO(NH ) C.KNO D.Ca(HPO )
2 3 2 2 3 2 4 2
2.下列物质中属于盐的是( )
A.NaCl B.CO C.NaOH D.HSO
2 2 4
3.氮肥能促进作物的茎、叶生长茂盛,叶色浓绿;钾肥能促进作物茎秆健壮,增强抗倒伏
能力;磷肥能促进作物根系发达.小李家的庄稼茎秆细小,出现倒伏现象,则小李家庄稼可选
择施用的化肥是( )
A.碳铵(NH HCO ) B.磷矿粉[Ca (PO )]
4 3 3 4 2
C.磷酸氢三铵[(NH )HPO ] D.氯化钾[KCl]
4 2 4
4.“分类”是化学学习和研究的重要方法之一,下列分类中不正确的是( )
A.硫酸铜、食盐、纯碱——盐
B.硫酸铵、硝酸铵、尿素——氮肥
C.空气、煤气、碘酒——混合物
D.硫元素、氧元素、氦元素——非金属元素
5.下列物质能大量共存于pH=13的水溶液中的是( )
A.硝酸、氯化钠 B.硝酸钾、氯化铜
C.碳酸铵、熟石灰 D.硝酸钠、氯化钡
6. 宿迁市骆马湖“生态农业科技园区”不仅是农业高新技术示范和推广基地,也将是
一个观光休闲的生态农业园区,在一些生产管理思路上你认为不妥的是( )
A.将农家肥与化肥综合使用,以提高增产效果
B.为了防治病虫害,提高农作物产量,可以大量使用农药
C.种植、养殖、制沼气相结合,既可以改善环境也可以提高农业、畜牧业的产量
D.园区内禁止大量地焚烧农作物秸秆
7.如图11-15所示是某加碘盐包装袋上的部分图表文字(I是碘元素的符号),由此你得
到的信息和作出的推测是 ( )
配料表
氯化钠(NaCl) ≥98.0%(以NaCl计)
碘酸钾(KlO ) (35±15mg/kg(以I计)
3
A.此食盐是纯净物B.“加碘盐”中的碘是指碘单质
C.1kg此食盐中含碘酸钾(35±15)mg
D.“菜未炒熟不宜加入碘盐”的原因可能是碘酸钾受热不稳定
8.下列各组物质混合后,不产生沉淀和气体,且能得到无色溶液的是 ( )
A.氯化钠溶液和稀硫酸 B.氧化铜粉末和稀硝酸
C.石灰水和稀盐酸 D.氯化铁溶液和烧碱溶液
9.鉴别氯化钠、硝酸根、碳酸钠三种无色溶液时,最好使用的试剂是 ( )
A.稀硝酸 B.硝酸钠
C.盐酸 D.氢氧化钠溶液
10.用括号内的试剂除去下列物质中的杂质,其中不正确的是 ( )
A.氢氧化钠溶液中混有碳酸钠(石灰水)
B.硝酸铜溶液中混有的硝酸银(铜粉)
C.二氧化碳中混有的氯化氢气体(氢氧化钠溶液)
D.氧气混有的水蒸气(浓硫酸)
11.为提高染发剂染色效果,一般先用碱剂等对头发预处理.某碱剂在染发时可闻到刺激
性气味,该气体能使湿润的红色石蕊试纸变蓝.则该气体为 ( )
A.CO B.O C.NH D.H
2 2 3 2
12.小雨的妈妈买了一条黄金项链,小雨想通过实验探究这条黄金项链是否为锌铜合金
制成的仿制品,她不能选用的试剂是 ( )
A.AlCl 溶液 B.Cu(NO) 溶液
3 3 2
C.H SO 溶液 D.AgNO 溶液
2 4 3
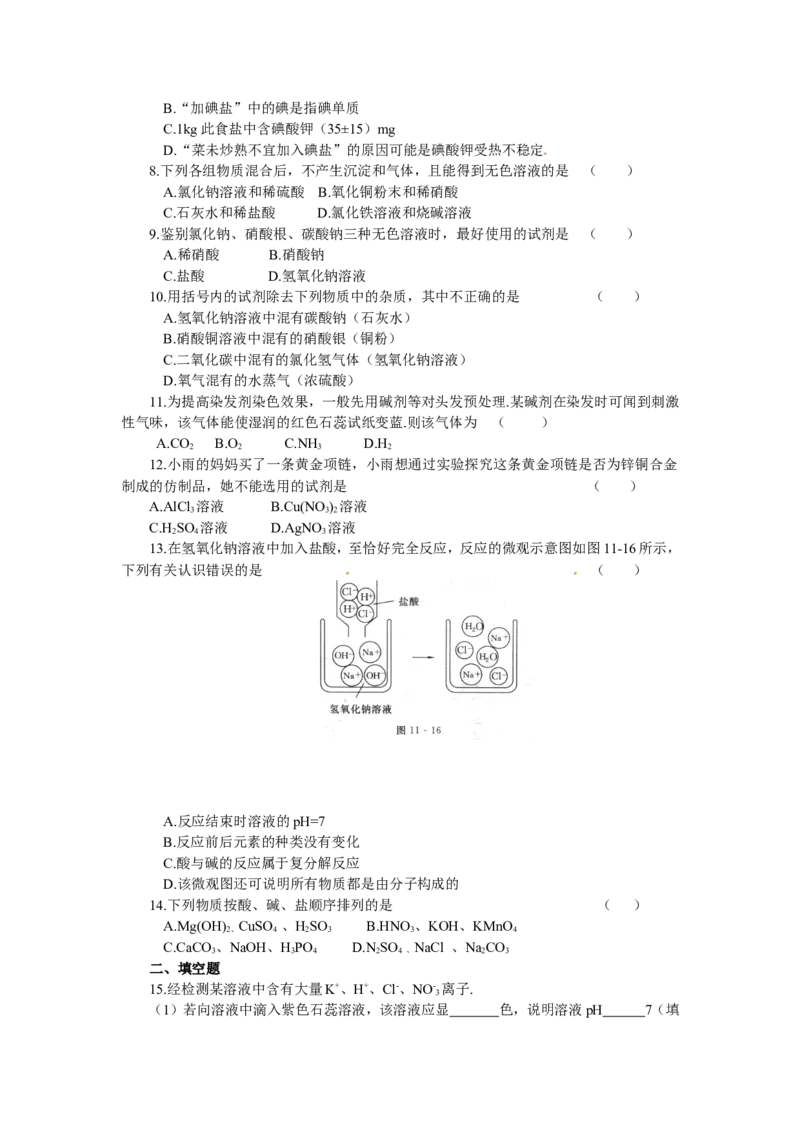
13.在氢氧化钠溶液中加入盐酸,至恰好完全反应,反应的微观示意图如图11-16所示,
下列有关认识错误的是 ( )
A.反应结束时溶液的pH=7
B.反应前后元素的种类没有变化
C.酸与碱的反应属于复分解反应
D.该微观图还可说明所有物质都是由分子构成的
14.下列物质按酸、碱、盐顺序排列的是 ( )
A.Mg(OH) CuSO 、HSO B.HNO 、KOH、KMnO
2、 4 2 3 3 4
C.CaCO 、NaOH、HPO D.NSO NaCl 、NaCO
3 3 4 2 4 、 2 3
二、填空题
15.经检测某溶液中含有大量K+、H+、Cl-、NO- 离子.
3
(1)若向溶液中滴入紫色石蕊溶液,该溶液应显 色,说明溶液pH 7(填“大于”“小于”或“等于”),若要配制该溶液,可以用盐酸和硝酸钾,也可以用 和
配制.
(2)若要除去溶液中的氯化物,而不引入其他杂质,宜加入适量试剂是 .
16.请结合图11-17提供的信息,回答下列问题:
(1)氯元素的原子序数为 .
(2)氯原子在化学反应中易 (填“得到”或“失
去”)电子.
(3)氯化钾是一种常见的钾肥,其化学式为 .
17.环境问题是人类可持续发展必须解决的一个重要问题.某校科学课外活动小组在一次
“环保”主题实践活动中,对小河旁两座化工厂的废水排放问题进行调查发现:①甲、乙两
厂排出的废水均澄清透明;②两厂废水中共含K+、H+、Ba2+、OH-、NO-、CO2- 六种离子,且每
3 3
厂各含三种不同的离子,两厂废水单独排放都会造成严重的污染.该活动小组的同学用所学
的科学知识,对两厂的废水进行探究后发出,若将两厂的废水按一定比例混合,经充分反应
及沉淀后,废水会变成只含一种溶质的无色澄清溶液,此溶质可做化肥.
(1)此可做化肥的溶质为 (填写物质的化学式).
(2)经检测甲厂废水明显呈碱性,则甲厂排放的废水中含有的三种离子是 .
18.(1)含有较多可溶性钙、镁化合物的水叫做硬水,生活中可以通过 的方法来降
低水的硬度.
(2)民间有“石灰煮鸡蛋”的说法,即生石灰与水反应时,能将鸡蛋煮熟,其原因是
.
19.下表是某实验报告中的一组数据:
实验序号 试剂1 试剂2 混合前温度/℃ 混合后最高或最
低温度/℃
① 3.2ml水 3.2gNa CO 固体 20 24.3(t)
2 3 1
② 35mL稀盐酸 3.2gNa CO 固体 20 25.1(t)
2 3 2
③ 35mL水 2.5gNaHCO 固体 20 18.5(t)
3 3
④ 35mL稀盐酸 2.5gNaHCO 固体 20 16.2(t)
3 4
(1)从实验①、③数据可知:NaCO 溶于水 热量,NaHCO 溶于水 热量.
2 3 3
(填“放出”或“吸收”)
(2)根据t t 可知NaCO 与稀盐酸反应 热量,根据t t 可知:NaHCO 与稀盐酸
2>1 2 3 4<3 3
反应 热量.(填“放出”或“吸收”)
三、实验题
20.查阅资料知道,鸡蛋壳的主要成分是碳酸钙.某同学为了验证鸡蛋壳的主要成分是碳
酸钙,设计了如图11-18所示的实验.
(1)实验过程中看到的现象 .
(2)小明认为该实验方案不完整,还需验证鸡蛋壳的主要成
分属于钙盐,方法是取反应后的上层清液加入 (填字母).
A.Na CO 溶液
2 3
B.AgNO 溶液
3
C.NaCl溶液
D.Ca(OH) 溶液
2(3)鸡蛋壳与盐酸反应的化学方程式为: .
21.在我市的化学实验操作考试中,有个实验是用温度计分别测定硝酸铵、氢氧化钠、氯
化钠溶于水后溶液温度的变化,实验完毕某班的同学们将废液倒入一个废液缸中,结果产生
了大量的有刺激性气味气体,让同学们个个眼泪汪汪,尝到了不按规定操作的苦头.请你写出
有关反应的化学方程式: .
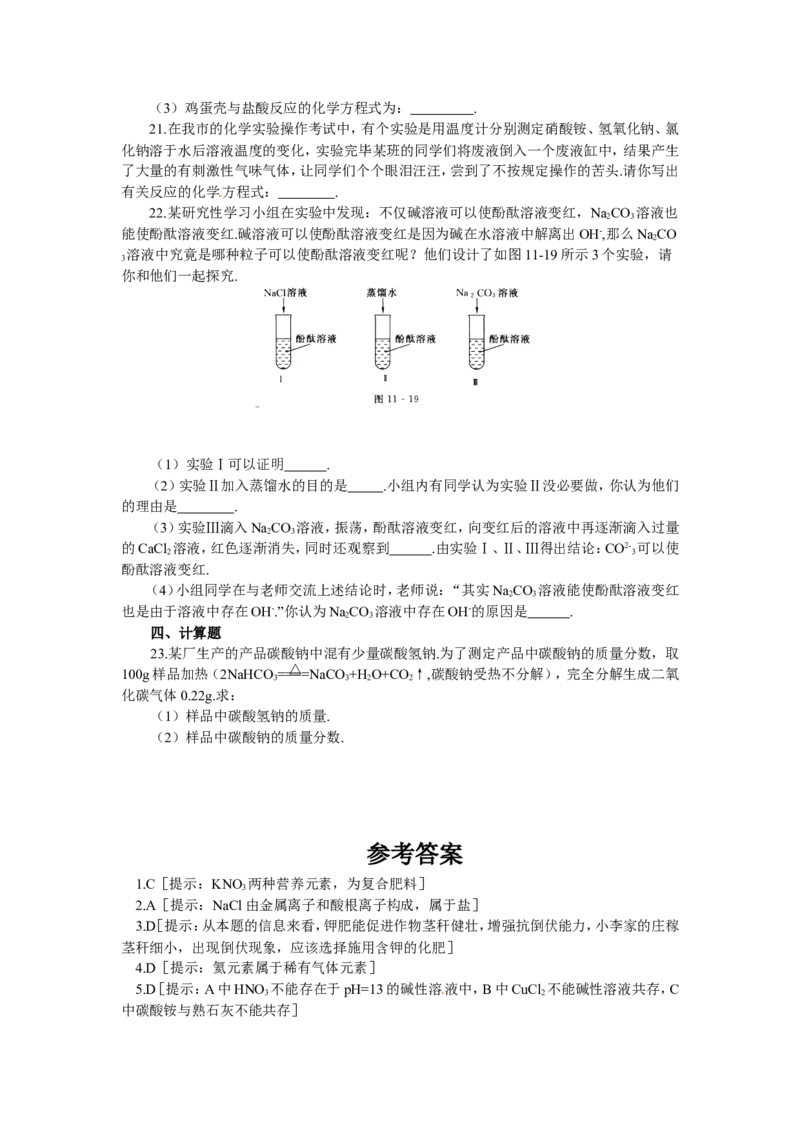
22.某研究性学习小组在实验中发现:不仅碱溶液可以使酚酞溶液变红,NaCO 溶液也
2 3
能使酚酞溶液变红.碱溶液可以使酚酞溶液变红是因为碱在水溶液中解离出OH-,那么NaCO
2
溶液中究竟是哪种粒子可以使酚酞溶液变红呢?他们设计了如图11-19所示3个实验,请
3
你和他们一起探究.
(1)实验Ⅰ可以证明 .
(2)实验Ⅱ加入蒸馏水的目的是 .小组内有同学认为实验Ⅱ没必要做,你认为他们
的理由是 .
(3)实验Ⅲ滴入NaCO 溶液,振荡,酚酞溶液变红,向变红后的溶液中再逐渐滴入过量
2 3
的CaCl 溶液,红色逐渐消失,同时还观察到 .由实验Ⅰ、Ⅱ、Ⅲ得出结论:CO2- 可以使
2 3
酚酞溶液变红.
(4)小组同学在与老师交流上述结论时,老师说:“其实NaCO 溶液能使酚酞溶液变红
2 3
也是由于溶液中存在OH-.”你认为NaCO 溶液中存在OH-的原因是 .
2 3
四、计算题
23.某厂生产的产品碳酸钠中混有少量碳酸氢钠.为了测定产品中碳酸钠的质量分数,取
△
100g样品加热(2NaHCO ====NaCO +H O+CO↑,碳酸钠受热不分解),完全分解生成二氧
3 3 2 2
化碳气体0.22g.求:
(1)样品中碳酸氢钠的质量.
(2)样品中碳酸钠的质量分数.
参考答案
1.C[提示:KNO 两种营养元素,为复合肥料]
3
2.A[提示:NaCl由金属离子和酸根离子构成,属于盐]
3.D[提示:从本题的信息来看,钾肥能促进作物茎秆健壮,增强抗倒伏能力,小李家的庄稼
茎秆细小,出现倒伏现象,应该选择施用含钾的化肥]
4.D[提示:氦元素属于稀有气体元素]
5.D[提示:A中HNO 不能存在于pH=13的碱性溶液中,B中CuCl 不能碱性溶液共存,C
3 2
中碳酸铵与熟石灰不能共存]6.B[提示:大量使用农药会污染环境]
7.D[提示:根据文字说明可知,此加碘盐为混合物,这里碘指碘元素,1kg此食盐中含碘元
素(35±15mg)
8.C[提示:石灰水与稀盐酸反应生成氯化钙和水,形成无色溶液]
9.C[提示:盐酸遇碳酸钠溶液产生气泡,遇硝酸银溶液产生白色沉淀,遇氯化钠溶液无明
显现象]
10.C[提示:氢氧化钠溶液不但能和氯化氢气体反应,而且还能和CO 反应]
2
11.C[提示:NH 有刺激性气味,溶于水显碱性,能使湿润的红色石蕊试纸变蓝]
3
12.A[提示Cu、Zn、都不能与AlCl 溶液反应,因为Al比Zn、Cu活泼]
3
13.D[提示:NaCl由Na+和Cl-构成]
14.B[提示:HNO 电离时生成的阳离子全部是H+,属于酸;KOH电离是生成的阴离子全
3
部是OH-,属于碱;KMnO 电离时生成金属离子(K+)和酸根离子(MnO-),属于盐]
4 4
15(. 1)小红;小于;KCl ;HNO (2)AgNO[提示:溶液中含大量H+,显酸性,pH<7,使紫色
3 3
石蕊溶液变红;这四种粒子既可形成
HCl和KNO,也可形成KCI和HNO.Ag+和CI-会生成AgCl沉淀]
3 3
16.(1)17
(2)得到、(3)KCl[提示:(1)从题给信息可以看出,氯元素的原子序数为17.(2)氯原
子的最外层电子数为7,属于非金属元素,在化学反应中,易得到1个电子,显-1价.
(3)根据元素的化合价,不难写出氯化钾的化学式]
17.(1)KNO (2)K+、OH-、
3
CO2- [提示:KNO 中含K、N两种营养元素,为复合肥料;甲厂废水呈碱性,一定含
3 3
OH-,则不能含H+,而CO2- 与Ba2+不能共存,CO2- 与H+不能共存,故甲厂排放
3 3
的废水中一定含K+、OH-、CO2-]
3
18.(1)煮沸 (2)生石灰与水反应是放热反应
(3)过磷酸钙;氯化钾[提示:(1)工业和科学实验中软化硬水的方法很多,在生活中常
通过煮沸的方法降低水的硬度.(2)生石灰与水反应时,放出大量的热,从而将鸡蛋煮
熟.(3)观察外观,白色晶体是硫酸铵和氯化钾,灰白色粉末是过磷酸钙;钾肥能促进
植物生长,增强农作物的抗倒伏能力,氯化钾是钾肥]
19 (1)放出;吸收 (2)放出;
吸收[提示:(1)对比实验①、③数据可知,NaCO 溶于水,温度由20℃升高到
2 3
24.3℃,说明放出热量,NaHCO 溶于水,温度由20℃降低到18.5℃,说明吸收热
3
量.(2)对比实验①、②数据可知,3.2 gNaCO 固体溶于35 mL水,温度由20℃升
2 3
高到24.3℃(t ),而3.2 g NaCO 固体与35 mL稀盐酸混合,温度由20℃升高到
1 2 3
25.1℃(t),比其溶于水温度升得更高了,即t>t,说明NaCO 与稀盐酸反应放
2 2 1 2 3
出热量;同样道理,对比实验③、④数据可知,NaHCOa固体与稀盐酸混合,温度由
20℃降低到16.2℃,比其溶于水温度降得更低了,即t