文档内容
北京市首师大附中 2019 级高一化学结业考试试题
一、单选题
1. 向浓硫酸中分别加入下列三种固体,对实验现象的分析正确的是( )
A. 对比实验①和②可知还原性:Br->Cl-
B. 对比实验①和③可知氧化性:Br >SO
2 2
C. 对比实验②和③可知酸性:HSO >HCl>HSO
2 4 2 3
D. 由实验可知浓硫酸具有强酸性、难挥发性、氧化性、脱水性
2. 对下列事实的解释错误的是
A. 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性
B. 浓硝酸在光照条件下颜色变黄,说明浓硝酸不稳定
C. 常温下浓硫酸、浓硝酸可以用铝罐贮存,说明浓硫酸、浓硝酸与铝不反应
D. 反应CuSO +H S=CuS↓+H SO 说明硫化铜既不溶于水,也不溶于稀硫酸
4 2 2 4
3. 足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO、NO 的混合气体,这些气体与1.68LO (标准状况
2 2
下)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol/LNaOH溶液至
Cu2+恰好完全沉淀,则消耗溶液NaOH的体积是( )
A. 60mL B. 45mL C. 30mL D. 15mL
4. 在标准状况下,在三个干燥的烧瓶内分别装有:①干燥且纯净的NH ;②含一半空气的氯化氢气体;
3
③NO 和O 体积比为4:1的混合气体。然后分别做喷泉实验,实验结束后假设三个烧瓶中所得溶液不扩
2 2
散,则三个烧瓶中所得溶液的物质的量浓度之比为
A. 5:5:4 B. 2:1:2 C. 1:1:1 D. 无法确定
5. X、Y、Z、N是短周期主族元素,且原子序数依次增大。已知X的最外层电子数是电子层数的3倍,
X、Z同主族,Y的原子在短周期主族元素中原子半径最大。下列说法正确的是
A. 可以用CS 洗涤附着在试管壁上的Z单质
2
B. YX和YX 都是碱性氧化物
2 2 2
C. Z与X形成的化合物对应的水化物一定是强酸
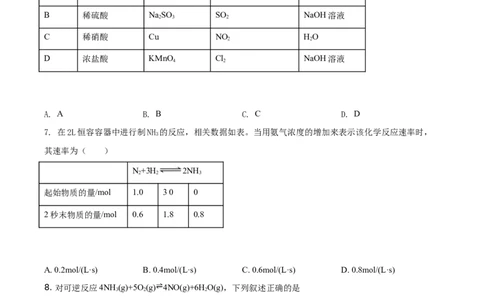
D. Z元素的非金属性比N元素的非金属性强6. 实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中
提供的物质完成相关实验,最合理的选项是
选项 a中的物质 b中的物质 c中收集的气体 d中的物质
A 浓氨水 CaO NH HO
3 2
B 稀硫酸 NaSO SO NaOH溶液
2 3 2
C 稀硝酸 Cu NO HO
2 2
D 浓盐酸 KMnO Cl NaOH溶液
4 2
A. A B. B C. C D. D
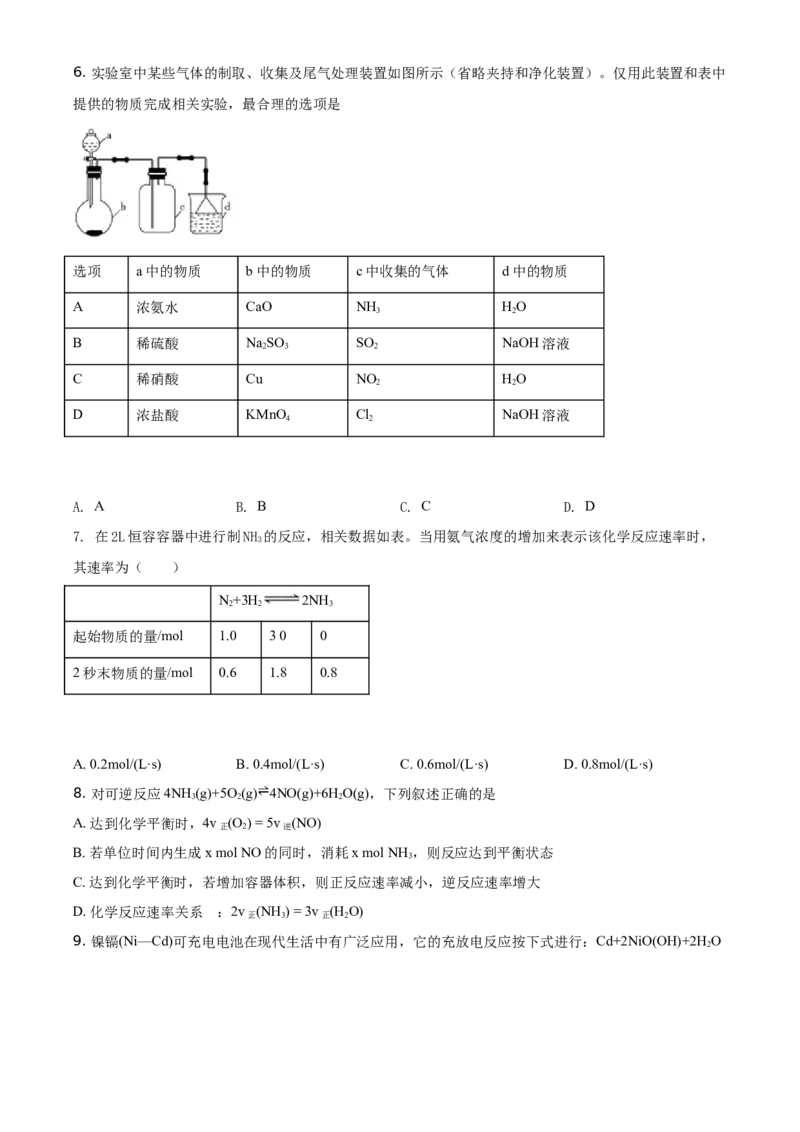
7. 在2L恒容容器中进行制NH 的反应,相关数据如表。当用氨气浓度的增加来表示该化学反应速率时,
3
其速率为( )
N+3H 2NH
2 2 3
.
起始物质的量/mol 1.0 30 0
2秒末物质的量/mol 0.6 1.8 0.8
A. 0.2mol/(L·s) B. 0.4mol/(L·s) C. 0.6mol/(L·s) D. 0.8mol/(L·s)
8. 对可逆反应4NH (g)+5O(g) 4NO(g)+6H O(g),下列叙述正确的是
3 2 2
A. 达到化学平衡时,4v (O ) = 5v (NO)
正 2 逆
B. 若单位时间内生成x mol NO的同时,消耗x mol NH ,则反应达到平衡状态
3
C. 达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D. 化学反应速率关系 是:2v (NH ) = 3v (H O)
正 3 正 2
9. 镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:Cd+2NiO(OH)+2H O
2Cd(OH) +2Ni(OH) ;由此可知,该电池放电时的负极材料是
2 2
A. Cd B. Ni(OH) C. Cd(OH) D. NiO(OH)
2 2
10. 有A、B、C、D四块金属片,进行如下实验,①A、B用导线相连后,同时插入稀HSO 中,A极为
2 4
负极 ②C、D用导线相连后,同时浸入稀HSO 中,电子由C→导线→D ③A、C相连后,同时浸入稀
2 4
HSO ,C极产生大量气泡 ④B、D相连后,同时浸入稀HSO 中,D极发生氧化反应,则四种金属的活动
2 4 2 4
性顺序为:
A. A>B>C>D B. A>C>D>B C. C>A>B>D D. B>D>C>A
11. 在密闭容器中X (g)+2Y (g) Z(g)的反应,X、Y、Z的起始浓度依次为0.2mol/L、0.3mol/L、
2 2 2 2
0.3mol/L,当反应达到其最大限度(即化学平衡状态)时,各物质的浓度有可能的是( )
A. c(Z) ═0.45mol/L B. c(X) ═0.3mol/L
2
C. c(X) ═0.5mol/L D. c(Y ) ═0.5mol/L
2 2
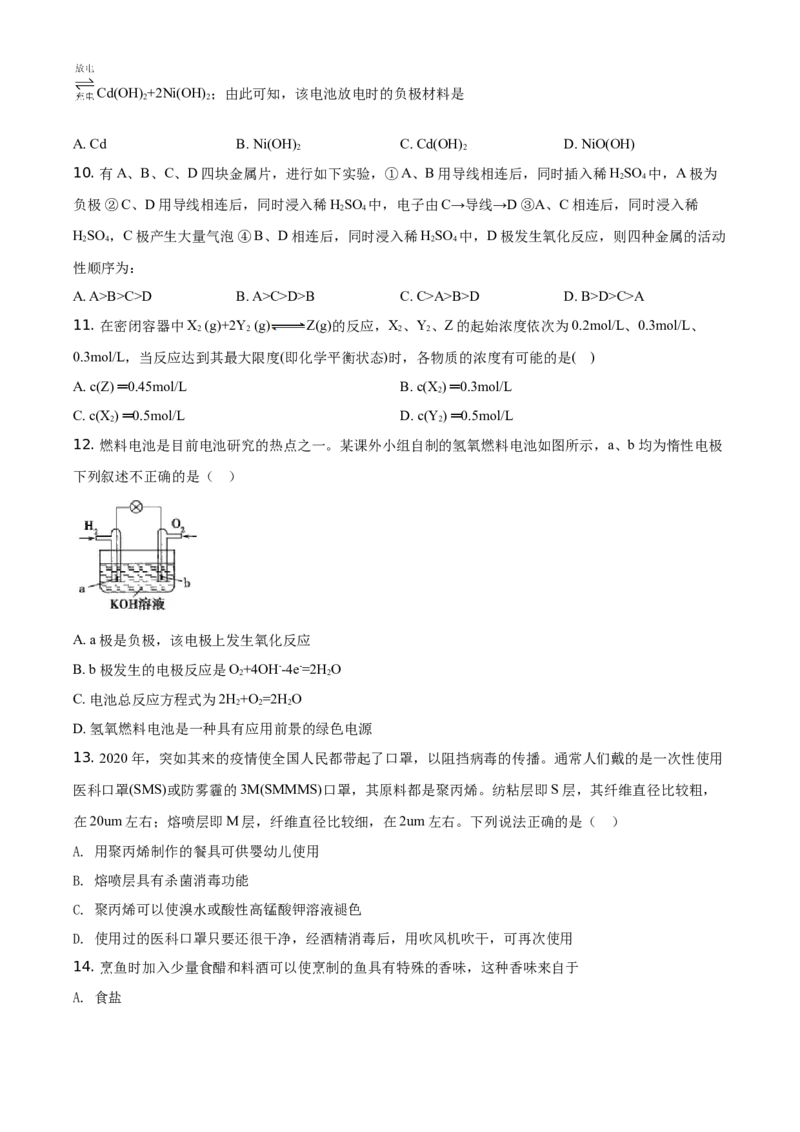
12. 燃料电池是目前电池研究的热点之一。某课外小组自制的氢氧燃料电池如图所示,a、b均为惰性电极
下列叙述不正确的是( )
A. a极是负极,该电极上发生氧化反应
B. b极发生的电极反应是O+4OH--4e-=2H O
2 2
C. 电池总反应方程式为2H+O =2H O
2 2 2
D. 氢氧燃料电池是一种具有应用前景的绿色电源
13. 2020年,突如其来的疫情使全国人民都带起了口罩,以阻挡病毒的传播。通常人们戴的是一次性使用
医科口罩(SMS)或防雾霾的3M(SMMMS)口罩,其原料都是聚丙烯。纺粘层即S层,其纤维直径比较粗,
在20um左右;熔喷层即M层,纤维直径比较细,在2um左右。下列说法正确的是( )
A. 用聚丙烯制作的餐具可供婴幼儿使用
B. 熔喷层具有杀菌消毒功能
C. 聚丙烯可以使溴水或酸性高锰酸钾溶液褪色
D. 使用过的医科口罩只要还很干净,经酒精消毒后,用吹风机吹干,可再次使用
14. 烹鱼时加入少量食醋和料酒可以使烹制的鱼具有特殊的香味,这种香味来自于
A. 食盐B. 食醋中的乙酸
C. 料酒中的乙醇
D. 料酒中的乙醇与食醋中的乙酸反应生成的乙酸乙酯
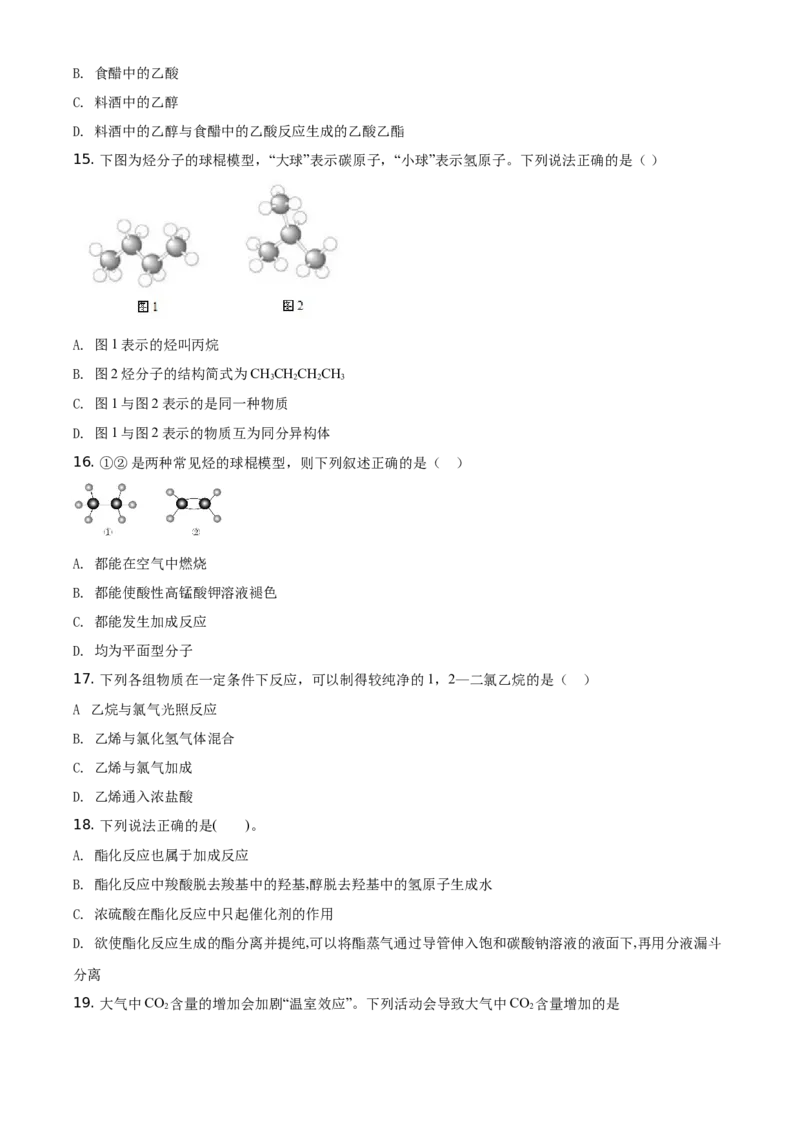
15. 下图为烃分子的球棍模型,“大球”表示碳原子,“小球”表示氢原子。下列说法正确的是( )
A. 图1表示的烃叫丙烷
B. 图2烃分子的结构简式为CHCHCHCH
3 2 2 3
C. 图1与图2表示的是同一种物质
D. 图1与图2表示的物质互为同分异构体
16. ①②是两种常见烃的球棍模型,则下列叙述正确的是( )
A. 都能在空气中燃烧
B. 都能使酸性高锰酸钾溶液褪色
C. 都能发生加成反应
D. 均为平面型分子
17. 下列各组物质在一定条件下反应,可以制得较纯净的1,2—二氯乙烷的是( )
.
A 乙烷与氯气光照反应
B. 乙烯与氯化氢气体混合
C. 乙烯与氯气加成
D. 乙烯通入浓盐酸
18. 下列说法正确的是( )。
A. 酯化反应也属于加成反应
B. 酯化反应中羧酸脱去羧基中的羟基,醇脱去羟基中的氢原子生成水
C. 浓硫酸在酯化反应中只起催化剂的作用
D. 欲使酯化反应生成的酯分离并提纯,可以将酯蒸气通过导管伸入饱和碳酸钠溶液的液面下,再用分液漏斗
分离
19. 大气中CO 含量的增加会加剧“温室效应”。下列活动会导致大气中CO 含量增加的是
2 2A. 燃烧煤炭供热 B. 利用风力发电 C. 增加植被面积 D. 节约用电用水
20. 下列说法不正确的是
A. 光--电转换的途径可以不需要发生化学反应
B. 天然气和沼气的主要成分都是甲烷,因此都是化石能源
C. 将厨余垃圾中的油脂分离出来,可以制造肥皂和油漆等
D. 人造丝、人造棉和铜氨纤维的主要化学成分都可表示为(C H O)
6 10 5 n
21. 下列因果关系不正确的是( )
选项 原因 结果
A 植树造林 温室效应
B 二氧化硫和二氧化氮大量排放 酸雨
C 汽车尾气的排放 光化学烟雾
D 含氮、磷等元素的生活废水的大量排放 赤潮
A. A B. B C. C D. D
22. 下列有关能源的说法不正确的是
A. 光电转换的基本装置就是太阳能电池,应用相当广泛
B. 利用蓝绿藻等低等植物和微生物在阳光作用下可使水分解产生氢气
C. 贮氢合金的发现和应用,开辟了解决氢气贮存、运输难题的新途径
D. 煤、石油、天然气、氢能中,天然气、氢能是可再生能源
23. 实验室模拟石油的分馏实验中,不需要用到的仪器是( )
A. B. C. D.
24. 化学与生活、生产、社会可持续发展密切相关。下列说法错误的是( )
A. 牙膏中添加的NaPO F、NaF所提供的氟离子浓度相等时,它们防治龋齿的作用相同
2 3
B. “光化学烟雾” “硝酸型酸雨”的形成都与氮氧化合物有关
C. 用聚氯乙烯代替木材,生产快餐盒,以减少木材的使用
D. 碳纳米管比表面积大,可用作新型储氢材料
25. 昆明市预计在2020年底前基本建成生活垃圾分类处理系统。下列关于垃圾处理的说法不正确 的是A. 废旧塑料瓶可回收利用 B. 废旧电池可直接掩埋
C. 电子垃圾可用适当的方法回收利用 D. 厨余垃圾可经生物技术处理堆肥
二、填空题
26. 氮及其化合物之间可以相互转化,请按照要求回答下列问题:
(1)下列有关NO和NO 的描述正确的是__________(填标号)。
2
a.均为无色气体 b.均为大气污染物 c.可用排水集气法收集NO
(2)写出二氧化氮与水反应的化学方程式_______,其中被氧化的N与被还原的N的物质的量之比为
__________。
(3)如下是生成NO 的几个化学反应:
2
①2NO+O =2NO ②Fe+ 6HNO(浓)= Fe (NO ) + 3NO↑+3H O ③4HNO O ↑+4NO↑+2H O
2 2 3 3 3 2 2 3 2 2 2
④NO 2NO
2 4 2
其中体现N元素还原性的是_____ (填标号,下同),体现N元素氧化性的是_____。
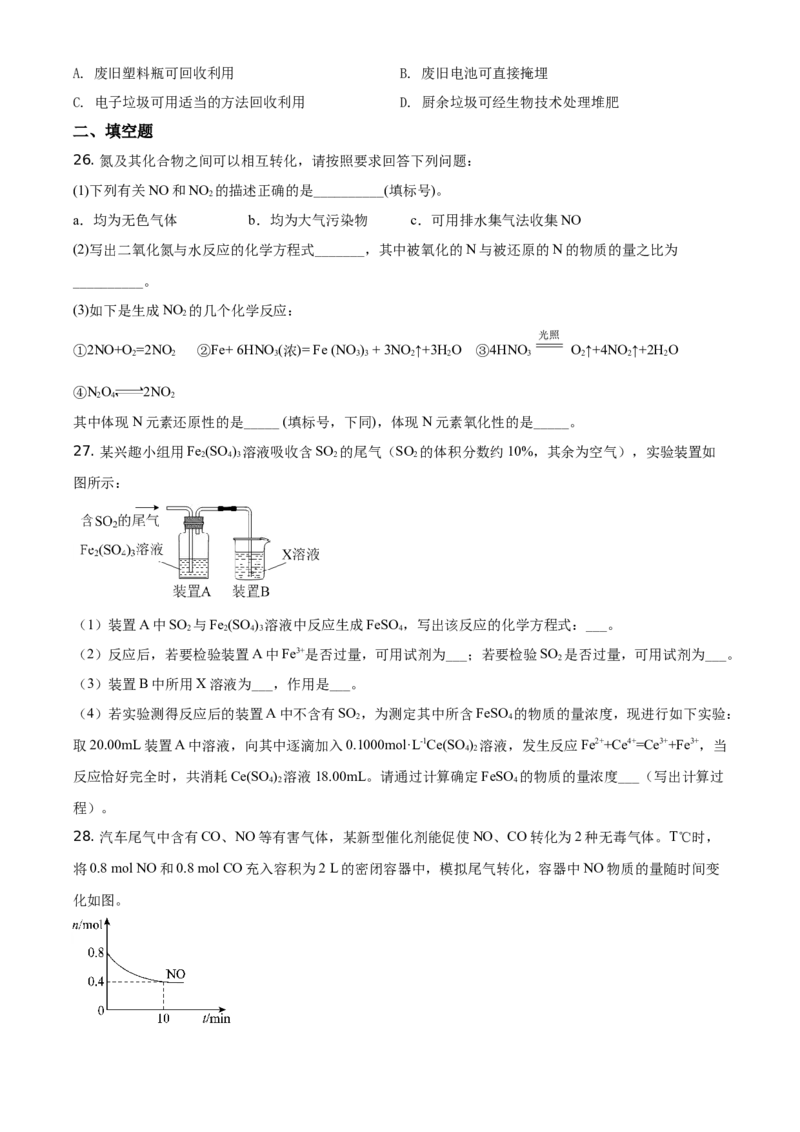
27. 某兴趣小组用Fe (SO ) 溶液吸收含SO 的尾气(SO 的体积分数约10%,其余为空气),实验装置如
2 4 3 2 2
图所示:
(1)装置A中SO 与Fe (SO ) 溶液中反应生成FeSO ,写出该反应的化学方程式:___。
2 2 4 3 4
(2)反应后,若要检验装置A中Fe3+是否过量,可用试剂为___;若要检验SO 是否过量,可用试剂为___。
2
(3)装置B中所用X溶液为___,作用是___。
(4)若实验测得反应后的装置A中不含有SO ,为测定其中所含FeSO 的物质的量浓度,现进行如下实验:
2 4
取20.00mL装置A中溶液,向其中逐滴加入0.1000mol·L-1Ce(SO) 溶液,发生反应Fe2++Ce4+=Ce3++Fe3+,当
4 2
反应恰好完全时,共消耗Ce(SO) 溶液18.00mL。请通过计算确定FeSO 的物质的量浓度___(写出计算过
4 2 4
程)。
28. 汽车尾气中含有CO、NO等有害气体,某新型催化剂能促使NO、CO转化为2种无毒气体。T℃时,
将0.8 mol NO和0.8 mol CO充入容积为2 L的密闭容器中,模拟尾气转化,容器中NO物质的量随时间变
化如图。(1)将NO、CO转化为2种无毒气体的化学方程式是______。
(2)反应开始至10 min,v(NO)=______mol/(L•min)。
(3)下列说法正确的是______。
a.新型催化剂可以加快NO、CO的转化
b.该反应进行到10 min时达到化学平衡状态
c.平衡时CO的浓度是0.4 mol/ L
29. 如图所示是原电池 的装置图。请回答:
(1)若C为稀HSO ,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为
2 4
___;反应进行一段时间后溶液酸性将__(填“增强”“减弱”或“基本不变”)。
(2)若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A(正极)极材料为___,B(负极)极
材料为__,溶液C为___。
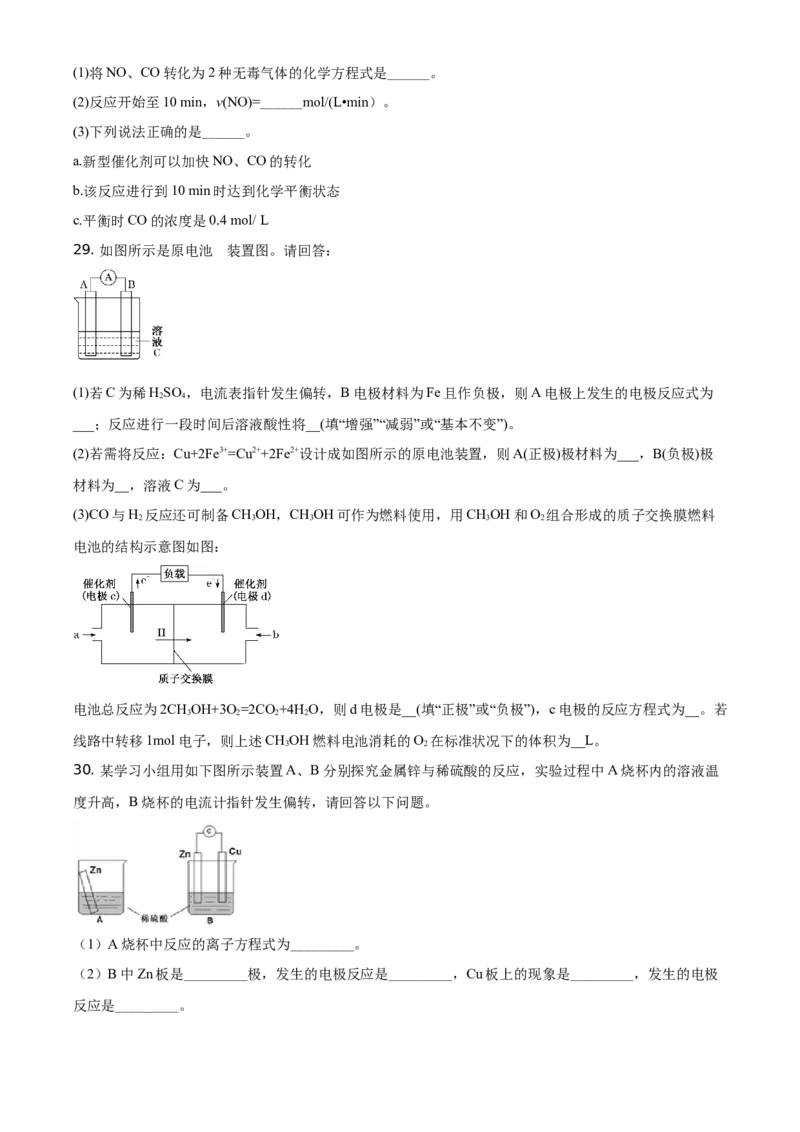
(3)CO与H 反应还可制备CHOH,CHOH可作为燃料使用,用CHOH和O 组合形成的质子交换膜燃料
2 3 3 3 2
电池的结构示意图如图:
电池总反应为2CHOH+3O =2CO +4H O,则d电极是__(填“正极”或“负极”),c电极的反应方程式为__。若
3 2 2 2
线路中转移1mol电子,则上述CHOH燃料电池消耗的O 在标准状况下的体积为__L。
3 2
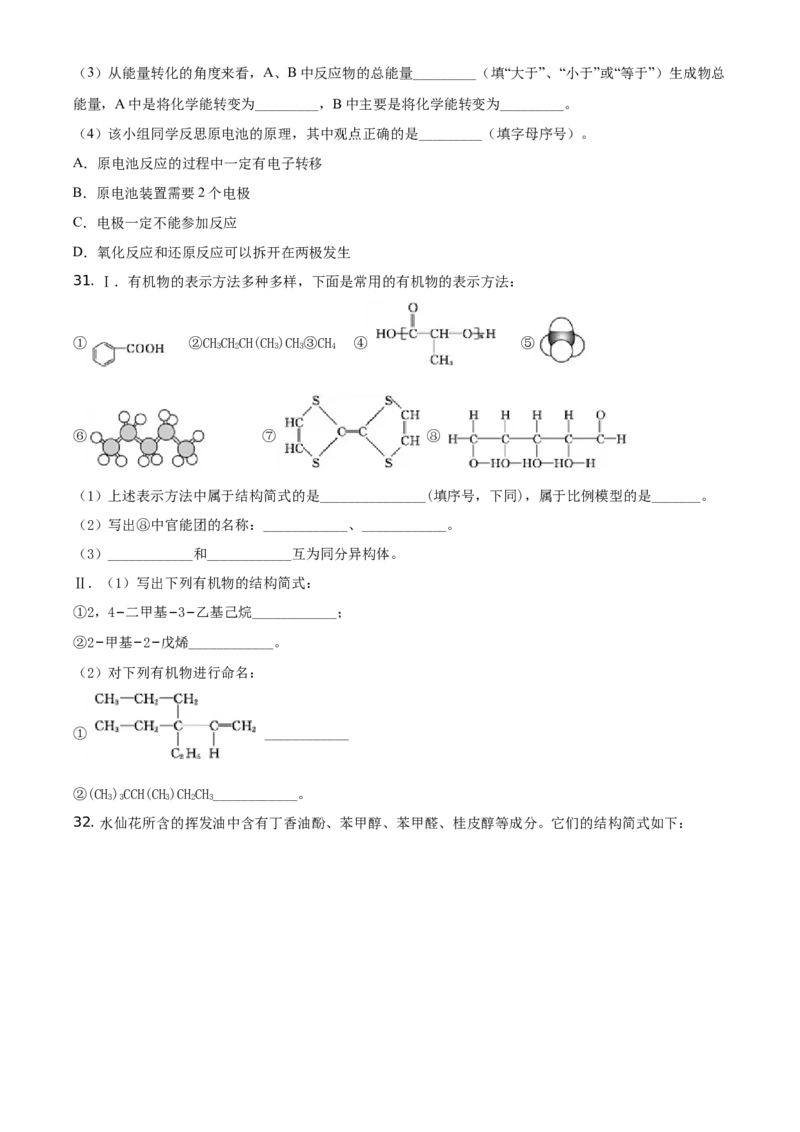
30. 某学习小组用如下图所示装置A、B分别探究金属锌与稀硫酸的反应,实验过程中A烧杯内的溶液温
度升高,B烧杯的电流计指针发生偏转,请回答以下问题。
(1)A烧杯中反应的离子方程式为_________。
(2)B中Zn板是_________极,发生的电极反应是_________,Cu板上的现象是_________,发生的电极
反应是_________。(3)从能量转化的角度来看,A、B中反应物的总能量_________(填“大于”、“小于”或“等于”)生成物总
能量,A中是将化学能转变为_________,B中主要是将化学能转变为_________。
(4)该小组同学反思原电池的原理,其中观点正确的是_________(填字母序号)。
A.原电池反应的过程中一定有电子转移
B.原电池装置需要2个电极
C.电极一定不能参加反应
D.氧化反应和还原反应可以拆开在两极发生
31. Ⅰ.有机物的表示方法多种多样,下面是常用的有机物的表示方法:
① ②CHCHCH(CH)CH③CH ④ ⑤
3 2 3 3 4
⑥ ⑦ ⑧
(1)上述表示方法中属于结构简式的是_______________(填序号,下同),属于比例模型的是_______。
(2)写出⑧中官能团的名称:____________、____________。
(3)____________和____________互为同分异构体。
Ⅱ.(1)写出下列有机物的结构简式:
①2,4−二甲基−3−乙基己烷____________;
②2−甲基−2−戊烯____________。
(2)对下列有机物进行命名:
。
① ____________
②(CH)CCH(CH)CHCH____________。
3 3 3 2 3
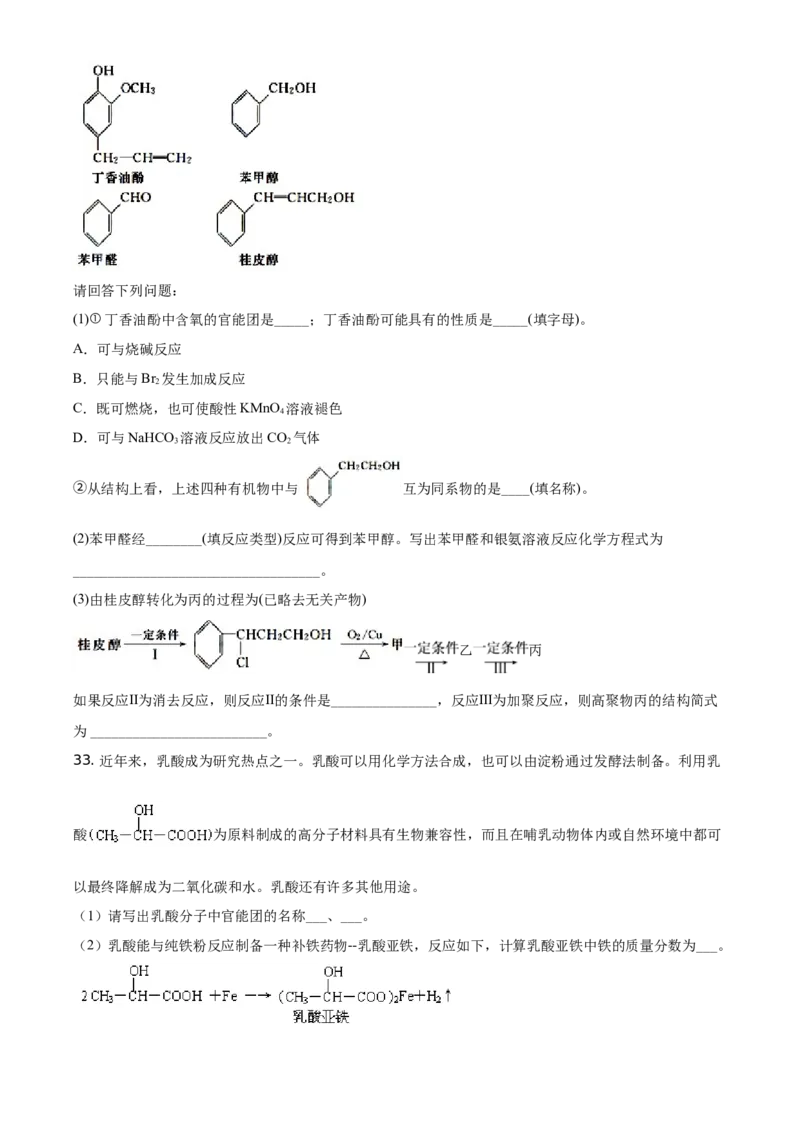
32. 水仙花所含的挥发油中含有丁香油酚、苯甲醇、苯甲醛、桂皮醇等成分。它们的结构简式如下:请回答下列问题:
(1)①丁香油酚中含氧的官能团是_____;丁香油酚可能具有的性质是_____(填字母)。
A.可与烧碱反应
B.只能与Br 发生加成反应
2
C.既可燃烧,也可使酸性KMnO 溶液褪色
4
D.可与NaHCO 溶液反应放出CO 气体
3 2
②从结构上看,上述四种有机物中与 互为同系物的是____(填名称)。
(2)苯甲醛经________(填反应类型)反应可得到苯甲醇。写出苯甲醛和银氨溶液反应化学方程式为
___________________________________。
(3)由桂皮醇转化为丙的过程为(已略去无关产物)
乙 丙
如果反应Ⅱ为消去反应,则反应Ⅱ的条件是_______________,反应Ⅲ为加聚反应,则高聚物丙的结构简式
为 _________________________。
33. 近年来,乳酸成为研究热点之一。乳酸可以用化学方法合成,也可以由淀粉通过发酵法制备。利用乳
酸 为原料制成的高分子材料具有生物兼容性,而且在哺乳动物体内或自然环境中都可
以最终降解成为二氧化碳和水。乳酸还有许多其他用途。
(1)请写出乳酸分子中官能团的名称___、___。
(2)乳酸能与纯铁粉反应制备一种补铁药物--乳酸亚铁,反应如下,计算乳酸亚铁中铁的质量分数为___。(3)乳酸聚合成的纤维非常适合做手术缝合线,其原因是___。
(4)乳酸发生下列变化:
所用的试剂是a___,b___(写化学式)
(5)请写出乳酸与少量的NaCO 溶液反应的化学方程式___。
2 3
(6)乳酸乙酯( )是一种食用香料,常用于调制果香型、乳酸型食用和酒用精。乳酸乙酯的同
分异构体M有如下性质:0.1molM分别与足量的金属钠和碳酸氢钠反应,产生的气体在相同状况下的体积
相同,则M的结构最多有___(不考虑空间异构)种。
34. 按要求回答下列问题:
(1)如图所示物质的有关结构,请回答:
①A、B、C三者的关系为_________(填写序号)。
a.同分异构体b.同素异形体c.同一种物质d.同位素
②固态时,A属于__________晶体(填“离子”、“原子”或“分子”)。
③有同学认为D、E互为同分异构体而G、H两者并不是同分异构体的关系。这句话正确吗?答:
__________(填写“正确”或“不正确”)
④有机物E用系统命名法命名的名称是__________。
(2)已知下列7种物质:a.P(白磷) b.SiO c.NH Cl d.NaOH e.NaCl f.干冰 g.金刚石,
4 2 4
固态时它们都为晶体,回答下列问题:(填写序号)
①晶体中既有离子键又有共价键的是__________
②熔化时只需要破坏共价键的是__________
③熔点最高的晶体是__________,沸点最低的晶体是__________