文档内容
第16讲 物质的检验与鉴别
一、选择题
1.(2015,扬州)下列鉴别方法不可行的是(B)
A.用灼烧法鉴别羊毛线和棉纱线
B.用点燃的木条鉴别氯酸钾和氯化钾
C.用肥皂水鉴别蒸馏水和氯化钙溶液
D.用酚酞试液鉴别稀硫酸与氢氧化钠溶液
2.(2014,衡阳)能将氢氧化钠、氯化钠和盐酸三种溶液一次性鉴别出来的是(A)
A.石蕊溶液 B.碳酸钠溶液
C.硫酸铜溶液 D.酚酞溶液
3.(2015,苏州)下列有关物质的鉴别方案错误的是(D)
A.用澄清石灰水鉴别氮气和二氧化碳
B.用肥皂水鉴别硬水和软水
C.用闻气味的方法鉴别白酒和白醋
D.用稀盐酸鉴别碳酸钠粉末和碳酸钙粉末
4.(2014,广州)区别下列各组物质的方法可行的是(B)
A.用盐酸区别澄清石灰水和氢氧化钠溶液
B.用二氧化锰区别过氧化氢溶液和纯水
C.用蒸馏水区别四氧化三铁粉末和铁粉
D.用铜片区别稀盐酸和稀硫酸
5.(2014,天津)下列区分物质的方法不正确的是(D)
A.用水区分碳酸钙粉末和碳酸钠粉末
B.用水区分硝酸铵固体和氢氧化钠固体
C.用硝酸钡溶液区分稀盐酸和稀硫酸
D.用酚酞溶液区分稀盐酸和食盐水
6.(2015,北京)下列实验方法一定能达到实验目的的是( D )
选项 实验目的 实验方法
A 检验一瓶气体是否为CO 将燃着的木条伸入瓶中
2
B 鉴别H 和CH 分别点燃,在火焰上方罩一干冷烧杯
2 4
C 鉴别石灰水和NaOH溶液 加入适量的稀盐酸
将Zn和Ag分别放入 CuSO 溶液
D 比较Zn、Cu、Ag的金属活动性 4
中
7.(2015,南充)除去下列物质中的少量杂质,所选试剂及操作方法都正确的是(B)
选项 物质(括号
内为杂质) 试剂 操作方法
A CaCO(CaO) — 高温煅烧
3
B KOH溶液
(KCO) 适量Ca(OH) 溶液 滴加试剂、过滤
2 3 2
C Ag(Fe) 适量CuSO 溶液 滴加试剂、过滤
4
D CO(CO) 足量NaOH溶液 洗气、干燥
2
8.(2015,济南)下列各组物质的鉴别中,所选的鉴别试剂不正确的是(C)
选项 待鉴别的物质 鉴别试剂
A 氧气、二氧化碳、空气 燃着的木条
B 氯化铵固体和氯化钠固体 氢氧化钠溶液
C 氢氧化钠溶液和碳酸钠溶液 酚酞试液
D 稀盐酸和稀硫酸 BaCl 溶液
2
9.(2015,益阳)下列物质的溶液,不另加试剂就不能鉴别出来的一组是(C)
A.CuSO BaCl HSO
4 2 2 4B.NaCO Ca(NO) HCl
2 3 3 2
C.NaSO KNO HCl
2 4 3
D.FeCl NaOH KMnO
3 4
10.(2014,衡阳)4.6 g某化合物在足量氧气中充分燃烧,生成 8.8 g二氧化碳和5.4 g水。下列对该化
合物组成的判断中,正确的是(C)
A.由碳、氢两种元素组成
B.由碳、氧两种元素组成
C.由碳、氢、氧三种元素组成
D.一定含有碳、氢两种元素,可能含有氧元素
11.(2014,呼和浩特)下列说法正确的是(D)
A.向某固体上滴加稀盐酸,有气泡产生,则该固体一定是碳酸盐
B.把燃着的木条插入某瓶无色气体中,木条熄灭,证明瓶中的气体是二氧化碳
C.取少量溶液于试管中,滴加氯化钡溶液,有白色沉淀生成,证明该溶液中一定有硫酸根离子
D.不用任何试剂就可以把KOH、HNO、CuSO、MgCl 四种溶液鉴别出来
3 4 2
12.(2015,潍坊)下列实验方案不能达到实验目的的是(B)
实验目的 实验方案
分别滴加稀盐酸,振荡,观察是否产生沉
A 鉴别AgNO 溶液与NaNO 溶液
3 3 淀
B 除去CO中混有的CO 将混合气体通过灼热的氧化铜
2
C 鉴别纯铝和硬铝 将两者相互刻划,比较硬度
将带火星的木条伸入集气瓶口,观察木条
D 检验集气瓶中是否集满氧气
能否复燃
二、推断题
13.(2014,佛山)现有一包白色粉末,可能是食盐、纯碱或干燥剂(主要成分生石灰)中的一种或几种物质
组成。为了研究白色粉末的组成,进行了如下实验:
(1)将部分粉末放入烧杯中,加适量水充分搅拌后,得澄清溶液,溶液温度升高,滴加酚酞试液,溶液变
红,得出:粉末中一定含有 干燥剂 ( 或 Ca O 或生石灰 ),可能有 食盐 ( 或 NaCl );
(2)向(1)中澄清溶液滴加过量稀硝酸,然后再滴加硝酸银溶液,发现有白色沉淀生成,请你写出该反应的
化学方程式 NaC l + AgN O = = =AgC l ↓+ NaN O。
3 3
14.(2014,河北)已知A~E是初中化学的常见物质。A和D是两种常见的碱;B是一种常见的酸,且只含
有两种元素;C是一种钠盐。它们相互间转化或发生反应的关系如图所示。(“-”表示两种物质间能发生
化学反应,“→”表示两种物质间存在转化关系)
请回答:
(1)B的化学式是HCl,C的化学式是NaCO。
2 3
(2)C→E发生的反应,属于复分解反应。(填基本反应类型)
(3)C与D反应的化学方程式是NaCO + Ca(OH ) = = =CaC O ↓+ 2NaO H。
2 3 2 3
15.(2014,益阳)材料:难溶于水的碱在加热的条件下,容易分解生成对应的金属氧化物和水。A、B、C是中学化学中常见的化合物,A溶液呈蓝色,C是一种黑色金属氧化物,A、B、C的转化关系如图
所示,请回答下列问题:
(1)向A中加入NaOH溶液时产生的现象是产生蓝色沉淀。
(2)写出下列两个化学方程式:
①A→BCuSO + 2NaO H = = =Cu(OH ) ↓+ N aSO。
4 2 2 4
②C→A Cu O + HSO = = =CuS O + HO。
2 4 4 2
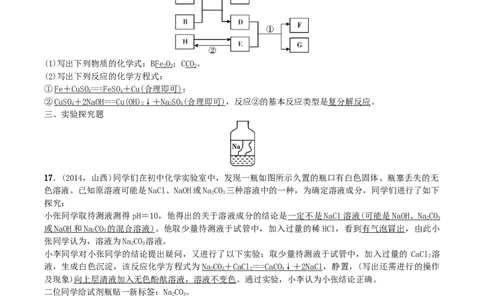
16.(2013,兰州)已知A~H均为初中化学常见的物质。其中A、C是组成元素相同的气体,且C能产生温
室效应;B为红棕色,是赤铁矿的主要成分;F是紫红色金属;H是蓝色沉淀。根据图示的转化关系(图中
反应条件均已略去),请回答:
(1)写出下列物质的化学式:BFeO;CCO。
2 3 2
(2)写出下列反应的化学方程式:
① F e + CuS O = = =FeS O + Cu ( 合理即可 );
4 4
②CuSO + 2NaO H = = =Cu(OH ) ↓+ N aSO ( 合理即可 ),反应②的基本反应类型是复分解反应。
4 2 2 4
三、实验探究题
17.(2014,山西)同学们在初中化学实验室中,发现一瓶如图所示久置的瓶口有白色固体、瓶塞丢失的无
色溶液。已知原溶液可能是NaCl、NaOH或NaCO 三种溶液中的一种,为确定溶液成分,同学们进行了如下
2 3
探究:
小张同学取待测液测得pH=10,他得出的关于溶液成分的结论是 一定不是 NaC l 溶液 ( 可能是 NaO H 、 N aCO
2 3
或 NaOH 和 N aCO 的混合溶液 ) 。他取少量待测液于试管中,加入过量的稀 HCl,看到有气泡冒出,由此小
2 3
张同学认为,溶液为NaCO 溶液。
2 3
小李同学对小张同学的结论提出疑问,又进行了以下实验:取少量待测液于试管中,加入过量的 CaCl 溶
2
液,生成白色沉淀,该反应化学方程式为NaCO + CaC l = = =CaC O ↓+ 2NaCl ,静置,(写出还需进行的操作
2 3 2 3
及现象)向上层清液加入无色酚酞溶液,溶液不变色。通过实验,小李认为小张结论正确。
二位同学给试剂瓶贴一新标签:NaCO。
2 3
实验结束后,同学们通过讨论认为试剂瓶原标签可能不是 NaCO ,你认为他们的理由是原标签可能是
2 3
NaOH。