文档内容
第19讲 中和反应
(满分50分,限时40分钟)
一、选择题(每小题2分,共18分)
1.下列应用与中和反应原理无关的是(A)(导学号 58504362)
A.用浓硫酸干燥湿润的氧气
B.用熟石灰改良酸性土壤
C.服用含氢氧化铝的药物治疗胃酸过多
D.用氢氧化钠溶液洗涤石油产品中的残留硫酸
2.(2017,枣庄)紫甘蓝是大众爱吃的蔬菜,含有丰富的花青素。花青素遇酸性溶液变红
色,遇碱性溶液变蓝色。在凉拌紫甘蓝丝时,观察到菜丝变成红色,可能是加入了下列哪种调
味品(C)
A.食盐 B.味精 C.食醋 D.香油
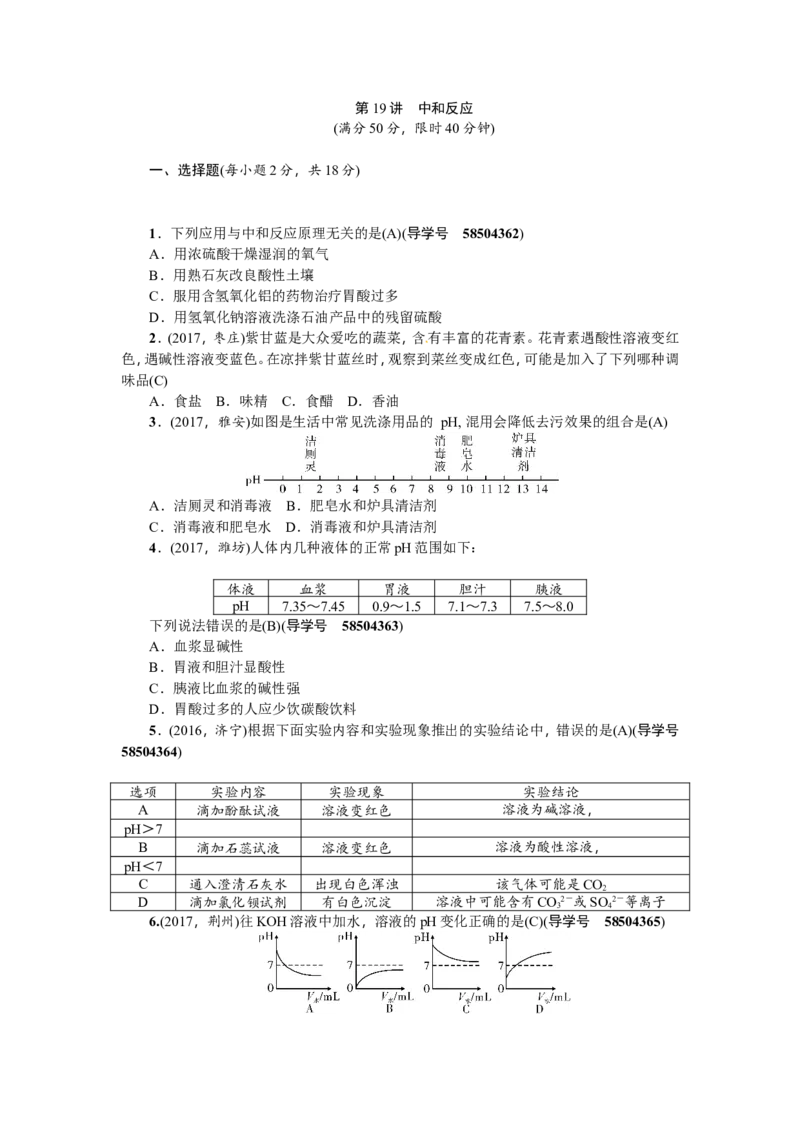
3.(2017,雅安)如图是生活中常见洗涤用品的 pH, 混用会降低去污效果的组合是(A)
[来源:学科网ZXXK]
A.洁厕灵和消毒液 B.肥皂水和炉具清洁剂
C.消毒液和肥皂水 D.消毒液和炉具清洁剂
4.(2017,潍坊)人体内几种液体的正常pH范围如下:
体液 血浆 胃液 胆汁 胰液
pH 7.35~7.45 0.9~1.5 7.1~7.3 7.5~8.0
下列说法错误的是(B)(导学号 58504363)
A.血浆显碱性
B.胃液和胆汁显酸性
C.胰液比血浆的碱性强
D.胃酸过多的人应少饮碳酸饮料
5.(2016,济宁)根据下面实验内容和实验现象推出的实验结论中,错误的是(A)(导学号
58504364)
选项 实验内容 实验现象 实验结论
A 滴加酚酞试液 溶液变红色 溶液为碱溶液,
pH>7
B 滴加石蕊试液 溶液变红色 溶液为酸性溶液,
pH<7
C 通入澄清石灰水 出现白色浑浊 该气体可能是CO
2
D 滴加氯化钡试剂 有白色沉淀 溶液中可能含有CO2-或SO 2-等离子
3 4
6.(2017,荆州)往KOH溶液中加水,溶液的pH变化正确的是(C)(导学号 58504365)7.(2017,内江)将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意
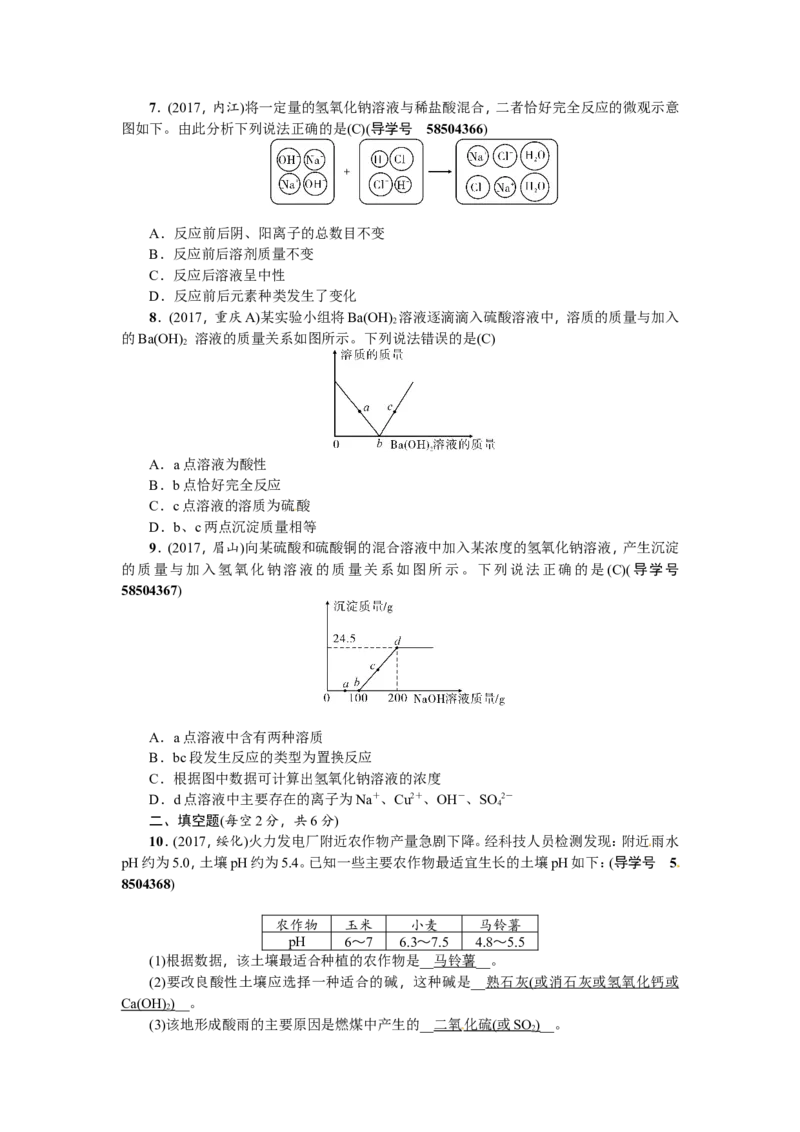
图如下。由此分析下列说法正确的是(C)(导学号 58504366)
A.反应前后阴、阳离子的总数目不变
B.反应前后溶剂质量不变
C.反应后溶液呈中性
D.反应前后元素种类发生了变化
8.(2017,重庆A)某实验小组将Ba(OH) 溶液逐滴滴入硫酸溶液中,溶质的质量与加入
2
的Ba(OH) 溶液的质量关系如图所示。下列说法错误的是(C)
2
A.a点溶液为酸性
B.b点恰好完全反应
C.c点溶液的溶质为硫酸
D.b、c两点沉淀质量相等
9.(2017,眉山)向某硫酸和硫酸铜的混合溶液中加入某浓度的氢氧化钠溶液,产生沉淀
的质量与加入氢氧化钠溶液的质量关系如图所示。下列说法正确的是(C)(导学号
58504367)
A.a点溶液中含有两种溶质
B.bc段发生反应的类型为置换反应
C.根据图中数据可计算出氢氧化钠溶液的浓度
D.d点溶液中主要存在的离子为Na+、Cu2+、OH-、SO 2-
4
二、填空题(每空2分,共6分)
10.(2017,绥化)火力发电厂附近农作物产量急剧下降。经科技人员检测发现:附近雨水
pH约为5.0,土壤pH约为5.4。已知一些主要农作物最适宜生长的土壤pH如下:(导学号 5
8504368)
农作物 玉米 小麦 马铃薯
pH 6~7 6.3~7.5 4.8~5.5
(1)根据数据,该土壤最适合种植的农作物是__马铃薯__。
(2)要改良酸性土壤应选择一种适合的碱,这种碱是__ 熟石灰 ( 或消石灰或氢氧化钙或
Ca(OH) )__。
2
(3)该地形成酸雨的主要原因是燃煤中产生的__二氧 化硫 ( 或 SO )__。
2三、实验探究题(共26分)
13.(10分)(2017,临沂)某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探
究活动。请你和他们一起完成以下实验探究。
【演示实验】将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中。该反应的化学方程式
是__ 2HCl + Ca (OH) == =CaCl + 2H O__。
2 2 2
【查阅资料】CaCl 溶液显中性。
2
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质的成分
是什么?
【猜想与假设】针对疑问,甲组同学猜想如下:
猜想Ⅰ:只有CaCl ;
2
猜想Ⅱ:有__CaCl 和 HC l__;
2
猜想Ⅲ:有CaCl 和Ca(OH) ;
2 2
猜想Ⅳ:有CaCl 、HCl和Ca(OH) 。
2 2
乙组同学对以上猜想提出质疑,认为猜想Ⅳ不合理,其理由是__ HCl 和 Ca(OH) 不能共
2
存__。
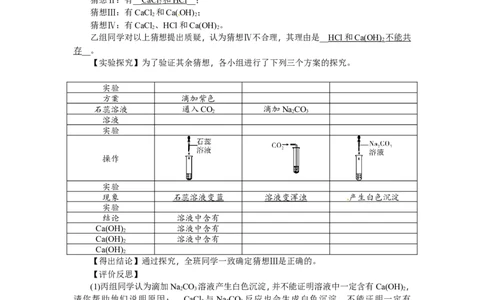
【实验探究】为了验证其余猜想,各小组进行了下列三个方案的探究。
实验
[来源:学科网ZXXK]
方案 滴加紫色
石蕊溶液 通入CO 滴加NaCO
2 2 3
溶液
实验
操作
实验
现象 石蕊溶液变蓝 溶液变浑浊 产生白色沉淀
实验
结论 溶液中含有
Ca(OH) 溶液中含有
2
Ca(OH) 溶液中含有
2
Ca(OH)
2
【得出结论】通过探究,全班同学一致确定猜想Ⅲ是正确的。
【评价反思】
(1)丙组同学认为滴加NaCO 溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH) ,
2 3 2
请你帮助他们说明原因:__CaCl 与 N aCO 反应也会生成白色沉淀 , 不能证明一定有
2 2 3
Ca (OH) 存在__。
2
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外,还需要考虑__反应物是
否过量__。
14. (16分)(2017,南京)兴趣小组的同学对碳酸氢钠、碳酸钠、氢氧化钠的某些性质进行
相关探究。
【提出问题】它们溶液的酸碱性及与酸反应时溶液的pH如何变化?(导学号 58504369)
【实验探究1】向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入几滴紫
甘蓝汁液,同时用蒸馏水进行对比实验,观察并记录现象如下:
液体名称 蒸馏水 碳酸氢钠溶液 碳酸钠
溶液 氢氧化
钠溶液
紫甘蓝汁液
显示的颜色 蓝紫色 蓝色 绿色 黄色
【查阅资料】
pH 7.5~9 10~11.9 12~14
紫甘蓝汁液显示的颜色 蓝色 绿色 黄色
【得出结论1】三种溶液的碱性由强到弱的顺序为__ 氢氧化钠溶液 > 碳酸钠溶液 > 碳酸氢
钠溶液。
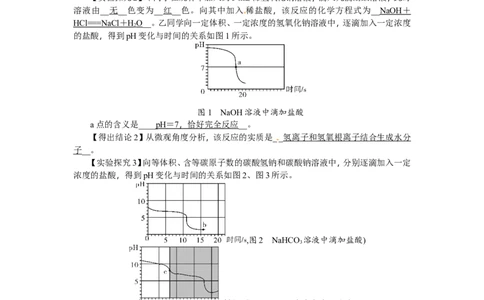
【实验探究2】甲同学在烧杯中加入约5 mL稀氢氧化钠溶液,滴入几滴酚酞溶液,此时
溶液由__无__色变为__红__色。向其中加入稀盐酸,该反应的化学方程式为__ NaOH +
HCl == =NaCl + H O__。乙同学向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度
2
的盐酸,得到pH变化与时间的关系如图1所示。
图1 NaOH溶液中滴加盐酸
a点的含义是____ pH = 7 , 恰好完全反应 __。
【得出结论2】从微观角度分析,该反应的实质是__氢离子和氢氧根离子结合生成水分
子__。
【实验探究3】向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定
浓度的盐酸,得到pH变化与时间的关系如图2、图3所示。
,图2 NaHCO 溶液中滴加盐酸)
3
,图3 NaCO 溶液中滴加盐酸)
2 3
【交流与反思】b点的溶质为__ NaCl 、 HCl __(写化学式),将图2和图3的阴影部分进行叠
加,发现两者基本重合,c点的溶质为__ NaCl 、 NaHCO __(写化学式)。
3
【得出结论3】通过上述分析,碳酸钠和盐酸反应过程,可以依次用以下两个化学方程式
表示:
__NaCO+_ HCl == =NaCl + _NaHCO __、
2 3 3_
__NaHCO +_HCl_ == = _ NaCl + _HO_ + CO ↑__。
3 2 2
【结论与反思】探究溶液的酸碱性及反应中pH的变化,可以认识反应的原理及进行的过
程。