文档内容
精选练习6 物质的构成
二、原子核外电子排布
1、电子层的划分
电子层(用n表示)1、2、3、4……
电子层符号 K、L、M、N……
离核距离 近远
能量高低 低高
2、核外电子排布规律
(1)各电子层最多容纳的电子数是2n2(n表示电子层)
(2)最外层电子数不超过8个(K层是最外层时,最多不超过2个);次外层电子数目不超
过18个;倒数第三层不超过32个。
(3)核外电子总是尽先排布在能量最低的电子层,然后由里向外从能量低的电子层逐步
向能量高的电子层排布.
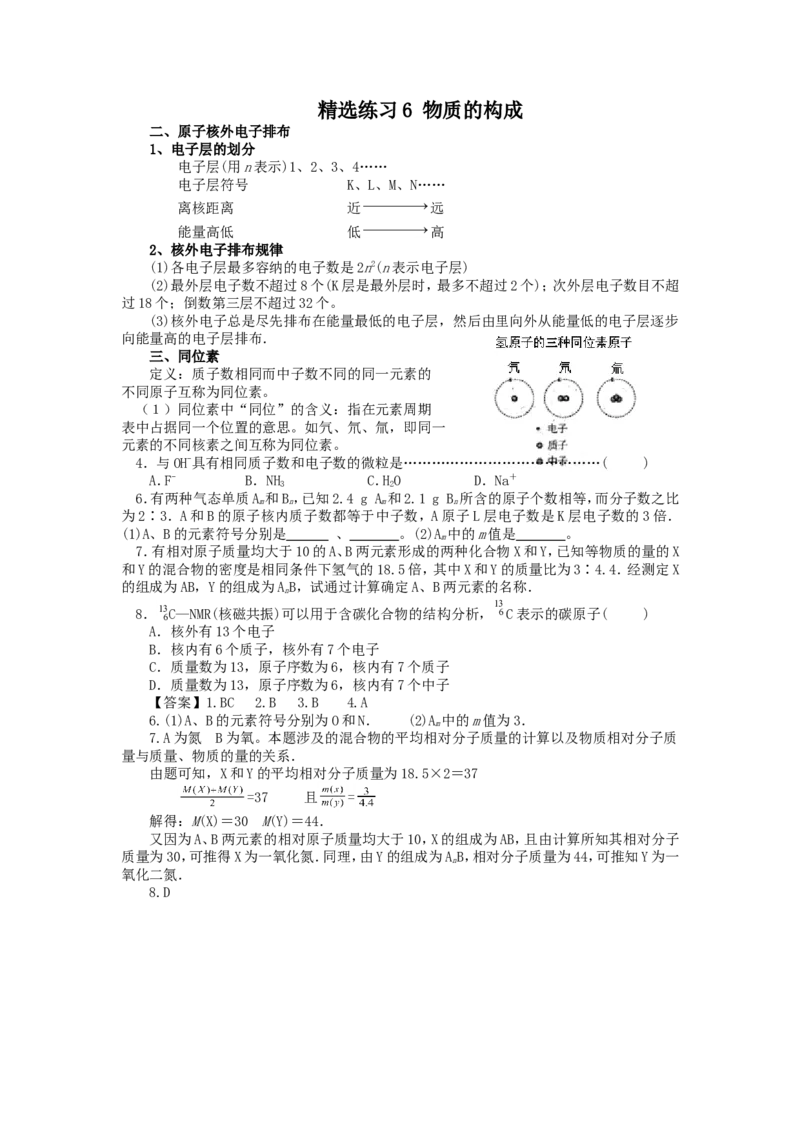
三、同位素
定义:质子数相同而中子数不同的同一元素的
不同原子互称为同位素。
(1)同位素中“同位”的含义:指在元素周期
表中占据同一个位置的意思。如氕、氘、氚,即同一
元素的不同核素之间互称为同位素。
4.与OH-具有相同质子数和电子数的微粒是……………………………………( )
A.F- B.NH C.HO D.Na+
3 2
6.有两种气态单质A 和B,已知2.4 g A 和2.1 g B 所含的原子个数相等,而分子数之比
m n m n
为2∶3.A和B的原子核内质子数都等于中子数,A原子L层电子数是K层电子数的3倍.
(1)A、B的元素符号分别是 、 。(2)A 中的m值是 。
m
7.有相对原子质量均大于10的A、B两元素形成的两种化合物X和Y,已知等物质的量的X
和Y的混合物的密度是相同条件下氢气的18.5倍,其中X和Y的质量比为3∶4.4.经测定X
的组成为AB,Y的组成为AB,试通过计算确定A、B两元素的名称.
n
13
8.13C—NMR(核磁共振)可以用于含碳化合物的结构分析, 6C表示的碳原子( )
6
A.核外有13个电子
B.核内有6个质子,核外有7个电子
C.质量数为13,原子序数为6,核内有7个质子
D.质量数为13,原子序数为6,核内有7个中子
【答案】1.BC 2.B 3.B 4.A
6.(1)A、B的元素符号分别为O和N. (2)A 中的m值为3.
m
7.A为氮 B为氧。本题涉及的混合物的平均相对分子质量的计算以及物质相对分子质
量与质量、物质的量的关系.
由题可知,X和Y的平均相对分子质量为18.5×2=37
=37 且 =
解得:M(X)=30 M(Y)=44.
又因为A、B两元素的相对原子质量均大于10,X的组成为AB,且由计算所知其相对分子
质量为30,可推得X为一氧化氮.同理,由Y的组成为AB,相对分子质量为44,可推知Y为一
n
氧化二氮.
8.D