文档内容
课题 2 原子的结构
教学目标
(1)了解原子是由质子、中子和电子构成的;
(2)知道原子核外电子是分层排布的;
(3)了解离子的形成,初步认识离子是构成物质的一种粒子;
(4)了解原子结构示意图的含义及原子最外层电子数与元素性质的关系。
(5)初步了解相对原子质量的概念,并会查相对原子质量表。
教学重点:构成原子的粒子间的关系。
教学难点:相对原子质量的概念形成。
教学过程
一、原子的构成
1897年,汤姆生发现了电子,从此叩开原子的大门,人们开始揭示原子内部的秘密。
卢瑟福通过实验证明原子是由原子核和核外电子两部分构成的。1911年卢瑟福等人为探索原子
的内部结构又进行了下面的实验:用一束带正电的、质量比电子大得多的高速运动的α粒子轰击金箔,
结果发现:①大多数α粒子能穿透金箔而不改变原来的运动方向;②一小部分α粒子改变了原来的运
动方向;③极少数粒子反弹回来。
α粒子轰击金箔
[设问] 产生上述现象的原因是什么呢?
[分析] ①大多数α粒子能穿透金箔而不改变原来的运动方向——原子内部有很大的空间。②一小部
分带正电的α粒子改变了原来的运动方向——原子核带正电,α粒子途经金原子核附近时,受到斥力
而改变了运动方向。③极少数粒子反弹回来——原子中有一个很小的原子核,原子核很小,但集中了
较大的质量。
[结论] 原子是由居于原子中心的带正电的原子核和核外带负电的电子构成的。
1.原子的结构
质子(带正电)
原子核(中心)
原子 中心(不带电)不显电性
核外电子(带负电)
表1 构成原子的粒子的电性和质量
粒子种类 电性 质量
质子 1个单位正电荷 1.672 6×10-27 kg
中子 不带电 1.674 9×10-27 kg
电子 1个单位负电荷 质子质量的1/1 863
表2 几种原子的构成
原子种类 质子数 中子数 核外电子数 相对原子质量
氢 1 0 1 1
碳 6 6 6 12
氧 8 8 8 16
钠 11 12 11 23
镁 12 12 12 24
氯 17 18 17 35
[思考] 原子中存在带电的粒子,为什么整个原子不显电性?(原子核所带正电荷(核电荷数)和核外
电子所带负电荷电量相等,但电性相反,所以整个原子不显电性。)
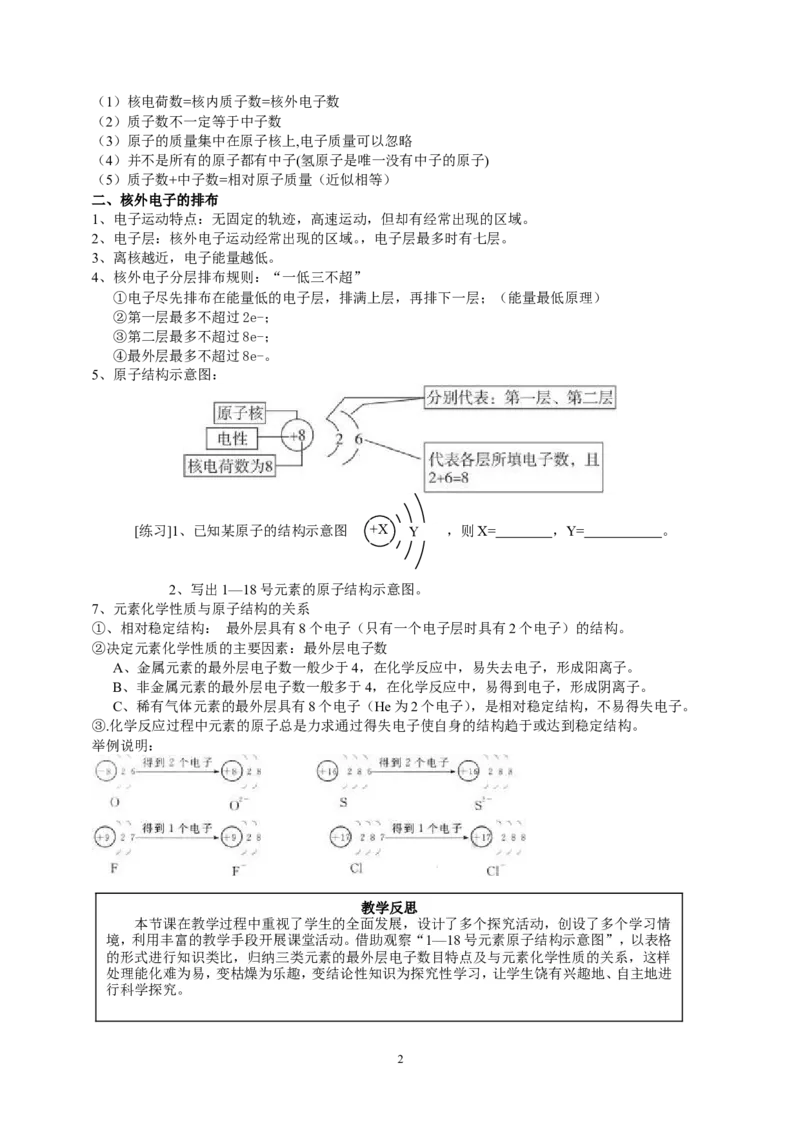
2.原子结构中的一些规律
1(1)核电荷数=核内质子数=核外电子数
(2)质子数不一定等于中子数
(3)原子的质量集中在原子核上,电子质量可以忽略
(4)并不是所有的原子都有中子(氢原子是唯一没有中子的原子)
(5)质子数+中子数=相对原子质量(近似相等)
二、核外电子的排布
1、电子运动特点:无固定的轨迹,高速运动,但却有经常出现的区域。
2、电子层:核外电子运动经常出现的区域。,电子层最多时有七层。
3、离核越近,电子能量越低。
4、核外电子分层排布规则:“一低三不超”
①电子尽先排布在能量低的电子层,排满上层,再排下一层;(能量最低原理)
②第一层最多不超过2e-;
③第二层最多不超过8e-;
④最外层最多不超过8e-。
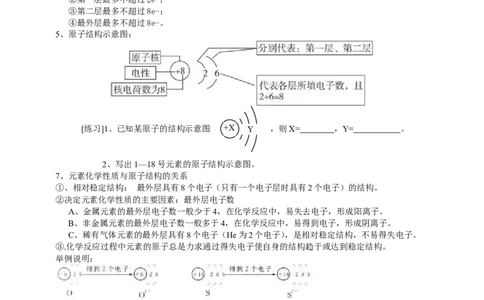
5、原子结构示意图:
[练习]1、已知某原子的结构示意图 + X Y ,则X= ,Y= 。
2、写出1—18号元素的原子结构示意图。
7、元素化学性质与原子结构的关系
①、相对稳定结构: 最外层具有8个电子(只有一个电子层时具有2个电子)的结构。
②决定元素化学性质的主要因素:最外层电子数
A、金属元素的最外层电子数一般少于4,在化学反应中,易失去电子,形成阳离子。
B、非金属元素的最外层电子数一般多于4,在化学反应中,易得到电子,形成阴离子。
C、稀有气体元素的最外层具有8个电子(He为2个电子),是相对稳定结构,不易得失电子。
③.化学反应过程中元素的原子总是力求通过得失电子使自身的结构趋于或达到稳定结构。
举例说明:
教学反思
本节课在教学过程中重视了学生的全面发展,设计了多个探究活动,创设了多个学习情
境,利用丰富的教学手段开展课堂活动。借助观察“1—18号元素原子结构示意图”,以表格
的形式进行知识类比,归纳三类元素的最外层电子数目特点及与元素化学性质的关系,这样
处理能化难为易,变枯燥为乐趣,变结论性知识为探究性学习,让学生饶有兴趣地、自主地进
行科学探究。
第二课时
2三、离子的形成
1、离子:带电荷的原子或原子团。
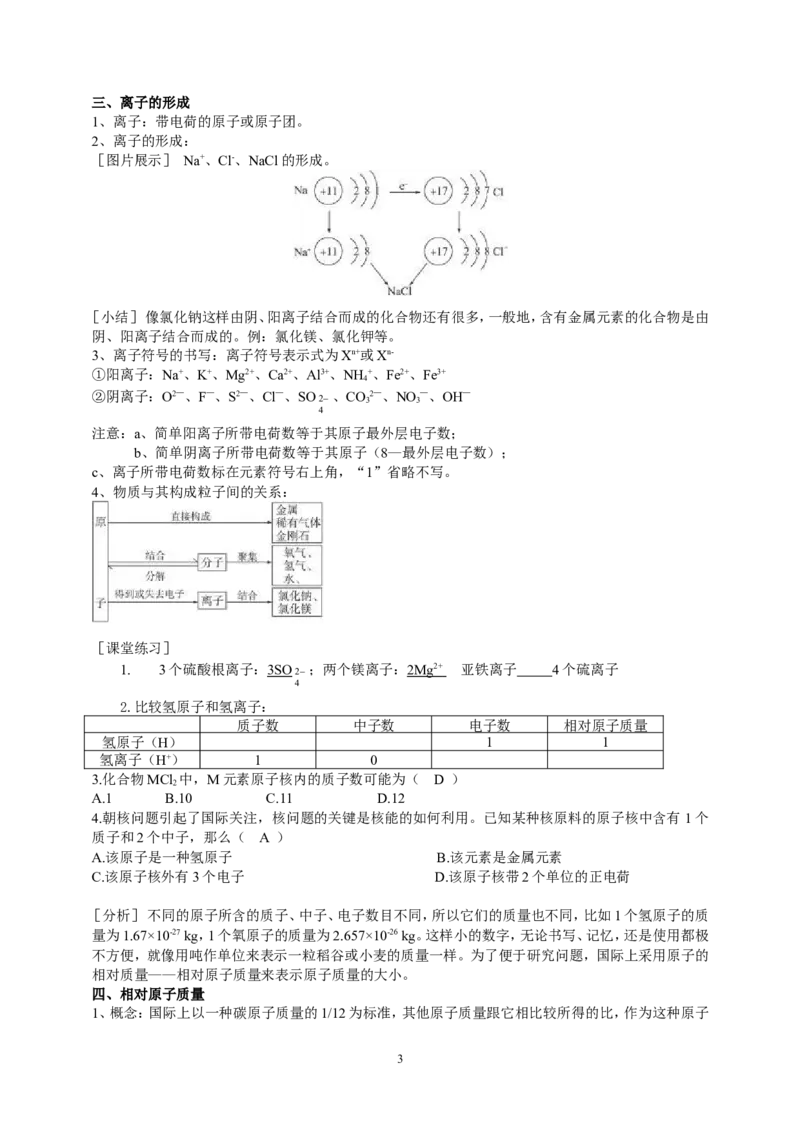
2、离子的形成:
[图片展示] Na+、Cl-、NaCl的形成。
[小结] 像氯化钠这样由阴、阳离子结合而成的化合物还有很多,一般地,含有金属元素的化合物是由
阴、阳离子结合而成的。例:氯化镁、氯化钾等。
3、离子符号的书写:离子符号表示式为Xn+或Xn-
①阳离子:Na+、K+、Mg2+、Ca2+、Al3+、NH +、Fe2+、Fe3+
4
②阴离子:O2—、F—、S2—、Cl—、SO2 、CO
3
2—、NO
3
—、OH—
4
注意:a、简单阳离子所带电荷数等于其原子最外层电子数;
b、简单阴离子所带电荷数等于其原子(8—最外层电子数);
c、离子所带电荷数标在元素符号右上角,“1”省略不写。
4、物质与其构成粒子间的关系:
[课堂练习]
1. 3个硫酸根离子:3SO2 ;两个镁离子: 2Mg 2+ 亚铁离子 4个硫离子
4
2.比较氢原子和氢离子:
质子数 中子数 电子数 相对原子质量
氢原子(H) 1 1
氢离子(H+) 1 0
3.化合物MCl 中,M元素原子核内的质子数可能为( D )
2
A.1 B.10 C.11 D.12
4.朝核问题引起了国际关注,核问题的关键是核能的如何利用。已知某种核原料的原子核中含有1个
质子和2个中子,那么( A )
A.该原子是一种氢原子 B.该元素是金属元素
C.该原子核外有3个电子 D.该原子核带2个单位的正电荷
[分析] 不同的原子所含的质子、中子、电子数目不同,所以它们的质量也不同,比如1个氢原子的质
量为1.67×10-27 kg,1个氧原子的质量为2.657×10-26 kg。这样小的数字,无论书写、记忆,还是使用都极
不方便,就像用吨作单位来表示一粒稻谷或小麦的质量一样。为了便于研究问题,国际上采用原子的
相对质量——相对原子质量来表示原子质量的大小。
四、相对原子质量
1、概念:国际上以一种碳原子质量的1/12为标准,其他原子质量跟它相比较所得的比,作为这种原子
3的相对原子质量。符号是Ar
该原子的质量
2、相对原子质量(A)=
r
1/12碳原子的质量
[分析] 也可以用比较形象的方法解释。
[展示投影]
3、相对原子质量只是一个比,不是原子的实际质量,单位是1通常不写。
[分析] 在相对原子质量计算中,所选用的一种碳原子是碳12,是含6个质子和6个中子的碳原子,它
的质量的1/12约等于1.66×10-27 kg。构成原子的粒子有质子、中子、电子,1个质子和1个中子的质量都
约等于1个电子质量的1 836倍,所以电子的质量与原子的质量相比可以忽略不计。因此相对原子质量
可以近似地表示为我们刚才从表2中推导出的:
4、相对原子质量(近似等于)=质子数+中子数
[课堂练习] 1、下列各微粒的示意图中,表示阳离子的是( )
2.我国著名化学家、中国科学院院士张青莲教授主持测定了铟、铱、锑、铕、铈、铒、锗、锌、镝等元素的
相对原子质量新值,其中他测定出核电荷数为63的铕元素的相对原子质量新值为152,则该元素的原
子中质子数为__63__,中子数为___89___,核外电子数为___63___。
3、某原子的质量为ag,相对原子质量为M,氧原子的质量为bg,则氧原子的相对原子质量为 。
教学反思
本节课着重体现学生的主体地位,让学生积极参与其中的思考和探究,教师重点在引导学
生正确的思维和探究,引导学生学习新的知识和技能,体现了三维目标。
4