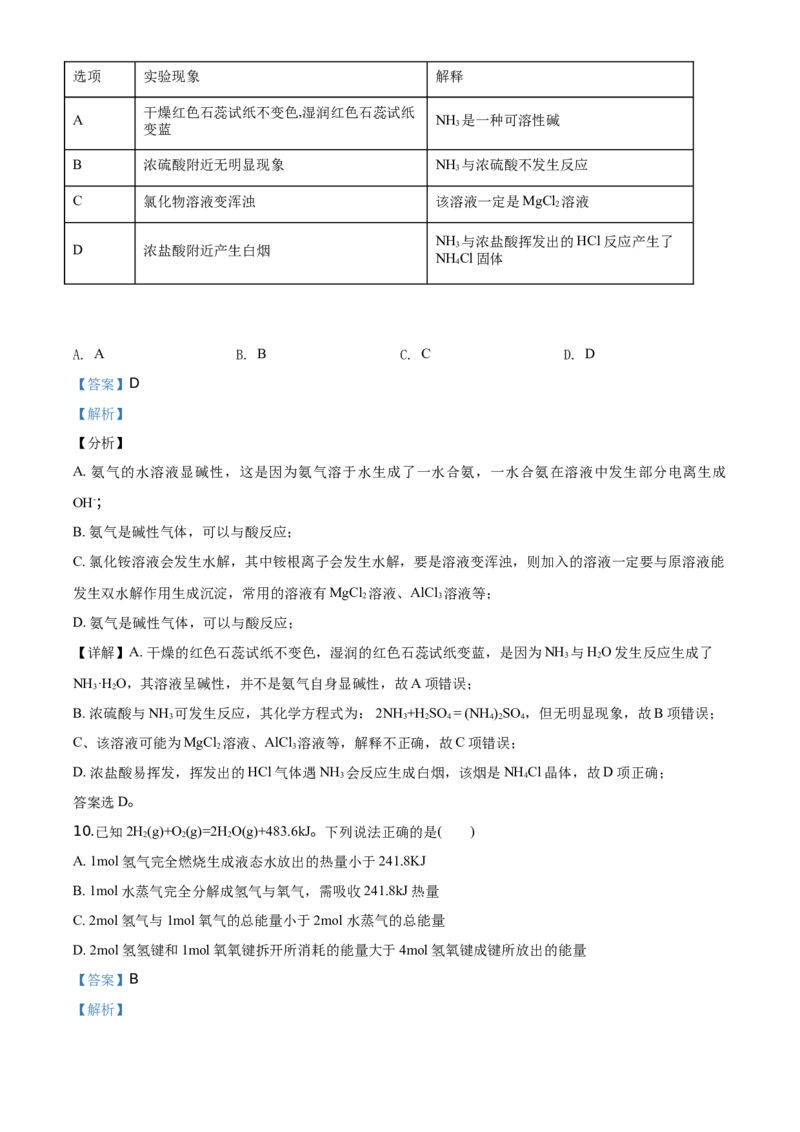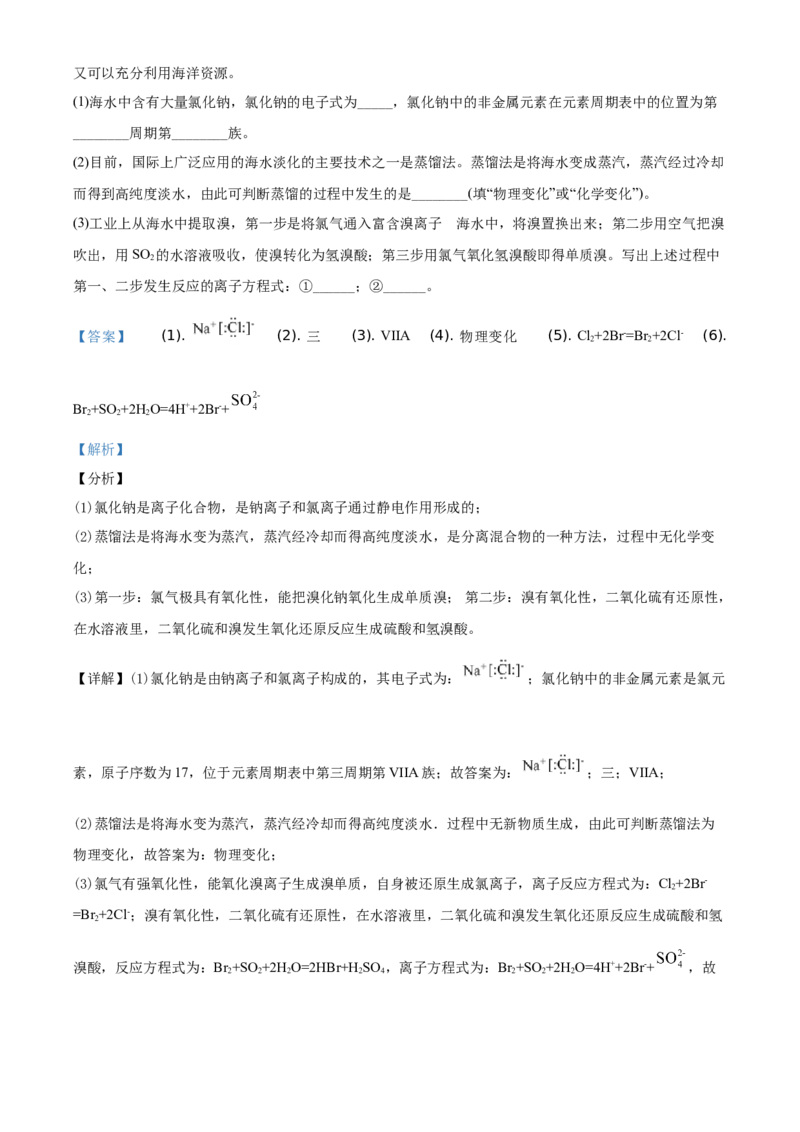文档内容
海南枫叶国际学校 2019 2020 学年第二学期
~
高一化学学科期末考试试卷
(范围:必修二)
一、单选题(本大题共8小题,共16分)
1.下列关于硫的叙述中,正确的是( )
A. 附着有硫的试管可以用酒精进行洗涤
B. 硫与铜在加热条件下反应生成CuS
C. 硫与氢气的反应中,硫是氧化剂
D. 硫在纯氧中燃烧生成三氧化硫
【答案】C
【解析】
【详解】A.硫易溶于二硫化碳,试管内壁上附着的硫可以用二硫化碳清洗,而不是用酒精清洗,故 A错
误;
B.S为弱氧化剂只能将铜氧化为低价铜,所以生成硫化亚铜,故B错误;
C.硫与氢气反应生成硫化氢,S元素的化合价降低,S体现氧化剂,故C正确;
D.硫在纯氧中燃烧生成二氧化硫,二氧化硫和氧气在催化剂、加热条件下反应生成三氧化硫,故D错误;
答案选C。
2.化学在生产生活和科学研究中具有重要的作用。下列说法正确的是( )
①石英的主要成分是二氧化硅
②三峡大坝使用了大量水泥,水泥是硅酸盐材料
③太阳能电池的主要成分是硅,太阳能电池在生活中的应用有利于环保、节能
④二氧化硅的熔点高,硬度大,所以可用来制造电子部件和光学器件
⑤水晶项链和餐桌上的瓷盘都是硅酸盐制品
A. ①②③ B. ②④⑤ C. ③④⑤ D. ①②③④
【答案】A
【解析】
【详解】①石英的主要成分是二氧化硅,正确;
②水泥 的成分是硅酸三钙、硅酸二钙、铝酸三钙,属于硅酸盐,正确;
③太阳能电池的主要成分是硅单质,太阳能是一种清洁能源,其应用有利于环保节能,正确;
④硅具有导电性,能作半导体材料等电子部件;二氧化硅具有良好的光学特性,能够用于制造光学器件,
错误;⑤水晶主要成分是二氧化硅,二氧化硅是氧化物,不是硅酸盐,错误;
故正确的有:①②③,答案选A。
3.化学与生产和生活密切相关,下列说法正确的是( )
A. 聚乙烯塑料的老化是因为发生了加成反应
B. 煤经过气化和液化等物理变化可转化为清洁燃料
C. 合成纤维、再生纤维及碳纤维都属于有机高分子材料
D. 石油裂解的目的是要得到甲烷、乙烯等化工原料
【答案】D
【解析】
【详解】A.乙烯含碳碳双键,发生加聚反应生成聚乙烯,聚乙烯中不存在双键,聚乙烯塑料不能发生加
成反应,故A错误;
B.煤的气化是煤和水在高温下反应生成H、CO等气体的过程,煤的液化是将煤与H 在催化剂作用下转
2 2
化为液体燃料或用水煤气合成液体燃料,所以煤经过气化和液化等变化是化学变化,故B错误;
C.合成纤维、再生纤维都属于有机高分子材料,碳纤维是碳的单质,不属于有机高分子材料,故C错误;
D.裂解是在一定条件下将相对分子质量较大、沸点较高的烃分解为相对分子质量较小、沸点较低的烃的
过程,所以裂解的目的是获得小分子化工原料,如乙烯、甲烷等化工原料,故D正确;
答案选D。
4.下列化学用语表示正确的是
① 甲基的电子式: ② 乙炔的最简式:C H
2 2
③ 蔗糖的分子式:C H O ④ 乙醛的结构简式:CHCOH
12 22 11 3
⑤苯分子的比例模型:
A. ①②④ B. ③⑤ C. ②③⑤ D. ④⑤
【答案】B
【解析】
【详解】①甲基不带电荷,甲基中碳原子的外层有 7个电子,甲基的电子式为 ,故①错误;
②C H 为乙炔的分子式,其最简式为CH,故②错误;③蔗糖的分子式为C H O ,故③正确;④乙醛中
2 2 12 22 11含有醛基,其正确的结构简式为:CHCHO,故④错误;⑤苯分子的比例模型为: ,故⑤正确;
3
故选B。
5.下列反应不属于加成反应的是( )
A. CH=CH +HCl CHCHCl
2 2 3 2
B. 2CHCH+7O 4CO+6HO
3 3 2 2 2
C. CHCH=CH+H CHCHCH
3 2 2 3 2 3
D. CH=CH +Br →CHBrCHBr
2 2 2 2 2
【答案】B
【解析】
【详解】A.该反应中乙烯的双键打开与氢气发生加成反应,故A不符合题意;
B.该反应为乙烷的燃烧,属于氧化反应,而不是加成反应,故B符合题意;
C.该反应为丙烯与氢气的加成反应,故C不符合题意;
D.该反应为乙烯和溴的加成反应,故D不符合题意;
综上所述答案为B。
6.滥用药物有碍健康,下列有关用药的叙述正确的是
A. 长期大量服用阿司匹林可预防感冒
B. 运动员长期服用麻黄碱可提高成绩
C. 服用氢氧化钠溶液可中和过多的胃酸
D. 注射青霉素前要先做皮肤敏感试验
【答案】D
【解析】
【详解】A.长期大量服用阿司匹林会导致不良的肠道反应,A不正确;
B.麻黄碱剩余兴奋剂类药物,不能真正提高成绩,应禁止使用,B不正确;
C.氢氧化钠具有腐蚀性,应该用胃舒平等药物,C不正确;
D.使用青霉素前一定要进行皮试,故D正确;
答案选D。
7.下列关于糖类的说法中,错误的是
A. 葡萄糖化学式为C H O,它能和银氨溶液反应产生光亮的银镜
6 12 6
B. 麦芽糖和蔗糖化学式(C H O )相同,它们是同分异构体
12 22 11C. 淀粉和纤维素化学式(C H O)n相同,它们是同分异构体
6 10 5
D. 多糖可以水解成单糖,单糖不能再水解成更小的糖分子
【答案】C
【解析】
【详解】A. 葡萄糖化学式为C H O,它是五羟基醛,它能和银氨溶液反应产生光亮的银镜,A项正确;
6 12 6
B.麦芽糖和蔗糖化学式(C H O )相同,结构不同,它们是同分异构体,B项正确;
12 22 11
C.淀粉和纤维素化学式【(C H O)n】相同,但它们的n值不同,所以它们不是同分异构体,C项错误;
6 10 5
D.多糖可以水解成单糖,单糖不能再水解成更小的糖分子,D项正确;
答案选C。
8.下列反应既属于氧化还原反应,又属于ΔH>0的是( )
A. 甲烷与O 的燃烧反应
2
B. Ba(OH) ·8H O与NH Cl的反应
2 2 4
C. 铝片与稀HSO 反应
2 4
D. 灼热的炭与CO 反应
2
【答案】D
【解析】
【详解】A. 甲烷与O 的燃烧反应是放热反应,故A不符合题意;
2
B. Ba(OH) ·8H O与NH Cl的反应是吸热反应,但不是氧化还原反应,故B不符合题意;
2 2 4
C. 铝片与稀HSO 反应是放热反应,故C不符合题意;
2 4
D. 灼热的炭与CO 反应方程式C + CO 2CO是吸热反应,C化合价升高,CO 中C化合价降低,反
2 2 2
应是氧化还原反应,故D符合题意。
综上所述,答案为D。
【点睛】放热反应主要是酸碱中和反应、燃烧反应、大多数化合反应、金属和酸或水的反应、大多数氧化
反应;吸热反应主要是大多数分解反应、CO、H、C为还原剂的氧化还原反应(燃烧除外)、Ba(OH) ·8H O
2 2 2
与NH Cl的反应,水解反应。
4
二、不定项选择(每题都有1或2个选项正确。本大题共6小题,共24分)
9.如下图,利用培养皿探究氨气的性质。实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面。
下表中对实验现象所做的解释正确的是( )选项 实验现象 解释
干燥红色石蕊试纸不变色,湿润红色石蕊试纸
A NH 是一种可溶性碱
变蓝 3
B 浓硫酸附近无明显现象 NH 与浓硫酸不发生反应
3
C 氯化物溶液变浑浊 该溶液一定是MgCl 溶液
2
NH 与浓盐酸挥发出的HCl反应产生了
D 浓盐酸附近产生白烟 3
NH Cl固体
4
A. A B. B C. C D. D
【答案】D
【解析】
【分析】
A. 氨气的水溶液显碱性,这是因为氨气溶于水生成了一水合氨,一水合氨在溶液中发生部分电离生成
OH-;
B. 氨气是碱性气体,可以与酸反应;
C. 氯化铵溶液会发生水解,其中铵根离子会发生水解,要是溶液变浑浊,则加入的溶液一定要与原溶液能
发生双水解作用生成沉淀,常用的溶液有MgCl 溶液、AlCl 溶液等;
2 3
D. 氨气是碱性气体,可以与酸反应;
【详解】A. 干燥的红色石蕊试纸不变色,湿润的红色石蕊试纸变蓝,是因为NH 与HO发生反应生成了
3 2
NH ·H O,其溶液呈碱性,并不是氨气自身显碱性,故A项错误;
3 2
B. 浓硫酸与NH 可发生反应,其化学方程式为: 2NH +H SO = (NH )SO ,但无明显现象,故B项错误;
3 3 2 4 4 2 4
C、该溶液可能为MgCl 溶液、AlCl 溶液等,解释不正确,故C项错误;
2 3
D. 浓盐酸易挥发,挥发出的HCl气体遇NH 会反应生成白烟,该烟是NH Cl晶体,故D项正确;
3 4
答案选D。
10.已知2H(g)+O(g)=2HO(g)+483.6kJ。下列说法正确的是( )
2 2 2
A. 1mol氢气完全燃烧生成液态水放出的热量小于241.8KJ
B. 1mol水蒸气完全分解成氢气与氧气,需吸收241.8kJ热量
C. 2mol氢气与1mol氧气的总能量小于2mol 水蒸气的总能量
D. 2mol氢氢键和1mol氧氧键拆开所消耗的能量大于4mol氢氧键成键所放出的能量
【答案】B
【解析】【详解】由氢气燃烧的热化学方程式可知,2mol氢气与1mol氧气燃烧生成2mol水蒸气放热483.6kJ,
A.水蒸气转化为液态水的过程是放热过程,所以 1mol 氢气完全燃烧生成液态水放出的热量大于
241.8kJ,故A错误;
B.根据方程式可知生成1mol水蒸气放出热量241.8kJ,则1mol水蒸气完全分解成氢气与氧气,需吸收
241.8kJ热量,故B正确;
C.反应是放热的,所以反应物的能量高于产物的能量,故C错误;
D.该反应为放热反应,焓变=反应物键能之和-生成物键能之和<0,所以2mol氢氢键和1mol氧氧键拆开
所消耗的能量小于4mol氢氧键成键所放出的能量,故D错误;
故选:B。
【点睛】焓变=反应物键能之和-生成物键能之和;互为逆过程的两个反应的焓变互为相反数。
11.人类的生产生活离不开化学,下列关于生活中的化学知识说法错误的是( )
A. 用氯气与石灰乳反应能制得漂白粉
B. 常温下,可用铝槽车装运浓硝酸
C. 二氧化碳、二氧化硫是形成酸雨的主要原因
D. 不需要通过化学反应就能从海水中获得食盐和淡水
【答案】C
【解析】
【详解】A.氯气和石灰乳反应生成氯化钙、次氯酸钙,氯化钙、次氯酸钙为漂白粉的主要成分,故 A说
法正确;
B.浓硝酸与铝发生钝化反应,可用铝槽车装运浓硝酸,故B说法正确;
C.导致酸雨的主要污染物为二氧化硫和氮氧化物,二氧化碳不能形成酸雨,故C说法错误;
D.海水中有大量的食盐和水,从海水中获得食盐和淡水,没有新物质生成,不需要通过化学反应实现,
故D说法正确;
答案选C。
12.如图是某同学设计的用来验证SO 性质的微型实验装置。分析实验,下列结论正确的是( )
2
A. 若a棉球褪色,则说明SO 具有漂白性
2
B. 若b棉球褪色,则说明SO 具有较强的氧化性
2C. 若c棉球蓝色褪去,则说明SO 具有酸性氧化物的性质
2
D. 可以使用高锰酸钾溶液或烧碱溶液吸收尾气
【答案】AD
【解析】
【分析】
亚硫酸钠与浓硫酸反应生成二氧化硫气体,二氧化硫与品红溶液,品红溶液褪色;二氧化硫与氢氧化钠反
应生成盐和水,则酚酞溶液褪色;二氧化硫与碘反应生成硫酸和碘化氢,则淀粉溶液褪色;二氧化硫有毒,
。
则进行尾气处理
【详解】A.若a棉球褪色,即品红溶液褪色,则说明SO 具有漂白性,A结论正确;
2
B.若b棉球褪色,为二氧化硫与氢氧化钠反应生成盐和水,则说明SO 的水溶液显酸性,B结论错误;
2
C.若c棉球蓝色褪去,为二氧化硫与碘反应生成硫酸和碘化氢,则说明SO 具有还原性,C结论错误;
2
D.二氧化硫为酸性氧化物,且具有还原性,则可以使用高锰酸钾溶液或烧碱溶液吸收尾气,D结论正确;
答案为AD。
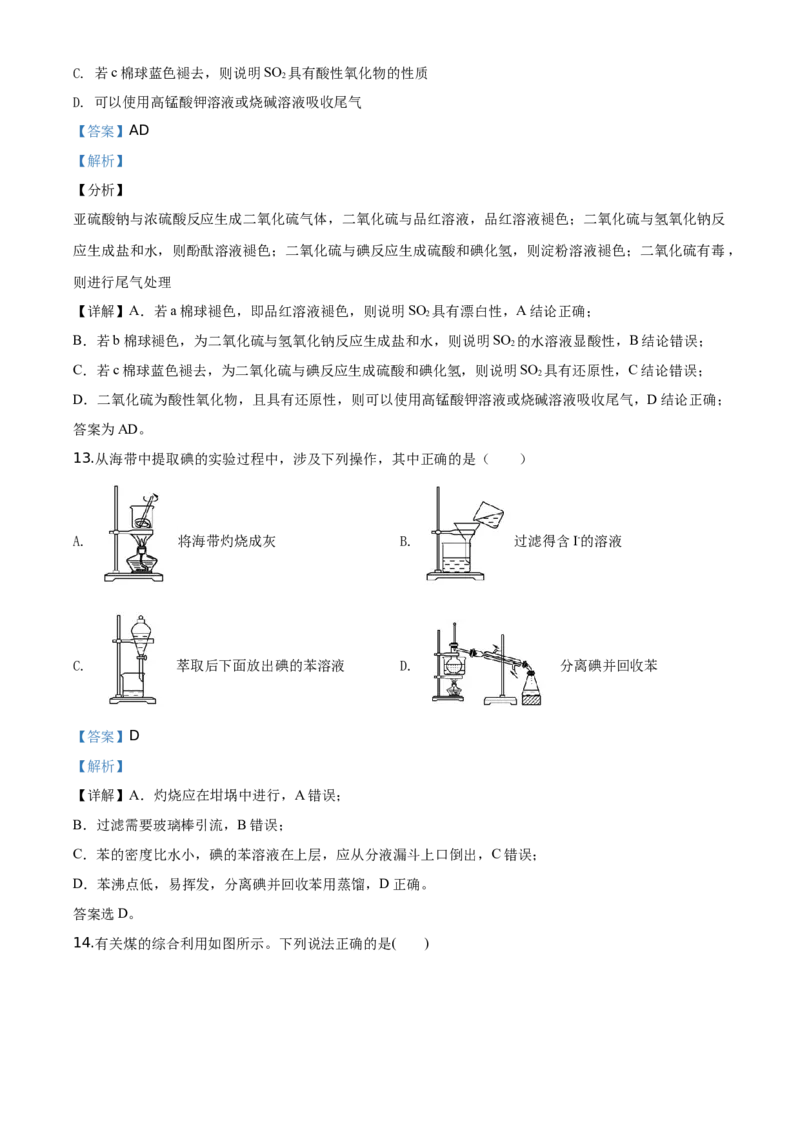
13.从海带中提取碘的实验过程中,涉及下列操作,其中正确的是( )
A. 将海带灼烧成灰 B. 过滤得含I-的溶液
C. 萃取后下面放出碘的苯溶液 D. 分离碘并回收苯
【答案】D
【解析】
【详解】A.灼烧应在坩埚中进行,A错误;
B.过滤需要玻璃棒引流,B错误;
C.苯的密度比水小,碘的苯溶液在上层,应从分液漏斗上口倒出,C错误;
D.苯沸点低,易挥发,分离碘并回收苯用蒸馏,D正确。
答案选D。
14.有关煤的综合利用如图所示。下列说法正确的是( )A. 煤和水煤气均是可再生能源
B. 煤中含有苯、甲苯、二甲苯等有机物
C. ①是将煤在空气中加强热使其分解的过程
D. 煤 的气化、液化和干馏是煤综合利用的主要方法
【答案】D
【解析】
【详解】A.煤作为化石能源是在短期内自然界无法得到补充 的,水煤气是由煤和水高温反应的产物,是
不可再生能源,故A错误;
B.煤是由无机物和有机物组成的复杂的混合物,通过干馏可得到苯、甲苯、二甲苯等有机物,故B错误;
C.①是煤的干馏,煤在隔绝空气的情况下加热的过程称为煤的干馏,故C错误;
D.煤的气化是煤与水蒸气反应生成CO和氢气,煤的液化是煤与氢气反应生成液体燃料,干馏煤是将煤
在隔绝空气的条件下加强热使之分解,则煤的综合利用有煤的气化、液化和干馏,故D正确;
答案选D。
三、填空题(本大题共5小题,共60分)
15.(1)某肉制品包装上印有相关配料:精选瘦肉、食盐、亚硝酸钠、苯甲酸钠,其中属于调味剂的是_____,
属于护色剂的是_______,属于防腐剂的是________。
(2)均衡营养和正确使用药物是保证身心健康的重要方面,现有下列四种物质:
A.葡萄糖 B.氨基酸 C.麻黄碱 D.阿司匹林
①蛋白质水解的最终产物是________(填序号,下同);
②人体内最重要的供能物质是________;
③具有解热镇痛作用,用于治疗感冒的是________;
④对支气管哮喘症有明显疗效的是________。
【答案】 (1). 食盐 (2). 亚硝酸钠 (3). 苯甲酸钠 (4). B (5). A (6). D (7). C
【解析】
【分析】
(1)精选瘦肉是主料;食盐为调味剂,用于调味;亚硝酸钠是发色剂、防腐剂,使肉制品颜色鲜艳;苯
甲酸钠做防腐剂,延长食品存放时间;
(2)葡萄糖在人体内氧化释放能量;蛋白质为氨基酸的缩聚产物;麻黄碱有止咳平喘的作用;阿司匹林
是一种常用的解热镇痛药。【详解】(1)向食品中加入调味剂,能改善或改变食品的口味.常见的调味剂为食盐;亚硝酸钠是发色
剂、防腐剂;苯甲酸钠是常用的防腐剂,故答案为:食盐;亚硝酸钠;苯甲酸钠;
(2)①蛋白质为氨基酸的缩聚产物,水解的最终产物为氨基酸,故答案为:B;
②葡萄糖在人体内氧化释放能量,为人体内最重要的供能物质,故答案为:A;
③阿司匹林是一种常用的解热镇痛药,具有解热镇痛作用,用于治疗感冒的是阿司匹林,故答案为:D;
④麻黄碱有止咳平喘的作用,对支气管哮喘症有明显疗效的是麻黄碱,故答案为:C。
16.已知下列热化学方程式:
回答下列问题:
(1).上述反应中属于放热反应的是________。
(2).H 的燃烧热 ________________;C的燃烧热 ________________。
2
(3).燃烧 生成液态水,放出的热量为________。
(4).写出CO燃烧的热化学方程式:________________________________。
【答案】 (1). (2). (3). (4).
(5).
【解析】
【分析】
(1).焓变小于零为放热反应;
(2).根据燃烧热的定义确定燃烧热的数值;
(3).物质的物质的量与焓变成正比,将质量换算成物质的量,进行计算;
(4).根据盖斯定律可知, 可得CO燃烧的热化学方程式;【详解】 的反应属于放热反应; 的反应属于吸热反应,根据给出的热化学方程式可知:
三个反应的 都属于放热反应,
故答案为: ;
根据燃烧热的定义知: 燃烧时生成液态水更稳定,所以
就是氢气的燃烧热化学方程式,其燃烧热 ; 碳燃烧时
生成 更稳定,所以 就是碳的燃烧热化学方程式,
其燃烧热 ,
故答案为: ; ;
由热化学方程式 可知: , 燃烧生成气
态水放出的热量为 ,则 燃烧生成气态水放出的热量为 ,
故答案为:1429kJ;
根据盖斯定律可知, 可得
,
故答案为: 。
【点睛】本题考查了焓变与反应吸热、放热的关系,燃烧热的定义以及盖斯定律的有关计算,是高考常考
知识。题目难度一般。 理解燃烧热是注意两点: 必须是1mol的物质; 生成的氧化物必须稳定
是关键,侧重基础知识的考查。
17.海水约占地球总储水量的97%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。
(1)海水中含有大量氯化钠,氯化钠的电子式为_____,氯化钠中的非金属元素在元素周期表中的位置为第
________周期第________族。
(2)目前,国际上广泛应用的海水淡化的主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却
而得到高纯度淡水,由此可判断蒸馏的过程中发生的是________(填“物理变化”或“化学变化”)。
(3)工业上从海水中提取溴,第一步是将氯气通入富含溴离子 的海水中,将溴置换出来;第二步用空气把溴
吹出,用SO 的水溶液吸收,使溴转化为氢溴酸;第三步用氯气氧化氢溴酸即得单质溴。写出上述过程中
2
第一、二步发生反应的离子方程式:①______;②______。
【答案】 (1). (2). 三 (3). VIIA (4). 物理变化 (5). Cl+2Br-=Br +2Cl- (6).
2 2
Br +SO+2H O=4H++2Br-+
2 2 2
【解析】
【分析】
(1)氯化钠是离子化合物,是钠离子和氯离子通过静电作用形成的;
(2)蒸馏法是将海水变为蒸汽,蒸汽经冷却而得高纯度淡水,是分离混合物的一种方法,过程中无化学变
化;
(3)第一步:氯气极具有氧化性,能把溴化钠氧化生成单质溴; 第二步:溴有氧化性,二氧化硫有还原性,
在水溶液里,二氧化硫和溴发生氧化还原反应生成硫酸和氢溴酸。
【详解】(1)氯化钠是由钠离子和氯离子构成的,其电子式为: ;氯化钠中的非金属元素是氯元
素,原子序数为17,位于元素周期表中第三周期第VIIA族;故答案为: ;三;VIIA;
(2)蒸馏法是将海水变为蒸汽,蒸汽经冷却而得高纯度淡水.过程中无新物质生成,由此可判断蒸馏法为
物理变化,故答案为:物理变化;
(3)氯气有强氧化性,能氧化溴离子生成溴单质,自身被还原生成氯离子,离子反应方程式为:Cl+2Br-
2
=Br +2Cl-;溴有氧化性,二氧化硫有还原性,在水溶液里,二氧化硫和溴发生氧化还原反应生成硫酸和氢
2
溴酸,反应方程式为:Br +SO+2H O=2HBr+HSO ,离子方程式为:Br +SO+2H O=4H++2Br-+ ,故
2 2 2 2 4 2 2 2答案为:①Cl+2Br-=Br +2Cl-;②Br +SO+2H O=4H++2Br-+ 。
2 2 2 2 2
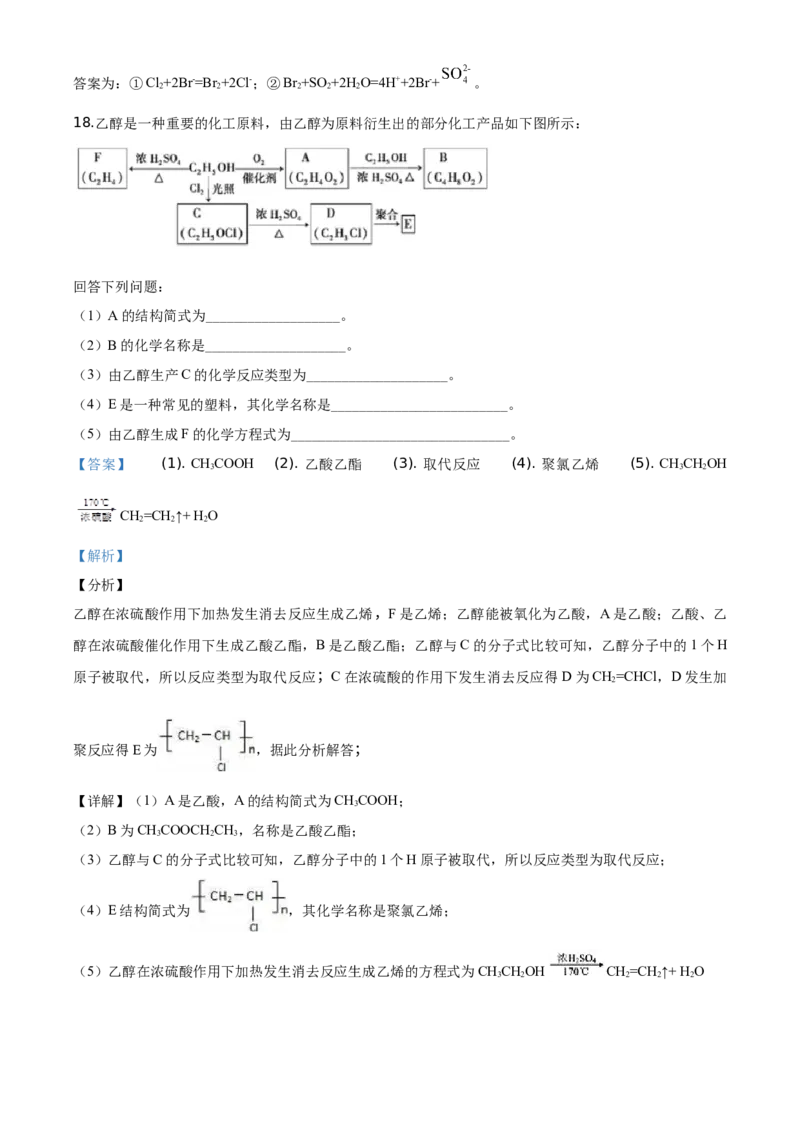
18.乙醇是一种重要的化工原料,由乙醇为原料衍生出的部分化工产品如下图所示:
回答下列问题:
(1)A的结构简式为___________________。
(2)B的化学名称是____________________。
(3)由乙醇生产C的化学反应类型为____________________。
(4)E是一种常见的塑料,其化学名称是_________________________。
(5)由乙醇生成F的化学方程式为_______________________________。
【答案】 (1). CHCOOH (2). 乙酸乙酯 (3). 取代反应 (4). 聚氯乙烯 (5). CHCHOH
3 3 2
CH=CH ↑+ H O
2 2 2
【解析】
【分析】
乙醇在浓硫酸作用下加热发生消去反应生成乙烯,F是乙烯;乙醇能被氧化为乙酸,A是乙酸;乙酸、乙
醇在浓硫酸催化作用下生成乙酸乙酯,B是乙酸乙酯;乙醇与C的分子式比较可知,乙醇分子中的1个H
原子被取代,所以反应类型为取代反应;C在浓硫酸的作用下发生消去反应得D为CH=CHCl,D发生加
2
聚反应得E为 ,据此分析解答;
【详解】(1)A是乙酸,A的结构简式为CHCOOH;
3
(2)B为CHCOOCH CH,名称是乙酸乙酯;
3 2 3
(3)乙醇与C的分子式比较可知,乙醇分子中的1个H原子被取代,所以反应类型为取代反应;
(4)E结构简式为 ,其化学名称是聚氯乙烯;
(5)乙醇在浓硫酸作用下加热发生消去反应生成乙烯的方程式为CHCHOH CH=CH ↑+ H O
3 2 2 2 219.在化学课上,围绕浓硫酸的化学性质进行了如下实验探究:将适量的蔗糖放入烧杯中,加入几滴水,
搅拌均匀。然后加入适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放
出有刺激性气味的气体。
请回答:
(1) 生成的黑色(单质)物质是________(填化学式)。
(2) 这种黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的主要污染
物之一,这种刺激性气味的气体成分是________(填名称),实验室经常用________溶液进行吸收,写出生
成这种气体的化学方程式分别为:__________________;
(3) 据蔗糖与浓硫酸反应的实验现象,说明浓硫酸具有_______________(填序号)。
A.酸性 B.吸水性 C.脱水性 D.强氧化性
(4) 将实验(2)产生的刺激性气味气体通入品红溶液,可以看到品红溶液________,加热后________。
(5) 能否用澄清石灰水鉴别这两种气体?____________(填“能”或“不能”)若不能填写两种能鉴别的试剂是
________________________。
【答案】 (1). C (2). 二氧化硫 (3). NaOH (4). C+2H SO CO↑+2SO↑+2H O (5). BCD
2 4 2 2 2
(6). 褪色 (7). 恢复红色 (8). 不能 (9). 品红、高锰酸钾溶液(溴水等)
【解析】
【详解】(1)将适量的蔗糖放入烧杯中,加几滴水,搅拌均匀,然后加入浓硫酸,把蔗糖中的氢元素和氧元
素按照2:1脱去变为水,生成的黑色物质是C;
(2)黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的主要污染物之一,
说明这种刺激性气味的气体是二氧化硫,反应的化学方程式为:C+2H SO (浓) CO↑+2H O+2SO ↑,
2 4 2 2 2
SO 是酸性氧化物,能够与碱反应,在实验室经常用NaOH溶液进行吸收;
2
(3)将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀,然后加入浓硫酸,生成黑色物质碳表现了浓硫酸的
脱水性,黑色物质继续与浓硫酸作用会产生两种气体,体现了浓硫酸的强氧化性,过程中表现为吸水性,
答案为BCD;
(4)有刺激性气味的气体是SO ,SO 通入品红溶液中,可以看到品红溶液褪色,表现了二氧化硫的漂白性,
2 2
SO 的漂白不稳定,加热后恢复红色;
2(5)根据化学反应CO+Ca(OH) =CaCO ↓+H O,SO +Ca(OH) =CaSO ↓+H O,二氧化硫和二氧化碳分别通入
2 2 3 2 2 2 3 2
澄清石灰水中,都会生成沉淀,溶液变浑浊,不能鉴别两种气体,可以利用品红试液鉴别,二氧化硫能使
品红试液褪色,二氧化碳无此现象;或加入酸性高锰酸钾溶液,能够使紫色褪去的为二氧化硫,二氧化碳
无此现象。
【点睛】本题考查浓硫酸的性质。①浓硫酸具有强氧化性,能和C发生反应生成CO、SO 和水;②浓硫
2 2
酸具有脱水性,将适量的蔗糖放入烧杯中,加几滴水,搅拌均匀,然后加入浓硫酸,生成黑色物质为碳,
体现的是浓硫酸的脱水性;③浓硫酸具有吸水性,能作干燥剂,用来干燥H、SO 等气体;④二氧化硫是
2 2
具有刺激性气味的气体,SO 通入品红溶液中褪色,是二氧化硫的漂白性;⑤二氧化碳、二氧化硫通入澄
2
清石灰水都能变浑浊,不能用来鉴别;可以利用品红鉴别两种气体。