文档内容
课题 3 水的组成
教学目标
1.认识水的组成,了解并区分单质和化合物。
2从人类认识水的组成的过程中体会科学探究和思维的方法,认识实验探究和创新思维的重要性;
3.了解人类认识物质世界的过程和方法,培养学生科学探究的精神。
教学重点 水的组成。
教学难点 对单质、化合物概念的理解。
教具准备 霍夫曼电解水装置、电源、酒精灯、火柴、水、氢氧化钠溶液,小木条。
教学过程
导入新课:水是一种无色透明的物质,历史上人们一直认为水是一种单一的物质,那么水这种物质里
究竟含有什么呢?研究氢气的燃烧实验是人们认识水组成的开始。
一、绿色能源----氢气
1.物理性质:无色、无臭、难溶于水。
2.化学性质:可燃性(产生淡蓝色火焰)
H+O →HO
2 2 2
3.验纯方法:收集一试管氢气,管口朝上,用拇指堵住试管口移近酒精灯火焰,移开拇指,若听到很小的
声音,则表示氢气已纯;若发出尖锐的爆鸣声则表示气体不纯。
4、H元素的检验:点燃氢气,在火焰上方罩一干冷小烧杯,烧杯内壁产生水雾。
5、制备:Zn+H SO →ZnSO+H
2 4 4 2
6、作能源的优点:①无污染;②发热量高;③来源广,可再生。
二、水的组成:
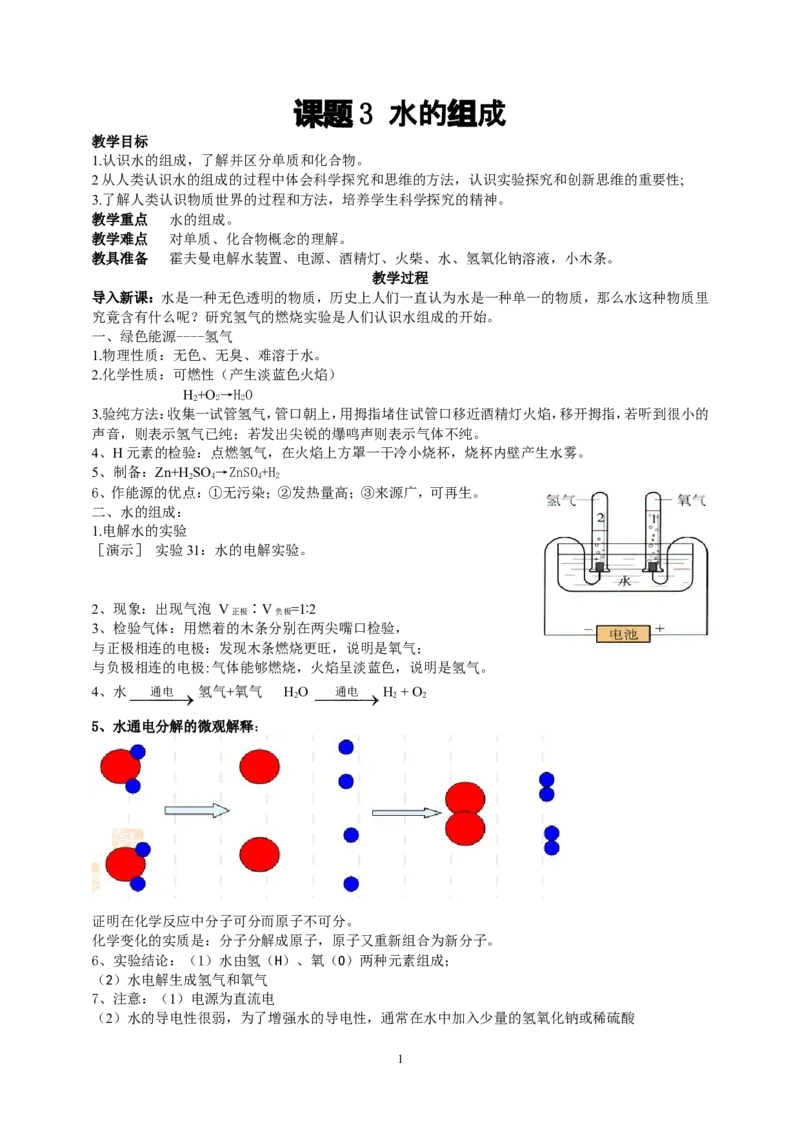
1.电解水的实验
[演示] 实验31:水的电解实验。
2、现象:出现气泡 V ∶V =1∶2
正极 负极
3、检验气体:用燃着的木条分别在两尖嘴口检验,
与正极相连的电极:发现木条燃烧更旺,说明是氧气;
与负极相连的电极:气体能够燃烧,火焰呈淡蓝色,说明是氢气。
4、水 通电 氢气+氧气 H
2
O 通电H
2
+ O
2
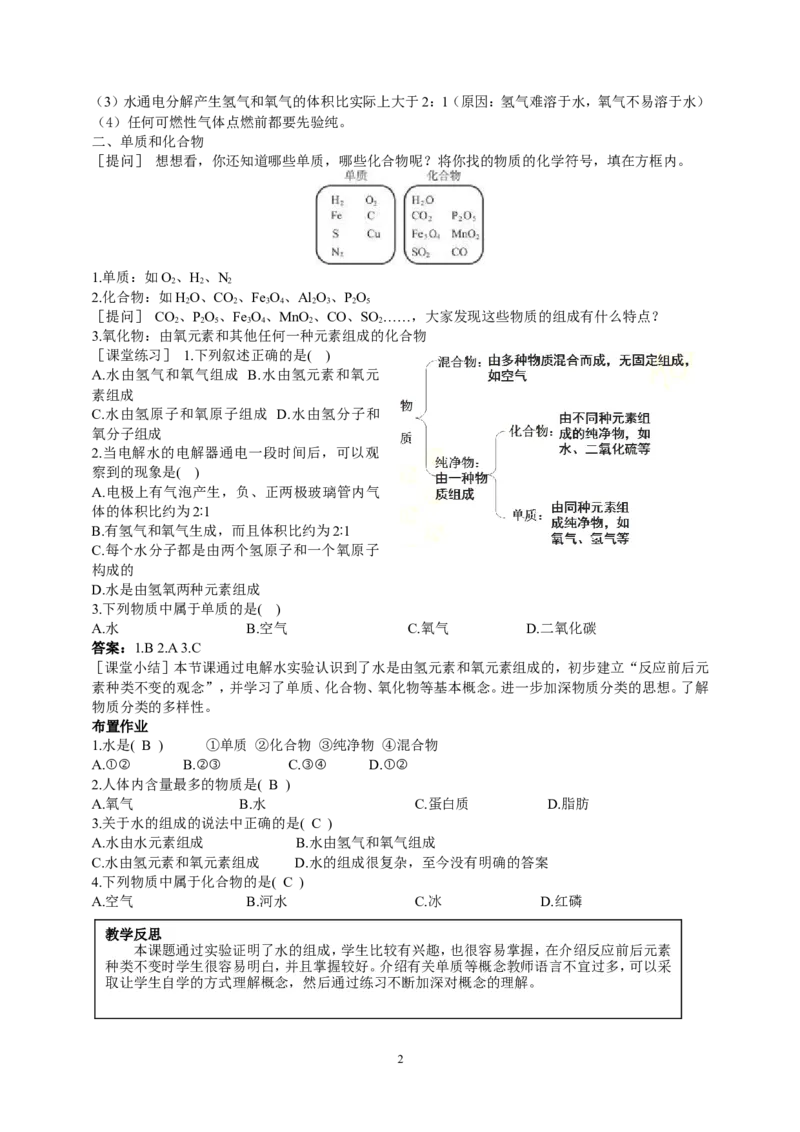
5、水通电分解的微观解释:
证明在化学反应中分子可分而原子不可分。
化学变化的实质是:分子分解成原子,原子又重新组合为新分子。
6、实验结论:(1)水由氢(H)、氧(O)两种元素组成;
(2)水电解生成氢气和氧气
7、注意:(1)电源为直流电
(2)水的导电性很弱,为了增强水的导电性,通常在水中加入少量的氢氧化钠或稀硫酸
1(3)水通电分解产生氢气和氧气的体积比实际上大于2:1(原因:氢气难溶于水,氧气不易溶于水)
(4)任何可燃性气体点燃前都要先验纯。
二、单质和化合物
[提问] 想想看,你还知道哪些单质,哪些化合物呢?将你找的物质的化学符号,填在方框内。
1.单质:如O、H、N
2 2 2
2.化合物:如HO、CO、Fe O、Al O、PO
2 2 3 4 2 3 2 5
[提问] CO、PO、Fe O、MnO 、CO、SO ……,大家发现这些物质的组成有什么特点?
2 2 5 3 4 2 2
3.氧化物:由氧元素和其他任何一种元素组成的化合物
[课堂练习] 1.下列叙述正确的是( )
A.水由氢气和氧气组成 B.水由氢元素和氧元
素组成
C.水由氢原子和氧原子组成 D.水由氢分子和
氧分子组成
2.当电解水的电解器通电一段时间后,可以观
察到的现象是( )
A.电极上有气泡产生,负、正两极玻璃管内气
体的体积比约为2∶1
B.有氢气和氧气生成,而且体积比约为2∶1
C.每个水分子都是由两个氢原子和一个氧原子
构成的
D.水是由氢氧两种元素组成
3.下列物质中属于单质的是( )
A.水 B.空气 C.氧气 D.二氧化碳
答案:1.B 2.A 3.C
[课堂小结]本节课通过电解水实验认识到了水是由氢元素和氧元素组成的,初步建立“反应前后元
素种类不变的观念”,并学习了单质、化合物、氧化物等基本概念。进一步加深物质分类的思想。了解
物质分类的多样性。
布置作业
1.水是( B ) ①单质 ②化合物 ③纯净物 ④混合物
A.①② B.②③ C.③④ D.①②
2.人体内含量最多的物质是( B )
A.氧气 B.水 C.蛋白质 D.脂肪
3.关于水的组成的说法中正确的是( C )
A.水由水元素组成 B.水由氢气和氧气组成
C.水由氢元素和氧元素组成 D.水的组成很复杂,至今没有明确的答案
4.下列物质中属于化合物的是( C )
A.空气 B.河水 C.冰 D.红磷
教学反思
本课题通过实验证明了水的组成,学生比较有兴趣,也很容易掌握,在介绍反应前后元素
种类不变时学生很容易明白,并且掌握较好。介绍有关单质等概念教师语言不宜过多,可以采
取让学生自学的方式理解概念,然后通过练习不断加深对概念的理解。
2