文档内容
遵义市2013年年初中毕业(升学)统一考试
化学模拟试题卷(三)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32 Cl-35.5
一、选择题(本大题包括10小题,每小题2分,共20分。每小题只有一个正确答案,请在答题
卡选择题栏内用2 B 铅笔将对应题目答案的标号涂黑。)
1.2013年3月22日是第二十一届“世界水日”,下列节水措施中不可取的是
A.工业废水处理达标后循环使用 B.农业浇灌推广使用喷灌、滴灌技术
C.大量开采使用地下水 D.洗菜、淘米、洗衣的水可以用来浇花、拖地、冲厕所
2.今天的午餐食谱是:主食——米饭;配菜和副食——炸鸡腿、炸薯片、牛排、牛奶。则该午餐
食谱缺乏的营养素是
A.糖类 B.脂肪 C.蛋白质 D.维生素
3.下列做法不符合“低碳环保”理念的是
A.为了节约用纸,两面使用草稿纸
B.为了“QQ”能够升级,长期把“QQ”挂在线上
C.开发新能源,逐渐取缔直接利用化石燃料的历史
D.减少使用私家车次数,多乘公交车、骑自行车或步行
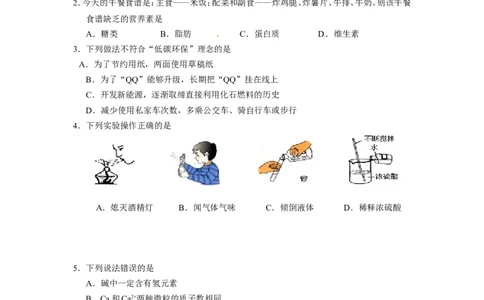
4.下列实验操作正确的是
A.熄灭酒精灯 B.闻气体气味 C.倾倒液体 D.稀释浓硫酸
5.下列说法错误的是
A.碱中一定含有氢元素
B.Ca和Ca2+两种微粒的质子数相同
C.用pH试纸测定溶液的pH时,应先用蒸馏水将试纸润湿
D.洗过的玻璃仪器内壁附着的水既不聚成水滴也不成股流下时,表示仪器已洗净
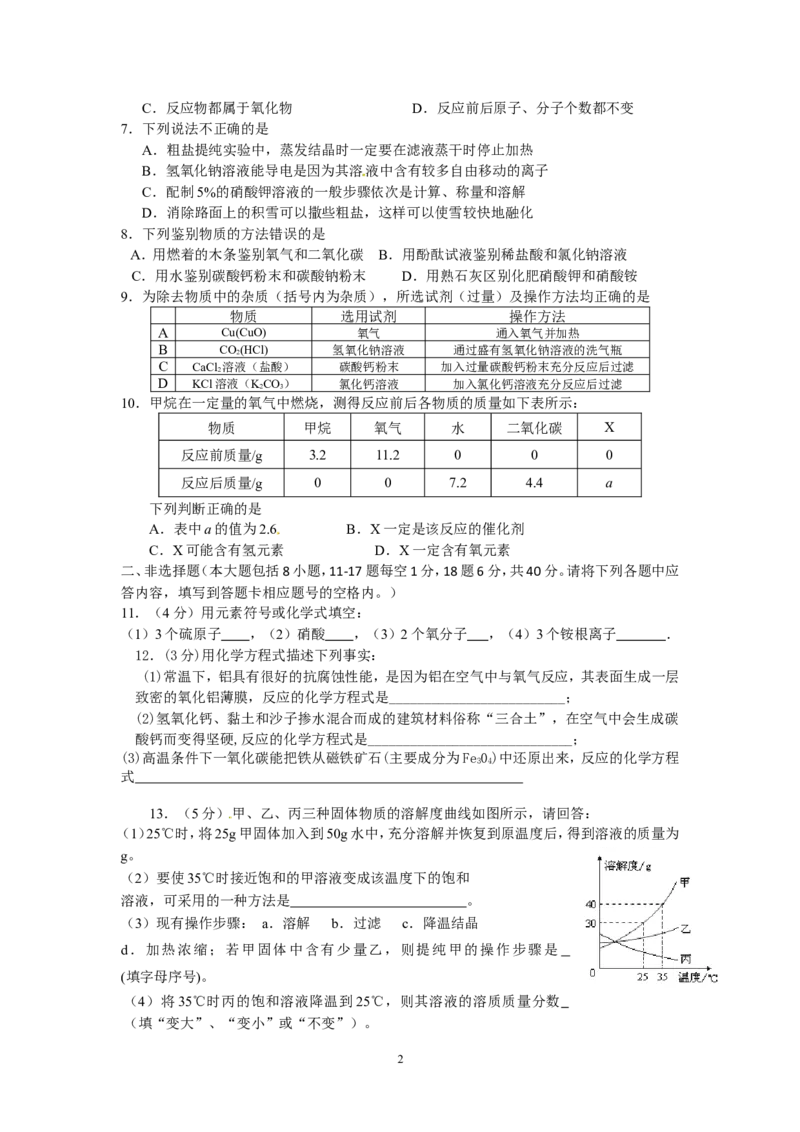
6.下图表示治理汽车尾气所涉及反应的微观过程。下列说法不正确的是
A.图中单质的化学式为N B.该反应使有毒气体转化为无毒气体
2
1C.反应物都属于氧化物 D.反应前后原子、分子个数都不变
7.下列说法不正确的是
A.粗盐提纯实验中,蒸发结晶时一定要在滤液蒸干时停止加热
B.氢氧化钠溶液能导电是因为其溶液中含有较多自由移动的离子
C.配制5%的硝酸钾溶液的一般步骤依次是计算、称量和溶解
D.消除路面上的积雪可以撒些粗盐,这样可以使雪较快地融化
8.下列鉴别物质的方法错误的是
A.用燃着的木条鉴别氧气和二氧化碳 B.用酚酞试液鉴别稀盐酸和氯化钠溶液
C.用水鉴别碳酸钙粉末和碳酸钠粉末 D.用熟石灰区别化肥硝酸钾和硝酸铵
9.为除去物质中的杂质(括号内为杂质),所选试剂(过量)及操作方法均正确的是
物质 选用试剂 操作方法
A Cu(CuO) 氧气 通入氧气并加热
B CO(HCl) 氢氧化钠溶液 通过盛有氢氧化钠溶液的洗气瓶
2
C CaCl 溶液(盐酸) 碳酸钙粉末 加入过量碳酸钙粉末充分反应后过滤
2
D KCl溶液(KCO) 氯化钙溶液 加入氯化钙溶液充分反应后过滤
2 3
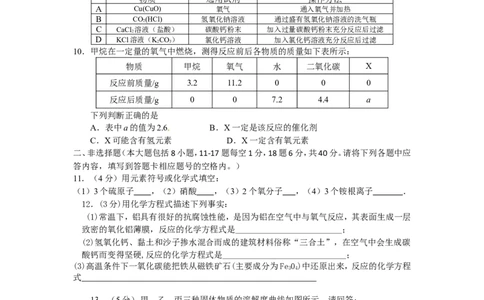
10.甲烷在一定量的氧气中燃烧,测得反应前后各物质的质量如下表所示:
物质 甲烷 氧气 水 二氧化碳 X
反应前质量/g 3.2 11.2 0 0 0
反应后质量/g 0 0 7.2 4.4 a
下列判断正确的是
A.表中a的值为2.6 B.X一定是该反应的催化剂
C.X可能含有氢元素 D.X一定含有氧元素
二、非选择题(本大题包括8小题,11-17题每空1分,18题6分,共40分。请将下列各题中应
答内容,填写到答题卡相应题号的空格内。)
11.(4分)用元素符号或化学式填空:
(1)3个硫原子 ,(2)硝酸 ,(3)2个氧分子 ,(4)3个铵根离子 .
12.(3分)用化学方程式描述下列事实:
(1)常温下,铝具有很好的抗腐蚀性能,是因为铝在空气中与氧气反应,其表面生成一层
致密的氧化铝薄膜,反应的化学方程式是_________________________;
(2)氢氧化钙、黏土和沙子掺水混合而成的建筑材料俗称“三合土”,在空气中会生成碳
酸钙而变得坚硬,反应的化学方程式是_____________________________;
(3)高温条件下一氧化碳能把铁从磁铁矿石(主要成分为Fe0)中还原出来,反应的化学方程
3 4
式
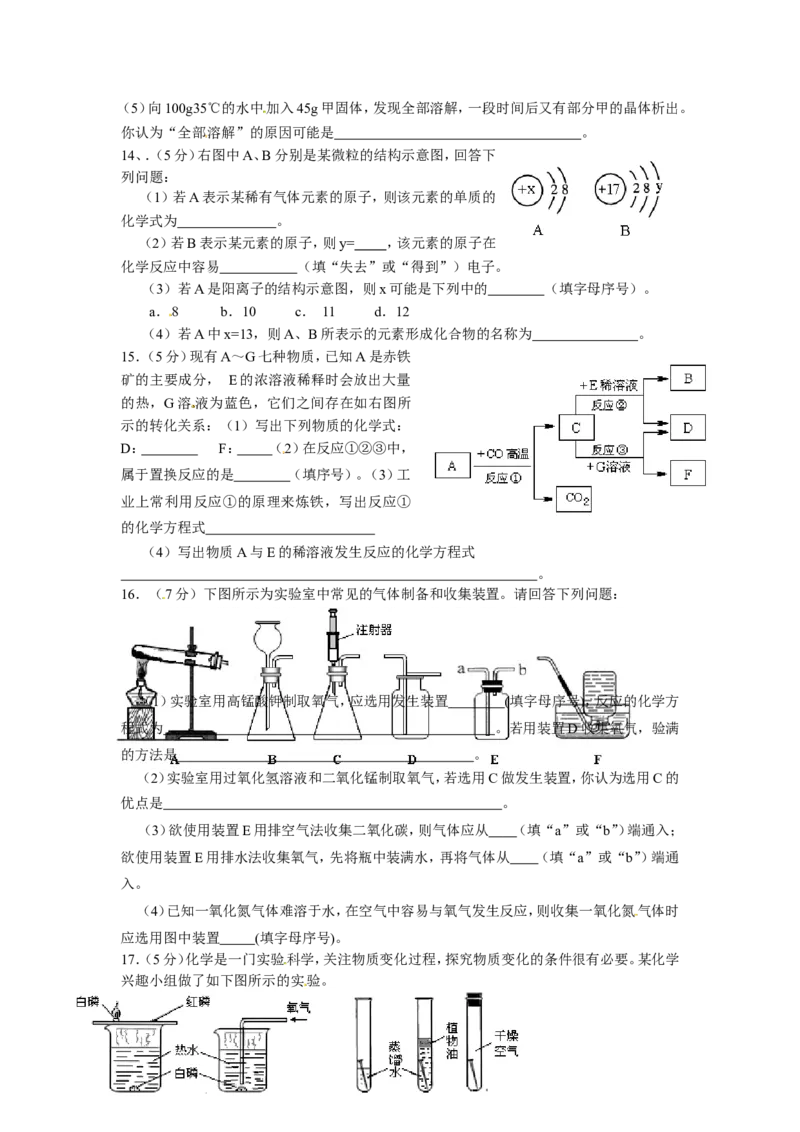
13.(5分)甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
(1)25℃时,将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量为
g。
(2)要使35℃时接近饱和的甲溶液变成该温度下的饱和
溶液,可采用的一种方法是 。
(3)现有操作步骤: a.溶解 b.过滤 c.降温结晶
d.加热浓缩;若甲固体中含有少量乙,则提纯甲的操作步骤是
(填字母序号)。
(4)将35℃时丙的饱和溶液降温到25℃,则其溶液的溶质质量分数
(填“变大”、“变小”或“不变”)。
2(5)向100g35℃的水中加入45g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出。
你认为“全部溶解”的原因可能是 。
14、.(5分)右图中A、B分别是某微粒的结构示意图,回答下
列问题:
(1)若A表示某稀有气体元素的原子,则该元素的单质的
化学式为 。
(2)若B表示某元素的原子,则y= ,该元素的原子在
化学反应中容易 (填“失去”或“得到”)电子。
(3)若A是阳离子的结构示意图,则x可能是下列中的 (填字母序号)。
a.8 b.10 c. 11 d.12
(4)若A中x=13,则A、B所表示的元素形成化合物的名称为 。
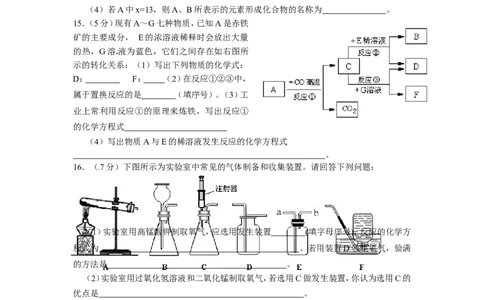
15.(5分)现有A~G七种物质,已知A是赤铁
矿的主要成分, E的浓溶液稀释时会放出大量
的热,G溶液为蓝色,它们之间存在如右图所
示的转化关系:(1)写出下列物质的化学式:
D: F: (2)在反应①②③中,
属于置换反应的是 (填序号)。(3)工
业上常利用反应①的原理来炼铁,写出反应①
的化学方程式
(4)写出物质A与E的稀溶液发生反应的化学方程式
。
16.(7分)下图所示为实验室中常见的气体制备和收集装置。请回答下列问题:
(1)实验室用高锰酸钾制取氧气,应选用发生装置 (填字母序号),反应的化学方
程式为 。若用装置D收集氧气,验满
的方法是 。
(2)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C做发生装置,你认为选用C的
优点是 。
(3)欲使用装置E用排空气法收集二氧化碳,则气体应从 (填“a”或“b”)端通入;
欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从 (填“a”或“b”)端通
入。
(4)已知一氧化氮气体难溶于水,在空气中容易与氧气发生反应,则收集一氧化氮气体时
应选用图中装置 (填字母序号)。
17.(5分)化学是一门实验科学,关注物质变化过程,探究物质变化的条件很有必要。某化学
兴趣小组做了如下图所示的实验。
3A .探究燃烧的条件 B.探究铁钉生锈的条件
根据上述实验,回答下列问题:
(1) 实验A 是通过控制哪些因素来探究可燃物燃烧的条件?
(2) 写出白磷燃烧的化学方程式
(3)实验B中,中间试管的实验目的是什么?
(4)请总结出铁制品发生锈蚀的主要条件
(5)写出防止铁制品锈蚀的一种方法 。
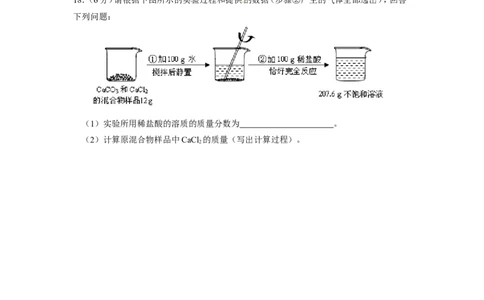
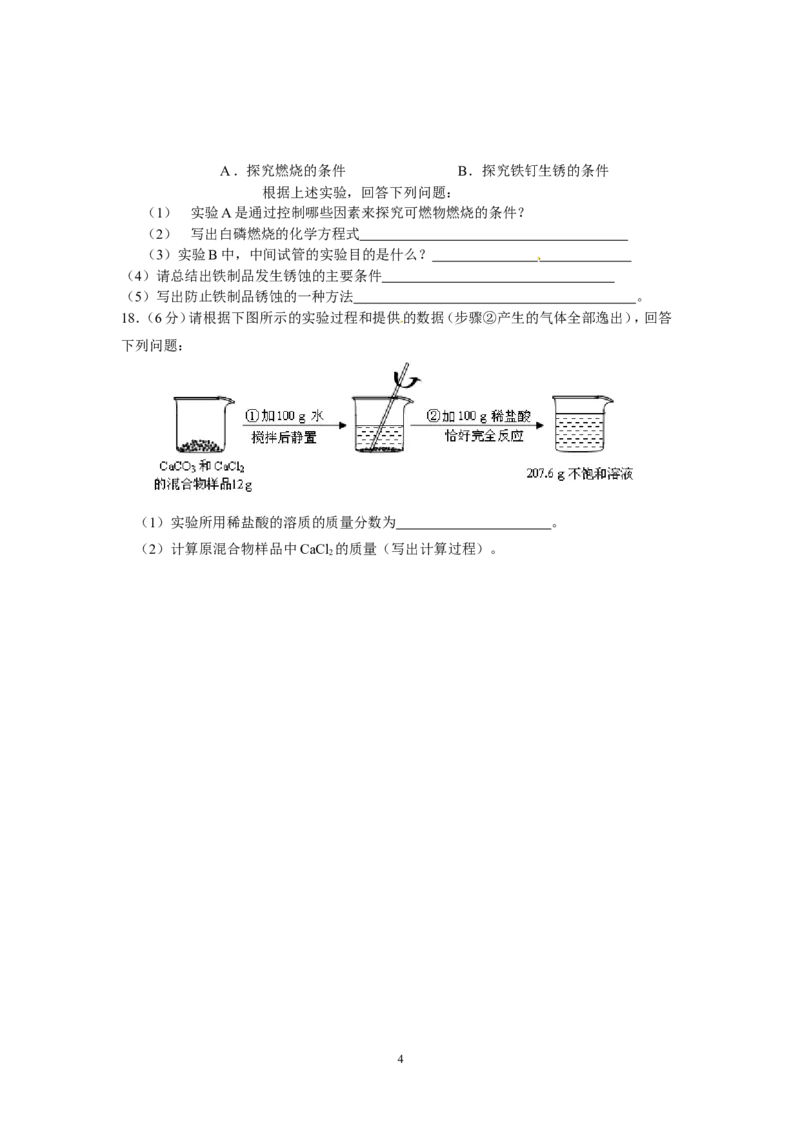
18.(6分)请根据下图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),回答
下列问题:
(1)实验所用稀盐酸的溶质的质量分数为 。
(2)计算原混合物样品中CaCl 的质量(写出计算过程)。
2
4遵义市2013年初中毕业生学业(升学)统一考试
综合理科模拟试题(三)参考答案及评分意见
化 学 部 分
说明:1.本参答案及评分意见供阅卷时使用,考生若写出其它正确答案同样给相应分数。
2.物质名称、化学专用名词有错别字均扣相应题目的分数。
3.化学方程式l分。书写时化学式有错不给分;化学式全对,但配平、反应条件、
气体、沉淀符号有错或未注明给O.5分。
一、选择题(本大题包括10个小题,每小题2分,共20分。)
题号 1 2 3 4 5 6 7 8 9 10
答案 C D B B C D A B C D
二、非选择题(本大题包括8个小题,11-17小题每空1分,18小题6分,共40分。)
11 (每空1分,共4分)
(1)3S (2)HNO (3)2O (4)NH +
3 2 4
12(每空1分,共3分)
(1)4Al3O 2Al O ;⑵Ca(OH) + CO === CaCO↓+ HO;
2 2 3 2 2 3 2
⑶Fe O 4CO高温3Fe4CO 。
3 4 2
13.(每空1分,共5分)
(1)65 (2)加入甲物质(溶质)或恒温蒸发溶剂(水)(3)adcb (4)不变)
(5)甲固体溶于水时放热(1分)
14.(每空1分,共5分)
(1)Ne (2)7 得到
(3)cd (4)氯化铝
15.(每空1分,共5分)
(1)FeSO Cu (2)②③
4
(3)Fe O+3CO 2 Fe+3CO
2 3 2
(4)Fe O+3H SO == Fe (SO )+3H O
2 3 2 4 2 4 3 2
16(每空1分,共7分)
(1)A 2KMnO KMnO + MnO+ O ↑
4 2 4 2 2
将带火星的木条置于集气瓶口,木条复燃,证明已集满
(2)控制氧气产生的快慢和量的多少
5(3)a b) (4)F
17.(每空1分,共5分)
(1)可燃物是否与氧气(或空气)接触,可燃物是否达到燃烧所需的温度
(2)4P+5O 2PO
2 2 5
(3)探究铁钉在隔绝空气(氧气)的条件下是否生锈
(4)铁制品同时与空气和水直接接触;
(5)在铁制品表面涂油、覆盖油漆或在表面镀一层抗腐蚀的金属等(1分,答出1种方法即
可)
18(6分)
(1)7.3% (1分)
(2)解:反应中生成CO 的质量为:12g+100g+100g-207.6g= 4.4g .........(1分)
2
设原混合物中 CaCO 的质量为x
3
CaCO + 2HCl == CaCl + H O + CO ↑ ........................................... (1分)
3 2 2 2
100 44
x 4.4g
......................................................................(1分)
x = 10g ..........................................................................(1分)
原混合物样品中CaCl 的质量为:12g-10g= 2g ..........................(1分)
2
答:原混合物样品中CaCl 的质量为2g。
2
6