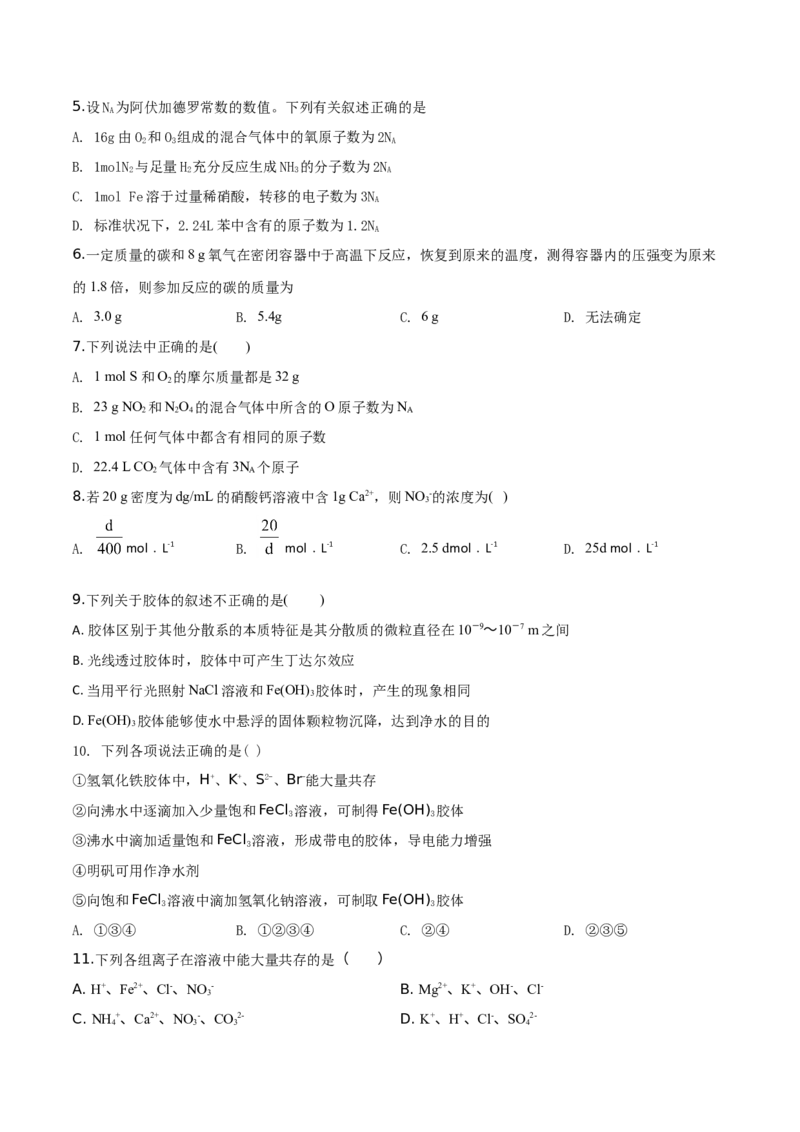文档内容
城郊市重点联合体期中考试高一年级化学试卷
可能用到的相对原子质量:O—16 C—12 S—32 N—14 Ca—40 Pd—106 Na—23 H—1
第Ⅰ卷(选择题 共60分)
一、选择题(本题包括20个小题,每小题3分,共60分。每小题只有一个选项符合题
意。)
1.明朝《菽园杂记》有海水提取食盐的记载:“烧草为灰,布在滩场,然后以海水渍之,侯晒结浮白,扫
而复淋”。该过程中“灰”的作用是( )
A. 萃取 B. 吸附 C. 结晶 D. 蒸发
2.粗盐水过滤后仍含有可溶性的CaCl 、MgCl 、NaSO 等杂质,通过如下几个实验步骤可以除去这些杂质。
2 2 2 4
①加入稍过量的NaCO 溶液; ②加入稍过量的NaOH溶液:
2 3
③加入稍过量的BaCl 溶液: ④过滤; ⑤滴入稀盐酸至无气泡产生。
2
正确的操作顺序是
A. ①③②④⑤ B. ③②①④⑤ C. ②③①⑤④ D. ③④②①⑤
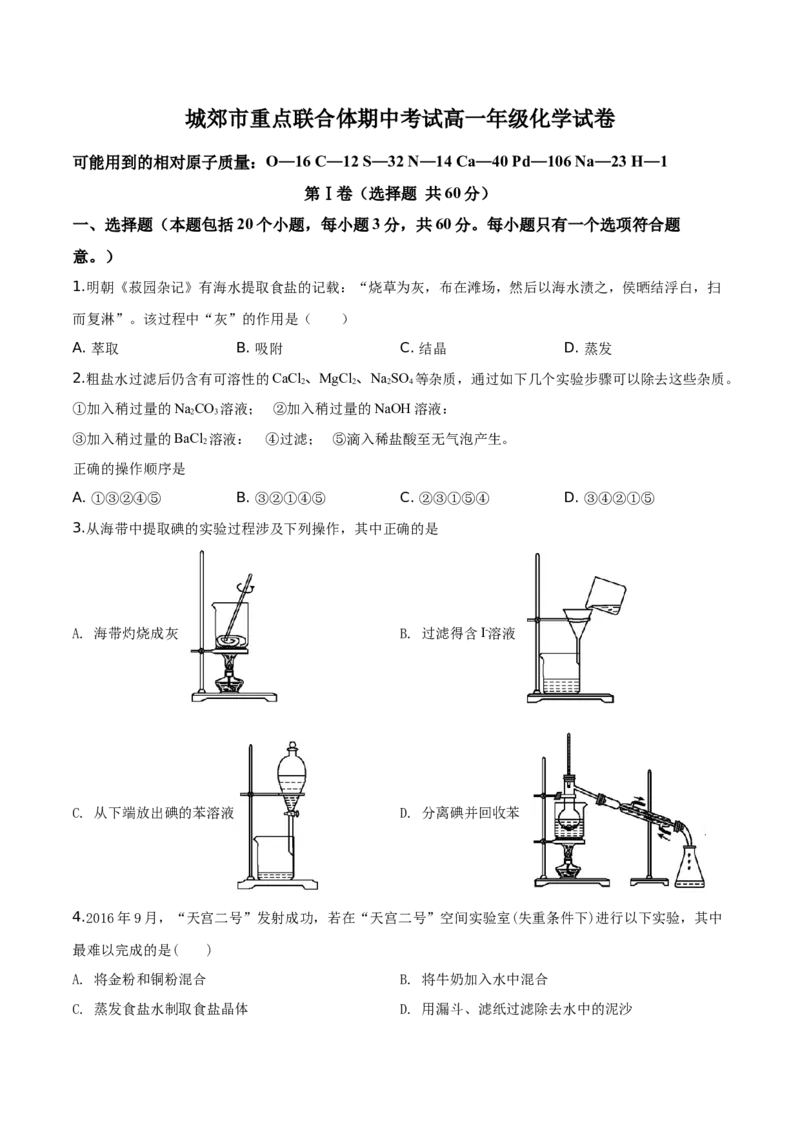
3.从海带中提取碘的实验过程涉及下列操作,其中正确的是
A. 海带灼烧成灰 B. 过滤得含I-溶液
C. 从下端放出碘的苯溶液 D. 分离碘并回收苯
4.2016年9月,“天宫二号”发射成功,若在“天宫二号”空间实验室(失重条件下)进行以下实验,其中
最难以完成的是( )
A. 将金粉和铜粉混合 B. 将牛奶加入水中混合
C. 蒸发食盐水制取食盐晶体 D. 用漏斗、滤纸过滤除去水中的泥沙5.设N 为阿伏加德罗常数的数值。下列有关叙述正确的是
A
A. 16g由O 和O 组成的混合气体中的氧原子数为2N
2 3 A
B. 1molN 与足量H 充分反应生成NH 的分子数为2N
2 2 3 A
C. 1mol Fe溶于过量稀硝酸,转移的电子数为3N
A
D. 标准状况下,2.24L苯中含有的原子数为1.2N
A
6.一定质量的碳和8 g氧气在密闭容器中于高温下反应,恢复到原来的温度,测得容器内的压强变为原来
的1.8倍,则参加反应的碳的质量为
A. 3.0 g B. 5.4g C. 6 g D. 无法确定
7.下列说法中正确的是( )
A. 1 mol S和O 的摩尔质量都是32 g
2
B. 23 g NO 和NO 的混合气体中所含的O原子数为N
2 2 4 A
C. 1 mol任何气体中都含有相同的原子数
D. 22.4 L CO 气体中含有3N 个原子
2 A
8.若20 g密度为dg/mL的硝酸钙溶液中含1g Ca2+,则NO -的浓度为( )
3
A. mol﹒L-1 B. mol﹒L-1 C. 2.5 dmol﹒L-1 D. 25d mol﹒L-1
9.下列关于胶体的叙述不正确的是( )
A. 胶体区别于其他分散系的本质特征是其分散质的微粒直径在10-9~10-7 m之间
B. 光线透过胶体时,胶体中可产生丁达尔效应
C. 当用平行光照射NaCl溶液和Fe(OH) 胶体时,产生的现象相同
3
D. Fe(OH) 胶体能够使水中悬浮的固体颗粒物沉降,达到净水的目的
3
10. 下列各项说法正确的是( )
①氢氧化铁胶体中,H+、K+、S2-、Br-能大量共存
②向沸水中逐滴加入少量饱和FeCl 溶液,可制得Fe(OH) 胶体
3 3
③沸水中滴加适量饱和FeCl 溶液,形成带电的胶体,导电能力增强
3
④明矾可用作净水剂
⑤向饱和FeCl 溶液中滴加氢氧化钠溶液,可制取Fe(OH) 胶体
3 3
A. ①③④ B. ①②③④ C. ②④ D. ②③⑤
11.下列各组离子在溶液中能大量共存的是( )
A. H+、Fe2+、Cl-、NO - B. Mg2+、K+、OH-、Cl-
3
C. NH +、Ca2+、NO -、CO2- D. K+、H+、Cl-、SO 2-
4 3 3 412.某工厂排放的工业废水中可能含有K+、Ag+、NH +、Mg2+、SO2-、Cl-、NO-、HCO-等离子.经检测
4 4 3 3
废水呈明显的碱性,则可确定该厂废水中肯定不含有的离子组合是
.
A Ag+、K+、NO-、HCO- B. K+、NH +、NO-、SO2-
3 3 4 3 4
C. Ag+、NH +、Mg2+、HCO- D. K+、Mg2+、SO2-、Cl-
4 3 4
13.OF 可以发生反应:HS+4OF=SF +2HF+4O。下列说法正确 的是( )
2 2 2 2 2 6 2
A. 氧气是氧化产物
B. OF 既是氧化剂又是还原剂
2 2
C. 若生成0.1molHF,则转移0.8mol电子
D. 还原剂与氧化剂的物质的量之比为1:4
14.下列氧化还原反应所标出的电子转移情况中没有错误的是( )
A. +2H O
2
B. +2HNO +9H O
3 2
C.
D. +3H O+KCl
2
15.已知常温下可用Co O 制备Cl,反应前后体系中共存在六种微粒:Co O、HO、Cl、H+、Cl-和Co2
2 3 2 2 3 2 2
+。下列有关该反应的叙述不正确的是( )
A. 氧化产物为Cl
2
B. 氧化剂与还原剂的物质的量之比为1∶2C. 当生成3 mol HO时,反应中转移2 mol电子
2
.
D 当生成2.24 L(标准状况下)Cl 时,反应中转移0.1 mol电子
2
16.Fe3+、SO 2-、Mg2+、和X四种离子以物质的量之比2∶3∶2∶4大量共存于同一种溶液中,X可能是(
4
)
A. NH + B. OH- C. CO2- D. Cl-
4 3
17.下列物质中含有Cl-的是( )
A. 液态氯化氢 B. 次氯酸钠溶液
C. 固体氯化钠 D. 四氯化碳
18.工业生产中需对空气中的CO进行监测,粉红色的PdCl 溶液可以检验空气中少量的CO。若空气中含
2
CO,则溶液中会产生黑色的Pd沉淀(反应中只有PdCl 作氧化剂)。每生成5.3gPd沉淀,反应转移的电子
2
数为
.
A 0.05 N B. 0.1 N C. 0.2 N D. 0.4 N
A A A A
19.下列反应中,氧化剂与还原剂的物质的量之比为1∶2的是( )
①2NaO+2HO=4NaOH+O ②3S+6NaOH 2NaS+NaSO +3HO ③SiO+3C SiC+2CO↑
2 2 2 2 2 2 3 2 2
④4HCl(浓)+MnO MnCl +Cl↑+2HO
2 2 2 2
A. 仅有② B. 仅有②④ C. 仅有③④ D. ①②③④
20.下列变化过程一定需要加入还原剂的是( )
A. KClO→KCl B. KCl→AgCl
3
C. H+→H D. C→CO
2 2
第Ⅱ卷(填空题 共40分)
21.配制400mL 0.5mol/L的NaOH溶液,试回答下列问题:
(1)计算:需要NaOH固体的质量为_______________.
(2)某学生用托盘天平称量一个小烧杯的质量,称量前把游码放在标尺的零刻度处,天平静止时发现指
针在分度盘的偏右位置,此时左边的托盘将____________(填“高于”或“低于”)右边的托盘.欲使天
平平衡,所进行的操作为___________________________________________,
假定最终称得小烧杯的质量为______(填“32.6g”或“31.61g”)。
(3)配制方法:设计五个操作步骤:
①向盛有NaOH 的烧杯中加入200mL蒸馏水使其溶解,并冷却至室温;
②继续往容量瓶中加蒸馏水至液面接近刻度线1~2cm处;
③将NaOH溶液沿玻璃棒注入500mL容量瓶中;④在烧杯中加入少量的蒸馏水,小心洗涤2~3次后移入容量瓶;
⑤改用胶头滴管加蒸馏水至刻度线,加盖摇匀.
试将以上操作排出先后顺序________________________________________.
(4)某学生实际配制NaOH溶液的浓度为0.48mol/L,原因可能是__________________.
A.使用滤纸称量氢氧化钠固体 B.容量瓶中原来存有少量蒸馏水
C.溶解NaOH的烧杯未经多次洗涤 D.胶头滴管加水后定容时仰视刻度
(5)在如图配制0.5mol/LNaOH溶液过程示意图中有错误的(填序号)____________.
22.NaClO 是一种重要的杀菌消毒剂,也常用来漂白织物等,其中一种生产工艺如下:步骤一,利用
2
NaClO 在硫酸作用下与SO 反应生成 ClO 和一种酸式盐。步骤二,将ClO 在NaOH溶液中与H O 反
3 2 2 2 2 2
应即可生成NaClO
2
回答下列问题:
(1)NaClO 中Cl的化合价为_____________。
2
(2)写出步骤一中生成ClO 的化学方程式____________________
2
(3) 步骤二反应中氧化剂与还原剂的物质的量之比为_________________,该反应中氧化产物是
____________________。
(4)亚氯酸钠(NaClO )在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为
2
HClO ―→ClO ↑+H++Cl-+H O(未配平)。在该反应中,当有1 mol ClO 生成时转移的电子个数约为
2 2 2 2
______________。
(5)Cl 、H O 、ClO (还原产物为Cl-)、O (1 mol O 转化为1 mol O 和1 mol H O)等物质常被用作
2 2 2 2 3 3 2 2
消毒剂。等物质的量的上述物质消毒效率最高的是________(填序号)。A.Cl B.H O C.ClO D.O
2 2 2 2 3
(6)H O 有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如
2 2
KCN),经以下反应实现:KCN+H O +H O=A+NH ↑,则生成物A的化学式为________,H O 被称为
2 2 2 3 2 2
“绿色氧化剂”的理由是___________________。
23.A、B、C、D、E均为可溶于水的固体,组成它们的离子有:
阳离子 Na+、Mg2+、Al3+、Ba2+
阴离子 OH﹣、Cl﹣、CO2﹣、SO 2﹣、HSO ﹣
3 4 4
分别取它们的水溶液进行实验.
已知:Al3+ + 3OH- = Al(OH) ↓,Al(OH) +OH-=AlO -+2H O结果如下:
3 3 2 2
①A溶液与B溶液反应生成白色沉淀,沉淀可溶于E溶液;
②A溶液与C溶液反应生白色沉淀,沉淀可溶于E溶液;
③A溶液与D溶液反应生成白色沉淀,沉淀可溶于盐酸;
④B溶液与适量D溶液反应生成白色沉淀,加入过量D溶液,沉淀量减少,但不消失.据此推断它们是:
A_________;B___________;C___________;D____________.