文档内容
辽宁省锦州市 2013 年中考化学模拟试卷 2
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Cl—35.5 S—32 Fe—56
Zn—65
一、 选择题(本大题包括12道小题,共16分。其中1~8小题每小题1分,9~12小题每小题
2分。每小题只有一个选项符合题意,请将符合题意选项前的字母填在下表内)
1.下列典故中,从物质变化的角度分析,主要体现化学变化的是( )
A.司马光砸缸 B.凿壁偷光 C.火烧赤壁 D.铁杵磨成针
2.“分类”是化学学习和研究的重要方法之一,下列分类中不正确的是( )
A.硫酸铜、食盐、纯碱— 盐
B.硫酸铵、硝酸钾、尿素—氮肥
C.空气、煤气、碘酒—混合物
D.硫元素、氧元素、氦元素—非金属元素
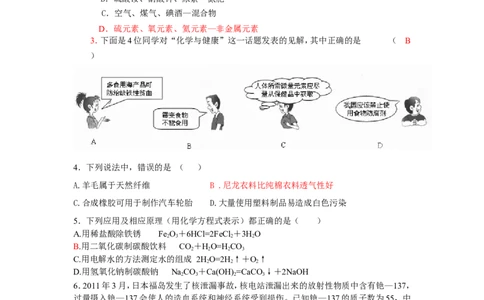
3.下面是4位同学对“化学与健康”这一话题发表的见解,其中正确的是 ( B
)
4.下列说法中,错误的是 ( )
A.羊毛属于天然纤维 B .尼龙衣料比纯棉衣料透气性好
C.合成橡胶可用于制作汽车轮胎 D.大量使用塑料制品易造成白色污染
5.下列应用及相应原理(用化学方程式表示)都正确的是( )
A.用稀盐酸除铁锈 Fe O+6HCl=2FeCl +3HO
2 3 2 2
B.用二氧化碳制碳酸饮料 CO+HO=HCO
2 2 2 3
C.用电解水的方法测定水的组成 2HO=2H↑+O↑
2 2 2
D.用氢氧化钠制碳酸钠 NaCO+Ca(OH) =CaCO ↓+2NaOH
2 3 2 3
6.2011年3月,日本福岛发生了核泄漏事故,核电站泄漏出来的放射性物质中含有铯—137,
过量摄入铯—137会使人的造血系统和神经系统受到损伤。已知铯—137的质子数为55,中
子数为82,下列有关铯—137的说法正确的是 ( )
A.铯—137原子的核外电子数为82
B.铯—137的相对原子质量为137 g
C.铯—137原子的核电荷数为55
D.铯—137属于非金属元素
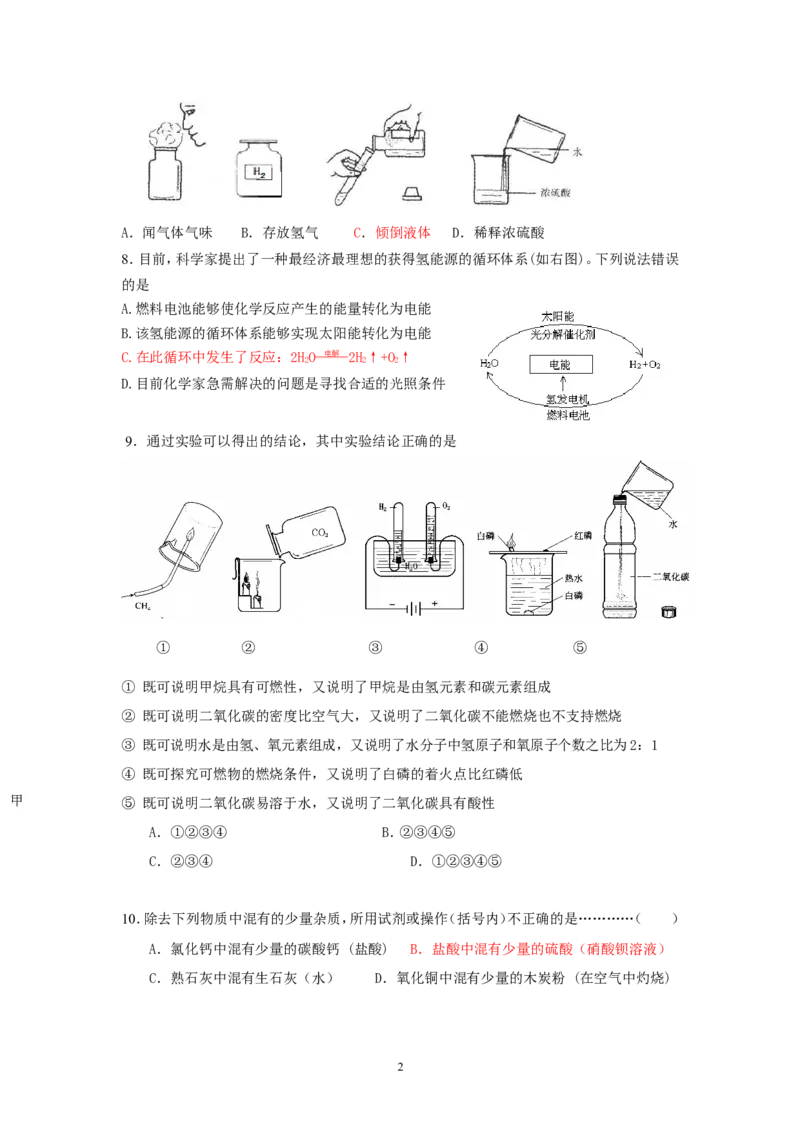
7.正确的化学实验操作对实验结果、人身安全都非常重要。在下图所示实验操作中正确的是
1A.闻气体气味 B.存放氢气 C.倾倒液体 D.稀释浓硫酸
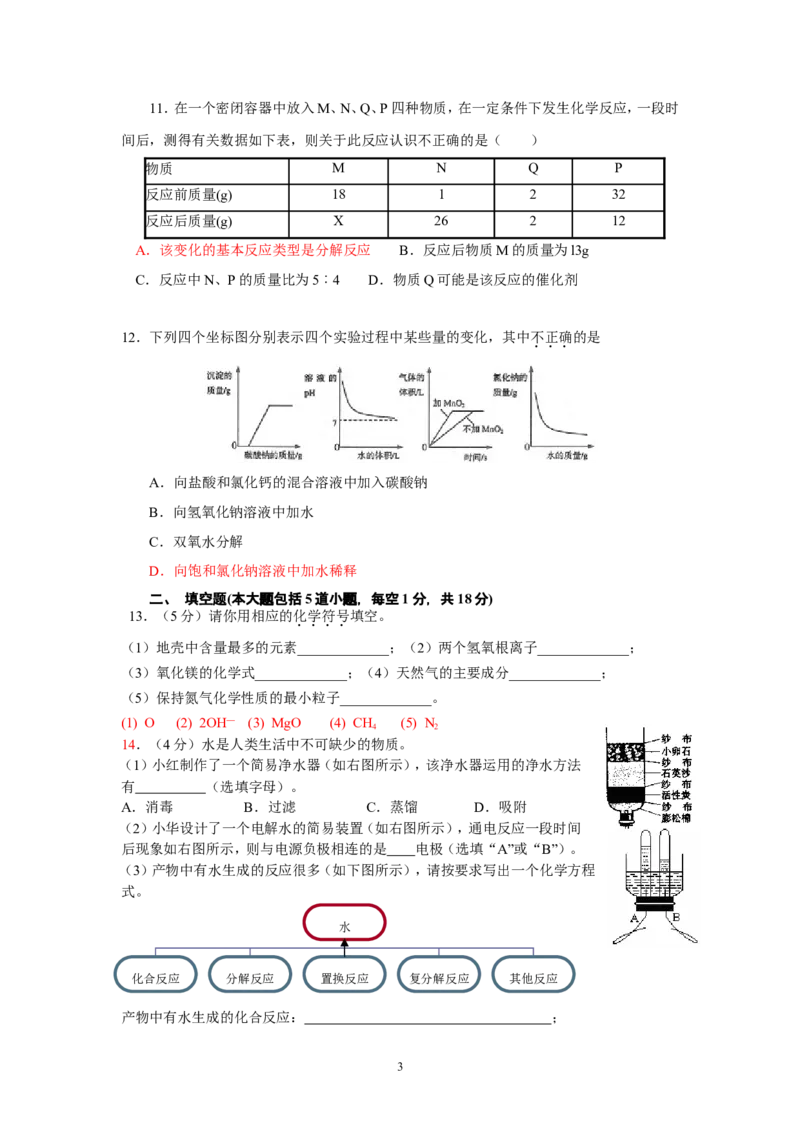
8.目前,科学家提出了一种最经济最理想的获得氢能源的循环体系(如右图)。下列说法错误
的是
A.燃料电池能够使化学反应产生的能量转化为电能
B.该氢能源的循环体系能够实现太阳能转化为电能
C.在此循环中发生了反应:2HO 电解 2H↑+O↑
2 2 2
D.目前化学家急需解决的问题是寻找合适的光照条件
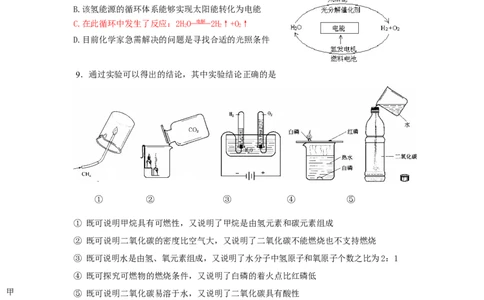
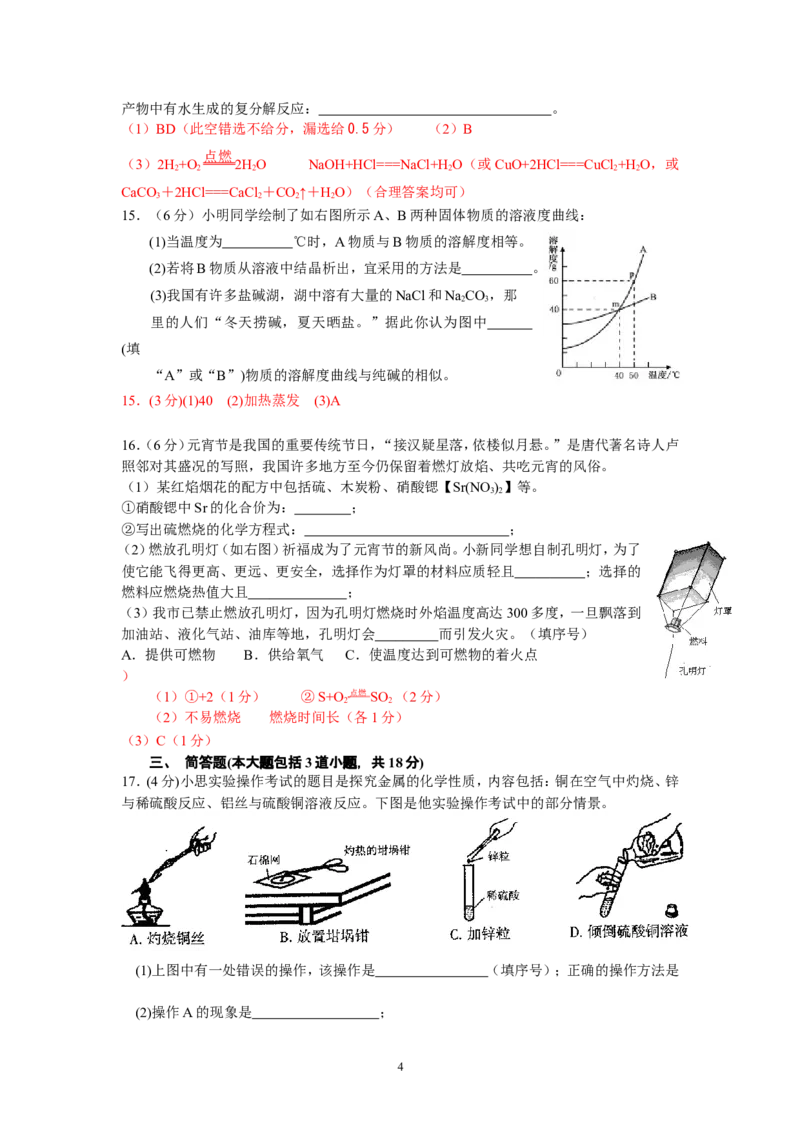
9.通过实验可以得出的结论,其中实验结论正确的是
① ② ③ ④ ⑤
① 既可说明甲烷具有可燃性,又说明了甲烷是由氢元素和碳元素组成
② 既可说明二氧化碳的密度比空气大,又说明了二氧化碳不能燃烧也不支持燃烧
③ 既可说明水是由氢、氧元素组成,又说明了水分子中氢原子和氧原子个数之比为2:1
④ 既可探究可燃物的燃烧条件,又说明了白磷的着火点比红磷低
甲 ⑤ 既可说明二氧化碳易溶于水,又说明了二氧化碳具有酸性
A.①②③④ B.②③④⑤
C.②③④ D.①②③④⑤
10.除去下列物质中混有的少量杂质,所用试剂或操作(括号内)不正确的是…………( )
A.氯化钙中混有少量的碳酸钙 (盐酸) B.盐酸中混有少量的硫酸(硝酸钡溶液)
C.熟石灰中混有生石灰(水) D.氧化铜中混有少量的木炭粉 (在空气中灼烧)
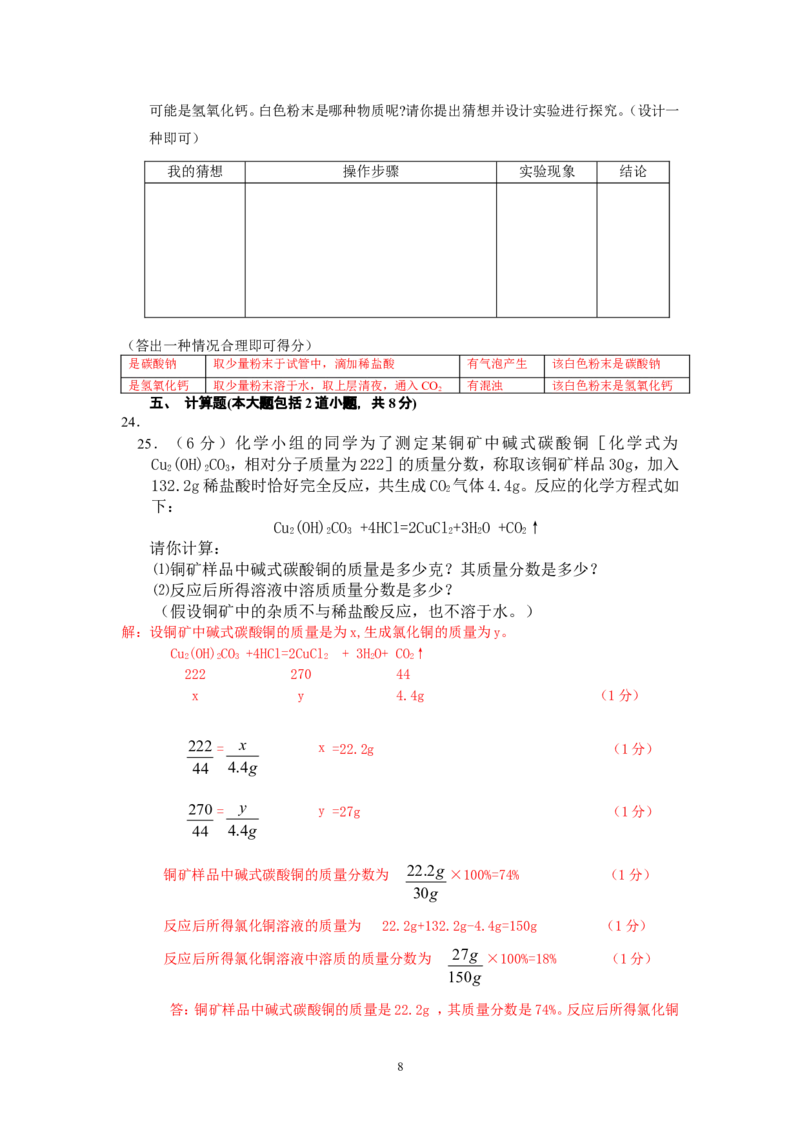
211.在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时
间后,测得有关数据如下表,则关于此反应认识不正确的是( )
物质 M N Q P
反应前质量(g) 18 1 2 32
反应后质量(g) X 26 2 12
A.该变化的基本反应类型是分解反应 B.反应后物质M的质量为l3g
C.反应中N、P的质量比为5︰4 D.物质Q可能是该反应的催化剂
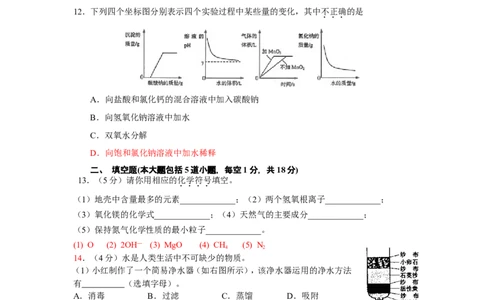
12.下列四个坐标图分别表示四个实验过程中某些量的变化,其中不正确的是
A.向盐酸和氯化钙的混合溶液中加入碳酸钠
B.向氢氧化钠溶液中加水
C.双氧水分解
D.向饱和氯化钠溶液中加水稀释
二、 填空题(本大题包括5道小题,每空1分,共18分)
13.(5分)请你用相应的化学符号填空。
(1)地壳中含量最多的元素_____________;(2)两个氢氧根离子_____________;
(3)氧化镁的化学式_____________;(4)天然气的主要成分_____________;
(5)保持氮气化学性质的最小粒子_____________。
(1) O (2) 2OH— (3) MgO (4) CH (5) N
4 2
14.(4分)水是人类生活中不可缺少的物质。
(1)小红制作了一个简易净水器(如右图所示),该净水器运用的净水方法
有 (选填字母)。
A.消毒 B.过滤 C.蒸馏 D.吸附
(2)小华设计了一个电解水的简易装置(如右图所示),通电反应一段时间
后现象如右图所示,则与电源负极相连的是 电极(选填“A”或“B”)。
(3)产物中有水生成的反应很多(如下图所示),请按要求写出一个化学方程
式。
水
化合反应 分解反应 置换反应 复分解反应 其他反应
产物中有水生成的化合反应: ;
3产物中有水生成的复分解反应: 。
(1)BD(此空错选不给分,漏选给0.5分) (2)B
点燃
(3)2H+O 2HO NaOH+HCl===NaCl+H O(或CuO+2HCl===CuCl +H O,或
2 2 2 2 2 2
CaCO +2HCl===CaCl +CO↑+HO)(合理答案均可)
3 2 2 2
15.(6分)小明同学绘制了如右图所示A、B两种固体物质的溶液度曲线:
(1)当温度为 ℃时,A物质与B物质的溶解度相等。
(2)若将B物质从溶液中结晶析出,宜采用的方法是 。
(3)我国有许多盐碱湖,湖中溶有大量的NaCl和NaCO,那
2 3
里的人们“冬天捞碱,夏天晒盐。”据此你认为图中
(填
“A”或“B”)物质的溶解度曲线与纯碱的相似。
15.(3分)(1)40 (2)加热蒸发 (3)A
16.(6分)元宵节是我国的重要传统节日,“接汉疑星落,依楼似月悬。”是唐代著名诗人卢
照邻对其盛况的写照,我国许多地方至今仍保留着燃灯放焰、共吃元宵的风俗。
(1)某红焰烟花的配方中包括硫、木炭粉、硝酸锶【Sr(NO)】等。
3 2
①硝酸锶中Sr的化合价为: ;
②写出硫燃烧的化学方程式: ;
(2)燃放孔明灯(如右图)祈福成为了元宵节的新风尚。小新同学想自制孔明灯,为了
使它能飞得更高、更远、更安全,选择作为灯罩的材料应质轻且 ;选择的
燃料应燃烧热值大且 ;
(3)我市已禁止燃放孔明灯,因为孔明灯燃烧时外焰温度高达300多度,一旦飘落到
加油站、液化气站、油库等地,孔明灯会 而引发火灾。(填序号)
A.提供可燃物 B.供给氧气 C.使温度达到可燃物的着火点
)
(1)①+2(1分) ②S+O 点燃 SO (2分)
2 2
(2)不易燃烧 燃烧时间长(各1分)
(3)C(1分)
三、 简答题(本大题包括3道小题,共18分)
17.(4分)小思实验操作考试的题目是探究金属的化学性质,内容包括:铜在空气中灼烧、锌
与稀硫酸反应、铝丝与硫酸铜溶液反应。下图是他实验操作考试中的部分情景。
(1)上图中有一处错误的操作,该操作是 (填序号);正确的操作方法是
(2)操作A的现象是 ;
4(3) 他 讲 铝 丝 插 入 到 硫 酸 铜 溶 液 中 , 未 出 现 任 何 现 象 , 其 原 因 是
。
(1)B 试管横放,将锌放在管口,再将试管慢慢竖立起来(2)铜丝表面变黑(3)可能是铝丝
表面的氧化氧化膜没有除去
18.(7分)2010年6月5日,世界环境日中国主题为“低碳减排,绿色生活”,旨在传递低碳
生活理念,提高公众环保意识。该主题倡导减少二氧化碳的排放,低能量、低消耗的生活方式,
从而减少对大气的污染,减缓生态恶化。
(1)下列做法中不符合“低碳绿色生活”理念的是(填序号) ____________。
①节约用水、用电 ②废物分类回收、利用 ③坚持每天测量空气中二氧化碳的含量
④减少一次性餐具的使用
(2)任何事物都有其两面性,二氧化碳在生活、生产中也有着广泛的应用。例如:
①日常生活中做灭火剂,这是利用了二氧化碳 和____________ 的性质。
②工业上用二氧化碳为原料制备纯碱。请写出检验纯碱中 CO2一的方法:
3
________________________________________________。
(3)大气中的二氧化碳利用植物光合作用能生成氧气,请写出实验室中制取氧气的化学
反应方程式________________________。
(4)开发和利用清洁而高效的新能源替代传统能源:
①氢气是未来最理想的能源,理想的制氢方法 。
②开发太阳能、风能、海水热能等能源。目前,烟台太阳能热水器的应用达到总户数的
48%以上;风电装机容量已达到37.4千瓦,居全省第一;并正在尝试利用海水热能来取暖。
这些新能源的利用,除了能减少CO 的排放外,还有哪些好处?
2
。(请列举一条)
(7分)(1)③ (2)①密度比空气大 不燃烧、不支持燃烧
②取少量纯碱,配成溶液,向其中加入少量稀盐酸,产生一种能使澄清石灰水变浑浊的
气体,则证明含有CO2一(试剂、现象合理就得分,试剂、现象各0.5分)
3
MnO
2
(3)2HO HO+O↑
2 2 2 2
(4)①利用太阳能分解水制氢气
②节约煤、石油等不可再生的能源(或降低对环境的污染等其它合理答案也可)
19.(7分)A、B、C、D、E、F、G、H、I都是初中化学学过的物质。其中B为红色固体单质,D为
混合物,E、H均为黑色固体,F是一种无色气体。它们之间有下图的转化关系(部分生成
物已省去)。
△
5(1)用化学式表示D的组成 、 。
(2)F→G的反应类型 。
(3)写出以下三个反应的化学方程式:
①F→E
②H→C
③G→I
(4)指出B的一种用途 。
(1)BaSO Cu (OH) (2) 化合反应
4 2
(3)①Fe O + 3CO 高温 2Fe + 3CO ②CuO + H SO = CuSO + H O
2 3 2 2 4 4 2
③CO + Ca(OH) = CaCO ↓+ H O (4)做导线等
2 2 3 2
四、 实验题(本大题包括4道小题,共20分)
20.(4分)某学生学习了双氧水制氧气的实验后,想起自己家里也有一瓶消毒
用双氧水,但由于标签已部分受损无法判断其是否变质,所以他将该瓶溶液带到学
校,进行了如图所示的研究。
试回答
(1)放入二氧化锰的作用是____________。
(2)如果该溶液未变质,应该观察到的现象是________________________________。
样品中发生反应的化学方程式是_________________________________________。
(3)达到环保要求,试验后二氧化锰的处理是 。
(4)参加动物体内化学反应所起作用与二氧化锰作用相同的有机物叫 。
(1)催化作用
(2)试管内有气泡产生,带火星的木条复燃
MnO
2
2 HO ====2 HO +O↑
2 2 2 2
(3)过滤、晾干备用,不能随意倒掉。 (4)酶或生物催化剂
621.(7分)实验室摆放着如下一排仪器,根据图示,按要求回答下列问题:
(1)仪器C为集气瓶,写出仪器A的名称_____________;在B、D、E中选择一种仪器,该
仪器在实验室主要用于___________________________________________,使用该仪器
时应当注意的问题是__________________________________(写一点)。
(2)按实验原理和气体的性质选择实验装置,可用上图中的仪器组装成实验室制取二氧
化碳气体的发生和收集装置,你选择的仪器是___________(填仪器编号),制取二氧化碳
气体的反应原理是____________________________ _(写化学方程式)。
(3)理论上,上述装置也可用于在二氧化锰作催化剂的条件下,分解过氧化氢水溶液制取
氧气;但实验室用该反应制取氧气时,一般不在是试管中而是在锥形瓶先加入二氧化锰,
且要通过分液漏斗逐滴滴入过氧化氢水溶液,请你说出这样操作的原因
_______________________________________________________________________。
(1)水槽;仪器B,用作少量试剂的反应容器;加热后不能骤冷;仪器D,用作配制溶液和较多
量试剂的反应容器;加热时应放置在石棉网上;仪器E,用于加热;用外焰加热;要
用火柴点燃;不能用嘴吹灭
(2)B、C、G、H;CaCO +2HCl CaCl +H O+CO↑
3 2 2 2
(3)过氧化氢在二氧化锰作催化剂的条件下,反应速度极快,滴加可以控制生成氧气
的速率;如果在试管这样小的空间内,迅速产生大量的气体,易引起瓶塞冲出,液体
喷出伤人
22.(6分)实验助手小娟走进实验室和老师一起检查每个
实验桌上的药品、仪器是否齐备,走到某组的时候,
看到了一个不和谐的“音符”(如右图):
⑴此情此景你首先想到的是它可能变质了,
该变质反应的化学方程式为:
;
⑵围绕此瓶NaOH溶液是否变质的问题,小娟利用实验室的三种试剂(氯化钙溶液、
稀盐酸、酚酞试液)展开了探究活动。①取少量溶液于试管中,滴加某种试剂,有气泡产生,
由此证明NaOH溶液已经变质。你认为小娟所加的试剂是 ;
②欲证明变质的溶液中尚存NaOH,请你帮助小娟完成以下探究方案:
探究目的 探究步骤 预计现象
①:取少量溶液于试管中,
除尽溶液中的CO2- 有白色沉淀产生
3 滴加足量的 试剂
②:向实验①所得溶液中滴
证明溶液中尚存NaOH
加酚酞试液
⑶通过上述探究,说明氢氧化钠溶液暴露在空气中容易变质,故应 保存。
⑴2NaOH+CO =Na CO+H O(2分) ⑵①稀盐酸②氯化钙,酚酞变红 ⑶密封
2 2 3 2
23.(4分)整理实验室时,小明发现实验台上有一瓶失落标签的白色粉末,可能是碳酸钠,也
7可能是氢氧化钙。白色粉末是哪种物质呢?请你提出猜想并设计实验进行探究。(设计一
种即可)
我的猜想 操作步骤 实验现象 结论
(答出一种情况合理即可得分)
是碳酸钠 取少量粉末于试管中,滴加稀盐酸 有气泡产生 该白色粉末是碳酸钠
是氢氧化钙 取少量粉末溶于水,取上层清夜,通入CO 有混浊 该白色粉末是氢氧化钙
2
五、 计算题(本大题包括2道小题,共8分)
24.
25.(6 分)化学小组的同学为了测定某铜矿中碱式碳酸铜[化学式为
Cu (OH) CO ,相对分子质量为222]的质量分数,称取该铜矿样品30g,加入
2 2 3
132.2g稀盐酸时恰好完全反应,共生成CO 气体4.4g。反应的化学方程式如
2
下:
Cu (OH) CO +4HCl=2CuCl +3H O +CO ↑
2 2 3 2 2 2
请你计算:
⑴铜矿样品中碱式碳酸铜的质量是多少克?其质量分数是多少?
⑵反应后所得溶液中溶质质量分数是多少?
(假设铜矿中的杂质不与稀盐酸反应,也不溶于水。)
解:设铜矿中碱式碳酸铜的质量是为x,生成氯化铜的质量为y。
Cu(OH)CO +4HCl=2CuCl + 3HO+ CO↑
2 2 3 2 2 2
222 270 44
x y 4.4g (1分)
222 = x x =22.2g (1分)
44 4.4g
270 = y y =27g (1分)
44 4.4g
22.2g
铜矿样品中碱式碳酸铜的质量分数为 ×100%=74% (1分)
30g
反应后所得氯化铜溶液的质量为 22.2g+132.2g-4.4g=150g (1分)
27g
反应后所得氯化铜溶液中溶质的质量分数为 ×100%=18% (1分)
150g
答:铜矿样品中碱式碳酸铜的质量是22.2g ,其质量分数是74%。反应后所得氯化铜
8溶液中溶质的质量分数是18%。
9