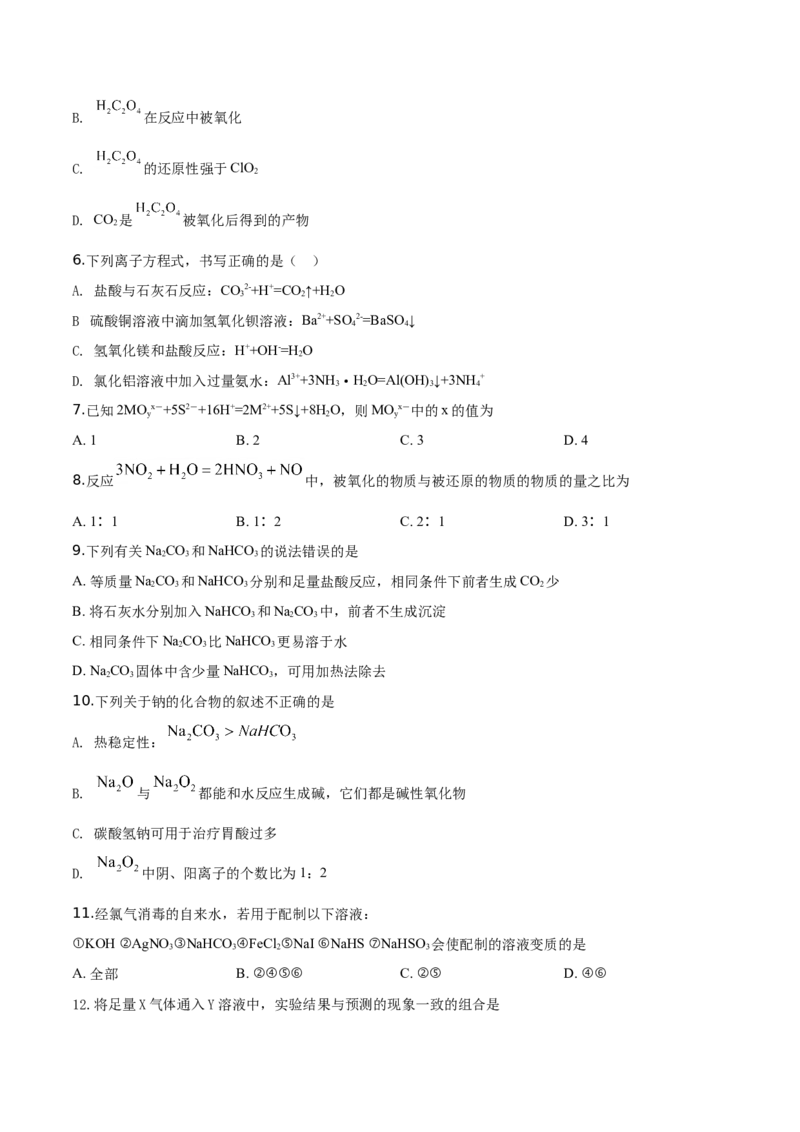文档内容
辽宁省滨海实验中学 2019-2020 学年高一上学期期末化学试题
(2019 新人教版)
一、单选题(本大题共28小题,共56分)
1.下列物质与常用危险化学品的分类不对应的是( )
A. NaOH——腐蚀品 B. Na——遇湿易燃物品
C. 浓硫酸——易爆品 D. KMnO ——氧化剂
4
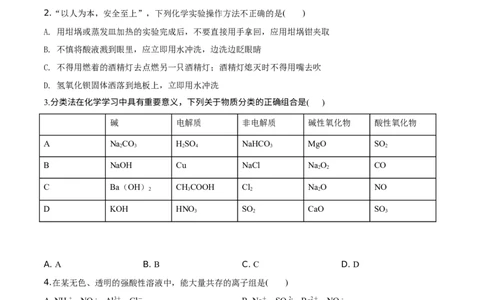
2.“以人为本,安全至上”,下列化学实验操作方法不正确的是( )
A. 用坩埚或蒸发皿加热的实验完成后,不要直接用手拿回,应用坩埚钳夹取
B. 不慎将酸液溅到眼里,应立即用水冲洗,边洗边眨眼睛
C. 不得用燃着的酒精灯去点燃另一只酒精灯;酒精灯熄灭时不得用嘴去吹
D. 氢氧化钡固体洒落到地板上,立即用水冲洗
3.分类法在化学学习中具有重要意义,下列关于物质分类的正确组合是( )
碱 电解质 非电解质 碱性氧化物 酸性氧化物
A NaCO HSO NaHCO MgO SO
2 3 2 4 3 2
B NaOH Cu NaCl NaO CO
2 2
C Ba(OH) CHCOOH Cl NaO NO
2 3 2 2
D KOH HNO SO CaO SO
3 2 3
A. A B. B C. C D. D
4.在某无色、透明的强酸性溶液中,能大量共存的离子组是( )
A. NH+、NO -、Al3+、Cl- B. Na+、SO 2-、Ba2+、NO -
4 3 4 3
.
C MnO-、K+、SO 2-、Na+ D. H+、SO 2-、HCO -、Na+
4 4 4 3
5.ClO 是一种杀菌消毒效率高、二次污染小的水处理剂。实验室中可通过以下反应制得ClO :
2 2
,下列说法不正确的是( )
A. 1mol 参加反应,转移2mol电子B. 在反应中被氧化
C. 的还原性强于ClO
2
D. CO 是 被氧化后得到的产物
2
6.下列离子方程式,书写正确的是( )
A. 盐酸与石灰石反应:CO2-+H+=CO ↑+H O
3 2 2
.
B 硫酸铜溶液中滴加氢氧化钡溶液:Ba2++SO2-=BaSO ↓
4 4
C. 氢氧化镁和盐酸反应:H++OH-=H O
2
D. 氯化铝溶液中加入过量氨水:Al3++3NH·HO=Al(OH) ↓+3NH+
3 2 3 4
7.已知2MO x-+5S2-+16H+=2M2++5S↓+8H O,则MO x-中的x的值为
y 2 y
A. 1 B. 2 C. 3 D. 4
8.反应 中,被氧化的物质与被还原的物质的物质的量之比为
A. 1:1 B. 1:2 C. 2:1 D. 3:1
9.下列有关NaCO 和NaHCO 的说法错误的是
2 3 3
A. 等质量NaCO 和NaHCO 分别和足量盐酸反应,相同条件下前者生成CO 少
2 3 3 2
B. 将石灰水分别加入NaHCO 和NaCO 中,前者不生成沉淀
3 2 3
C. 相同条件下NaCO 比NaHCO 更易溶于水
2 3 3
D. Na CO 固体中含少量NaHCO ,可用加热法除去
2 3 3
10.下列关于钠的化合物的叙述不正确的是
A. 热稳定性:
B. 与 都能和水反应生成碱,它们都是碱性氧化物
C. 碳酸氢钠可用于治疗胃酸过多
D. 中阴、阳离子的个数比为1:2
11.经氯气消毒的自来水,若用于配制以下溶液:
①KOH ②AgNO ③NaHCO ④FeCl ⑤NaI ⑥NaHS ⑦NaHSO 会使配制的溶液变质的是
3 3 2 3
A. 全部 B. ②④⑤⑥ C. ②⑤ D. ④⑥
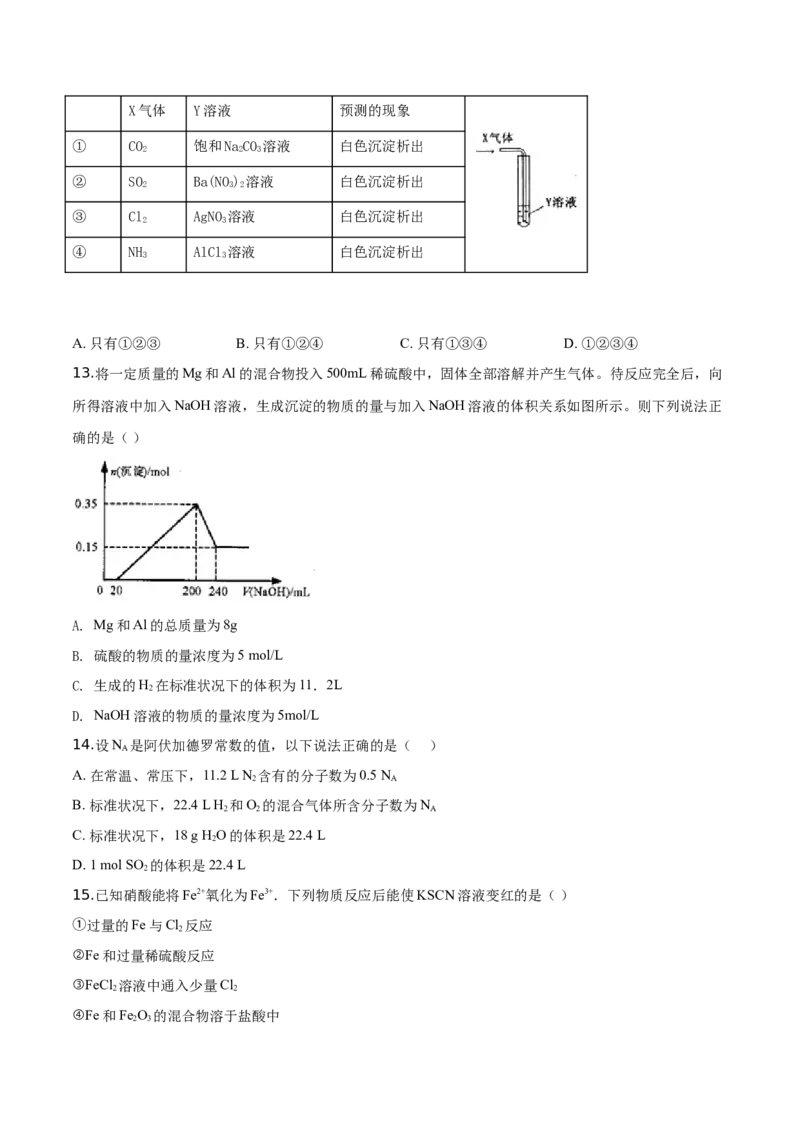
12.将足量X气体通入Y溶液中,实验结果与预测的现象一致的组合是X气体 Y溶液 预测的现象
① CO 饱和NaCO 溶液 白色沉淀析出
2 2 3
② SO Ba(NO) 溶液 白色沉淀析出
2 3 2
③ Cl AgNO 溶液 白色沉淀析出
2 3
④ NH AlCl 溶液 白色沉淀析出
3 3
A. 只有①②③ B. 只有①②④ C. 只有①③④ D. ①②③④
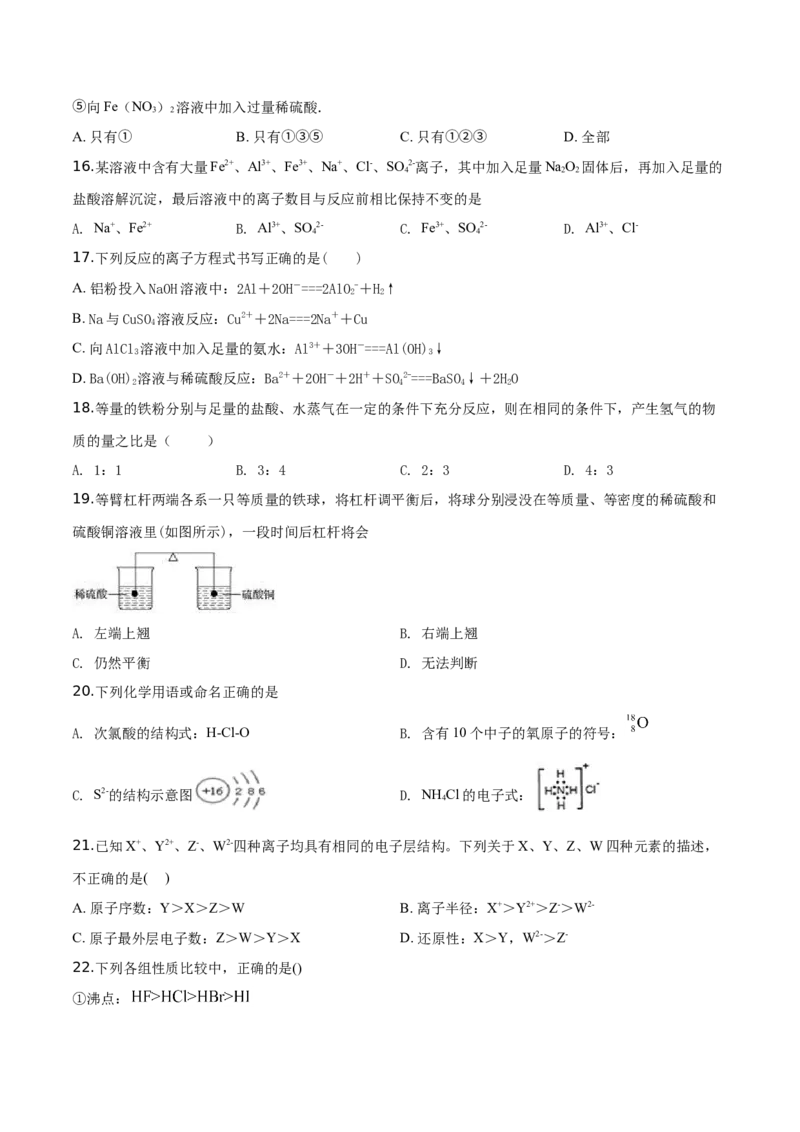
13.将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向
所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。则下列说法正
确的是( )
A. Mg和Al的总质量为8g
B. 硫酸的物质的量浓度为5 mol/L
C. 生成的H 在标准状况下的体积为11.2L
2
D. NaOH溶液的物质的量浓度为5mol/L
14.设N 是阿伏加德罗常数的值,以下说法正确的是( )
A
A. 在常温、常压下,11.2 L N 含有的分子数为0.5 N
2 A
B. 标准状况下,22.4 L H 和O 的混合气体所含分子数为N
2 2 A
C. 标准状况下,18 g HO的体积是22.4 L
2
D. 1 mol SO 的体积是22.4 L
2
15.已知硝酸能将Fe2+氧化为Fe3+.下列物质反应后能使KSCN溶液变红的是( )
①过量的Fe与Cl 反应
2
②Fe和过量稀硫酸反应
③FeCl 溶液中通入少量Cl
2 2
④Fe和Fe O 的混合物溶于盐酸中
2 3⑤向Fe(NO ) 溶液中加入过量稀硫酸.
3 2
A. 只有① B. 只有①③⑤ C. 只有①②③ D. 全部
16.某溶液中含有大量Fe2+、Al3+、Fe3+、Na+、Cl-、SO 2-离子,其中加入足量NaO 固体后,再加入足量的
4 2 2
盐酸溶解沉淀,最后溶液中的离子数目与反应前相比保持不变的是
A. Na+、Fe2+ B. Al3+、SO 2- C. Fe3+、SO 2- D. Al3+、Cl-
4 4
17.下列反应的离子方程式书写正确的是( )
A. 铝粉投入NaOH溶液中:2Al+2OH-===2AlO-+H↑
2 2
B. Na与CuSO 溶液反应:Cu2++2Na===2Na++Cu
4
C. 向AlCl 溶液中加入足量的氨水:Al3++3OH-===Al(OH)↓
3 3
D. Ba(OH) 溶液与稀硫酸反应:Ba2++2OH-+2H++SO2-===BaSO↓+2HO
2 4 4 2
18.等量的铁粉分别与足量的盐酸、水蒸气在一定的条件下充分反应,则在相同的条件下,产生氢气的物
质的量之比是( )
A. 1:1 B. 3:4 C. 2:3 D. 4:3
19.等臂杠杆两端各系一只等质量的铁球,将杠杆调平衡后,将球分别浸没在等质量、等密度的稀硫酸和
硫酸铜溶液里(如图所示),一段时间后杠杆将会
A. 左端上翘 B. 右端上翘
C. 仍然平衡 D. 无法判断
20.下列化学用语或命名正确的是
A. 次氯酸的结构式:H-Cl-O B. 含有10个中子的氧原子的符号:
C. S2-的结构示意图 D. NH Cl的电子式:
4
21.已知X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构。下列关于X、Y、Z、W四种元素的描述,
不正确的是( )
A. 原子序数:Y>X>Z>W B. 离子半径:X+>Y2+>Z->W2-
C. 原子最外层电子数:Z>W>Y>X D. 还原性:X>Y,W2->Z-
22.下列各组性质比较中,正确的是()
①沸点:②离子还原性:
③酸性:
④金属性:
⑤气态氢化物稳定性:
⑥半径:
.
A ①②③ B. ③④⑤⑥ C. ②③④ D. ①③④⑤⑥
23.下列物质中,既有离子键又有共价键的是( )
A. MgCl B. Ca(OH) C. HO D. N
2 2 2 2
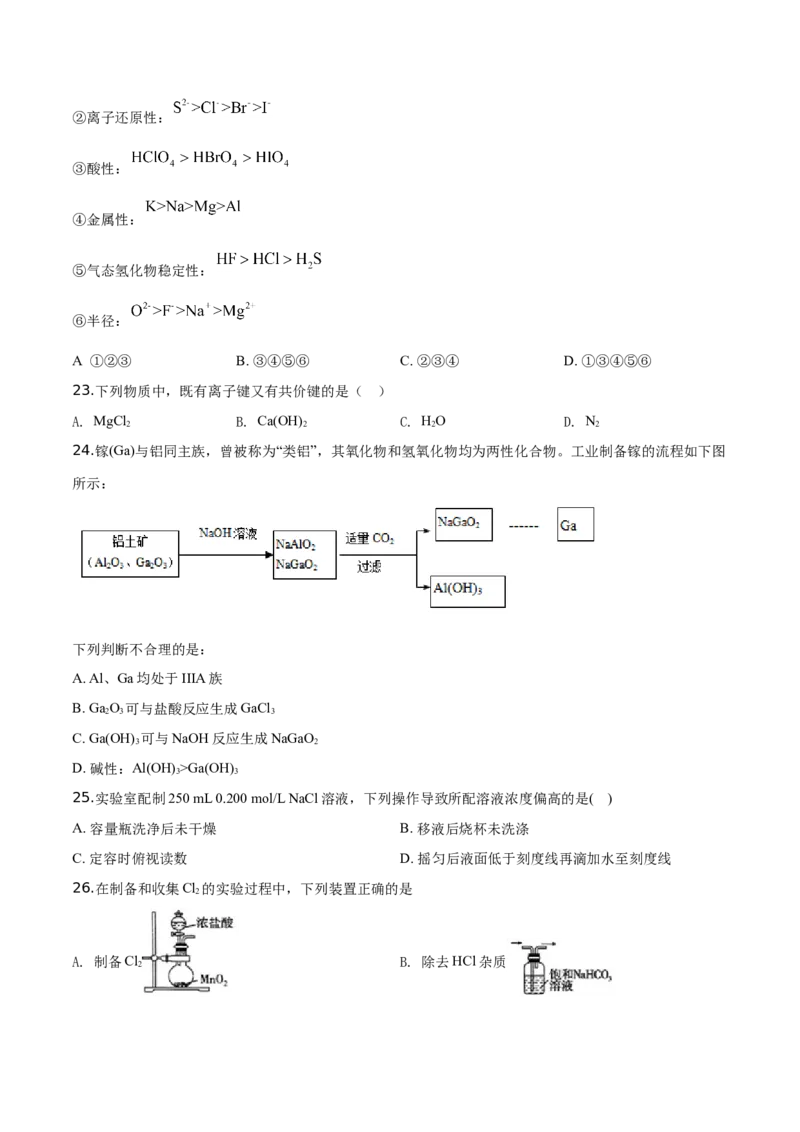
24.镓(Ga)与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。工业制备镓的流程如下图
所示:
下列判断不合理的是:
A. Al、Ga均处于IIIA族
B. Ga O 可与盐酸反应生成GaCl
2 3 3
C. Ga(OH) 可与NaOH反应生成NaGaO
3 2
D. 碱性:Al(OH) >Ga(OH)
3 3
25.实验室配制250 mL 0.200 mol/L NaCl溶液,下列操作导致所配溶液浓度偏高的是( )
A. 容量瓶洗净后未干燥 B. 移液后烧杯未洗涤
C. 定容时俯视读数 D. 摇匀后液面低于刻度线再滴加水至刻度线
26.在制备和收集Cl 的实验过程中,下列装置正确的是
2
A. 制备Cl B. 除去HCl杂质
2.
C 排空气法收集 Cl D. 尾气吸收
2
27.在制作印刷电路板的过程中常利用FeCl 溶液与Cu反应,其反应方程式为:
3
2FeCl +Cu=2FeCl +CuCl 。现向FeCl 溶液中加入a g Cu粉,完全溶解后,再加入b g Fe粉,充分反应后
3 2 2 3
尚有c g残余固体。若c<a,则下列说法正确的是
A. 残余固体全部是Cu
B. 残余固体可能为Fe和Cu的混合物
C. 最后得到的溶液可能含有Fe3+
D. 残余固体是Fe,溶液中一定不含Cu2+
28.用如图所示实验装置进行相关实验探究,其中装置不合理的是( )
A. 鉴别纯碱与小苏打 B. 证明NaO 与水反应放热
2 2
C. 证明Cl 能与烧碱溶液反应 D. 探究钠与Cl 反应
2 2
二、填空题(本大题共2小题,共30分)
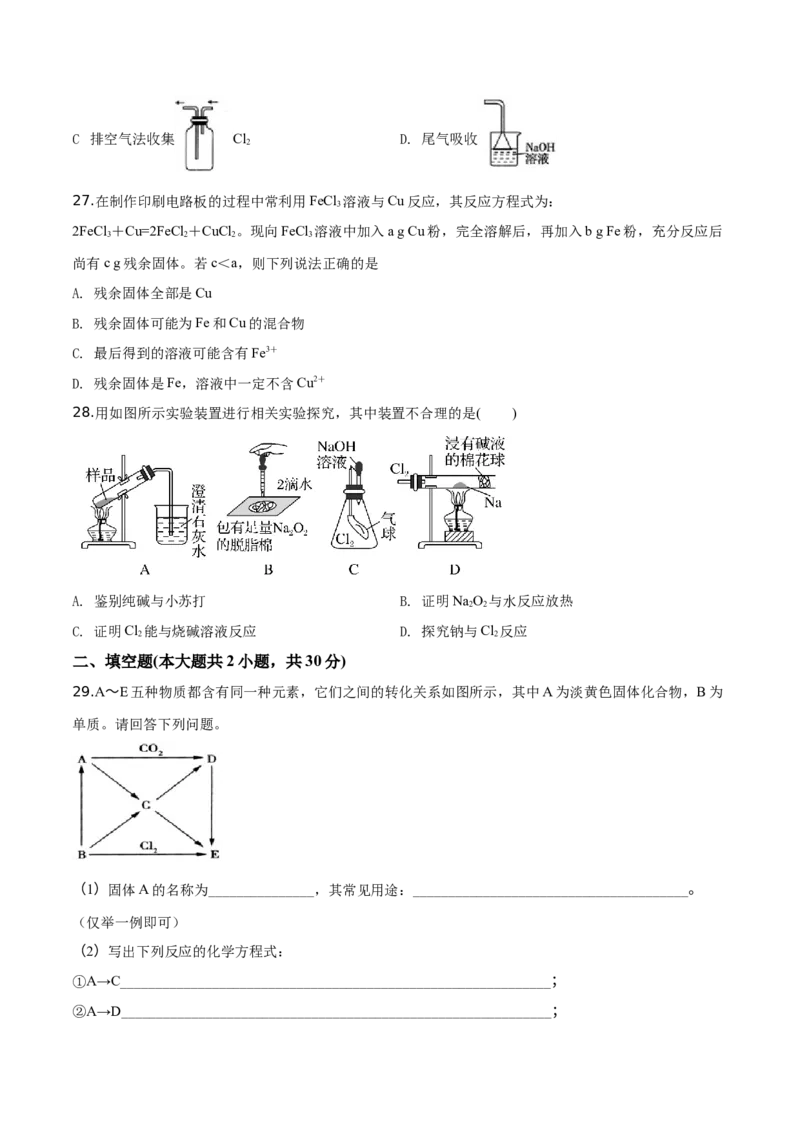
29.A~E五种物质都含有同一种元素,它们之间的转化关系如图所示,其中A为淡黄色固体化合物,B为
单质。请回答下列问题。
(1)固体A的名称为_______________,其常见用途:_______________________________________。
(仅举一例即可)
(2)写出下列反应的化学方程式:
①A→C_____________________________________________________________;
②A→D_____________________________________________________________;③B→A_____________________________________________________________;
④B→C_____________________________________________________________。
30.从古至今,铁及其化合物在人类的生产生活中都起了巨大的作用。
(1)实验室在配制 FeSO 溶液时为了防止 FeSO 溶液变质,经常向其中加入铁粉,其原因是
4 4
______________(用离子方程式表示)。
(2)向FeSO 溶液中滴加氨水的现象为 ______________________,请用化学用语解释出现此现象的原因
4
___________________;_____________________
(3)现有配制所得的 100mL 6mol/L FeSO 溶液,往其中滴入一定量稀硝酸,请回答下列问题:
4
①配平该反应的离子方程式:____Fe2+____NO -+____H+ = ___Fe3++____NO↑+_____HO(在横线上写
3 2
上化学计量数)
②要检验该反应后的溶液中是否还含有 Fe2+,可选用下列的一种试剂为_______
A.酸性 KMnO 溶液 B.KSCN 溶液 C. Cl
4 2
③写出上述②的具体实验方案(含操作、现象、结论):____________________。
④经检验,上述反应后 的溶液中不存在 Fe2+,则该反应过程中产生的 NO 体积为(标准状况
下)____________________L。
三、实验题(本大题共1小题,共14分)
31.某Al O 样品中含有一定量的Cu、Fe、Fe O 杂质。现通过下列生产过程,从该样品中回收铁红。流程如
2 3 2 3
下:
(1)操作a是________,在实验室进行该操作需要的玻璃仪器有烧杯、漏斗和_______。
(2) 试剂①是_______,固体II是_________(填化学式)。
(3)红褐色沉淀的成分是_________;写出白色沉淀转化为红褐色沉淀的化学方程式:______________。
(4)溶液II中铁元素的存在形式是_______(填离子符号),如何用实验证明:__________。