文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
专题 03 金属活动性顺序的验证与探究
【题型一】验证金属活动性顺序
[例题1] (2023•万荣县四模)某些化学小组设计了验证Fe、Cu、Ag的金属活动性顺序
的四种方案,各个方案选用的试剂如下,其中不可行的是( )
A.Fe、CuSO 溶液、Ag
4
B.FeCl 溶液、Cu、AgNO 溶液
2 3
C.Ag、CuSO 溶液、FeSO 溶液
4 4
D.Fe、Cu、AgNO 溶液、盐酸
3
【解答】解:A、铁能置换出硫酸铜中的铜,得出金属活动性铁大于铜,银不能置换出硫酸铜中
的铜,得出金属活动性铜大于银,能验证Fe、Cu、Ag的金属活动性顺序。故A正确。
B、铜不能置换出氯化亚铁中的铁,但置换出硝酸银中的银,说明金属活动性是铁大于铜,铜大
于银。能验证Fe、Cu、Ag的金属活动性顺序。故B正确。
C、银不能置换出硫酸铜中的铜,硫酸亚铁中的铁,能得出铁、铜的活泼性大于银,不能比较铁、
铜的活泼性。故C错误。
D、通过铁能与盐酸反应生成氢气。铜不能与盐酸反应,得出铁的活泼性大于铜;通过铜能置换
出硝酸银中的银,说明金属活动性是铜大于银。能验证 Fe、Cu、Ag的金属活动性顺序。故D
正确。
故选:C。
[例题2] (2023•宁津县二模)为比较 X、Y、Z 三种金属活动性大小,进行如图所示的
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
实验。下列实验结论正确的是( )
A.X>Y>Z B.Z>Y>X C.X>Y、Z>Y D.Y>X、Y>Z
【解答】解:现有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X产生氢气,Y不反
应,说明X的金属活动性比氢强,Y的金属活动性比氢弱,即X>H>Y;如果把Y和Z分别放
入硝酸银溶液中,过一会儿,在Y表面有银析出,而Z没有变化,说明Y的金属活动性比银强,
Z的金属活动性比银弱,即Y>Ag>Z;则X、Y和Z的金属活动性顺序为:X>Y>Z。
故选:A。
1.验证两种金属活动性顺序的方法:
(1)两种金属均在氢后:金属与金属盐溶液反应
(2)两种金属均在氢前或一种金属氢前,另一种金属在氢后:
①金属与稀酸反应
②金属与金属盐溶液反应
2.验证三种金属活动性顺序的方法:
(1)两金夹一盐:金属活动性最强和最弱两种金属的单质与活动性居中金属的盐溶液。
(2)两盐夹一金:金属活动性最强和最弱两种金属的盐溶液与活动性居中的金属单质
【题型二】金属活动性顺序的探究
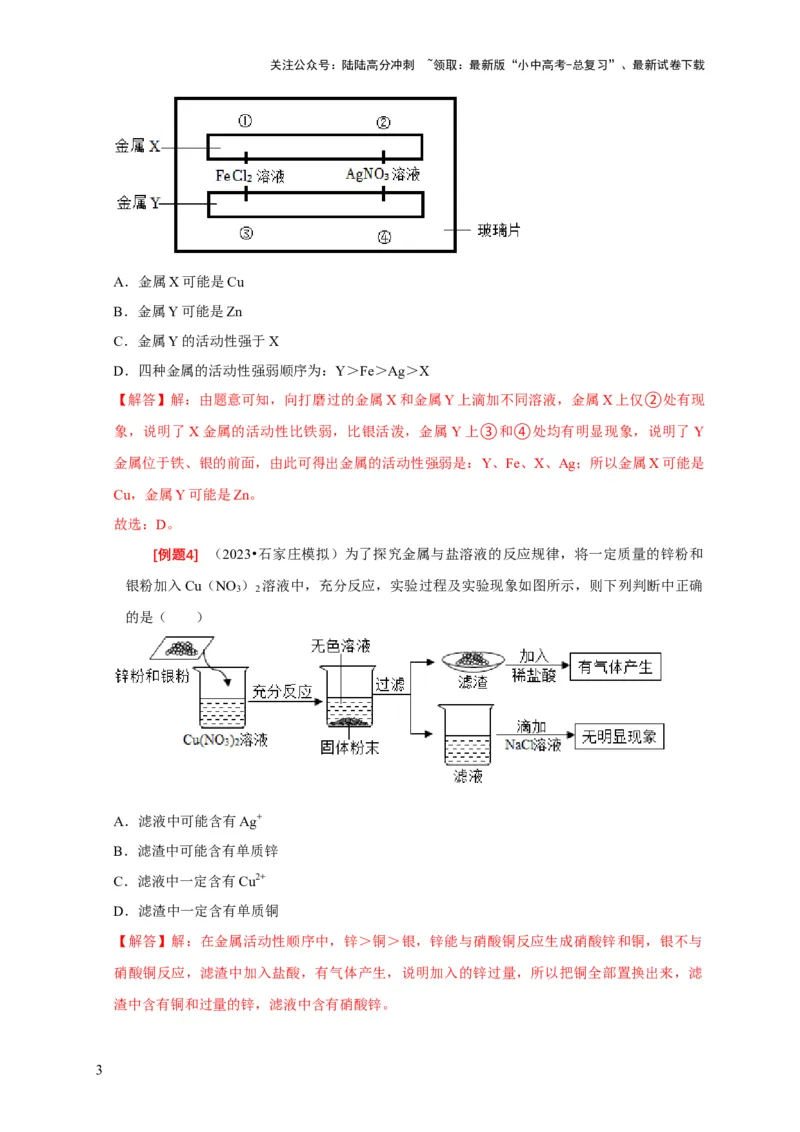
[例题3] (2023•衡阳二模)为了测定金属活动性强弱,某同学设计了如图所示的实验,
向打磨过的金属X和金属Y上滴加不同溶液,金属
X上仅②处有明显现象,金属Y上③和④处均有明显现象。关于该实验下列说法不正确的是
( )
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.金属X可能是Cu
B.金属Y可能是Zn
C.金属Y的活动性强于X
D.四种金属的活动性强弱顺序为:Y>Fe>Ag>X
【解答】解:由题意可知,向打磨过的金属X和金属Y上滴加不同溶液,金属X上仅②处有现
象,说明了X金属的活动性比铁弱,比银活泼,金属 Y上③和④处均有明显现象,说明了Y
金属位于铁、银的前面,由此可得出金属的活动性强弱是:Y、Fe、X、Ag;所以金属X可能是
Cu,金属Y可能是Zn。
故选:D。
[例题4] (2023•石家庄模拟)为了探究金属与盐溶液的反应规律,将一定质量的锌粉和
银粉加入Cu(NO ) 溶液中,充分反应,实验过程及实验现象如图所示,则下列判断中正确
3 2
的是( )
A.滤液中可能含有Ag+
B.滤渣中可能含有单质锌
C.滤液中一定含有Cu2+
D.滤渣中一定含有单质铜
【解答】解:在金属活动性顺序中,锌>铜>银,锌能与硝酸铜反应生成硝酸锌和铜,银不与
硝酸铜反应,滤渣中加入盐酸,有气体产生,说明加入的锌过量,所以把铜全部置换出来,滤
渣中含有铜和过量的锌,滤液中含有硝酸锌。
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A、银与硝酸铜不反应,滤液中不可能含有Ag+,故A错;
B、滤渣中加入盐酸,有气体产生,说明,滤渣中一定含有锌,故B错;
C、滤渣中加入盐酸,有气体产生,说明加入的锌过量,所以把铜全部置换出来,滤液中不含有
Cu2+,故C错;
D、滤渣中加入盐酸,有气体产生,说明加入的锌过量,所以把铜全部置换出来,滤渣中含有铜
和过量的锌,故D正确。
故选:D。
(以Fe、Cu、x为例)
1.首先将已知金属按活动性顺序排序:铁和铜的活动性顺序为Fe>Cu。
2.猜想陌生金属可能存在的位置:猜想一:X>Fe>Cu;猜想二:Fe>X>Cu;猜想三:Fe>Cu>X
3.实验验证:通过两金夹一盐或两盐夹一金等来验证。
4.特别提醒:
(1)实验前,需将金属打磨,除去表面的氧化膜和污物。
(2)金属与盐反应,盐必须可溶。
【题型三】金属活动性顺序的应用
[例题5] (2023•聊城三模)为验证铁、铜、银的金属活动性顺序,某同学设计了以下四
组实验。下列说法错误的是( )
A.通过实验①、②,能验证金属活动性:Fe>Cu
B.通过实验①、②、③,能验证金属活动性:Fe>Cu>Ag
C.若实验④中X为Ag,Y为H SO ,利用①、④能验证金属活动性:Fe>(H)>Ag
2 4
D.若实验④中X为Cu,Y为AgNO ,利用①、②、④能验证金属活动性:Fe>Cu>Ag
3
【解答】解:A、①中产生气泡,是因为铁和稀硫酸反应生成了氢气,说明铁排在氢前面,②
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
中铜与硫酸不反应,说明铜排在氢后面,能验证金属活动性:Fe>Cu,故正确,该选项不符合
题意;
B、①中产生气泡,是因为铁和稀硫酸反应生成了氢气,说明铁排在氢前面,②中铜与硫酸不
反应,说明铜排在氢后面,能验证金属活动性:Fe>Cu,③中铁表面析出银白色固体,是因为
铁和硝酸银反应生成了银,说明铁比银活泼,不能比较铜和银的活泼性,故错误,该选项符合
题意;
C、若X是银,Y是H SO ,是因为银不能和硫酸反应,而Fe可以与硫酸反应,说明铁比银活
2 4
泼,故正确,该选项不符合题意;
D、若X是铜,则Y是硝酸银,铜表面析出银白色固体,是因为铜和硝酸银反应生成了银,说
明铜比银活泼,故正确,该选项不符合题意;
故选:B。
[例题6] (2023•舒城县校级模拟)用金属与酸溶液反应比较金属活动性强弱,对比反应
放出热量比对比化学反应速率更具科学性。科学探究小组同学用三套相同装置进行实验并记录
数据。下列说法不正确的是( )
金属 起始温度/℃ 反应过程中的最高温度/℃
Zn 20.5 46.3
Mg 20.5 60.1
Fe 20.5 23.6
A.应保持金属的形状、质量和酸的体积、浓度等变量相同
B.试管中有气泡放出,溶液最终均为无色
C.长颈漏斗可缓冲瓶内压强,以防塞子松动
D.实验证明:Mg>Zn>Fe
【解答】解:A、该实验为对比实验,变量为金属的种类,则控制变量应保持金属的形状、质量
和酸的体积、浓度等变量相同,说法正确,故该选项不符合题意;
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
B、金属活动性顺序表中,Zn、Mg、Fe均位于氢之前,均能与酸反应生成氢气,因此试管中均
有气泡产生,但铁与酸反应生成的亚铁盐溶液呈浅绿色,则溶液最终不是均为无色,说法不正
确,故该选项符合题意;
C、金属与酸反应放热,装置内气体受热膨胀,气压增大,长颈漏斗可缓冲瓶内压强,以防塞子
松动,说法正确,故该选项不符合题意;
D、由表格数据可知,放出热量Mg>Zn>Fe,则金属活动性Mg>Zn>Fe,说法正确,故该选
项不符合题意;
故选:B。
1.在金属活动性顺序里,金属的位置越靠前,金属的活动性越强。
2.在金属活动性顺序里,位于氢前面的金属能与稀盐酸或稀硫酸发生置换反应;位于氢后面的金属不
能与稀盐酸或稀硫酸发生置换反应
3.在金属活动性顺序里,位于前面的金属(K、Ca、Na除外)能把位于后面的金属从它们的盐溶液里
置换出来。
1. (2023•临清市二模)A、B、C、D是四种金属单质,能发生如下反应:A+2HCl=盐
+H ↑;C+2HCl=盐+H ↑;B+D(NO ) =B(NO ) +D;B+HCl→不反应,且相同条件下
2 2 3 2 3 2
A比C反应剧烈。则四种金属的活动性由强到弱的顺序是( )
A.A>C>D>B B.B>A>C>D C.A>B>C>D D.A>C>B>D
【解答】解:A+2HCl=盐+H ↑、C+2HCl=盐+H ↑,且相同条件下 A 比 C 反应剧烈;
2 2
B+HCl→不反应,则B排在氢元素的后面,故A、C、H的活动性:A>C>H>B。
B+D(NO ) =B(NO ) +D,则B、D的活动性:B>D。
3 2 3 2
四种金属的活动性由强到弱的顺序是A>C>B>D。
故选:D。
2. (2023•安次区二模)为验证锌、铜、银的金属活动性顺序,某同学设计了如图实验
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(实验所用的金属丝已提前用砂纸打磨)。
实验①:将铜丝插入硝酸银溶液中,观察到铜丝表面有银白色固体附着,溶液变为蓝色。
实验②:取出铜丝,插入锌丝,观察到锌丝表面有红色固体附着后,取出锌丝。
以下分析不正确的是( )
A.插入锌丝前,试管中溶液可能有一种溶质
B.该实验能够验证金属活动性顺序:锌>铜>银
C.实验结束后,试管中溶液可能是无色的
D.实验结束后的溶液中最多有3种溶质
【解答】解:A、将铜丝插入硝酸银溶液中,铜和硝酸银反应生成硝酸铜和银,观察到铜丝表面
有银白色固体附着,溶液变为蓝色,若铜是过量的,且反应完全,试管中溶液只有硝酸铜一种
溶质,故选项说法正确。
B、实验①说明铜的金属活动性比银强,锌和硝酸铜反应生成硝酸锌和铜,说明锌的金属活动
性比铜强,该实验能够验证金属活动性顺序:锌>铜>银,故选项说法正确。
C、锌和硝酸铜溶液反应生成硝酸锌溶液和铜,若锌和过量的,且反应完全,实验结束后,试管
中溶液是硝酸锌溶液,试管中溶液可能是无色的,故选项说法正确。
D、实验①反应的溶液中一定含有硝酸铜,可能含有硝酸银,插入锌丝,锌先与硝酸银反应生
成硝酸锌和银,再与硝酸铜反应生成硝酸锌和铜,观察到锌丝表面有红色固体附着后,取出锌
丝,硝酸铜可能有剩余,实验结束后的溶液中最多有硝酸锌、硝酸铜2种溶质,故选项说法错误。
故选:D。
3. (2023•禹城市二模)向等质量的四种金属X、Y、Z、M分别加入等浓度等体积的足
量稀盐酸;再将Y投入MNO 溶液中充分反应。得到如图两个关系图,据此得出四种金属的
3
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
活动性强弱顺序正确的是( )
A.Z>X>M>Y B.X>Z>Y>M C.X>Z>M>Y D.Y>M>Z>X
【解答】解:由图象可知,等质量的X、Z能和稀盐酸反应,并且X和稀盐酸反应时间短,说明
X比Z活泼;Y、M不能和稀盐酸反应,说明Y、M不如X、Z活泼。Y能和MNO 反应,说明
3
Y比M活泼,因此四种金属的活动性顺序为:X>Z>Y>M。
故选:B。
4. (2023•东港区校级二模)为探究锌、铜、铁三种金属的活动性顺序,小青设计了如
图所示实验。待试管中的反应完全停止后,她将试管①、试管②内的物质全部倒入烧杯乙中,
充分反应后发现烧杯中的红色固体物质明显增多。下列说法正确的是( )
A.反应后烧杯中的固体一定含有铁
B.试管②中反应后固体一定含铜,可能含铁
C.反应后烧杯中的溶液一定含有氯化锌和氯化铁
D.烧杯中最后所得固体的质量一定大于2ag
【解答】解:A、三种金属的活动性顺序是锌、铁、铜,所以铁不会与氯化锌反应,铁会置换出
氯化铜中的铜,将试管①、试管②内的物质全部倒入同一烧杯中,充分反应后发现烧杯中的红
色固体物质明显增多,说明铁又会置换出氯化铜中的铜,所以:铁会置换出氯化铜中的铜,但
是氯化铜的量不能确定,所以反应后烧杯中的固体中是否含铁,不能确定,故错误;
B、两支试管中的物质加入烧杯中后,会继续生成铜,所以试管②中一定含有氯化铜,滤渣中
一定不含铁,故错误;
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C、通过上面的分析可知,铁会置换出氯化铜中的铜,生成氯化亚铁,而不是氯化铁,故错误;
D、通过题中的分析可知,加入铁的质量是2ag,每56份质量的铁会置换出64份质量的铜,所
以反应后固体的质量大于2ag,故正确。
故选:D。
5. (2023•鞍山三模)为验证铁、铜、银的金属活动性顺序,某同学设计了如图四组实
验。下列说法错误的是( )
A.实验④中X为Cu,Y为FeSO 溶液,能验证金属活动性:Fe>Cu
4
B.实验④中X为Cu,Y为AgNO 溶液,能验证金属活动性:Cu>Ag
3
C.通过实验①、②,能验证金属活动性:Fe>Cu
D.通过实验①、②、③,能验证金属活动性:Fe>Cu>Ag
【解答】解:A、若X是铜,则Y是硫酸亚铁,是因为铜不能和硫酸亚铁反应,说明铁比铜活
泼,故正确;
B、实验④中X为Cu,Y为AgNO 溶液,铜表面析出银白色固体,是因为铜和硝酸银反应生成
3
了银,说明铜比银活泼:Cu>Ag,故正确;
C、①中产生气泡,是因为铁和稀硫酸反应生成了氢气,说明铁排在氢前面,②中铜与硫酸不
反应,说明铜排在氢后面,能验证金属活动性:Fe>Cu,故正确;
D、①中产生气泡,是因为铁和稀硫酸反应生成了氢气,说明铁排在氢前面,②中铜与硫酸不
反应,说明铜排在氢后面,能验证金属活动性:Fe>Cu,③中铁表面析出银白色固体,是因为
铁和硝酸银反应生成了银,说明铁比银活泼,不能比较铜和银的活泼性,故错误。
故选:D。
6. (2023•姑苏区校级二模)通过下列实验,可以比较铁、铜、银三种金属的活动性强
弱的是( )
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A. B.
C. D.
【解答】解:A、由于铜、银都不能与稀硫酸反应,无法比较铜、银二种金属的活动性强弱,故
不符合题意;
B、由于铜、银、铁都不能与硫酸亚铁反应,无法比较铜、银二种金属的活动性强弱,故不符合
题意;
C、由于铜、银都不能与硫酸亚铁反应,无法比较铜、银二种金属的活动性强弱,故不符合题意;
D、由于铁能与硫酸铜反应,银不能与硫酸铜反应,可比较出铁、铜、银三种金属的活动性强弱
是铁>铜>银,故符合题意。
故选:D。
7. (2023•红桥区三模)某同学参加实验操作考试,为验证镁、锌、铜三种金属的活动
性顺序依次减弱,他设计了以下四种实验方案,其中能达到目的的是( )
A.将镁片、锌片分别放入Cu(NO ) 溶液中
3 2
B.将锌片、铜片分别放入Mg(NO ) 溶液中
3 2
C.将镁片、铜片分别放入Zn(NO ) 溶液中
3 2
D.将镁片分别放入Zn(NO ) 溶液、Cu(NO ) 溶液中
3 2 3 2
【解答】解:A、镁片、锌片都能与Cu(NO ) 溶液反应,证明镁、锌的活动性比铜强,但不
3 2
能比较镁、锌的活动性的强弱,故错误;
B、锌片、铜片都不能与Mg(NO ) 溶液反应,证明镁的活动性比铜、锌强,但不能比较铜、
3 2
锌的活动性的强弱,故错误;
C、将镁片、铜片分别放入Zn(NO ) 溶液中,镁能置换出锌,铜不与硝酸锌反应,可得:三
3 2
种金属活动性镁>锌>铜,故正确;
D、镁与Zn(NO ) 溶液、Cu(NO ) 溶液都反应,证明镁的活动性比铜、锌强,但不能比较
3 2 3 2
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
铜、锌的活动性的强弱,故错误。
故选:C。
8. (2023•海口二模)钯﹣镍合金在电子工业等方面有广泛应用。已知钯(Pd)、镍
(Ni)、铜三种金属的活动性顺序是Ni>Cu>Pd。下列实验组合中能验证出三种金属活动性
顺序的是( )
A.③④ B.②④ C.①④ D.①②
【解答】解:①镍与稀硫酸反应,生成硫酸镍、氢气,可观察到试管中有气泡产生,说明活动
性:Ni>H;
②钯与稀硫酸不发生反应,试管中无气泡产生,说明活动性:H>Pd;
③钯与硫酸铜不发生反应,说明活动性:Cu>Pd;
④铜与硫酸镍不发生反应,说明活动性:Ni>Cu。
综合③④,可得出三种金属的活动性顺序为:Ni>Cu>Pd,
B、C、D选项不能验证出三种金属活动性顺序,不符合题意;A选项符合题意。
故选:A。
9. (2023•莱西市二模)验证铝、铜、银的金属活动性强弱,小明设计了以下四组实验,
下列说法错误的是( )
A.通过实验①②,可以证明金属活动性Al>Cu
B.若要用实验④证明金属活动性Cu>Ag,X可以是Cu,Y为AgNO 溶液
3
C.该实验可以替换为将铜丝分别放入盛有Al(NO ) 溶液和AgNO 溶液的试管中,观察现象
3 3 3
D.通过实验①②③即可证明金属活动性Al>Cu>Ag
【解答】解:A、通过①②实验可知,①中产生气泡,②中无明显现象,说明铝能和稀硫酸
反应,铜不能和稀硫酸反应,可以证明金属活动性Al>Cu,该选项说法正确;
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
B、若要用实验④证明金属活动性Cu>Ag,X可以为Cu,Y为AgNO 溶液,X为Ag,Y为
3
CuSO 溶液,根据能否反应,可以比较铜、银的活动性强弱,该选项说法正确;
4
C、该实验可以替换为将铜丝分别伸入盛有Al (SO ) 溶液和AgNO 溶液的试管中,观察现象,
2 4 3 3
根据铜不能与将铝置换出来能将银置换出来,能比较三种金属的活动性,该选项说法正确;
D、通过①②③实验,可以证明铝最活泼,不能证明铜和银的活泼性强弱,该选项说法不正确。
故选:D。
10. (2023•宿迁一模)有X、Y、Z三种金属,把X、Z分别投入稀硫酸中,只有X表面
有气泡产生,把Z投入Y的盐溶液中,Z表面有Y析出。以下判断错误的是( )
A.若Z是Cu,则Y一定是Ag
B.金属活动性顺序一定是:X>Z>Y
C.Y投入X的盐溶液中,无X析出
D.加盐酸溶解后过滤,可以除去Y中的X
【解答】解:把X、Z分别投入稀硫酸中,只有X表面有气泡产生,说明活动性X>H>Z;把
Z投入Y的盐溶液中,Z表面有Y析出,说明活动性Z>Y,则三种金属的活动性X>Z>Y。
A、若Z是Cu,则Y可能是活动性比铜弱的Hg、Ag等,故选项说法错误。
B、由分析可知金属活动性顺序是X>Z>Y,故选项说法正确。
C、由于金属活动性顺序是X>Y,则Y投入X的化合物溶液中,无X析出,故选项说法正确。
D、由于活动性X>H>Y,X可以与盐酸反应,Y不可以与盐酸反应,除去Y中的杂质X,加
盐酸溶解后过滤,故选项说法正确。
故选:A。
11. (2023•东昌府区一模)某同学为探究Fe、Cu、Ag三种金属的活动性,设计了下列
四组实验:①将Fe、Cu、Ag三种金属分别插入到稀硫酸中②将Cu片分别插入到硫酸亚铁溶
液和硝酸银溶液中③将Ag片插入到硫酸铜溶液中,将铜片插入到硫酸亚铁溶液中④将Fe、
Ag分别插入到硫酸铜溶液中。其中可以达到目的的是( )
A.①③④ B.②③④ C.①②③ D.①②④
【解答】解:①将Fe、Cu、Ag三种金属分别插入到稀硫酸中,铁能和稀硫酸反应,铜和银不
能反应,说明铁最活泼,不能比较铜和银的活动性,该选项不正确。
②将Cu片分别插入到硫酸亚铁溶液和硝酸银溶液中,铜不能和硫酸亚铁反应,说明铁比铜活泼,
铜能和硝酸银反应,说明铜比银活泼,该选项正确。
③将Ag片插入到硫酸铜溶液中,不能反应,说明铜比银活泼,将铜片插入到硫酸亚铁溶液中,
不能反应,说明铁比铜活泼,该选项正确。
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
④将Fe、Ag分别插入到硫酸铜溶液中,铁能够反应,银不能反应,说明铁比铜活泼,铜比银
活泼,该选项正确。
故选:B。
12. (2023•青秀区校级模拟)人类文明进步与金属材料的发展关系十分密切,金属在生
活生产中有着非常广泛的应用请回答下列问题:
(1)制作智能手机充电线的主要原料是铜,这是利用了铜的导电性和 性。
(2)2022年12月9日,国产大飞机C919正式进入中国民航运输市场。飞机外壳采用铝锂合金
材料,铝锂合金与常规金属材料相比,优点有 。
(3)如图为锌与硫酸镍和硫酸锰混合溶液充分反应的后粒子变化微观示意图。
①Ni、Zn、Mn三种金属活动性由强到弱的顺序 。
②写出烧杯中发生的化学方程式 。
(4)从金、银、铁、铝混合金属中回收金、银。将混合金属放入一定量硝酸银溶液中充分反应
后过滤,得到滤渣和浅绿色溶液。则滤液中一定含有的金属离子是 。
【解答】解:(1)制作智能手机充电线的主要原料是铜,这是利用了铜的导电性和延展性。
(2)飞机外壳采用铝锂合金材料,铝锂合金与常规金属材料相比,优点有密度小、强度高、硬
度大等。
(3)①由微观示意图可知,该微观上该反应是锌原子和镍离子反应生成锌离子和镍原子,锌原
子不能与锰离子反应,说明锌的金属活动性比镍强,比锰弱,则三种金属活动性由强到弱的顺
序是Mn>Zn>Ni。
②烧杯中锌和硫酸镍反应生成硫酸锌和镍,发生的化学方程式为Zn+NiSO ═ZnSO +Ni。
4 4
(4)由金属活动性Al>Fe>Ag>Au,将混合金属放入一定量硝酸银溶液中充分反应后过滤,
金不与硝酸银溶液反应,铝先与硝酸银溶液反应生成硝酸铝溶液和银,铝反应完,若还有硝酸
银溶液,铁再与硝酸银溶液反应生成硝酸亚铁溶液和银。得到滤渣和浅绿色溶液,说明发生了
铁和硝酸银溶液的反应,无法确定硝酸银是否有剩余,则滤液中一定含有的金属离子是铝离子、
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
亚铁离子。
13. (2023•碑林区校级三模)金属及其制品是现代生活中不可缺少的材料和工具,请回
答下列问题。
(1)天问一号探测器应用了世界上目前最轻的金属结构材料——新型镁锂合金,该合金由镁和
锂 两 种 金 属 熔 合 而 成 。 合 金 与 其 组 成 的 金 属 相 比 , 具 有 的 特 点 是
(写一点)。
(2)某同学在探究金属与盐溶液反应的实验时,向铝粉和锌粉的混合物中加入一定质量的Mg
(NO ) 和AgNO 混合溶液,充分反应后,过滤,可得到滤渣和滤液。反应中涉及的化学方程
3 2 3
式是 (只写一个)。
(3)要验证Al、Zn、Ag的金属活动性顺序,用下列各组药品进行实验,不能达到实验目的的
是 (填字母)。
A.Al、Zn、Ag、稀盐酸
B.Al(NO ) 溶液、Zn、Ag
3 3
C.Al、ZnSO 溶液、Ag
4
D.Al(NO ) 溶液、Zn、AgNO 溶液
3 3 3
【解答】解:(1)多数合金熔点低于其组分中任一种金属的熔点,硬度一般比其组分中任一金
属的硬度大,抗腐蚀能力更强,故填:硬度大(或抗腐蚀能力更强,合理即可);
(2)金属活动性:Mg>Al>Zn>Ag,铝粉和锌粉的混合物中加入一定质量的Mg (NO ) 和
3 2
AgNO 混合溶液,铝、锌不与硝酸镁反应,铝先和硝酸银反应生成硝酸铝和银,如果硝酸银剩
3
余,硝酸银才会和锌反应生成硝酸锌和银,发生反应方程式是:Al+3AgNO =Al(NO ) +3Ag
3 3 3
或Zn+2AgNO =Zn(NO ) +2Ag;
3 3 2
(3)金属活动性:Al>Zn>H>Ag:
A、锌、铝均能与稀盐酸反应,均产生气泡,且铝产生气泡的速率快,说明在金属活动性顺序里:
Al>Zn>H,银和稀盐酸不反应,说明在金属活动性顺序里,H>Ag,可得出三种金属的活动性
顺序:Al>Zn>Ag,不符合题意;
B、Zn、Ag均与硝酸铝不反应,说明在金属活动性顺序里:Al>Zn,Al>Ag,但是无法探究锌、
银的金属活动性顺序,符合题意;
C、铝能与硫酸锌反应生成硫酸铝和锌,说明在金属活动性顺序里:Al>Zn,银和硫酸锌不反应,
说明在金属活动性顺序里:Zn>Ag,可以探究三种金属的活动性顺序:Al>Zn>Ag,不符合题
意;
D、锌能与硝酸银反应生成硝酸锌和银,说明在金属活动性顺序里:Zn>Ag,锌和硝酸铝不反
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
应,说明在金属活动性顺序里:Al>Zn,可以探究三种金属的活动性顺序:Al>Zn>Ag,不符
合题意。
故选:B。
14. (2023•兴庆区校级模拟)人类历史发展的不同阶段曾以不同金属材料的使用作为标
志。
(1)在生产生活实践中,人类逐渐掌握了多种金属的冶炼技术。
①比较两种铁矿石赤铁矿(主要成分Fe O )和菱铁矿(主要成分FeCO ),从化学的角度分析
2 3 3
“赤铁矿作炼铁原料更具优势”,其原因是 。
②近代工业上采用电解熔融氧化铝(Al O )的方法冶炼铝,Al O 分解后得到两种单质,该反
2 3 2 3
应的化学方程式为 。
△
(2)钛和钛合金是21世纪重要的金属材料。工业制钛的其中一个反应为:TiF +2H SO
4 2 4
¯
❑
4HF+2X+TiO ,X的化学式为 。
2
(3)某同学为验证锌、铜、银三种金属的活动性顺序,设计了以下四种方案,其中能达到目的
的是 。
A.将锌丝、银丝分别放入硫酸铜溶液中
B.将锌丝分别放入硫酸铜溶液、硝酸银溶液中
C.将铜丝分别放入硝酸锌溶液、硝酸银溶液中
D.将锌丝、铜丝分别放入稀硫酸中,将银丝放入硫酸铜溶液中
(4)某化学兴趣小组为研究金属的化学性质,向含有硝酸银和硝酸铜的废液加入一定质量的铁
粉,充分反应后过滤,得到滤渣和滤液。向滤渣中加入稀盐酸,观察到有气泡产生。则滤渣中
一定含有的金属是 ,滤液中一定含有的阳离子是 。
56×2
【解答】解:(1)①氧化铁中铁元素质量分数为 ×100%=70%;碳酸亚铁中铁
56×2+16×3
56
元素质量分数为 ×100%≈48.3%,氧化铁中铁元素质量分数大于碳酸亚铁中铁元
56+12+16×3
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
素质量分数,故赤铁矿作炼铁原料更具优势。
②由质量守恒定律知,反应前后元素种类不变,则电解 Al O 分解后得到的两种单质为铝和氧
2 3
通电
气,化学方程式为2Al O 4Al+3O ↑。
2 3 2
¯
❑
(2)根据质量守恒定律,反应前后原子的种类、数目不变,反应前Ti、F、H、S、O的原子个
数分别为1、4、4、2、8,反应后Ti、F、H、S、O的原子个数分别为1、4、4、0、2,2X中含
有2个硫原子和6个氧原子,X的化学式为SO 。
3
(3)A、锌和硫酸铜反应生成硫酸锌和铜,说明锌的金属活动性强于铜,银和硫酸铜不反应,
说明银的金属活动性比铜弱,可以得出锌、银、铜三种金属活动性由强到弱的顺序为:锌>铜
>银,故正确;
B、锌能和硫酸铜反应,锌能和硝酸银反应,说明锌的金属活动性强于铜和银,不能比较铜和银
的金属活动性强弱,故错误;
C、铜和硝酸锌不反应,和硝酸银反应,说明铜的金属活动性弱于锌,强于银,可以得出锌、银、
铜三种金属活动性由强到弱的顺序为:锌>铜>银,故正确;
D、锌和稀硫酸反应,铜和稀硫酸不反应,说明锌比氢活泼,氢比铜活泼,银和硫酸铜不反应,
说明银金属活动性弱于铜,可以得出锌、银、铜三种金属活动性由强到弱的顺序为:锌>铜>
银,故正确。
(4)铁的金属活动性比银、铜强,在硝酸银、硝酸铜的混合溶液中加入一定量铁粉,铁先与硝
酸银溶液反应生成硝酸亚铁溶液和银,硝酸银反应完,若还有铁粉,铁才能与硝酸铜溶液反应
生成硝酸亚铁溶液和铜,充分反应后过滤,得到滤渣和滤液。向滤渣中加入稀盐酸,有气泡产
生,说明滤渣中含有能与稀盐酸反应的金属,铜、银均不与稀盐酸反应,该金属应为铁,说明
铁是过量的。故滤渣中一定含有的金属是银、铜、铁,滤液中一定含有的阳离子是亚铁离子。
15. (2023•南关区一模)金属材料的使用见证了人类文明发展的过程,我们可以从多角
度了解。
(1)我国在三星堆遗址发掘出了黄金面具残片,将黄金敲打成面具是利用了金的 性。
(2)我国西汉时期的湿法炼铜工艺是利用铁和硫酸铜溶液反应制取铜,有关的化学反应方程式
为 。
(3)不同面值的硬币图案、重量不同。2019年发行的硬币(1角、5角、1元)是钢质材料,表
面 镀 镍 工 艺 。 若 要 选 择 制 造 硬 币 的 材 料 , 你 会 考 虑 的 因 素 之 一 是
。
16关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(4)依据金属活动性顺序,下列说法中正确的是 。
A.Al、Cu、Au都能和氧气反应,但难易程度不同
B.金属都能和稀盐酸发生置换反应生成氢气
C.比较Mg、Zn、Fe三种金属的活动性强弱,可以将Mg、Fe分别放入ZnSO 溶液中
4
D.当FeCl 溶液中混有少量CuCl 时,可以加入铁粉去除
2 2
【解答】解:(1)将黄金敲打成面具是利用了金的延展性。故答案为:延展;
(2)铁和硫酸铜生成铜和硫酸亚铁,化学方程式为 Fe+CuSO =Cu+FeSO 。故答案为:
4 4
Fe+CuSO ═FeSO +Cu;
4 4
(3)选择制造硬币的材料需考虑:材料性质稳定、不易被腐蚀、硬度大,耐磨损,不易变形;
对环境和人体健康无害;制备这些合金的资源较为丰富,原料易得,成本低等合理即可。故答
案为:性质稳定、不易被腐蚀(硬度大,耐磨损,不易变形;对环境和人体健康无害;制备这
些合金的资源较为丰富,原料易得,成本低等合理即可);
(4)A、铝常温下和氧气反应,铜和氧气加热条件下反应,金和氧气即使在高温下也不反应,
选项错误;
B、位于氢前面的金属能置换出酸中的氢气,选项错误;
C、镁和硫酸锌反应,说明镁比锌活泼;铁不和硫酸锌反应,说明锌比铁活泼;可得出三种金属
的活动性从强到弱为镁、锌、铁,选项正确;
D、铁和氯化铜生成氯化亚铁和铜,过滤,得到氯化亚铁溶液,选项正确。
故选:CD。
16. (2023•新城区校级二模)我国古代曾用“湿法炼铜”、“火法炼铜”。
(1)“湿法炼铜”的原理是“曾青得铁则化为铜”,其中“曾青”即硫酸铜溶液。反应过程中
的明显现象是 ,溶液由蓝色变为浅绿色。若固体质量会增大a克,则
溶液质量会减小 克。
高温
(2)“火法炼铜”用辉铜矿(主要成分 Cu S),反应原理是:①Cu S+2O 2CuO+X
2 2 2
¯
❑
高温
②Cu
2
S+2CuO 4Cu+X↑,其中生成物X的化学式为 。
¯
❑
(3)验证Ag、Fe、Cu三种金属活动性顺序,仅用下列提供的试剂不可行的是 (填序
号)。
17关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
①Fe、Ag、CuSO 溶液
4
②Cu、Ag、FeSO 溶液
4
③Cu、FeSO 溶液、AgNO 溶液
4 3
【解答】解:(1)“湿法炼铜”的原理是“曾青得铁则化为铜”,其中“曾青”即硫酸铜溶液。
反应时铁表面生成红色固体,溶液由蓝色变为浅绿色。若固体质量会增大a克,根据质量守恒定
律,则溶液质量会减小a克;
(2)根据质量守恒定律,化学反应前后,元素的种类和原子的个数不发生改变,由化学反应方
程式①知,反应物有2个铜原子,1个硫原子,4个氧原子,生成物有2个铜原子,2个氧原子,
则X中含有1个硫原子,2个氧原子,故X为二氧化硫,化学式为SO ;
2
(3)三种金属的活动性由强到弱依次为Fe、Cu、Ag。
①Fe、Ag、CuSO 溶液,铁与硫酸铜反应生成硫酸亚铁和铜,铁表面生成红色固体,则铁的金
4
属活动性比铜强;银不与硫酸铜发生反应,则银金属活动性比铜弱,故能验证 Ag、Fe、Cu三种
金属活动性顺序,不符合题意;
②Cu、Ag、FeSO 溶液,铜、银均不能和硫酸亚铁发生反应,不能验证 Ag、Fe、Cu三种金属
4
活动性顺序,符合题意;
③Cu、FeSO 溶液、AgNO 溶液,铜和硫酸亚铁不发生反应,则铜的金属活动性比铁弱;铜与
4 3
硝酸银生成硝酸铜和银,铜表面生成银白色固体,故能验证Ag、Fe、Cu三种金属活动性顺序,
不符合题意。
17. (2023•海州区校级一模)铜、铁、铝是重要的金属材料,在历史上被大规模开发利
用的先后顺序是铜、铁、铝。
(1)有同学认为影响金属大规模开发利用的先后顺序的因素有:①地壳中金属元素的含量②
金属的导电性③金属的活动性④金属冶炼的难易程度。其中正确的是 (填序号)。
(2)为验证铜、铁、铝的金属活动性顺序,某同学设计了图1的四组实验。其中没有必要做的
实验是 (填序号)。
18关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(3)西汉时期的《淮南万毕术》曾记载“曾青得铁则化为铜”,曾青指硫酸铜溶液,这是古代
的湿法炼铜,该反应的化学方程式为 。
(4)明代《天工开物》中记载“炒钢法”的生产工艺可用如图2表示。该过程中把铁矿石和煤
捣碎的目的是 。“炒钢”是将熔化的生铁倒入
方塘(敞口放置)中并不断翻炒,以降低生铁中的含碳量,请用化学方程式表示反应原理 。
【解答】解:(1)金属的活动性越强,冶炼的程度越难,利用的越晚,故填:③④;
(2)通过实验①、②,铁能和稀硫酸反应,铜不能和稀硫酸反应,能验证金属活动性:Fe>H
>Cu;通过实验③,铝能置换硫酸亚铁中的铁,则能验证金属活动性是 Al>Fe;实验④中铜
不能和硫酸亚铁反应,能验证金属活动性:Fe>Cu;则要验证铜、铁、铝的金属活动性顺序可
以是①、②、③组合,则④不需要做;或③④组合,则没有必要①②;故填:①②或④;
(3)铁能与硫酸铜反应生成铜和硫酸亚铁,反应的化学方程式为Fe+CuSO =FeSO +Cu;
4 4
(4)把铁矿石和煤捣碎,能增加反应物的接触面积,使反应充分进行;将生铁不断翻炒,其中
点燃
的碳在空气中燃烧生成二氧化碳,则含碳量降低,反应的化学方程式为 。
C+O ¯ CO
2 ❑ 2
18. (2023•南明区校级三模)金属及其化合物是中学化学学习的重要内容。
(1)《梦溪笔谈》中记载:“古人以剂钢为刃,柔铁为茎干,不尔则多断折。……”,剂钢、
柔铁均为铁的合金,说明合金比纯金属 (填字母)。
a.硬度大、耐腐蚀
b.硬度小、熔点高
c.熔点高、耐腐蚀
19关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)某兴趣小组为探究Zn、Fe、Cu、Ag四种金属的活动性,进行如图甲、乙、丙三个实验。
①请写出丙实验中的现象 ,甲中发生反应
的化学方程式为 。
②小组同学随后发现该实验无法得出四种金属的活动性顺序,于是补充图丁实验,最终得出四
种金属活动性顺序。若图丁中的溶液B为稀盐酸,则A是 。
(3)某校化学实验室废液桶中收集了溶有大量 FeSO 、CuSO 的废液,他们想从中回收金属铜
4 4
和硫酸亚铁晶体,设计了如图实验方案。结合实验方案回答下列问题:
①金属X为 ,加入适量溶液Y的目的是 。
②理论上所得硫酸亚铁晶体的质量 (填“>”、“<”或“=”)原废液中硫酸亚铁的
质量。
【解答】解:(1)《梦溪笔谈》中所记剂刚、柔铁均为铁的合金。这主要因为合金比纯金属硬
度大、耐腐蚀。故选a。
(2)①丙实验中铜与硝酸银反应生成硝酸铜和银,故实验现象为铜片上有银白色固体析出,溶
液由无色变蓝色;甲实验中,锌能置换稀盐酸中的氢,故化学方程式为 Zn+2HCl=
ZnCl +H ↑。
2 2
②甲实验中锌能置换稀盐酸中的氢,说明锌的活动性大于氢,乙实验中铁与盐酸反应,说明铁
排在氢的前面,甲中气泡比乙中气泡快,说明锌比铁活泼,丙实验中铜与硝酸银反应,说明铜
的活动性大于银,甲乙丙三实验,无法比较铁与铜的活动性强弱,若图丁中的固体A为铜,溶
液B是稀盐酸,铜与盐酸不反应,说明铜的活动性小于氢,则可证明铁比铜活泼,由此可得出
四种金属活动性:锌>铁>铜>银。
(3)①该实验的目的是从溶有大量硫酸亚铁、硫酸铜的废液中回收金属铜和硫酸亚铁晶体,故
20关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
金属X应为铁粉,铁可以置换出硫酸铜中的铜,同时生成硫酸亚铁,因为加入的铁粉是过量的,
所以析出的铜中混有铁粉,故加入溶液Y为稀硫酸,把铁变成硫酸亚铁,从而过滤出铜,所以
加入适量稀硫酸的目的是除去混在铜粉里的铁粉。②理论上所得硫酸亚铁晶体的质量一定大于
原溶液中硫酸亚铁的质量,因为原溶液中的硫酸铜加入铁后会生成硫酸亚铁,过量的金属铁和
硫酸反应也会生成硫酸亚铁,从而增加了硫酸亚铁晶体的质量。
21