文档内容
2018 年陕西省中考化学副题
可能用到的相对原子质量:H-1 O-16 Na-23 Mg-24 Al-27 Cl-35.5
一、选择题(共7小题,每小题2分,计14分。每小题只有一个选项是符合题意的)
1. 我国2018年世界环境日的主题是“美丽中国,行动有我”。下列做法不符合这一主题的是
A. 发展公共交通,提倡绿色出行 B. 积极植树造林,美化生态环境
C. 推行垃圾分类,回收利用资源 D. 就地焚烧秸杆,增加土壤肥效
【答案】D
【解析】
【详解】A、发展公共交通,提倡绿色出行,做法符合这一主题;故选项正确;
B、积极植树造林,美化生态环境,做法符合这一主题;故选项正确;
C、推行垃圾分类,回收利用资源,做法符合这一主题;故选项正确;
D、就地焚烧秸杆生成有害气体和烟尘,做法不符合这一主题;故选项错误;
故选:D。
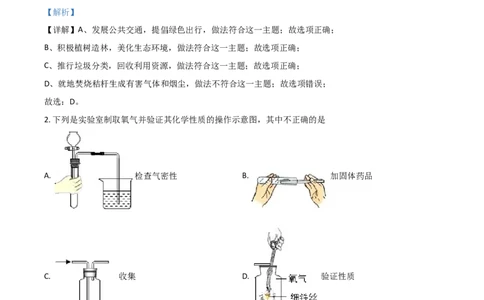
2. 下列是实验室制取氧气并验证其化学性质的操作示意图,其中不正确的是
A. 检查气密性 B. 加固体药品
C. 收集 D. 验证性质
【答案】D
【解析】
【详解】A、检查装置气密性的方法:把导管的一端浸没在水里,双手紧握试管,若导管口有气泡冒出,
移开手一段时间后导管内形成一段水柱,装置不漏气,此选项正确;
B、取用粉末状或小颗粒状药品,先使试管倾斜或横放,用镊子或纸槽,把盛有药品的药匙或纸槽小心地送至试管底部,然后使试管直立起来,此选项正确;
C、氧气的密度比空气的密度大,用万用瓶收集密度比空气大的气体,气体从长导气管进入,此选项正确;
D、做铁丝在氧气中燃烧实验,集气瓶底部放少量的水,以防瓶底炸裂,此选项错误。
故选D。
3. 对下列做法的解释正确的是
A. 用煮沸的方法降低水的硬度——水中的钙、镁离子转化成了沉淀
B. 用风力灭火机灭火——降低了可燃物的着火点
C. 用生石灰作食品干燥剂——生石灰吸收了包装袋中的二氧化碳
D. 用汽油洗涤衣服上的油污——汽油能乳化油污
【答案】A
【解析】
【详解】A.硬水在加热煮沸的过程中,水中的钙、镁离子转化成了沉淀,从而降低了水的硬度,选项说
法正确;
B.用风力灭火机灭火是因为空气流通导致温度降低,低于可燃物的着火点而灭火,选项说法错误;
C.生石灰能吸收包装袋内的水蒸气,所以生石灰可用作食品干燥剂,选项说法错误;
D.油污能溶解于汽油中,所以可用汽油洗涤衣服上的油污,选项说法错误。
故选:A。
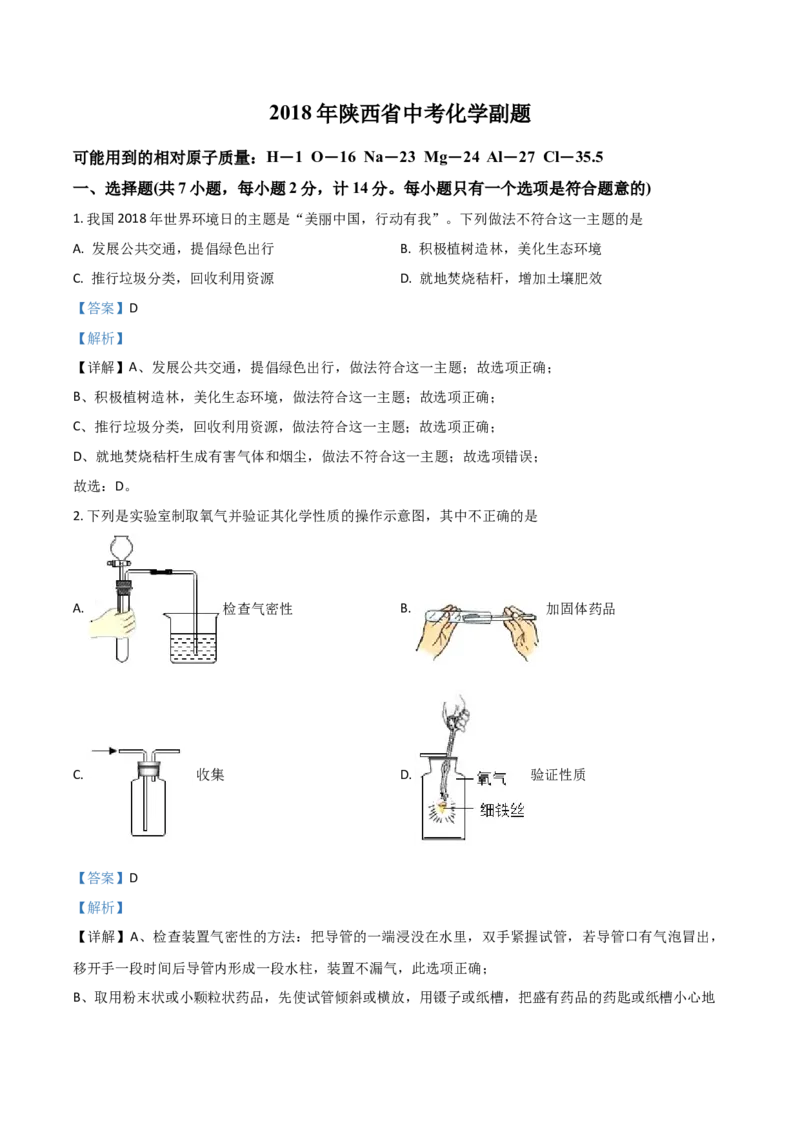
4. 对下列图示信息的分析正确的是
A. 图①②对应元素形成的化合物只有一种 B. 图③④对应元素的离子核外电子排布相同
C. 图①③对应元素的化学性质相似 D. 图①②③对应的三种元素形成的化合物水溶液
pH>7
【答案】D
【解析】
【详解】A.图①的质子数为1,是氢元素,②的质子数为8,是氧元素,氢元素与氧元素可以组成水、过
氧化氢两种化合物,选项说法错误;
B.图③是钠原子结构示意图,在化学反应中易失去最外层的1个电子而形成核外有两个电子层,第一层2
个电子、第二层8个电子的结构;④是硫元素,硫原子的核外有三个电子层,最外层有6个电子,在化学反应中易得到2个电子而形成第一层2个电子,第二次8个电子,第三层8个电子的结构,选项说法错误;
C.①③对应元素分别是氢元素和钠元素,氢元素是非金属元素,钠元素属于金属元素,虽然它们原子的
最外层电子数均为1,但化学性质不相似,选项说法错误;
D.①②③分别是氢元素、氧元素、钠元素,三种元素形成的化合物是氢氧化钠,水溶液显碱性,pH>7,
选项说法正确。
故选:D。
5. 纸质电池被称为“软电池”,总反应为 。该电池采用薄层纸片
作传导体,避免了传统电池带来的污染,使用后可作为一般废弃物处理。下列说法正确的是
A. MnO 是该电池反应的催化剂 B. 电池反应中锌元素化合价升高
2
C. 电池工作时将电能转化为化学能 D. 该反应属于复分解反应
【答案】B
【解析】
【详解】A、催化剂是能加快或抑制化学反应速率,本身的质量和化学性质在反应前后不变的物质,由反
应为 可知,反应物中含有MnO ,生成物中不含,则MnO 不是该
2 2
电池反应的催化剂,故A不正确;
B、反应物中,锌为单质,化合价为零,生成物锌元素在氧化锌中,氧元素的化合价为-价,设锌元素的化
合价为x,化合物中各元素的正负化合价代数和为零,则 , ,则氧化锌中锌元素的化合
价为+2价,则电池反应中锌元素化合价升高,故B正确;
为
C、电池工作时将化学能转化 电能,故C不正确;
D、反应为 ,反应物为三种,不符合两种化合物相互交换成分,不
属于复分解反应,故D不正确。故选B。
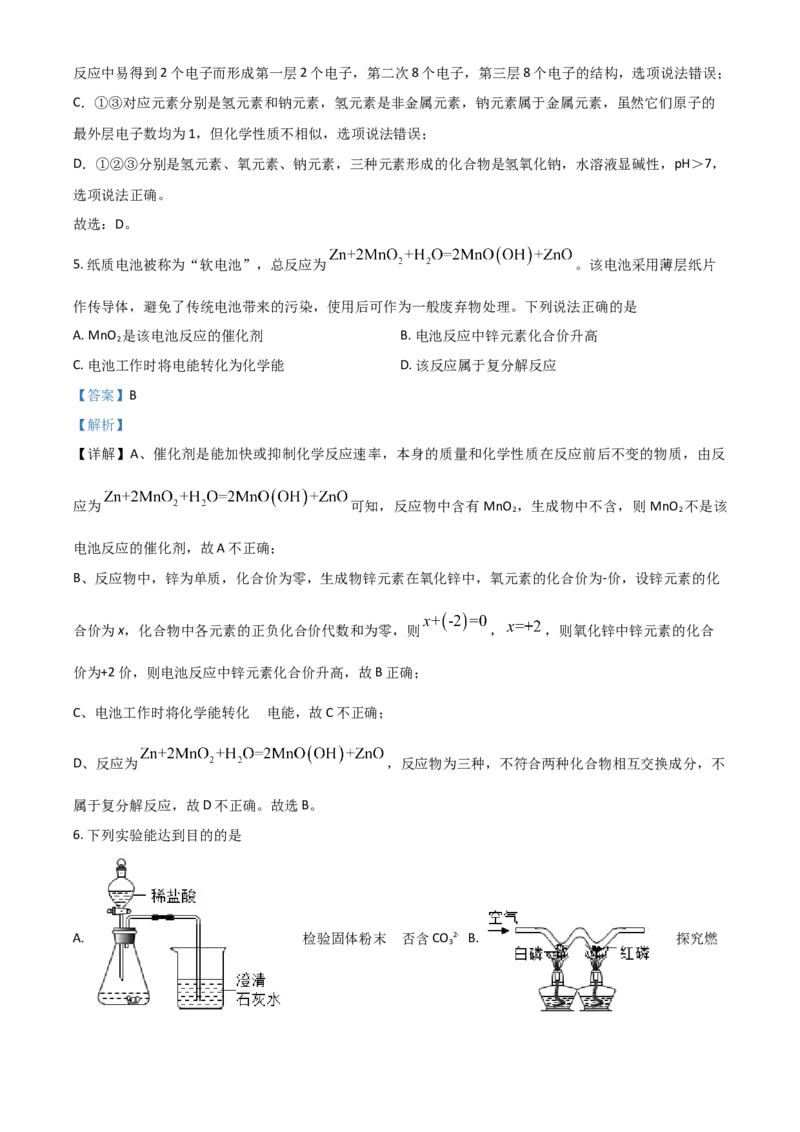
6. 下列实验能达到目的的是
A. 检验固体粉末 否含CO 2- B. 探究燃
3
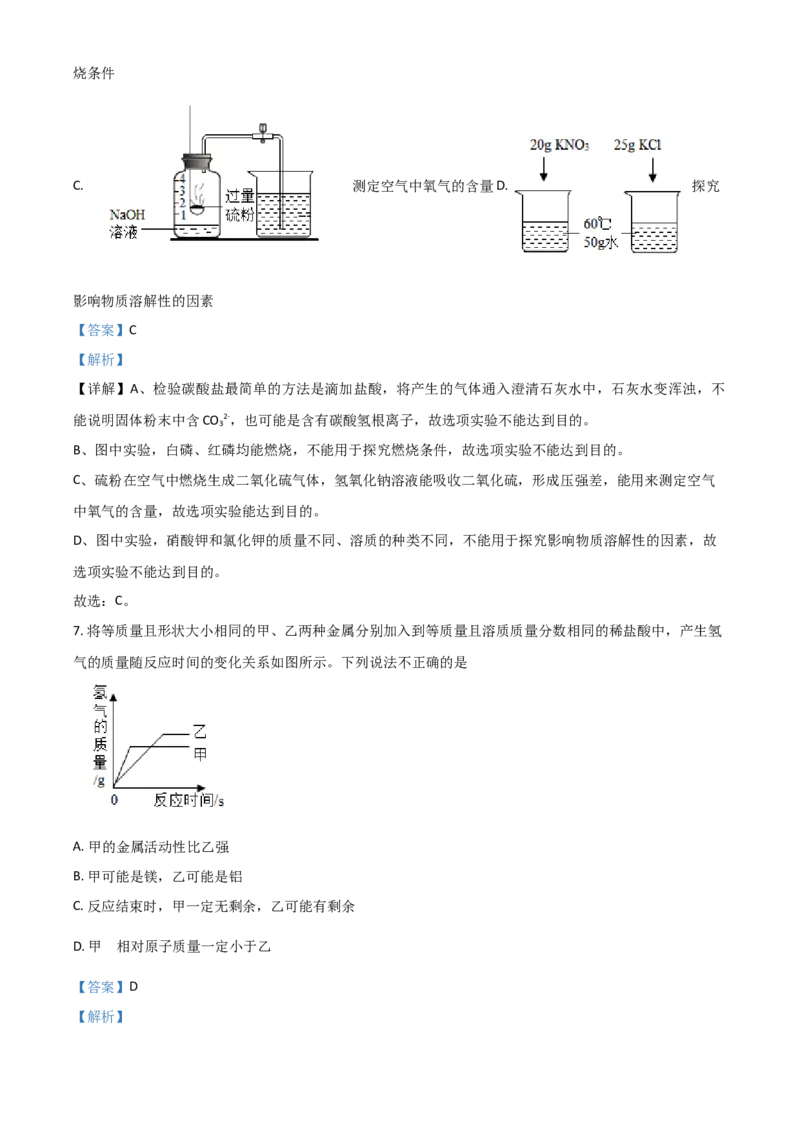
是烧条件
C. 测定空气中氧气的含量D. 探究
影响物质溶解性的因素
【答案】C
【解析】
【详解】A、检验碳酸盐最简单的方法是滴加盐酸,将产生的气体通入澄清石灰水中,石灰水变浑浊,不
能说明固体粉末中含CO 2-,也可能是含有碳酸氢根离子,故选项实验不能达到目的。
3
B、图中实验,白磷、红磷均能燃烧,不能用于探究燃烧条件,故选项实验不能达到目的。
C、硫粉在空气中燃烧生成二氧化硫气体,氢氧化钠溶液能吸收二氧化硫,形成压强差,能用来测定空气
中氧气的含量,故选项实验能达到目的。
D、图中实验,硝酸钾和氯化钾的质量不同、溶质的种类不同,不能用于探究影响物质溶解性的因素,故
选项实验不能达到目的。
故选:C。
7. 将等质量且形状大小相同的甲、乙两种金属分别加入到等质量且溶质质量分数相同的稀盐酸中,产生氢
气的质量随反应时间的变化关系如图所示。下列说法不正确的是
A. 甲的金属活动性比乙强
B. 甲可能是镁,乙可能是铝
C. 反应结束时,甲一定无剩余,乙可能有剩余
的
D. 甲 相对原子质量一定小于乙
【答案】D
【解析】【详解】A、从图象中不难看出,金属甲完全反应需要的时间短,说明金属甲的反应速率快,即金属甲的
金属活动性强,金属甲比乙活泼,选项正确,不符合题意;
B、根据反应方程式, ,54:6=18:2,即等质
量的金属,镁产生的气体比铝少,且镁比铝活泼,镁产生的气体速率比铝快,故甲、乙两种金属可能分别
为镁、铝,选项正确,不符合题意;
C、乙产生的氢气更多,所以消耗的盐酸更多,而两实验盐酸的量相同,故与甲反应的盐酸一定剩余,甲
已经完全反应,选项正确,不符合题意;
D、金属与酸反应产生的量与金属相对原子质量和金属的化合价有关,由于金属的化合价不确定,不能比
较金属的相对原子质量,,选项错误,符合题意。故选D。
【点睛】对于活泼金属,活动性越强的金属与酸反应越剧烈,即反应放出氢气的速度越快;化合价相同的
等质量金属完全反应放出氢气的质量与金属的相对原子质量成反比。
二、填空及简答题(共5小题,计19分)
8. 中国的许多用具独具一格,既表现了中华民族不同于其他民族的风俗,又为世界文化的进步和发展作出
了贡献,其中典型的有被誉为“文房四宝”的笔、墨、纸、砚。
(1)制作毛笔“笔毫”的原料之一是白羊毛,生活中可用________法将其与合成纤维区分开。
(2)古代文人用墨作的字画可以保存至今而不褪色的原因是________。
(3)砚台是“文房四宝”之首,以石砚居多。制作石砚的过程发生了___(填“物理”或“化学”)变化。
【答案】 ①. 灼烧闻气味 ②. 碳单质在常温下化学性质稳定 ③. 物理
【解析】
【详解】(1) 合成纤维近火时先收缩,后燃烧,冒黑烟,有臭味,余烬呈黑色圆球;羊毛燃烧时发泡,有火
焰,有烧焦羽毛的气味,余烬呈黑褐色,则制作毛笔“笔毫”的原料之一是白羊毛,生活中可用灼烧法将
其与合成纤维区分开。
(2)墨的主要成分是碳,常温下化学性质稳定,则古代文人用墨作的字画可以保存至今而不褪色的原因是碳
单质在常温下化学性质稳定。
(3) 制作石砚过程中只是材料的形状发生了变化,没有新物质生成,属于物理变化,则制作石砚的过程发生
了物理变化。
的
9. 化学是研究物质 组成、结构、性质及变化规律的科学。
(1)下列符号能表示2个原子的是______(填序号)。
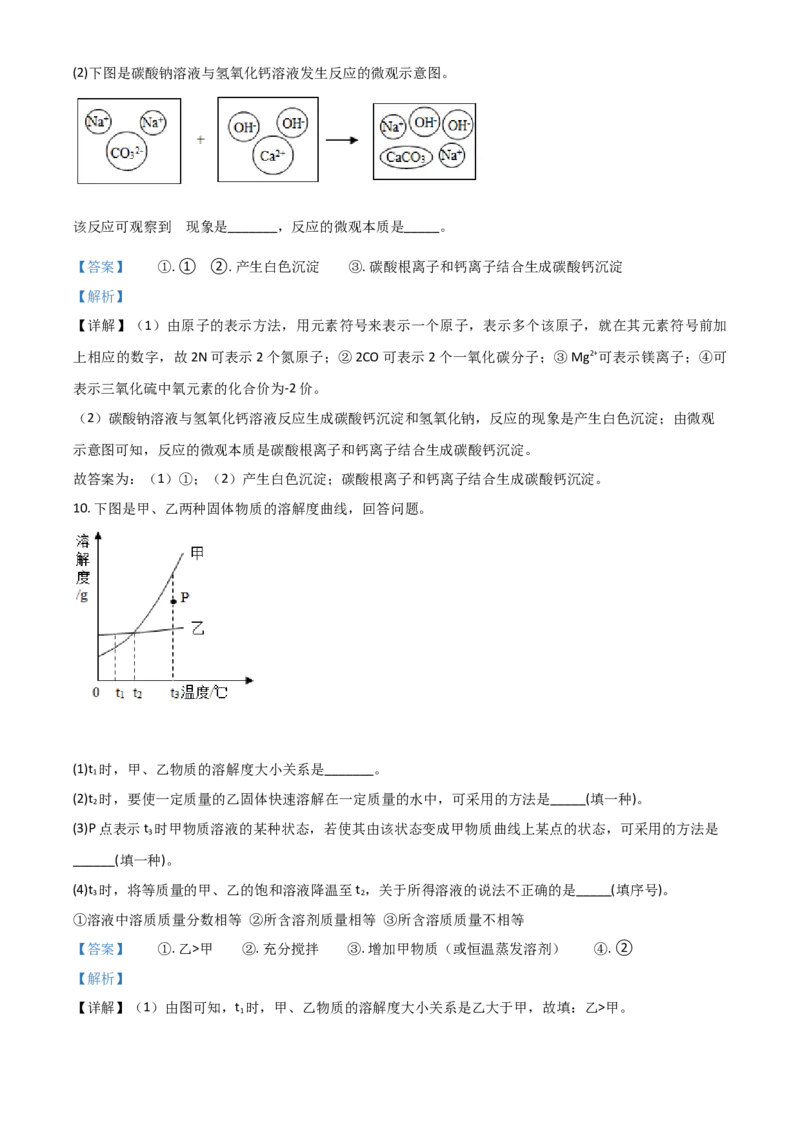
①2N ②2CO ③Mg2+④(2)下图是碳酸钠溶液与氢氧化钙溶液发生反应的微观示意图。
的
该反应可观察到 现象是_______,反应的微观本质是_____。
【答案】 ①. ① ②. 产生白色沉淀 ③. 碳酸根离子和钙离子结合生成碳酸钙沉淀
【解析】
【详解】(1)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加
上相应的数字,故2N可表示2个氮原子;②2CO可表示2个一氧化碳分子;③Mg2+可表示镁离子;④可
表示三氧化硫中氧元素的化合价为-2价。
(2)碳酸钠溶液与氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,反应的现象是产生白色沉淀;由微观
示意图可知,反应的微观本质是碳酸根离子和钙离子结合生成碳酸钙沉淀。
故答案为:(1)①;(2)产生白色沉淀;碳酸根离子和钙离子结合生成碳酸钙沉淀。
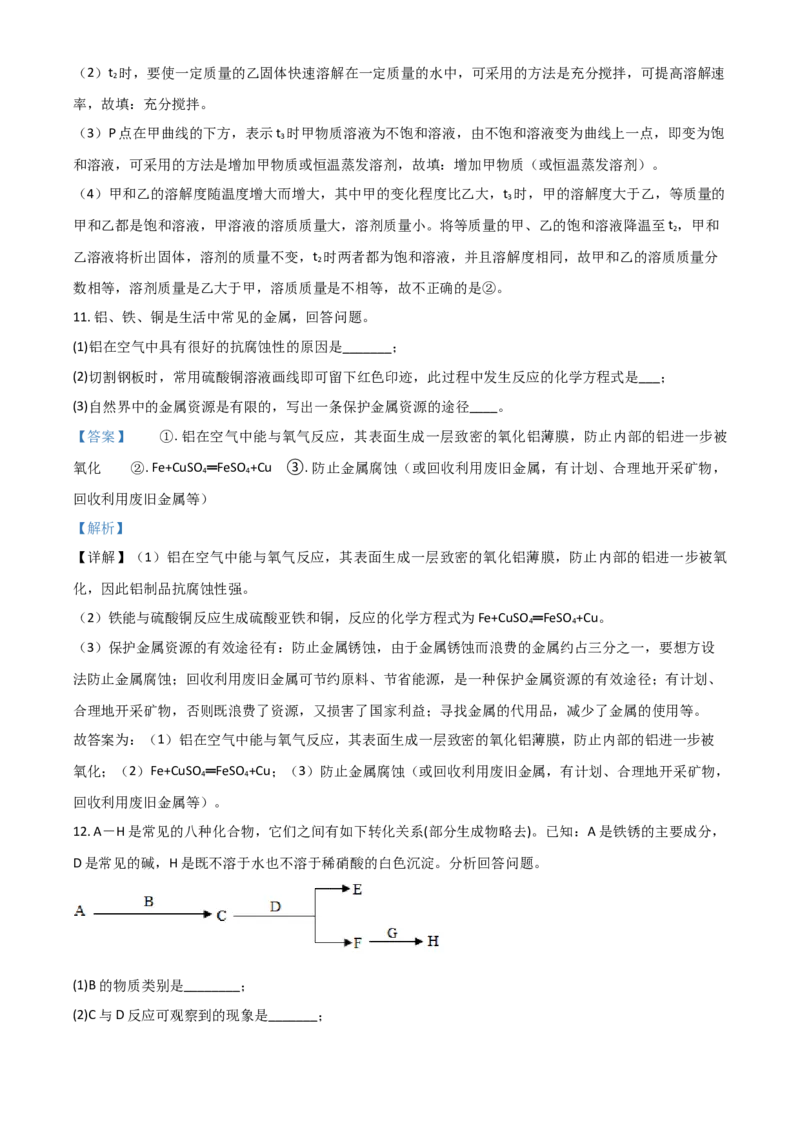
10. 下图是甲、乙两种固体物质的溶解度曲线,回答问题。
(1)t 时,甲、乙物质的溶解度大小关系是_______。
1
(2)t 时,要使一定质量的乙固体快速溶解在一定质量的水中,可采用的方法是_____(填一种)。
2
(3)P点表示t 时甲物质溶液的某种状态,若使其由该状态变成甲物质曲线上某点的状态,可采用的方法是
3
______(填一种)。
(4)t 时,将等质量的甲、乙的饱和溶液降温至t ,关于所得溶液的说法不正确的是_____(填序号)。
3 2
①溶液中溶质质量分数相等 ②所含溶剂质量相等 ③所含溶质质量不相等
【答案】 ①. 乙>甲 ②. 充分搅拌 ③. 增加甲物质(或恒温蒸发溶剂) ④. ②
【解析】
【详解】(1)由图可知,t 时,甲、乙物质的溶解度大小关系是乙大于甲,故填:乙>甲。
1(2)t 时,要使一定质量的乙固体快速溶解在一定质量的水中,可采用的方法是充分搅拌,可提高溶解速
2
率,故填:充分搅拌。
(3)P点在甲曲线的下方,表示t 时甲物质溶液为不饱和溶液,由不饱和溶液变为曲线上一点,即变为饱
3
和溶液,可采用的方法是增加甲物质或恒温蒸发溶剂,故填:增加甲物质(或恒温蒸发溶剂)。
(4)甲和乙的溶解度随温度增大而增大,其中甲的变化程度比乙大,t 时,甲的溶解度大于乙,等质量的
3
甲和乙都是饱和溶液,甲溶液的溶质质量大,溶剂质量小。将等质量的甲、乙的饱和溶液降温至t ,甲和
2
乙溶液将析出固体,溶剂的质量不变,t 时两者都为饱和溶液,并且溶解度相同,故甲和乙的溶质质量分
2
数相等,溶剂质量是乙大于甲,溶质质量是不相等,故不正确的是②。
11. 铝、铁、铜是生活中常见的金属,回答问题。
(1)铝在空气中具有很好的抗腐蚀性的原因是_______;
(2)切割钢板时,常用硫酸铜溶液画线即可留下红色印迹,此过程中发生反应的化学方程式是___;
(3)自然界中的金属资源是有限的,写出一条保护金属资源的途径____。
【答案】 ①. 铝在空气中能与氧气反应,其表面生成一层致密的氧化铝薄膜,防止内部的铝进一步被
氧化 ②. Fe+CuSO ═FeSO +Cu ③. 防止金属腐蚀(或回收利用废旧金属,有计划、合理地开采矿物,
4 4
回收利用废旧金属等)
【解析】
【详解】(1)铝在空气中能与氧气反应,其表面生成一层致密的氧化铝薄膜,防止内部的铝进一步被氧
化,因此铝制品抗腐蚀性强。
(2)铁能与硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为Fe+CuSO ═FeSO +Cu。
4 4
(3)保护金属资源的有效途径有:防止金属锈蚀,由于金属锈蚀而浪费的金属约占三分之一,要想方设
法防止金属腐蚀;回收利用废旧金属可节约原料、节省能源,是一种保护金属资源的有效途径;有计划、
合理地开采矿物,否则既浪费了资源,又损害了国家利益;寻找金属的代用品,减少了金属的使用等。
故答案为:(1)铝在空气中能与氧气反应,其表面生成一层致密的氧化铝薄膜,防止内部的铝进一步被
氧化;(2)Fe+CuSO ═FeSO +Cu;(3)防止金属腐蚀(或回收利用废旧金属,有计划、合理地开采矿物,
4 4
回收利用废旧金属等)。
12. A-H是常见的八种化合物,它们之间有如下转化关系(部分生成物略去)。已知:A是铁锈的主要成分,
D是常见的碱,H是既不溶于水也不溶于稀硝酸的白色沉淀。分析回答问题。
(1)B的物质类别是________;
(2)C与D反应可观察到的现象是_______;(3)分离E和F的操作名称是__________;
(4)写出F与G发生反应的化学方程式________。
【答案】 ①. 酸 ②. 有红褐色沉淀生成 ③. 过滤 ④. NaCl+AgNO =NaNO +AgCl↓或
3 3
Na SO +Ba(NO ) =2NaNO +BaSO ↓。
2 4 3 2 3 4
【解析】
【详解】(1)A-H是常见的八种化合物,A是铁锈的主要成分,所以A是氧化铁,D是常见的碱,H是既
不溶于水也不溶于稀硝酸的白色沉淀,所以H是氯化银或硫酸钡,氧化铁转化成的C会与碱D反应,所以
B可以是盐酸或硫酸,C是氯化铁或硫酸铁,氯化铁和氢氧化钠反应生成氢氧化铁沉淀和氯化钠,所以E是
氢氧化铁沉淀,F是氯化钠或硫酸钠,D可以是氢氧化钠,氯化钠和硝酸银反应生成氯化银沉淀和硝酸钠,
硫酸钠和硝酸钡反应生成硫酸钡沉淀和硝酸钠,所以G是硝酸银或硝酸钡,经过验证,推导正确,所以B
的物质类别是酸;
(2)C与D的反应是铁盐和碱反应生成氢氧化铁沉淀和盐,可观察到的现象是:有红褐色沉淀生成;
(3)分离E和F即分离固体和液体,操作名称是过滤;
(4)F与G发生的反应是氯化钠和硝酸银反应生成氯化银沉淀和硝酸钠,或硫酸钠和硝酸钡反应生成硝酸
钠和硫酸钡沉淀,化学方程式为:NaCl+AgNO =NaNO +AgCl↓或Na SO +Ba(NO ) =2NaNO +BaSO ↓。
3 3 2 4 3 2 3 4
故答案为:(1)酸;(2)有红褐色沉淀生成;(3)过滤;(4)NaCl+AgNO =NaNO +AgCl↓或
3 3
Na SO +Ba(NO ) =2NaNO +BaSO ↓。
2 4 3 2 3 4
三、实验及探究题(共2小题,计12分)
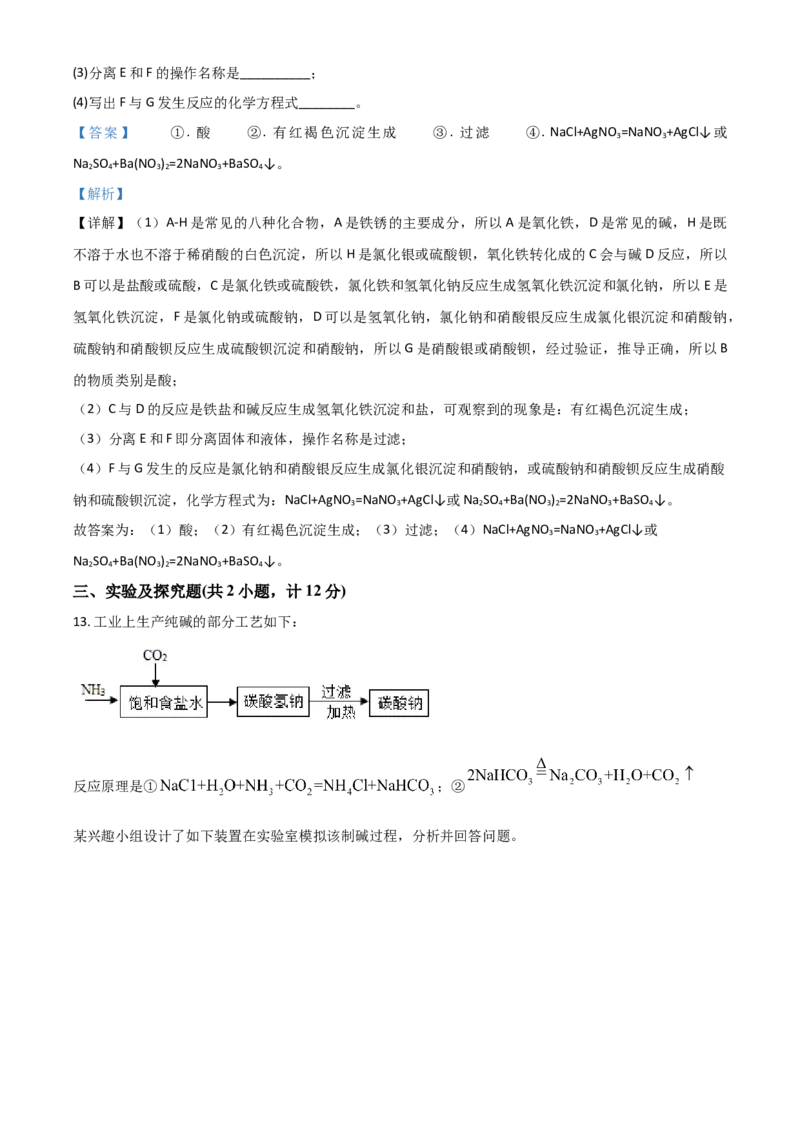
13. 工业上生产纯碱的部分工艺如下:
反应原理是① ;②
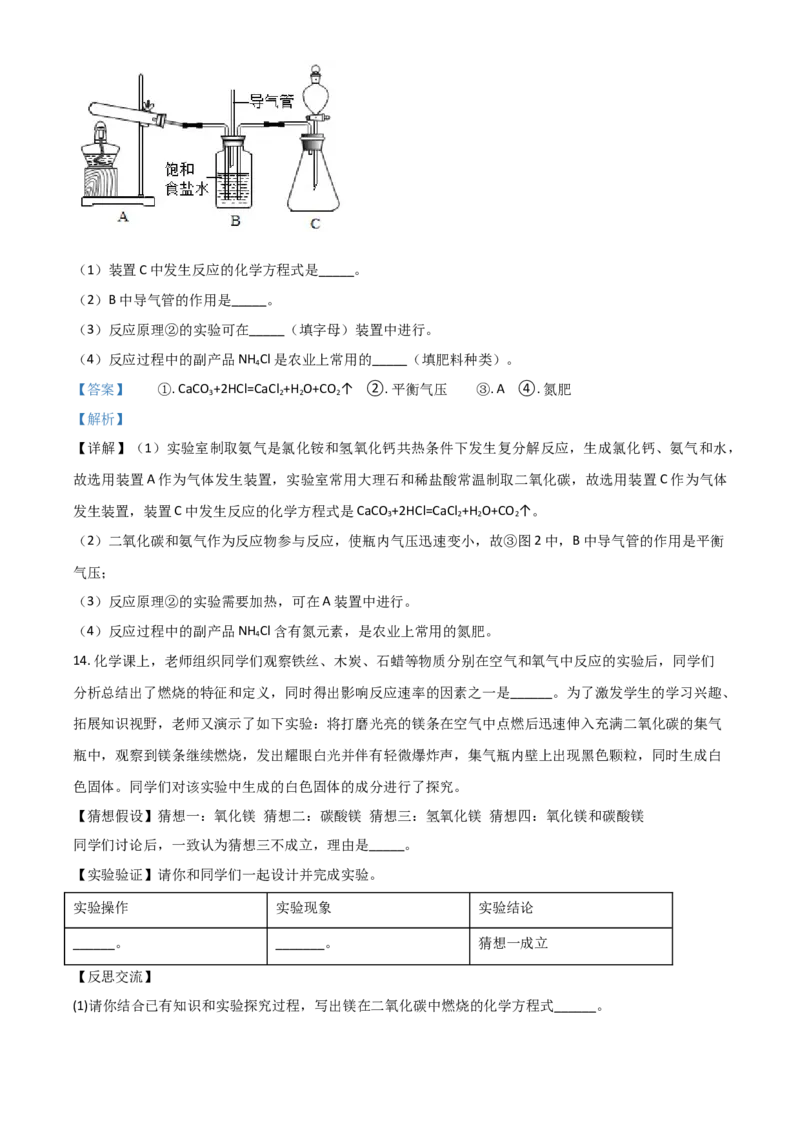
某兴趣小组设计了如下装置在实验室模拟该制碱过程,分析并回答问题。(1)装置C中发生反应的化学方程式是_____。
(2)B中导气管的作用是_____。
(3)反应原理②的实验可在_____(填字母)装置中进行。
(4)反应过程中的副产品NH Cl是农业上常用的_____(填肥料种类)。
4
【答案】 ①. CaCO +2HCl=CaCl +H O+CO ↑ ②. 平衡气压 ③. A ④. 氮肥
3 2 2 2
【解析】
【详解】(1)实验室制取氨气是氯化铵和氢氧化钙共热条件下发生复分解反应,生成氯化钙、氨气和水,
故选用装置A作为气体发生装置,实验室常用大理石和稀盐酸常温制取二氧化碳,故选用装置C作为气体
发生装置,装置C中发生反应的化学方程式是CaCO +2HCl=CaCl +H O+CO ↑。
3 2 2 2
(2)二氧化碳和氨气作为反应物参与反应,使瓶内气压迅速变小,故③图2中,B中导气管的作用是平衡
气压;
(3)反应原理②的实验需要加热,可在A装置中进行。
(4)反应过程中的副产品NH Cl含有氮元素,是农业上常用的氮肥。
4
14. 化学课上,老师组织同学们观察铁丝、木炭、石蜡等物质分别在空气和氧气中反应的实验后,同学们
分析总结出了燃烧的特征和定义,同时得出影响反应速率的因素之一是______。为了激发学生的学习兴趣、
拓展知识视野,老师又演示了如下实验:将打磨光亮的镁条在空气中点燃后迅速伸入充满二氧化碳的集气
瓶中,观察到镁条继续燃烧,发出耀眼白光并伴有轻微爆炸声,集气瓶内壁上出现黑色颗粒,同时生成白
色固体。同学们对该实验中生成的白色固体的成分进行了探究。
【猜想假设】猜想一:氧化镁 猜想二:碳酸镁 猜想三:氢氧化镁 猜想四:氧化镁和碳酸镁
同学们讨论后,一致认为猜想三不成立,理由是_____。
【实验验证】请你和同学们一起设计并完成实验。
实验操作 实验现象 实验结论
______。 _______。 猜想一成立
【反思交流】
(1)请你结合已有知识和实验探究过程,写出镁在二氧化碳中燃烧的化学方程式______。(2)综合上述实验,你对燃烧或二氧化碳性质的新认识是________(写一条)。
【答案】 ①. 氧气浓度 ②. 反应前不含有氢元素,违反质量守恒定律 ③. 取少量固体加入试管,
滴加稀盐酸 ④. 固体溶解,无气泡产生 ⑤. 2Mg+CO 2MgO+C ⑥. 燃烧不一定只需要氧气
2
(或二氧化碳也可以支持燃烧)
【解析】
【详解】空气和氧气中氧气浓度不同,物质燃烧的的现象不同,氧气中燃烧更剧烈,燃烧更快,说明氧气
浓度高加快反应速率;
故答案为:氧气浓度。
猜想假设:
根据质量守恒定律,反应前后元素种类不变,在反应物中没有出现氢元素,所以反应后产物也不应含有氢
元素,故猜想三不成立;
故答案为:反应前不含有氢元素,违反质量守恒定律。
实验验证:
碳酸镁与盐酸反应生成氯化镁、水和二氧化碳,氧化镁与盐酸反应生成氯化镁和水。实验结论为猜想一成
立,则说明不含有碳酸镁,因此固体加入盐酸,若不生成二氧化碳气体,看不到气泡,证明猜想一成立;
故答案为:取少量固体加入试管,滴加稀盐酸;固体溶解,无气泡产生。
反思交流:
(1)镁放入二氧化碳继续燃烧,此时生成白色固体为氧化镁,根据质量守恒定律和出现黑色颗粒,则另
一个生成物为碳,所以反应为镁与二氧化碳在点燃条件下反应生成氧化镁和碳,据此书写化学方程式,注
意配平及反应条件,所以为2Mg+CO 2MgO+C;
2
故答案为:2Mg+CO 2MgO+C。
2
(2)镁可以在二氧化碳中燃烧,说明燃烧可以不需要氧气,而二氧化碳在此处支持了镁的燃烧,说明二
氧化碳可以支持燃烧;
故答案为:燃烧不一定只需要氧气(或二氧化碳也可以支持燃烧)。
四、计算与分析题(5分)15. 为测定一瓶未知浓度的盐酸的溶质质量分数,化学兴趣小组向含有酚酞的100g 4% 的氢氧化钠溶液中滴
加该盐酸,恰好完全反应时溶液总质量为150g。(酚酞质量不计)
(1)恰好完全反应时的现象是_______。
(2)计算盐酸的溶质质量分数。
【答案】(1)红色褪去
(2)由质量守恒定律可知,滴入稀盐酸的质量为:150g-100g=50g,
设盐酸的溶质质量分数为x
x=7.3%
答:盐酸的溶质质量分数为7.3%。
【解析】
【详解】(1)含有酚酞的氢氧化钠溶液是红色的,盐酸和氢氧化钠反应生成氯化钠和水,恰好完全反应
时溶液呈中性,所以现象是红色褪去。故填:红色褪去。
(2)见答案。